Apuntes Biologia 2º 2011 204635
This document was ed by and they confirmed that they have the permission to share it. If you are author or own the copyright of this book, please report to us by using this report form. Report r6l17
Overview 4q3b3c
& View Apuntes Biologia 2º 2011 as PDF for free.
More details 26j3b
- Words: 79,378
- Pages: 281
BIOLOGÍA
2º BACHILLERATO
IES Fuentesnuevas
BLOQUE I LA BASE MOLECULAR Y FISICO-QUÍMICA DE LA VIDA
TEMA 1. LA BASE FÍSICO QUÍMICA DE LA VIDA
Parte 1. La Materia de los seres vivos Parte 2. Glúcidos y Lípidos Parte 3. Proteínas y ácidos nucleicos
TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA Parte 1. LA MATERIA DE LOS SERES VIVOS. LOS COMPUESTOS INORGÁNICOS 1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS. 1.1. 1.2. 2.
NIVELES DE ORGANIZACIÓN DE LOS SERES VIVOS COMPOSICIÓN QUÍMICA DE LOS SERES VIVOS BIOELEMENTOS
Propiedades del carbono Clasificación de los bioelementos Funciones de los bioelementos 3.
LAS BIOMOLÉCULAS
4.
EL AGUA
Estructura química Propiedades físico-químicas Funciones biológicas 5.
LAS SALES MINERALES
Funciones biológicas de las sales minerales
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
1
1. CARACTERÍSTICAS DE LOS SERES VIVOS La vida se define sobre una serie de características comunes a todos los seres vivos: ■ Todos los seres vivos están formados por células y todas las células, a su vez, están compuestas por los mismos tipos de moléculas, moléculas que intervienen en la construcción de los distintos componentes celulares, en las reacciones metabólicas o en la conservación y transmisión de la información genética. ■ En todos los organismos existen distintos niveles de organización, de forma que los organismos están constituidos por células y éstas pueden presentar distintas estructuras y orgánulos. ■ Nutrición: los seres vivos tienen la capacidad de crecer a expensas de los nutrientes que toman del medio externo. Dichos nutrientes son transformados, a través de una serie de reacciones metabólicas, en energía (catabolismo) y compuestos orgánicos (anabolismo o biosíntesis). ■ Relación con el medio ambiente y con otros organismos por medio de: La recepción e intercambio de señales (incluso dentro del propio organismo existen moléculas, como las hormonas, que llevan distintos tipos de señales de un órgano a otro, y de una célula a otra dentro de un mismo tejido). La capacidad de elaborar respuestas a distintos tipos de estímulos tanto internos como externos. ■ Las células y los organismos tienen además la capacidad de reproducirse y originar descendientes, que pueden ser genéticamente idénticos al individuo parental (reproducción asexual) u originarse por el intercambio de genes de distintos sexo (reproducción sexual). Estas tres últimas características (nutrición, relación y reproducción) son las funciones típicas de los seres vivos, y se conocen como funciones vitales. Hasta hace algunos años, a los seres vivos se les caracterizaba a través de sus funciones vitales, pero hoy en día, de acuerdo con la Teoría de Sistemas, también los podemos describir como un sistema ordenado de moléculas, ya que en definitiva los fenómenos vitales son reacciones reguladas por las biomoléculas presentes en los seres vivos. Todos los organismos se caracterizan por poseer, entre otras, dos biomoléculas: ácidos nucleicos y proteínas. Por ello, una definición moderna de ser vivo es aquella que considera a los seres vivos como cuerpos naturales que poseen ácidos nucleicos y proteínas y que son capaces de sintetizar dichas moléculas por sí mismos.
Las formas acelulares Pese a todas las características que acabamos de señalar para definir a un ser vivo, existen algunas formas de vida que se encuentran en la frontera entre lo vivo y lo inerte, son las formas acelulares de vida: virus, tiroides y priones. Los virus son complejos moleculares de proteínas y ácidos nucleicos que penetran en las células que parasitan y donde se multiplican con ayuda del material de la célula huésped, por lo que son parásitos obligados. Fuera de la célula son totalmente inertes y algunos han podido ser cristalizados. Gozan por tanto de algunas características de los seres vivos, como la capacidad de reproducción y mutación, por lo que no se pueden considerar seres inertes, pero no son capaces por sí mismos de fabricar sus propias proteínas y ácidos nucleicos y para ellos se ven obligados a parasitar una célula. Los viroides son moléculas de ARNm (ARN monocatenario circular) que carecen de envolturas externas. Son causantes de enfermedades en las algunas plantas (tomates, tubérculos,…) ya que interfieren en la regulación de los genes. Los priones son proteínas causantes de enfermedades neurodegenerativas (scrapie, enfermedad de las vacas locas,…). Las proteínas patógenas provocan cambios conformaciones en las proteínas normales.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
2
La dificultad para diferenciar la materia viva de la inerte es lógica su consideramos que los seres vivos se originaran a partir de la materia inerte, por un proceso gradual que fue la evolución biológica. Ahora bien, estas tres formas acelulares (virus, tiroides y priones), no son seres vivos primitivos o formas de transición entre la materia inerte y la materia viva, ya que son parásitos y necesitan de células para sobrevivir. 1.1. NIVELES DE ORGANIZACIÓN EN LOS SERES VIVOS Si algo caracteriza a los seres vivos y los diferencia de la materia inerte es su complejidad, su elevada organización y su diversidad. Estas propiedades están presentes en todos sus niveles de organización y son consecuencia de una característica intrínseca a la materia y que consiste en que bajo ciertas condiciones (consumiendo energía) evoluciona hacia formas más complejas. El siguiente cuadro muestra los niveles de organización en los seres vivos, desde lo más simple a lo más complejo, diferenciando los niveles abióticos (sin vida) y los bióticos (con vida).
En concreto, en lo que respecta a los niveles molecular y macromolecular, la mayoría de las moléculas que forman parte de los seres vivos son orgánicas, o sea, moléculas formadas por cadenas de átomos de carbono que adquieren una gran longitud y complejidad. Para comprender la enorme diversidad de compuestos orgánicos que se podrían formar, basta señalar la cantidad de palabras que se podrían escribir (no solo las que existen) en todas las lenguas con alfabeto latino. No obstante, esta gran variedad de compuestos orgánicos parte de muy pocos elementos estructurales sencillos que, combinados, constituyen las complejas macromoléculas. De forma que con unas pocas clases diferentes de moléculas sencillas (moléculas sillares o monómeros) se pueden obtener una gran diversidad de macromoléculas. Así, por ejemplo, con solo 20 aminoácidos combinados en numerosas secuencias distintas, se pueden originar miles de proteínas diferentes. Las moléculas sillares o monómeros son idénticos en todos los organismos. El hecho de que todos los seres vivos empleen estas mismas moléculas, indica que proceden de un antepasado común, origen de la gran biodiversidad actual. Aunque las “casas” sean diferentes, todos los organismos están hechos de los mismos “ladrillos”.
http://www.educa.madrid.org/web/ies.rayuela.mostoles/deptos/dbiogeo/recursos/Apuntes/ApuntesBioBach2/Tablas/TabCompQimCelulares.png
http://www.educa.madrid.org/web/ies.rayuela.mostoles/deptos/dbiogeo/recursos/Apuntes/ApuntesBioBach2/Tablas/TabCompQimCelulares.png05/11/2007 19:19:59
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
3
1.2. COMPOSICIÓN QUÍMICA DE LOS SERES VIVOS Como hemos visto, todos los seres vivos estamos formados por los mismos tipos de moléculas, que por este motivo, se denominan biomoléculas. Estas biomoléculas están formadas a su vez por una serie de elementos químicos o bioelementos. Entre las moléculas inorgánicas presentes en los seres vivos se encuentran principalmente el agua y algunas sales minerales. El agua es la molécula más abundante y es esencial para que tengan lugar los procesos bioquímicos necesarios para la actividad vital. En cuanto a las sales minerales, pueden encontrarse tanto en forma insoluble (como en las conchas o los caparazones de muchos animales), como soluble (participando en procesos enzimáticos o fisiológicos). Los constituyentes orgánicos de los seres vivos se pueden clasificar en cuatro grandes grupos o principios inmediatos: glúcidos, lípidos, proteínas y ácidos nucleicos (ADN y ARN). Estos últimos, los ácidos nucleicos, contienen toda la información genética de la célula y aseguran la herencia de ésta y la traducción del “código genético” en las proteínas necesarias para las funciones vitales. La combinación de los cuatro principios inmediatos orgánicos da lugar a la gran variedad de estructuras celulares, que permiten la nutrición, el metabolismo, la percepción y la respuesta a estímulos externos y la división y la reproducción de las células y los organismos. La vida no solo es la suma de todas estas moléculas independientes, sino que es el resultado de una interacción compleja entre dichas moléculas, que origina una estructura y unas funciones que definimos como vitales. Así por ejemplo, una hoja de papel esta formada por celulosa, pero no está viva; sin embargo, las células vegetales son formas vivas que presentan celulosa como uno de los constituyentes de su pared celular.
2. BIOELEMENTOS La materia que forma parte de los seres vivos está compuesta por moléculas, también denominadas biomoléculas, formadas a su vez por la unión de átomos de ciertos elementos químicos. Estos elementos presentes en las biomoléculas reciben el nombre de bioelementos o elementos biogénicos, de los que existen unos 70 diferentes. Todos los bioelementos se encuentran incluidos en la tabla periódica, es decir, no hay elementos exclusivos de los seres vivos. Sin embargo, los bioelementos mayoritarios no coinciden (salvo el oxígeno) con los elementos más abundantes de la corteza terrestre, que son el O, el Si y el Al. Los bioelementos más abundantes en los seres vivos son el C, el H, el O, el N, el P y el S. Estos elementos químicos fueron seleccionados por las propiedades que presentan: Los seis elementos tienen capas electrónicas externas incompletas, lo que les permite formar fácilmente enlaces covalentes y así originar las biomoléculas constituyentes de las estructuras biológicas. Poseen un número atómico bajo, por lo que los electrones compartidos en la formación de los enlaces covalentes se hallan próximos al núcleo y las moléculas originadas son estables. Dado que el oxígeno y el nitrógeno son elementos electronegativos, muchas biomoléculas son polares y, por ello, solubles en agua, requisito imprescindible para que tengan lugar las reacciones biológicas fundamentales de la actividad vital. Se pueden incorporar fácilmente a los seres vivos desde el medio externo, ya que se encuentran en moléculas (CO2, H2O, nitratos, sulfatos, fosfatos) que se pueden captar de manera sencilla. Esto asegura el intercambio constante de materia entre los organismos vivos y su ambiente.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
4
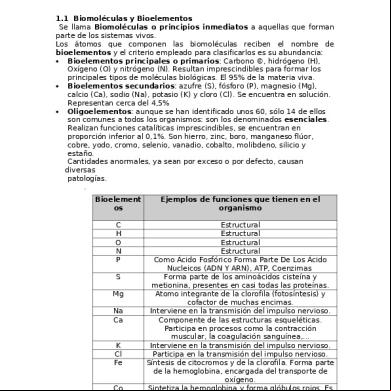
Propiedades del carbono Entre los bioelementos, el carbono desempeña un papel fundamental. El carbono se localiza en el grupo 14 del sistema periódico y tiene cuatro orbitales con electrones desapareados que se disponen en una estructura tetraédrica (configuración tetraédrica). Los electrones desapareados del carbono le permiten formar enlaces covalentes (simples, dobles y triples) con otros átomos de carbono, dando lugar a la formación de cadenas carbonadas estables de tamaño y forma variables (lineales, ramificadas y anilladas). Estas cadenas carbonadas actúan como el esqueleto molecular de las biomoléculas, permitiéndoles formar estructuras espaciales complejas y estables. Por otra parte, los átomos de carbono pueden formar enlaces covalentes con otros átomos distintos (hidrógeno, oxígeno, nitrógeno y azufre), dando lugar a diferentes grupos funcionales, que confieren propiedades concretas a las moléculas que los poseen. CLASIFICACIÓN DE LOS BIOELEMENTOS De los 70 bioelementos descritos, 25 de ellos están presentes en todos los seres vivos y el resto solo aparece en determinados grupos. Según la proporción en que se encuentran en la materia viva se clasifican en: Bioelementos primarios o plásticos. Son el grupo formado por el carbono (C), hidrógeno (H), oxígeno (O), nitrógeno (N), fósforo (P) y azufre (S). Constituyen, aproximadamente el 99% del total de la materia viva y son los componentes fundamentales de las biomoléculas. Bioelementos secundarios. Forman parte de todos los seres vivos, aunque menor proporción que los anteriores (a excepción del calcio). Se incluyen en este grupo el sodio (Na), potasio (K), calcio (Ca), magnesio (Mg) y el cloro (Cl). Oligoelementos o elementos traza. Se encuentran en proporciones inferiores al 0,1 %, pero son elementos imprescindibles ya que desempeñan funciones especiales en diferentes procesos bioquímicos y fisiológicos. Algunos oligoelementos, como el hierro (Fe), el cobre (Cu), el cinc (Zn), el manganeso (Mn), el yodo (I), el níquel (Ni) y el cobalto (Co), aparecen en la mayoría de los seres vivos y otros, como el silicio (Si), el fluor (F), el cromo (Cr), el litio (Li), el boro (B), el molibdeno (Mo) y el aluminio (Al), solo están presentes en grupos concretos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
FUNCIONES DE LOS BIOELEMENTOS PRIMARIOS y SECUNDARIOS
5
Biología 2º Bachillerato. Tema 1. Bioelementos OLIGOELEMENTOS ESENCIALES El ser humano no puede producir oligoelementos pero los necesita para vivir y preservar su salud. Son sustancias que intervienen en las funciones respiratoria, digestiva, neurovegetativa y muscular, como reguladores y equilibrantes. Todos ellos deben estar presentes en nuestra alimentación porque, si no ingerimos las pequeñas pero importantes dosis de ellos que precisa nuestro organismo, podemos enfermar. HIERRO: Los pulmones no podrían captar el oxígeno y transportarlo a todas las células sin la presencia del hierro. La carencia de ese oligoelemento puede frenar la producción de glóbulos rojos, ocasionar fatiga y aumentar la sensibilidad a diversas afecciones respiratorias. La carne, el pescado, el hígado, los riñones, el cacao, las espinacas, las habichuelas, el perejil, los mejillones, las habas, la soja, los frutos secos y el pan son alimentos ricos en hierro. COBRE: Estimula el sistema inmunitario. Podemos obtenerlo en los vegetales verdes, el pescado, los guisantes, las entejas, el hígado, los moluscos y los crustáceos. CROMO: Potencia la acción de la insulina y favorece la entrada de glucosa a las células. Su contenido en los órganos del cuerpo decrece con la edad. Los berros, las algas, las carnes magras, las hortalizas, las aceitunas y los cítricos (naranjas, limones, toronjas, etc.), el hígado y los riñones son excelentes proveedores de cromo. YODO: Forma parte de las hormonas tiroideas, que influyen fundamentalmente en el crecimiento y maduración del organismo, y afecta sobre todo a la piel, el pelo, las uñas, los dientes y los huesos. Las algas, los pescados, los mariscos, lo cereales, la carne magra, los huevos, la leche, el ajo, la cebolla, el limón, la naranja, la piña, las hortalizas de hoja verde y los frutos secos con ricos en yodo. MANGANESO: Es necesario para los huesos y juega un papel importante en las funciones reproductoras. Se puede encontrar en el pan integral, las hortalizas, la carne, la leche y sus derivados, los crustáceos y los frutos secos. SELENIO: Es un potentísimo antioxidante. Además, garantiza el buen funcionamiento de los músculos, protege nuestro sistema cardiovascular y puede evitar la aparición de cataratas. Está presente en las carnes de ave, vacuno y cerdo, en los cereales integrales, la levadura de cerveza, el germen de trigo, el ajo, el limón, la cebolla, las setas, el salmón, las verduras y los mariscos. ZINC: Interviene en el funcionamiento de ciertas hormonas y desempeña un importante papel en el crecimiento, la producción de insulina, las funciones psicológicas, la formación de espermatozoides y la defensa del sistema inmunitario. Se halla en alimentos como las ostras, el hígado de pato, la leche, el pan integral, las carnes de vacuno y cerdo, las legumbres, los pescados, las verduras de hoja verde y las nueces COBALTO: Es un componente esencial de la vitamina B12. Contribuye a reducir la presión arterial y a dilatar los vasos sanguíneos, y favorece la fijación de la glucosa en los tejidos. Podemos encontrarlo en las ostras, las legumbres, los cereales integrales, la cáscara de arroz, el ajo, la cebolla, el sésamo y el ginseng. FLÚOR: Previene la aparición de caries al mantener el esmalte de los dientes en buenas condiciones, ayuda a frenar la aparición de osteoporosis y tiene incidencia en el crecimiento. E pescado, los mariscos, el te, las verduras, las hortalizas, los cereales integrales, las legumbres y la cebolla son ricos en flúor. LITIO: Actúa sobre el sistema nervioso y es útil en las afecciones cardiacas. Se encuentra en los cereales integrales, las legumbres, a patata, el tomate, el nabo, el pimiento, las fresas, las frambuesas y la soja germinada. NÍQUEL: Potencia el crecimiento y es recomendable para combatir anemias, y enfermedades infecciosas, y en general, para estados carenciales y convalecencias. Los moluscos, la levadura de cerveza, el arroz integral y las legumbres son las principales suministradores de níquel. SILICIO: Aumenta la elasticidad y resistencia de los huesos, previene la arteriosclerosis, retrasa el envejecimiento y equilibra el sistema nervioso. Se encuentra en los cereales integrales, la levadura de cerveza, el maíz, la calabaza, la sandía y la cola de caballo.
Principales Elementos Químicos de los Seres Vivos Nombre Símbolo
N.A. Valencia P.A.
Electneg
% At
% Peso
Formas químicas
Función
Hidrógeno H
1 2
-1 +1
2.1
63
10
C-H
H+ H2 O
Protón Agua
Agua Iones ácidos H+ Compuestos orgánicos: Saturación de los grupos orgánicos
Carbono C
6 12
-4 +4
2.5
10
12
C-C C=C
CO3= CO3H-
Carbonato Bicarbonato
Compuestos orgánicos : Esqueleto de las moléculas orgánicas Carbonatos
Nitrógeno N
7 14
-3 +5
3.0
1.5
3.3 C-NH2 C=N-
Amino
Oxigeno O
8 16
-2
3.5
25
63
Alcohol COOH Aldehido.Cetona H2O
Azufre S
16 32
-2 +6
2.5
0.05
0.25 C-SH C-S-S-C
Fósforo P
15 31
+5
2.1
0.20
0.98 PO4---
Fosfato
Uniones entre compuestos orgánicos Enlaces ricos en energía. Tampones de pH
Sodio Na
11 23
+1
0.9
0.03
0.11 Na+
Ión Sodio
Ión en disolución: Principal catión extacelular
Potasio K
19 39
+1
0.8
0.05
0.31 K+
Ión Potasio
Ión en disolución : Principal catión intracelular
Magnesio Mg
12 24
+2
1.2
0.01
0.04 Mg++
Ión Magnesio
Ión en disolución Enzimas
Calcio Ca
20 40
+2
1.0
0.30
1.9 Ca++
Ión Calcio
Ión en disolución Mensajero celular Ión precipitado : esqueletos
Cloro Cl
17 35
-1
3.0
0.10
0.56 Cl-
Ión Cloro
Ión en disolución: Principal anión inorgánico
C-OH C=O
Sulfhidrilo Bisulfuro
Compuestos orgánicos: Grupos reacctivos con carga +
SO4=
Acido Agua
Agua Compuestos orgánicos : Grupos reactivos con carga -
Sulfato
Compuestos orgánicos : Enlaces reversibles
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
6
3. LAS BIOMOLÉCULAS Los átomos de los diferentes bioelementos se unen entre sí mediante enlaces químicos para formar las moléculas constituyentes de los organismos vivos, que reciben el nombre de biomoléculas o principios inmediatos. Mediante diferentes técnicas de análisis basadas en métodos físicos, como la filtración, la destilación, la centrifugación y la decantación, es posible separar las biomoléculas de un ser vivo sin destruirlas. A pesar de la gran variedad de biomoléculas (una célula contiene más de 10.000 moléculas distintas), todas se agrupan en dos grandes clases, según su naturaleza: Biomoléculas inorgánicas: agua y algunas sales minerales. Biomoléculas orgánicas: glúcidos, lípidos, proteínas y ácidos nucleicos. Algunas como las enzimas, vitaminas y hormonas, se encuadran químicamente en los grupos de biomoléculas orgánicas.
El enlace químico en las biomoléculas La mayoría de las sustancias que existen en la naturaleza son sustancias compuestas, en las que los átomos tienden a unirse de forma espontánea mediante un enlace químico. Existen dos tipos básicos de enlaces entre átomos: iónico y covalente. Además, unas moléculas se pueden unir a otras mediante enlaces intermoleculares. Todos estos enlaces contribuyen a la formación de las distintas biomoléculas, pero en la materia viva son especialmente importantes los enlaces covalentes e intermoleculares. Enlace iónico: se produce entre átomos con electronegatividades (tendencia a ganar electrones) muy diferentes; se produce por la atracción electrostática de cargas opuestas, resulta de la pérdida de electrones por parte de un átomo y la ganancia por parte de otros. El átomo que capta los electrones se transforma en un ión negativo o anión, y el que los pierde, en un ión positivo o catión. En solución los iones están libres, mientras que en estado sólido unos iones se rodean de otros de carga opuesta, formando un entramado ordenado que origina una estructura cristalina. De esta forma (sólidas o solubilizadas), se encuentran las sales minerales presentes en los seres vivos. Enlace covalente: se produce entre átomos que comparten uno o más pares de electrones, cuya electronegatividad es igual o parecida. En el primer caso se originan moléculas apolares (como el N2, O2 e H2). Cuando unos átomos atraen más que otros los electrones, se originan moléculas polares, con un polo positivo (+) y otro negativo (-), formando dipolos moleculares, como el H2O, NH3, SH2, etc.,… Enlaces intermoleculares: se establecen entre átomos de moléculas distintas y por lo tanto unen moléculas. Entre los enlaces intermoleculares destacan: ▪ Puentes o enlaces de hidrógeno: se estable entre un átomo de H y otros átomos muy electronegativos, como F, O y N. Los átomos de H quedan próximos a otros átomos de moléculas adyacentes y se establecen pequeñas fuerzas de atracción entre ellos. Este enlace asegura la cohesión entre las moléculas de agua y contribuye a la conformación espacial de moléculas como las proteínas y los ácidos nucleicos. ▪ Interacciones iónicas: se producen entre moléculas que poseen grupos funcionales con cargas eléctricas distintas. Se da en las proteínas. ▪ Interacciones hidrofóbicas: se deben a que las moléculas apolares tienden a agruparse en un medio acuoso. Son importantes en la formación de las membranas celulares. ▪ Otros: el enlace glucosídico, que une monosacáridos; el enlace peptídico, que une aminoácidos; el enlace fosfodiéster, que une nucleótidos. Son todos enlaces de tipo covalente que se establecen entre átomos de diferentes moléculas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
7
4. EL AGUA El agua es un componente fundamental de los seres vivos, ya que es la molécula más abundante en todos los organismos (supone, aproximadamente, entre el 50 y 90 % de su peso). La cantidad de agua presente en los seres vivos depende de tres factores: ▪ Especie. Los organismos acuáticos contienen un porcentaje de agua muy elevado, que puede alcanzar el 99% de su peso, mientras que los valores más bajos corresponden a especies adaptadas a zonas desérticas. ▪ Edad del individuo. Las estructuras biológicas de los individuos jóvenes presentan una mayor proporción de agua que la de los individuos de más edad. ▪ Tipo de tejido u órgano. Dado que las reacciones biológicas se llevan a cabo en un medio acuoso, los tejidos con mayor actividad bioquímica contienen una proporción de agua mayor que los más pasivos. En cambio, las estructuras esqueléticas animales que constituyen órganos de sostén del individuo, poseen los porcentajes más bajos. El agua en los organismos pluricelulares se encuentra en forma de agua intracelular (en el interior de las células) aproximadamente en dos tercios del total, y en forma de agua extracelular (en los espacios intersticiales de las células o como parte del agua circulante en la sangre o en la savia vegetal) en otro tercio. El elevado contenido de agua en los seres vivos pone de manifiesto, además, la importancia de las funciones que desempeña en ellos, las cuales derivan de sus propiedades físico-químicas y estas, a su vez, de su estructura química.
Estructura química del agua La molécula de agua consta de un átomo de oxígeno y dos de hidrógeno, unidos mediante enlaces covalentes, en los que cada átomo de hidrógeno de una molécula comparte un par de electrones con el átomo de oxígeno. Como la electronegatividad del oxígeno es mayor que la del hidrógeno, los pares de electrones compartidos se ven atraídos con más fuerza por el núcleo del oxígeno que por el del hidrógeno. Esto, unido al hecho de que el oxígeno posee cuatro electrones más sin compartir, da lugar a dos consecuencias: Los enlaces no se disponen en línea recta, sino formando un ángulo de 104,5º. El átomo de oxígeno presentan una cierta carga negativa (-) y los átomos de hidrógeno cierta carga positiva (+), creándose una asimetría eléctrica. Por esta razón, a pesar de ser eléctricamente neutra en su conjunto, la molécula de agua tiene carácter dipolar, es un dipolo eléctrico.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
8
Esta polaridad favorece que las moléculas de agua próximas entre sí tiendan a asociarse, de manera que la zona con carga negativa de una de ellas es atraída por la zona con carga positiva de otra, estableciéndose entre ambas un tipo de enlace denominado enlace o puente de hidrógeno, que convierte al agua en una sustancia altamente cohesiva, ya que cada molécula de agua puede establecer cuatro puentes de hidrógeno con otras tantas moléculas.
Propiedades físico-químicas del agua Las propiedades físicas y químicas del agua derivan de su polaridad y de la cohesión entre sus moléculas. Las más importantes y sus consecuencias biológicas son: Gran poder disolvente. El agua es uno de los mejores (por no decir el mejor) disolventes líquidos. El agua disuelve compuestos iónicos y polares y dispersa moléculas anfipáticas (como los ácidos grasos) y de elevado peso molecular (como las proteínas). Si se introduce en un medio acuoso un compuesto iónico o polar, las moléculas de agua rodean a cada ión o polo con sus zonas de carga opuesta, fenómeno conocido como solvatación. Como consecuencia de ello, se produce un reparto en toda la extensión de la masa de agua, o sea, una verdadera disolución. Elevada tensión superficial. En la superficie de o con otro medio, la polaridad de las moléculas de agua no se equilibra y la cohesión entre ellas es mayor, lo que proporciona una especie de película superficial bastante resistente. Esta propiedad es la causante de la mayoría de las deformaciones celulares y de los movimientos citoplasmáticos.
Capilaridad. La unión entre las moléculas de agua mediante puentes de hidrógeno les confiere un grado de cohesión muy alto, lo que combinado con la adhesión a la superficie de otras estructuras (debida a su polaridad), permite que el agua pueda ascender a lo largo de conductos estrechos. Esta propiedad resulta fundamental para el ascenso de la savia bruta por los tubos del xilema en las plantas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
9
Líquido prácticamente incompresible. El volumen de agua líquida no disminuye apreciablemente aunque se apliquen presiones muy altas, debido al elevado grado de cohesión entre sus moléculas. Esta propiedad permite que el agua actúe como esqueleto hidrostático en las células vegetales y determina las deformaciones citoplasmáticas. Elevado calor específico. El calor específico de una sustancia (Ce) es la cantidad de calor (medida en calorías) necesaria para elevar 1º C la temperatura de un gramo de dicha sustancia. A unos 15 ºC, el Ce del agua es de 1 cal/g ºC, lo que comparado con otros compuestos es muy elevado. Esto se debe a que parte de la energía comunicada al agua se emplea en romper los puentes de hidrógeno y no en elevar la temperatura. Esto permite que el agua sea un amortiguador térmico, o sea, el agua absorbe o libera grandes cantidades de calor sin que haya grandes variaciones en su temperatura. Alta conductividad. La conductividad del calor del agua es relativamente alta y evita la acumulación local de calor. Elevado calor de vaporización. Para pasar del estado líquido al gaseoso es necesario que los puentes de hidrógeno se rompan, lo que requiere un aporte considerable de energía. Esta energía se toma del entorno, por lo que la evaporación del agua absorbe mucho calor y disminuye la temperatura de su entorno. Por eso, la formación y evaporación del sudor en los humanos y el jadeo en los perros son mecanismos refrigerantes que ayudan a regular la temperatura corporal. Mayor densidad del hielo que del agua líquida. Cuando la temperatura del agua disminuye por debajo de 4 ºC, cada molécula de agua puede formar enlaces de hidrógeno con otras cuatro, y cuando la temperatura alcanza los O ºC se forma una red espacial de moléculas de agua que ocupa un mayor volumen que el agua líquida, por lo que el hielo formado es menos denso y flota en ella. Esta propiedad permite la vida acuática en los climas fríos, ya que se forman capas de hielo superficiales que actúan como aislante térmico, lo que permite la supervivencia de las especies acuáticas en invierno.
Bajo grado de ionización. En el agua líquida existe una pequeña cantidad de moléculas ionizadas (disociadas en sus iones), debido a la pequeña masa del hidrógeno y a que su electrón se halla fuertemente unido al oxígeno. Cuando una molécula de agua se ioniza se obtienen dos iones, H3O+ y OH-, con carga opuesta y en igual concentración (los H3O+ suelen representarse simplemente como H+). El producto de las concentraciones de los iones (H3O+ y OH-) es constante, y se denomina producto iónico. Su valor para el agua pura a 25 ºC es: Kw = [H3O ] [OH- ] = 1 1014
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
10
En el agua pura las concentraciones de iones H3O+ y OH- es la misma e igual a 1 10-7, sin embargo en una disolución acuosa la proporción de iones varía, pudiendo ser: Neutras, si la concentración de iones H3O+ y OH- es igual. Ácidas, si la concentración de iones H3O+ es mayor que la de OH-. Básicas, si la concentración de iones OH- es mayor de que de H3O+. El agua y sus productos de ionización participan en una serie de reacciones biológicas importantes, entre las que destacan las reacciones de hidrólisis, en las que una molécula de agua rompe una molécula orgánica. La hidrólisis es el procedimiento empleado para obtener moléculas sencillas a partir de macromoléculas, como sucede en la digestión.
Funciones biológicas del agua Las funciones que el agua desempeña en los seres vivos derivan de las propiedades que acabamos de ver. El agua en los seres vivos actúa, principalmente como: ▪ Medio de transporte de sustancias. Debido a su poder disolvente y dispersante, puede transportar sustancias de una zona a otra de los organismos (ejemplo: sangre y savia). Además, gracias al transporte de sustancias las células pueden intercambiar materia con el medio a través de las membranas celulares. ▪ Medio de reacción. Gracias al poder disolvente, la mayoría de las biomoléculas están disueltas en el agua y pueden reaccionar entre sí. ▪ Reactivo químico. Participa en algunas reacciones químicas, como las reacciones de hidrólisis, en las que se rompen enlaces introduciendo la molécula de agua. ▪ Agente regulador de la temperatura. El agua es un excelente amortiguador térmico, debido al elevado calor específico, evitando cambios bruscos de temperatura en los organismos. Las reacciones biológicas generan calor, pero no se produce un aumento de temperatura ya que el agua lo absorbe. Además la alta conductividad térmica evita la acumulación de calor en un determinado punto del organismo. Asimismo, el elevado calor de vaporización facilita la regulación de la temperatura corporal, refrigerando el organismo al evaporarse el sudor. Otras funciones del agua son: Función estructural: proporciona turgencia a las células debido a su carácter incompresible. Algunos animales (como gusanos perforadores), presentan esqueletos hidrodinámicos, que al hincharse les permite perforar el fondo marino. Amortigua los golpes, como el líquido cefalorraquídeo que protege al cerebro de los golpes que sufre el cráneo. Lubrica las articulaciones, como el líquido sinovial, que evita el rozamiento de los huesos en la articulación.
5. LAS SALES MINERALES y SUS FUNCIONES BIOLÓGICAS Los organismos vivos están formados también por sales minerales, compuestos inorgánicos que pueden encontrarse en dos formas: ■ En estado sólido, cuando son insolubles en agua y se encuentran precipitadas, formando parte de estructuras esqueléticas, como huesos, conchas o caparazones. ■ En disolución, cuando son solubles en agua y se encuentran disociadas en sus correspondientes iones (aniones y cationes). Entres los aniones y cationes más frecuentes figuran los siguientes: Aniones: Cl-; CO32- ; HCO-3 ; PO34- ; SO24 Cationes: Na+; K+; Ca2+; Mg2+; Fe2+; Fe3+ Algunos cationes pueden aparecer asociados a determinadas moléculas orgánicas (proteínas) como el ión ferroso, que interviene en el transporte de oxígeno asociado a la hemoglobina.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
11
Funciones de las sales minerales Constitución de estructuras esqueléticas. Los huesos, las conchas, los caparazones y las espículas de algunos organismos están formadas por sales precipitadas, como fosfatos (Ca3(PO4)2), carbonato cálcico (CO3Ca) e incluso sílice (SiO2). Funciones fisiológicas y bioquímicas. Muchos procesos biológicos solo se pueden realizar con la intervención de determinados cationes. En el cuadro de los bioelementos se recogen los más importantes. Regulación del equilibrio osmótico. Todos los medios líquidos biológicos (sangre, plasma intersticial, líquido cefalorraquídeo, etc.,…) constituyen disoluciones de sales en agua cuyo grado de concentración depende de la estabilidad celular y la realización de algunas funciones fundamentales. Cuando existen dos disoluciones de diferente concentración separadas por una membrana semipermeable que no deja pasar el soluto pero sí el disolvente, se produce el paso del disolvente (agua en los medios celulares) desde la disolución más diluida (hipotónica o hipoosmótica) hacia la más concentrada (hipertónica o hiperosmótica) a través de la membrana. Este fenómeno se conoce como ósmosis. Cuando el agua pasa a la disolución hipertónica, esta se diluye, mientras que la disolución hipotónica se concentra al perder agua. El proceso continua hasta que ambas disoluciones igualan su concentración, es decir, se hacen isotónicas o isoosmóticas (como el suero fisiológico, de 0,9% de concentración salina, que es una solución isotónica con las células del cuerpo humano). Para evitar el paso del agua sería necesario aplicar una presión, denominada presión osmótica, tanto más intensa cuanto mayor fuera la diferencia de concentración entre ambas disoluciones.
Como la membrana plasmática es semipermeable, es necesario mantener una concentración salina dentro de la célula igual a la del medio externo para que la célula no tenga pérdida ni ganancia de agua. Cuando esto no sucede se producen dos tipos de fenómenos osmóticos: ▪ Si la concentración del medio intracelular es mayor que la del medio externo, la entrada masiva de agua producirá un hinchamiento, conocido como turgencia celular. Si la célula es animal puede llegar a estallar (lisis osmótica) y si es vegetal se hincha ligeramente ya que la pared celular equilibra la presión osmótica, comprimiéndose el citoplasma contra la pared. ▪ Si, por el contrario, la concentración del medio interno es menor que en el medio externo, la célula pierde agua y disminuye su volumen, fenómeno conocido como plasmólisis. La célula se arruga y la pérdida de agua puede llegar a la muerte celular. En las células vegetales la vacuola disminuye su tamaño, arrastrando al citoplasma y la membrana se despega de la pared.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
12
Todos los seres vivos, acuáticos o terrestres, están obligados a la osmorregulación o regulación de la presión osmótica. Muchos de ellos han conseguido sobrevivir en medios hipotónicos o hipertónicos mediante mecanismos físicos o químicos que evitan los cambios de presión osmótica en su medio interno. Mantenimiento del pH. En los líquidos biológicos siempre existen unas ciertas cantidades de iones H3O+ (hidrogeniones) y OH- (hidroxilos) que proceden de la disociación del agua y de sustancias ácidas y básicas. (los iones H3O+ suelen representar simplemente como H+). Cuando la [H+ ] es mayor que la [OH- ] la disolución es ácida y cuando la [H+ ] es menor que la de [OH ] decimos que dicha disolución es básica. Si ambas concentraciones son igual, dicha disolución es neutra. Para medir el grado de acidez de una disolución se utiliza el término pH, que se define como el logaritmo inverso de la [ H+]. pH = log
1 = - log [H+] [H ]
Así, por ejemplo, el pH de una disolución cuya [H+] es de 10-5 será de 5. La utilización de valores de pH permite simplificar el manejo de los valores exponenciales y bajo de la [H+]. Los valores de pH pueden oscilar entre 0 y 14. ▪ pH= 7 pH neutro ▪ pH < 7 pH ácido ▪ pH > 7 pH básico Para el buen funcionamiento, las células requieren un pH cercano al neutro. Sin embargo, como consecuencia de las reacciones metabólicas, continuamente se están produciendo sustancias ácidas o básicas que varían el pH. Para evitarlo, el organismo dispone de ciertos mecanismos químicos, los sistemas amortiguadores o tampón, que evitan los cambios de pH, constituidos por un ácido débil y una sal del mismo ácido. Existen diversos sistemas tampón, los más importantes son el sistema tampón bicarbonato que mantiene el pH de los líquidos extracelulares y el sistema tampón fosfato, que actúa en el medio intracelular. (más adelante se expone su forma de actuación).
Biología 2º Bachillerato APÉNDICE TEMA 1. FÍSICO-QUÍMICA DE LAS DISPERSIONES ACUOSAS El agua es el disolvente biológico ideal, disuelve con facilidad una gran variedad de constituyentes de los seres vivos, entre ellos iones, azúcares y muchos aminoácidos. Debido a su gran poder disolvente, el agua se encuentra en el interior de todos los seres vivos formando disoluciones de diversos solutos. Una disolución o dispersión es una mezcla homogénea de moléculas distintas, que son las del disolvente o fase dispersante y las de soluto o fase dispersa. Según el tamaño de las partículas dispersas en el agua se distinguen dos tipos de disoluciones: Disoluciones verdaderas: cuando el tamaño de las moléculas de soluto es pequeño, debido a lo cual el aspecto de la disolución es igual que el disolvente puro. Las disoluciones verdaderas poseen unas propiedades, llamadas coligativas que dependen de la concentración del soluto (como el aumento de la temperatura de ebullición). Forman disoluciones verdaderas las sales minerales y moléculas orgánicas de bajo peso molecular (monosacáridos, disacáridos, aminoácidos,…) Disoluciones o dispersiones coloidales: cuando las moléculas de soluto son de gran peso molecular y tamaño. No son disoluciones verdaderas porque las moléculas de soluto se pueden separar por ultracentrifugación. En estas dispersiones los solutos son macromoléculas como las proteínas, los ácidos nucleicos y los polisacáridos. Las partículas dispersas pueden provocar tres fenómenos en relación con su movimiento en el seno del agua: difusión, diálisis y ósmosis. La difusión sería el fenómeno por el cual las moléculas disueltas tienden a distribuirse uniformemente en el seno del agua. Puede ocurrir también a través de una membrana si es lo suficientemente permeable, de manera que las moléculas de soluto pueden atravesar la membrana desde una zona de alta concentración hacia otra de baja concentración, es decir, a favor del gradiente de concentración. Un ejemplo es el movimiento del CO2 hacia el exterior de la célula o el movimiento de los iones de Na hacia el interior de las células nerviosas cuando conducen el impulso nervioso. La ósmosis es la difusión de agua a través de una membrana semipermeable en presencia de al menos un soluto para el que la membrana es impermeable. La difusión de las moléculas de agua se realiza de la zona más diluida a la más concentrada hasta alcanzar un equilibrio de concentraciones (equilibrio osmótico). En clase ya hemos estudiado qué sucede cuando no se da tal equilibrio. La diálisis es un proceso relacionado con la ósmosis. En este caso pueden atravesar la membrana además del disolvente, moléculas de bajo peso molecular y éstas pasan atravesando la membrana desde la solución más concentrada a la más diluida. El movimiento se produce desde la zona de mayor presión a la zona de menor presión, como sucede en el riñón cuando el agua y los solutos pequeños salen de los vasos sanguíneos para formar la orina. Mediante la diálisis, si se tiene una disolución de dos tipos de sustancias, una de ellos de elevado peso molecular y otra bajo peso molecular, se puede conseguir una separación parcial de esta última. Para ello, se prepara la disolución en un recipiente separado, por medio de una membrana semipermeable, de otro que contiene agua destilada. El soluto de bajo peso molecular se distribuye a través de la membrana hasta que se alcanza la misma concentración en ambos recipientes, mientras que las moléculas de gran tamaño no atravesarán la membrana y se quedarán en el recipiente original. La diálisis es el fundamento de la hemodiálisis que intenta sustituir la filtración renal deteriorada. Mediante esta técnica se consigue eliminar las sustancias tóxicas de la sangre (como la urea) en caso de insuficiencia renal.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
1
ACTIVIDADES TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA. PARTE 1. LA MATERIA DE LOS SERES VIVOS. LOS COMPUESTOS INORGÁNICOS. 1. En qué nivel de organización de la materia incluirías: Proteína Pradera Rebaño de ovejas Epidermis Hueso Núcleo celular Oligoelemento Colonia de protozoos Bacteria Raíz 2. • • • • • • • • • • • • •
Busca qué ramas científicas de la Biología están relacionadas con el estudio de: Moléculas y procesos químicos en los seres vivos Células y orgánulos celulares Tejidos Microorganismos Animales Vegetación Características físicas animales y plantas Funcionamiento de órganos, aparatos y sistemas en animales y plantas ADN y transmisión de caracteres hereditarios Desarrollo embrionario en animales Fósiles Comportamiento animal Ecosistemas
3. El Silicio es un elemento muy abundante en la corteza terrestre. Busca datos referentes a sus propiedades físico-químicas y trata de explicar porqué el carbono y no el silicio, siendo tan abundante, ha permitido la formación de la materia viva. 4. Trata de explicar: a) ¿Porqué el oxígeno permite obtener tanta energía a partir de la materia orgánica?. b) ¿Porqué el fósforo permite almacenar energía de pronto uso?. c) ¿Porqué se cree que la vida apareció en el medio acuoso?. 5. ¿Qué es un Oligoelemento?. Cita cinco ejemplos y su importancia en los seres vivos. 6. ¿Significa lo mismo materia viva y materia orgánica?. ¿Las moléculas orgánicas se encuentran solamente en los seres vivos?. Razona la respuesta. 7. ¿Por qué la carne de ternera es más blanda que la de vaca, pero esta última, a igualdad de peso, proporciona más nutrientes?. 8. Explica sucintamente si la proposición que sigue es verdadera o falsa: “Todas las células viven en un medio acuoso, excepto las de los reptiles, que prefieren ambiente seco”. 9. ¿A qué se debe la fuerte cohesión entre las moléculas de agua?. 10. ¿Porqué a temperatura ambiente el agua es un líquido, siendo el SO2, un gas?. 11. ¿Porqué el agua es un gran disolvente?. ¿Porqué no disuelve los hidrocarburos?.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
2
12. Explica: a) ¿Porqué las regiones costeras tienen un clima más suave que las zonas interiores de los continentes?. ¿Qué relación tiene esta pregunta con los seres vivos?. b) ¿Porqué al depositar suavemente una hoja de afeitar sobre la superficie del agua esta no se hunde?. 13. ¿Cuál es el pH de dos disoluciones en las que [H+] es 1,4 x 10-8 y 4 x 10-6?. 14. Hasta hace poco tiempo, cuando una comida copiosa provocaba acidez de estómago, al segregarse gran cantidad de HCl, se tomaba bicarbonato sódico (HCO3Na) para su digestión. a) Explica cómo tiene lugar el proceso de neutralización en el estómago b) Actualmente no se aconseja abusar del bicarbonato, ¿sabes por qué?. 15. Busca en algún libro las diferencias entre ósmosis y diálisis. 16. Lee atentamente estos experimentos y responde a las siguientes cuestiones: Experimento 1. Extraemos un fragmento de tejido y lo introducimos en un recipiente con un medio acuoso (medio A), dejándolo reposar cinco minutos. Retiramos el tejido del medio y al observar el microscopio, vemos que sus células presentan un aspecto arrugado. Experimento 2. Realizamos un experimento similar, introduciendo esta vez el tejido en otro medio (medio B). Al observar las células al microscopio aparecen hinchadas. a) ¿Cómo sería el medio A y el medio B?. b) ¿Cómo se denomina el fenómeno que sufren las células en cada experimento?. c) Explica el proceso físico que ha sucedido en cada uno de los experimentos. 17. ¿Porqué las hojas de lechuga se ponen turgentes cuando se dejan en agua y luego al aliñar se arrugan?. 18. ¿Porqué las soluciones que se istran en inyección endovenosa deben ser isotónicas para las glóbulos rojos?. ¿Qué podría ocurrir si así no fuera?.
TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA PARTE II. GLÚCIDOS y LÍPIDOS 1.
CONCEPTO DE GLÚCIDO, FUNCIONES y CLASIFICACIÓN
2.
MONOSACÁRIDOS
2.1. 2.2. 2.3. 2.4. 2.5.
Composición química y nomenclatura Propiedades químicas Propiedades físicas Fórmulas cíclicas Importancia biológica de los monosacáridos
3.
ENLACE O-GLUCOSÍDICO
4.
DISACÁRIDOS
5.
POLISACÁRIDOS
6.
HETERÓSIDOS
7.
FUNCIONES BIOLÓGICAS DE LOS GLÚCIDOS
8.
LÍPIDOS: CARACTERÍSTICAS GENERALES y CLASIFICACIÓN
9.
LOS ÁCIDOS GRASOS
10. LÍPIDOS SAPONIFICABLES 10.1. LÍPIDOS SIMPLES SAPONIFICABLES
GRASAS CERAS
10.2. LÍPIDOS COMPLEJOS SAPONIFICABLES
FOSFOGLICÉRIDOS ESFINGOLÍPIDOS
11. LÍPIDOS INSAPONIFICABLES TERPENOS ESTEROIDES PROSTAGLANDINAS 12. FUNCIONES BIOLÓGICAS DE LOS LÍPIDOS
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
1
1. CONCEPTO DE GLÚCIDO, FUNCIONES y CLASIFICACIÓN Los glúcidos son moléculas orgánicas que contienen átomos de C, H y O. A menudo se les denominan azúcares, ya que muchos de ellos tienen sabor dulce y también reciben el nombre de hidratos de carbono o carbohidratos, porque muchos de ellos responden a la fórmula empírica Cn(H2O)n que parece corresponder a combinaciones de carbono con agua. Sin embargo, esta última denominación resulta incorrecta, pues los glúcidos son polialcoholes con un grupo funcional carbonilo (aldehído o cetona); es decir, son polihidroxialdehídos o polihidroxicetonas. Esta composición química es común a todos los glúcidos. Los glúcidos se encuentran en todos los seres vivos, donde desempeñan fundamentalmente una función energética, aunque también existen otros glúcidos no energéticos que cumplen otras funciones (estructural, reconocimiento celular, etc.) Los glúcidos se clasifican según su complejidad en: MONOSACÁRIDOS u OSAS: comprenden los glúcidos más simples y no pueden ser hidrolizados (no hidrolizables). Contienen entre 3 y 7 átomos de carbono. En este grupo se incluyen también sus derivados. Entre ellos se encuentran la glucosa, fructosa o la ribosa. ÓSIDOS: son glúcidos compuestos por la unión de varios monosacáridos ( o sus derivados). Estos glúcidos son hidrolizables, ya que pueden experimentar reacciones de hidrólisis que liberan los monosacáridos que los componen. Se subdividen en dos grupos: ▪ Holósidos: formados únicamente por monosacáridos. Según el número de monosacáridos que presentan pueden ser: - Oligosacáridos: compuestos por la unión de dos a diez monosacáridos. Entre ellos destacan los disacáridos, como la sacarosa, lactosa o maltosa. - Polisacáridos: formados por un elevado número de monosacáridos. Destacan el almidón, glucógeno, celulosa y quitina. ▪ Heterósidos: formados por una parte glucídica (monosacáridos) y otra no glucídica que recibe el nombre de aglucón. Si la parte no glucídica es una proteína hablamos de glucoproteínas y si se trata de un lípido, de glucolípidos.
2. MONOSACÁRIDOS Los monosacáridos son los glúcidos más sencillos, por eso las células pueden utilizarlos directamente como fuente de energía.
2.1.
Composición química y nomenclatura
Los monosacáridos contienen entre 3 y 7 átomos de carbono, denominándose triosas, tetrosas, pentosas, hexosas o heptosas si el número de carbonos es, respectivamente, 3, 4, 5, 6, o 7. Químicamente los monosacáridos son polihidroxialdehídos o polihidroxicetonas, es decir, están formados por varios grupos alcohol (-OH) con un grupo aldehído (-CHO) o cetona (-CO). Según el grupo funcional principal que lleven, se clasifican en : ■ Aldosas: tienen un grupo aldehído en el primer carbono (C1) y grupos hidroxilo en el resto de los carbonos. ■ Cetosas: tienen un grupo cetona en el segundo carbono (C2) y grupos hidroxilo en el resto. Los monosacáridos se nombran anteponiendo el prefijo aldo- o ceto- al nombre que indica el número de carbonos, seguido de la terminación –osa. Por ejemplo, un monosacárido de tres átomos de carbono cuyo grupo funcional principal es un aldehído se denomina aldotriosa y será cetotriosa si el grupo funcional es una cetona. Además de la nomenclatura sistemática, la forma de nombrar a los monosacáridos más utilizada es mediante nombres vulgares o comunes, que hacen referencia a alguna característica, utilizando la terminación –osa (glucosa, fructosa, ribosa, galactosa, etc.).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
FÓRMULAS DE LOS MONOSACÁRIDOS (PROYECCIÓN DE FISCHER)
2
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
3
2.2. Propiedades químicas Todos los monosacáridos tienen carácter reductor debido a la presencia de los grupos aldehído o cetona, que pueden oxidarse a carboxilos. Esta propiedad se utiliza para determinar la presencia de monosacáridos en un material biológico, mediante diferente tipo de reacciones. Entre ellas destaca la reacción de Fehling, en la que se emplea sulfato de cobre (SO4Cu) en un medio alcalino (NaOH) y es reducido a óxido de cobre (Cu2O), produciendo una coloración rojo ladrillo. Además el grupo aldehído o cetona participan en la formación de distintos enlaces: ▪ Hemiacetálicos internos, originando formas cíclicas ▪ Enlaces glucosídicos entre monosacáridos, originando disacáridos y polisacáridos.
2.3. Propiedades físicas Todos los monosacáridos son sólidos cristalinos y blancos, perfectamente solubles en agua, y tienen sabor dulce. Todos los monosacáridos, a excepción de la Dihidroxiacetona, presentan carbonos asimétricos, es decir, carbonos unidos a cuatro radicales distintos, lo que les otorga dos propiedades físicas muy importantes: Estereoisomería o isomería espacial Actividad óptica
Estereoisomería La estereoisomería es la existencia de moléculas que presentan la misma fórmula estructural pero distinta disposición espacial de sus átomos. Esto sucede debido a la presencia de algún átomo de CARBONO ASIMÉTRICO, es decir, un carbono que está unido a cuatro radicales diferentes. Los carbonos asimétricos son frecuentes en los glúcidos y se identifican en la molécula con un asterisco (*). carbono asimétrico
Cada carbono asimétrico determina la existencia de dos ISOMÉROS ESPACIALES o ESTEREOISÓMEROS (DIASTEROISÓMEROS), dos moléculas con la misma fórmula estructural pero diferente configuración espacial. Vamos a verlo, con el ejemplo del gliceraldehído, un monosacárido de tres carbonos con un grupo aldehído en el carbono primero. Para representar en el plano la molécula de gliceraldehído, se utiliza habitualmente la PROYECCIÓN DE FISCHER, en la que la cadena carbonada se dispone en vertical y los grupos unidos a los carbonos asimétricos se sitúan a la derecha y a la izquierda de estos.
Biología 2º Bachillerato
4
Tema 1. La base físico-química de la vida.
Los dos estéreo isómeros del gliceraldehído se representan de la forma siguiente según la proyección de Fischer:
Cada uno de los estereoisómeros del gliceraldehído recibe un nombre distinto, de manera que se pueden distinguir dos formas espaciales: Forma D: en la que el grupo –OH del carbono asimétrico está situado hacia la derecha. Se denomina D-gliceraldehído. Forma L: en la que el grupo –OH del carbono asimétrico está situado hacia la izquierda. Se denomina L-gliceraldehído. Pero, la mayoría de los monosacáridos llevan más de un carbono asimétrico, por lo que el número de isómeros espaciales o estereoisómeros de cada sustancia es mayor de dos. Para poder calcular el número de esteroisómeros posibles de un monosacáridos aplicaremos la fórmula 2n, siendo n el número de carbonos asimétricos. Para todos aquellos monosacáridos que posean más de un carbono asimétrico, se ha establecido, por convenio, que los prefijos D y L se refieran sólo al carbono asimétrico más alejado del grupo carbonilo, es decir, el carbono asimétrico de mayor numeración.
Formas D
Formas L
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
5
Dentro de los estereoisómeros se pueden diferenciar: ■ ENANTIÓMEROS o ENANTIOMORFOS: son imágenes especulares entre sí y no superponibles. Los enantiómeros conservan el mismo nombre, añadiendo la denominación D o L. ■ EPÍMEROS: no son imágenes especulares entre sí y se diferencian en la posición de un grupo –OH diferente al que se toma como referencia para la serie D o L. No conservan el mismo nombre.
Actividad óptica La presencia de carbonos asimétricos determina una importante propiedad de los monosacáridos en disolución: la actividad óptica. Esta es la capacidad que poseen para desviar el plano de polarización de un haz de luz polarizada que atraviesa la disolución. Cuando desvían el plano de polarización a la derecha se denominan dextrógiros y se simboliza con el signo (+). Cuando desvían el plano de polarización a la izquierda se denominan levógiros y se simboliza con el signo (-). Hay que aclarar que no existe relación entre la actividad óptica, dextrógira o levógira , y el carácter D o L de un determinado estereoisómero. Así el D-gliceraldehído o la D-glucosa son dextrógiros, mientras que la D-fructosa es levógira.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
6
2.4. Fórmulas cíclicas Las fórmulas de los monosacáridos en Proyección de Fischer (cadena lineal) son correctas para las triosas y las tetrosas. Sin embargo, en el caso de las aldopentosas y las hexosas, no explican algunas de sus propiedades en disolución. Esto es debido a que estos monosacáridos adoptan estructuras cíclicas de forma pentagonal o hexagonal, la denominada proyección de Haworth. Estas formas cíclicas se originan al reaccionar el grupo carbonilo con uno de los grupos hidroxilo. Se obtiene así un enlace hemiacetal (en las aldosas) o hemicetal (en las cetosas). Este enlace no implica pérdida ni ganancia de átomos, sino una reorganización de los mismos. Las formas cíclicas resultantes pueden tener forma pentagonal, denominados los monosacáridos furanosas o hexagonal llamándose piranosas. Como resultado de la ciclación, el carbono del grupo carbonilo (llamado ahora carbono anomérico), pasa a ser asimétrico y, por tanto se originan dos nuevos estereoisómeros, denominados ANÓMEROS: Anómero alfa (): el –OH del carbono anomérico queda por debajo del plano, en posición TRANS (distinto lado) respecto al –CH2OH unido al penúltimo carbono. Anómero beta (): el –OH del carbono anomérico queda por debajo del plano, en posición CIS (mismo lado) respecto al –CH2OH unido al penúltimo carbono. La conformación real de los monosacáridos en disolución varía con respecto a la propuesta por Haworth, ya que, debido a la presencia de enlaces covalentes sencillos, las moléculas no pueden ser planas, adoptando una configuración en silla y en bote (figura 7). La configuración en silla es más estable porque existen menos repulsiones electrostáticas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
7
2.5. Importancia biológica de los monosacáridos Los monosacáridos tienen una gran interés, por ser los monómeros constituyentes de todos los glúcidos. También se presentan libres y actúan como nutrientes de las células para la obtención de energía, o como metabolitos intermediarios de importantes procesos biológicos, como la respiración o la fotosíntesis. Los monosacáridos más importantes son: Triosas: son el D-gliceraldehído y la dihidroxiacetona. Su importancia radica en que son compuestos intermediarios del metabolismo de la glucosa y otros glúcidos. Tetrosas: destaca la D-eritrosa, que es un compuesto intermediario de la fotosíntesis. Pentosas: D-ribosa: es un componente de nucleótidos en estado libre, como el ATP y, de ácidos nucleicos, como el ácido ribonucleico (ARN). D-desoxirribosa: se encuentra en el ácido desoxirribonucleico (ADN). D-ribulosa: actúa como intermediario activo en la fijación del CO2 atmosférico en la fotosíntesis. Hexosas: D-glucosa: también llamada azúcar de la uva. Es la molécula energética más utilizada por los seres vivos. Se localiza en estado libre en el citoplasma celular, en el plasma sanguíneo (en concentraciones constantes) y en algunos frutos, como las uvas o los dátiles. Constituye asimismo, la unidad componente de los polisacáridos más comunes (almidón, glucógeno y celulosa). D-galactosa: forma parte de la lactosa (disacárido de la leche), de polisacáridos complejos y de heterósidos. D-fructosa: se encuentra libre en las frutas o unido a la glucosa formando el disacárido sacarosa. Se encuentra en el semen como nutriente de los espermatozoides. Las células hepáticas la transforman en glucosa, por lo que tiene un valor nutritivo equivalente.
3. ENLACE O-GLUCOSÍDICO Los monosacáridos se pueden unir entre sí para formar otros glúcidos más complejos. Esta unión se lleva a cabo al reaccionar dos grupos hidroxilo (-OH) de dos moléculas distintas. Se produce entonces la liberación de una molécula de agua y la unión de los dos monosacáridos por el oxígeno de uno de los grupos hidroxilo implicados. El enlace así creado se denomina O-glucosídico.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
8
4. DISACÁRIDOS
Los disacáridos están formados por la unión de dos monosacáridos mediante un enlace O-glucosídico. La unión entre los monosacáridos puede ser de dos tipos: Enlace monocarbonílico: se establece entre dos grupos –OH, en el que uno de ellos pertenece al carbono anomérico. El disacárido resultante tiene poder reductor, ya que le queda un grupo anomérico libre, como a los monosacáridos. El disacárido que se origina puede aparecer en forma o en forma , según el segundo monosacárido tenga una u otra conformación. Ejemplos de este enlace se encuentran en la maltosa, lactosa y celobiosa. Enlace dicarbonílico: se establece cuando los dos grupos –OH implicados en el enlace son anoméricos. El disacárido resultante no tiene carácter reductor, pues no posee grupos –OH anoméricos libres, como sucede en la sacarosa.
Nomenclatura El nombre del disacárido debe indicar claramente los monosacáridos constituyentes y los carbonos que participan en el enlace O-glucosídico. Se siguen las siguientes reglas: 1º. Se escribe el nombre del primer monosacárido, con la terminación –osil. 2º. Se expresa entre paréntesis los carbonos participantes en el enlace, separados por una flecha corta. 3º. Se escribe el nombre del segundo monosacárido, con la terminación –osa, si el enlace es monocarbonílico, o con la terminación –ósido si es dicarbonílico. Sin embargo, normalmente se emplea una denominación más corta, que alude a los productos donde se encuentra. Por ejemplo, la D-galactopiranosil (14) -D-galactopiranosa recibe también el nombre de lactosa, por estar presente en la leche. Propiedades de los disacáridos Los disacáridos presentan las mismas propiedades que los monosacáridos: son solubles en agua, cristalizables, blancos y tienen sabor dulce. Su capacidad reductora está condicionada por la existencia de un grupo anomérico libre. Disacáridos más importantes Maltosa: -D-glucopiranosil (14) -D-glucopiranosa. La maltosa procede de la hidrólisis del almidón y del glucógeno. Se encuentre en las semillas en germinación (como la malta), que comienzan a emplear la reserva de almidón acumulada. La maltosa puede estar constituida por una glucosa y otra (la que emplea su carbono 4 en el enlace O-glucosídico). Esta forma se denomina y esta más estable en las disoluciones que la forma . Lactosa: -D-galactopiranosil (14) -D-glucopiranosa. La lactosa se encuentra libre en la leche y unida a otras moléculas constituyendo algunos glucolípidos. Sacarosa: -D-glucopiranosil (12) -D-fructofuranósido. La sacarosa es el azúcar de consumo habitual, tanto de caña como de remolacha. Es uno de los principales componentes de la savia elaborada. No tiene carácter reductor. Celobiosa:-D-glucopiranosil (14) -D-glucopiranosa. La celobiosa se obtiene de la hidrólisis de la celulosa. En la página siguiente están representadas las fórmulas y los constituyentes de cada uno de estos disacáridos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
9
5. POLISACÁRIDOS Los polisacáridos están formados por largas cadenas de monosacáridos unidos mediante enlaces Oglucosídicos, por lo que se trata de macromoléculas. La formación de los polisacáridos a partir de monosacáridos es un ejemplo de polimerización, en la que se libera una molécula de agua por cada enlace O-glucosídico creado. La rotura de estos enlaces de realiza, pues, por hidrólisis.
Propiedades Al ser macromoléculas, los polisacáridos no se disuelven fácilmente en agua y pueden ser insolubles, como la celulosa, o formar dispersiones coloidales, como el almidón. Además no son cristalinos, ni tienen sabor dulce. Tampoco tienen carácter reductor, ya que no poseen carbonos anoméricos con grupos hidroxilo libres.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
10
Clasificación Según sus componentes se distinguen dos grupos de polisacáridos: Homopolisacáridos: formados por un tipo de monosacáridos. Son los más abundantes en la naturaleza, y desarrollan dos tipos de funciones biológicas: De reserva energética: presentan enlaces de tipo , y se pueden hidrolizar fácilmente liberando los monosacáridos que los componen. Los más importantes son el almidón y el glucógeno. Estructural: presentan enlaces de tipo , que les confieren gran resistencia a la hidrólisis. Los más importantes son la celulosa y la quitina. Heteropolisacáridos: formados por más de un tipo de monosacáridos. Entre ellos se encuentran los peptidoglucanos, pectinas, agar-agar, goma arábiga, ácido hialurónico y heparina.
Homopolisacáridos de reserva Se localizan, generalmente, en forma de grandes gránulos en el citoplasma celular. Los más importantes son el almidón, el glucógeno y los dextranos. Almidón. Es un homopolisacárido de -D-glucopiranosa, formado por dos constituyentes distintos: ▪ Amilosa. Está formada por largas cadenas de -D-glucopiranosa, no ramificadas, en las que las moléculas de glucosa se unen mediante enlaces (14). Las cadenas adoptan formas helicoidales y tienen seis moléculas de glucosa por vuelta. ▪ Amilopectina. Está formada por cadenas de -D-glucopiranosa con enlaces (14), con ramificaciones. En los puntos de ramificación los enlaces son (16). Las ramificaciones están formadas por 12 unidades de glucosa y, aparecen, por término medio, cada 24 a 30 restos del glucosa. El almidón es el polisacárido de reserva en los vegetales y se acumula en los órganos de reserva, como semillas, raíces y tubérculos, en forma de granos en el interior de los amiloplastos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
11
Glucógeno. Constituye el polisacárido de reserva propio de los hongos y de los animales, en los que forma gránulos visibles y abundantes en el hígado y en los músculos estriados. El glucógeno es un polímero de -D-glucopiranosa con una estructura semejante a la amilopectina, aunque con más ramificaciones (aproximadamente, cada ocho o diez moléculas de glucosa), lo que facilita su hodrólisis. Dextranos. Son los polisacáridos de reserva en las bacterias y levaduras y están compuestos por -D-glucopiranosas que dan lugar a cadenas ramificadas, pero las uniones son variadas: (12), (13),…
Homopolisacáridos estructurales Este tipo de polisacáridos tienen enlaces O-glucosídicos de tipo , por lo que son difíciles de hidrolizar, característica que les permite constituir estructuras biológicas resistentes. Destacan entre ellos: Celulosa. Es un polímero lineal de -D-glucopiranosa, con enlaces (14), formado por largas cadenas (en ocasiones de hasta 15.000 glucosas) sin ramificar. La celulosa es el principal componente de las paredes celulares de los tejidos vegetales, siendo el compuesto orgánico más abundante de la biosfera. Se encuentra por tanto, en productos de consumo humano, como el papel, la madera o el algodón. La mayoría de los animales no pueden utilizar la celulosa como nutriente porque carecen del enzima celulasa, que la hidroliza. No obstante, herbívoros e insectos fitófagos (como las termitas) se nutren con celulosa ya que, su aparato digestivo posee microorganismos simbiontes capaces de hidrolizarla. Sin embargo, a pesar de no poderla utilizar como nutriente, la celulosa es necesaria en la dieta humana porque forma parte de la llamada fibra alimentaria: restos de alimentos no digeribles, que pasan al intestino grueso y estimulan los movimientos peristálticos, con lo que se facilita la eliminación de las heces fecales.
Quitina. Es un polímero de N-acetil--Dglucosamina, un derivado de la glucosa. La quitina es una molécula lineal, con enlaces (14), y es el principal componente del esquelete externo de los insectos, crustáceos y de la pared celular de los hongos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
Heteropolisacáridos Por hidrólisis dan lugar a diferentes monosacáridos o derivados de estos. 1. Origen bacteriano: PEPTIDOGLUCANOS o MUREÍNAS Formados por NAG (N-acetil glucosalina) y NAM (N-acetil murámico). Aparecen en la pared bacteriana Destruidos por la lisozima (enzima de la saliva) 2. Origen Vegetal PECTINAS Formados por Metil-D-galacturonato Aparecen en la pared de las células vegetales (manzana, pera, membrillo, ciruela) Al hidratarse formar geles que se aprovechan para fabricar MERMELADAS AGAR-AGAR Formado por galactosa y ácido sulfúrico Se obtiene de las algas rojas Utilizado para preparar medios de cultivo GOMA-ARÁBIGA Formada por galactosa, arabinosa, ácido glucurónico y ramnosa Es segregada por las plantas para cerrar sus heridas Utilizada para fabricar cola 3. Origen Animal (MUCOPOLISACÁRIDOS o PROTEOGLUCANOS ) ÁCIDO HIALURÓNICO: aparece en la sustancia intercelular de tejidos conjuntivos, óseos y cartilaginosos. Abunda en líquido sinovial y humor vítreo. CONDROITINA: aparece en la matriz extracelular del cartílago, córnea y hueso. HEPARINA: aparece en la matriz extracelular de pulmón, hígado, y paredes arteriales. Actúa como anticoagulante (saliva de insectos hematófagos)
6. HETERÓSIDOS Son moléculas formadas por la asociación de glúcidos con otras sustancias NO glucídicas (AGLUCÓN). GLUCOLÍPIDOS: componentes de las membranas celulares GLUCOPROTEÍNAS: Peptidoglucanos Mucopolisacáridos Mucoproteínas: sustancias muy viscosas. Tracto digestivo: lubrican el bolo alimenticio Tracto respiratorio: mucus Glucoproteínas de la sangre: Inmunoglobulinas (Anticuerpos) Glucoproteínas de las membranas celulares: función antigénica OTRAS: Digitalina: utilizada en tratamiento de enfermedades cardiovasculares Estreptomicina: antibiótico Amigdalósidos: hueso de melocotón y albaricoque Antocianósidos: responsables del color de las flores Nucleótidos: derivados de la ribosa y desoxirribosa.
12
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
7. FUNCIONES BIOLÓGICAS DE LOS GLÚCIDOS
13
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
14
8. CARACTERÍSTICAS GENERALES y CLASIFICACIÓN DE LOS LÍPIDOS Los lípidos son un grupo muy heterogéneo de moléculas, tanto en lo que se refiere a su composición química, como a la función que desempeñan. No obstante todos los lípidos comparten una serie de propiedades físicas que permite agruparlos juntos: Básicamente están formados por largas cadenas hidrocarburadas, que pueden estar sustituidas o no por grupos alcohólicos, aminos, fosfatos, etc. No son solubles en agua ni en otros disolventes polares, pero sí lo son en disolventes orgánicos (no polares), como el benceno, éter, acetona, etc. Presentan un aspecto graso, es decir, poseen un brillo característico y son untuosos al tacto. Los lípidos contienen átomos de C, H y O, y algunos también de P y N. Los lípidos desarrollan funciones muy variadas: - Reserva energética: como las grasas. - Estructural: como los lípidos de membrana. - Protectora: como las ceras. - Vitamínica: como las vitaminas liposolubles. - Hormonal: como las hormonas sexuales. Clasificación de los lípidos Dado que los lípidos son un grupo de moléculas tan diverso, su clasificación ofrece cierta dificultad, ya que se pueden aplicar diferentes criterios. La clasificación más aceptada actualmente es la que los divide en dos grupos: lípidos saponificables e insaponificables. Lípidos saponificables: contienen ácidos grasos en su composición, que se liberan por hidrólisis. El término saponificable hace referencia a que al calentarlos en medio alcalino originan jabones. Químicamente son ésteres. Se dividen en dos grupos: ▪ Lípidos simples: incluyen los glicéridos (grasas) y las ceras. Contienen únicamente átomos de C, H y O. ▪ Lípidos complejos: incluyen los fosfoglicéridos y los esfingolípidos. Contienen además de C, H y O, átomos de N y P. Lípidos insaponificables: no contienen ácidos grasos en su composición, por lo que no pueden originar jabones. Comprenden un grupo muy variado de compuestos: terpenos, esteroides y prostaglandinas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
15
9. LOS ÁCIDOS GRASOS Uno de los componentes de los lípidos saponificables son los ácidos grasos. Son ácidos carboxílicos formados por largas cadenas carbonadas, con un número par de carbonos. Los más comunes son los ácidos grasos de 16 a 18 carbonos. En resumen, los ácidos grasos son largas cadenas hidrocarburadas (o hidrocarbonadas) con un grupo carboxilo en el extremo. Pueden ser de dos tipos: Saturados: cuando solo tienen enlaces simples en la cadena, como el ácido palmítico (16 C) y el esteárico (18 C). Insaturados: cuando presentan uno o más dobles enlaces en la cadena, como el ácido oleico, linoleico y araquidónico. Dependiendo del número de dobles enlaces, se distinguen: ▪ Monoinsaturados: presentan un doble enlace. El más importante es el ácido oleico presente en el aceite de oliva, que se representa de forma sistemática como 18:1 9. ▪ Poliinsaturados: presentan más de un doble enlace. Entre ellos se encuentran: ─ Ácido linoleico, de nombre sistemático 18:2 6. Se encuentra presente en el aceite de semillas (girasol, maíz, etc.). ─ Ácido -linolénico, de nombre sistemático 18:3 3. Abunda en los aceites de pescado graso (atún, salmón, sardina,etc.).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
16
Los ácidos grasos que necesitan los mamíferos, los consiguen mediante síntesis metabólica o en la dieta. Sin embargo, existen unos ácidos grasos denominados esenciales, que el organismo no los puede fabricar y por tanto, tiene que incorporarlos necesariamente en la dieta, por lo que en ocasiones se designan con el término vitamina F. En el ser humano son el ácido linoleico, linolénico y araquidónico, y su carencia impide la síntesis de otras moléculas, como las prostaglandinas.
Propiedades de los ácidos grasos A. Propiedades físicas: Son moléculas anfipáticas (del griego amphi, ambos), ya que la cadena carbonada o alifática es apolar, y por lo tanto insoluble en agua (hidrófoba) y, por otra parte, el grupo carboxilo (-COOH) es polar y soluble en agua (hidrófilo). Esto permite que en cada molécula haya una parte soluble en agua, representada por una cabeza, y otra parte insoluble en agua, representada por una cola. Debido a esta característica, al entrar en o con el agua, los ácidos grasos orientan las cabezas polares hacia ella, mientras que las colas apolares se sitúan en la posición opuesta. Esto da lugar a la formación de diferentes estructuras en empalizada, que pueden ser monocapas o bicapas o estructuras esféricas (micelas). ▪ Monocapas: se produce cuando los ácidos grasos se sitúan en la interfase entre el agua y el aire, las colas se sitúan en el medio aéreo (apolar) y las cabezas se introducen dentro del agua. (A) ▪ Micelas: son agrupaciones esféricas que se forman en el agua, en las que en el interior están las colas y en el exterior las cabezas. (B) ▪ Bicapas: son agrupaciones que separan dos medios acuosos, en las que las cabezas se orientan a cada uno de esos medios y las colas se sitúan enfrentadas. (C)
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
17
El punto de fusión de los ácidos grasos aumenta con el tamaño del ácido graso y disminuye con el grado de instauración (dobles enlaces). Esto es debido a que los ácidos grasos saturados presentan cadenas extendidas que se pueden empaquetar mediante interacciones de Van der Waals entre los átomos de las cadenas vecinas. Esto provoca que a temperatura ambiente, los ácidos grasos saturados adquieran una consistencia cérea y se encuentren en estado sólido. Por el contrario, las cadenas insaturadas muestran ángulos que no permiten un empaquetamiento tan fuerte como las saturadas, por lo que las interacciones entre ellas son más débiles y más fáciles de desordenar por efecto del calor. Por esta razón su punto de fusión es más bajo, y a temperatura ambiente son líquidos oleosos.
Propiedades químicas Las propiedades químicas dependen de la presencia del grupo carboxilo, lo que permite la realización de varias reacciones que dan lugar a la formación de ésteres y sales. Forman ésteres mediante una reacción de esterificación. Los ácidos grasos son capaces de formar enlaces éster al reaccionar el grupos carboxilo (-COOH) con los grupos alcohol (-OH) de otras moléculas, con la eliminación de una molécula de agua. Mediante este tipo de reacciones se originan las grasas, ceras y lípidos complejos. La reacción inversa es la hidrólisis del éster, que origina el ácido graso y el alcohol. Formas sales, mediante la reacción de saponificación. Los ácidos grasos reaccionan con álcalis (una base o hidroxilo), y se obtienen las sales correspondientes de los ácidos grasos, denominadas jabones.
La presencia de dobles enlaces facilita la oxidación de los ácidos grasos, sobre todo de los poliinsaturados, lo cual puede conducir a la rotura de sus cadenas con la consiguiente formación de aldehídos volátiles de cadena corta responsables del olor y sabor a rancio. Este proceso de oxidación se contrarresta en los seres vivos con la presencia de vitamina E, que tiene carácter antioxidante.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
18
10. LÍPIDOS SAPONIFICABLES Todos los lípidos saponificables son ésteres formados por la unión de ácidos grasos y un alcohol. Según el tipo de alcohol presente se les clasifica en triglicéridos o grasas, ceras, fosfoglicéridos y esfingolípidos. 10.1. LÍPIDOS SIMPLES SAPONIFICABLES GRASAS (TRIACILGLICÉRIDOS, TRIGLICÉRIDOS) Son moléculas orgánicas abundantes en todos los organismos vivos. Son ésteres del alcohol glicerina (propanotriol) con tres ácidos grasos. Los triglicéridos se forman mediante reacciones de esterificación. Se trata pues de sustancias hidrolizables y en los seres vivos se hidrolizan por acción de unas enzimas llamadas lipasas, separándose los ácidos grasos y la glicerina.
Las grasas se pueden clasificar en varios tipos según diferentes criterios: 1. Según sean los ácidos grasos iguales o distintos: ▪ Grasas simples: si los tres ácidos grasos son iguales. Se nombran con el prefijo tri- seguido del nombre del ácido graso, al que se le añade la terminación –ina. Por ejemplo, la trioleina o aceite de oliva, donde el ácido graso es el ácido oleico. ▪ Grasas mixtas: cuando los ácidos grasos son distintos. Se designan según cuáles sean los ácidos grasos, cambiando la terminación –ico por –oil, indicando su posición y añadiendo la palabra glicérido. 2. Según el punto de fusión, pueden ser: ▪ Líquidas (aceites): con un punto de fusión inferior a 15 ºC, debido a que presentan una mayor proporción de ácidos grasos insaturados, como el aceite de oliva, aceite de girasol o aceites de pescado. Los aceites, a excepción del pescado, predominan en las plantas. ▪ Sólidas (mantecas y sebos): poseen un punto de fusión por encima de 40 ºC, porque en ellas predominan los ácidos grasos saturados. Son la grasa de cerdo, buey, cordero, propias de los animales. ▪ Semisólidas: se encuentran en un punto intermedio, como las mantequillas y las margarinas, que contienen ácidos grasos saturados e insaturados.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
19
3. Según el grado de instauración de los ácidos grasos: ▪ Grasas saturadas: presentan ácidos grasos saturados en su composición. Son las grasas animales presentes en la carne, leche, huevos y el aceite de coco. Son perjudiciales para el organismo, ya que elevan los niveles de colesterol en sangre. ▪ Grasas insaturadas: presentan ácidos grasos insaturados. Son los aceites vegetales (oliva y girasol) y de los pescados azules. Son beneficiosas para la salud ya que disminuyen los niveles de colesterol sanguíneo. Función biológica Las grasas son las moléculas que generan más cantidad de energía: un gramo de grasa metabolizada produce 9 Kcal, más del doble de energía que un gramos de glúcido (3,75 kcal/g). Por esta razón, y debido también a su insolubilidad en agua (lo que permite almacenarlas en grandes cantidades sin afectar a la presión osmótica celular) las grasas constituyen la reserva energética de los seres vivos, sobre todo de los animales, donde se acumulan en el tejido adiposo formando el tocino y las mantecas de las membranas mesentéricas. Si en la dieta se aporta un exceso de glúcidos hasta que se satura la capacidad de almacenamiento del glucógeno, dicho exceso se transforma en grasas, por eso los glúcidos en exceso engordan. Por el contrario, las grasas no podemos transformarlas en glúcidos. Las plantas también almacenan grasas, principalmente en frutos y semillas, pero en ellas la principal reserva de energía es el almidón. Las grasas desempeñan, además, otras funciones y actúan como amortiguadores mecánicos (grasa de la palma de las manos y la planta de los pies), como aislantes térmicos (animales de climas fríos presentan una gruesa capa de grasa debajo de la piel) y como vehículos de transporte de las vitaminas liposolubles (A, D, E y K). CERAS (CÉRIDOS) Las ceras o céridos son moléculas estructurales que se pueden encontrar en algunos animales y, especialmente, en las plantas. Su composición química es simple, ya que son ésteres de un ácido graso de cadena larga y un monoalcohol de cadena larga también. Debido a su elevado grado de insolubilidad, las ceras desempeñan principalmente una función de protección, ya que protegen de la humedad y evitan la pérdida de agua. Aparecen recubriendo la superficie de órganos vegetales paras evitar la evaporación, como frutos y hojas; y en los animales impermeabilizan algunas estructuras tegumentarias, como las plumas de las aves, y la piel y el pelo de los mamíferos. Algunas ceras son la cera de las abejas, la lanolina de la lana y el cerumen de los oídos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
20
10.2 LÍPIDOS COMPLEJOS SAPONIFICABLES Son compuestos de carácter antipático, que forman parte de las membranas celulares, por lo que se conocen también como lípidos de membrana, junto con el colesterol, que es un lípido insaponificable.
FOSFOGLICÉRIDOS Al igual que las grasas, los fosfoglicéridos son ésteres de glicerina con ácidos grasos, pero solo llevan dos ácidos grasos, ya que el tercer alcohol de la glicerina está unido a un ácido ortofosfórico, por eso se denominan también fosfolípidos. La molécula resultante se denomina ácido fosfatídico, igual en todos los fosfoglicéridos. A ella se une un aminoalcohol al ácido ortofosfórico, formando el fosfoglicérido completo. Los fosfoglicéridos se caracterizan por su comportamiento antipático, es decir, presentan una parte polar (y, por tanto, soluble en agua) y otra apolar (insoluble). La zona polar corresponde a la porción donde se sitúa el ácido ortofosfórico y el aminoalcohol, mientras que la zona apolar corresponde al resto de la molécula (ácidos grasos). De esta propiedad deriva su función biológica. Todas las membranas celulares están formadas por una doble capa de fosfolípidos en la que las colas apolares de ambas capas se quedan enfrentadas, mientras que las cabezas polares se orientan hacia el medio externo e interno, ambos acuosos. Según el aminoalcohol presente, se diferencian varias clases de fosfoglicéridos: cefalina (fosfatidiletanolamina) si el aminoalcohol es la etanolamina; lecitina (fosfatidilcolina) si contiene colina y fosfatidilserina si tiene serina.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
21
Comportamiento anfipático de los fosfolípidos y su disposición en las membranas
ESFINGOLÍPIDOS Los esfingolípidos también son componentes de las membranas celulares, y abundan en el tejido nervioso. Al igual que los fosfoglicéridos, tienen carácter antipático. Los esfingolípidos son ésteres formados por la unión del alcohol esfingosina y un ácido graso mediante un enlace amida, que da lugar a una molécula denominada ceramida, a la que se une una molécula polar para constituir el esfingolípido completo. Según la naturaleza de la molécula polar que se une a la ceramida se distinguen dos clases de esfingolípidos: Esfingolmielinas. Presentan una molécula de fosforilcolina o fosforiletanolamina unida a la ceramida. Son abundantes en las vainas de mielina que rodean los axones neuronales. Glucoesfingolípidos. Su molécula polar es un glúcido. Estas moléculas desempeñan un papel fundamental como antígenos celulares, es decir, moléculas identificativas de células concretas que permiten el reconocimiento entre ellas. Los antígenos se relacionan con múltiples procesos, principalmente inmunitarios. Se diferencian dos tipos: Cerebrósidos: si el glúcido es un monosacárido (frecuentemente galactosa). Gangliósidos: si el glúcido es un oligosacárido.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
22
11. LÍPIDOS INSAPONIFICABLES Se incluyen en este grupo los lípidos que no contienen ácidos grasos en su composición (tampoco son ésteres) y, por tanto, no pueden formar jabones mediante reacciones de saponificación. Aunque aparecen en menor cantidad que los lípidos saponificables, este grupo comprende algunos compuestos biológicamente muy activos que desempeñan importantes funciones. Se distinguen tres tipos de lípidos insaponificables: terpenos, esteroides y prostaglandinas.
TERPENOS Químicamente, los terpenos son polímeros de la molécula de isopreno (2-metil-1,3-butadieno), por lo que también se les denomina lípidos isoprenoides. Estas moléculas se encuentran en las plantas.
Según el número de isoprenos que componen el terpeno se clasifican en: ▪ Monoterpenos. Contienen dos moléculas de isopreno. Este grupo comprende compuestos volátiles responsables de ciertos aromas (mentol, alcanfor, geraniol,…) ▪ Diterpenos. Están formados por la unión de cuatro isoprenos. El fitol, componente de la clorofila, se incluye en este grupo. ▪ Triterpenos. Formados por seis moléculas de isopreno. Entre ellos se encuentra el escaleno, un precursor del colesterol. ▪ Tetraterpenos. Formados por la unión de ocho moléculas de isopreno. Destacan en este grupo los carotenoides, pigmentos que participan en la fotosíntesis absorbiendo energía lumínica de longitudes de onda distintas a la que absorbe la clorofila. Entre los carotenoides más importantes se encuentran la xantofila (amarilla), el licopeno (rojo) y el -caroteno (anaranjado). El -caroteno es también un precursor de la vitamina A, ya que la rotura del enlace central del -caroteno origina dos moléculas de esta vitamina, que interviene en la visión y protege los tejidos epiteliales. Politerpenos. Formados por muchas moléculas de isopreno. El caucho es el politerpeno más importante y se encuentra en el látex del árbol Hevea brasilensis (árbol del caucho).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
23
ESTEROIDES Constituyen un grupo de lípidos muy importante, que derivan del esterano o ciclopentano perhidrofenantreno (F). Este compuesto cíclico está formado por tres anillos de ciclohexano y uno de ciclo pentano, en donde se unen diferentes radicales.
Los esteroides son sustancias muy abundantes y desempeñan funciones muy variadas. Se diferencian en la existencia de dobles enlaces y en la presencia de diferentes sustituyentes en algunas posiciones. En los siguientes cuadros se exponen los esteroides más importantes y sus funciones.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
24
PROSTAGLANDINAS Las prostaglandinas son lípidos presentes en la mayor parte de los tejidos animales. Se forman por la ciclación de ácidos grasos poliinsaturados, como el ácido araquidónico. Todas estas moléculas poseen una estructura química semejante. Se consideran hormonas locales, ya que actúan en las células que las sintetizan y en la adyacentes. Las funciones de las prostaglandinas son muy variadas: - Estimulan la agregación de plaquetas. - Activan las respuestas inflamatorias de los tejidos al iniciar la vasodilatación de los capilares. - Provocan la subida de la temperatura corporal(fiebre). - Controlan el descenso de la presión arterial al favorecer la eliminación de sustancias en el riñón. - Intervienen el la contracción del útero durante el parto. - Disminuyen la secreción de jugos gástricos. - Regulan la secreción de mucus protector del tracto digestivo (estómago e intestino). Además de las prostaglandinas, existen otros compuestos químicamente relacionados con ellas. Son los tromboxanos y los leucotrienos, que tienen funciones fisiológicas variadas entre las cuales destacan las respuestas inflamatorias. Prostaglandinas, tromboxanos y leucotrienos son conocidos como eicosanoides, por ser moléculas derivadas de ácidos grasos poliinsaturados de 20 átomos de carbono (eicosa=veinte).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
12. FUNCIONES BIOLÓGICAS DE LOS LÍPIDOS
25
DE LA ACEITUNA AL ACEITE La recogida Tiene lugar entre los meses de octubre y enero, en función de la maduración que se desee y del clima de la región. Cuanto mayor sea la madurez de la oliva, más intenso será el sabor y el aroma del aceite. La recogida debe realizarse de la forma que dañe menos el fruto. Las aceitunas que cayeron solas al madurar suelen estar un poco estropeadas y producen peores aceites.
El lavado y almacenaje Las aceitunas se lavan, con el fin de eliminar las sustancias extrañas que pudieran contaminar el aceite y transmitir sabores extraños. Si se almacenan temporalmente, las aceitunas necesitan estar ventiladas para evitar su fermentación.
La selección Una vez en la almazara, la aceituna se clasifica según su estado y su destino.
El prensado 1 , batido 2 y centrifugado 3 La pasta se prensa (así se extrae aceite en frío, aunque en una cantidad mínima), luego se calienta moderadamente (con resistencias) y, por último, se centrifuga hasta obtener los diferentes aceites de oliva virgen.
La molturación Las aceitunas se trituran hasta formar una pasta que se recoge en unos moldes circulares.
Orujo Es el residuo de los huesos y las pieles de aceituna, que todavía contiene cierta cantidad de aceite que se extrae por medio de disolventes. Una vez eliminados y refinado se mezcla con aceite de oliva virgen y se comercializa como aceite de orujo de oliva.
1 2 Aceite de oliva virgen Es el que se obtiene de la aceituna por medios físicos, sin ayuda de disolventes. Según su calidad se clasifica en:
A
3 Aceite lampante No es apto para el consumo. Presenta una excesiva acidez (superior a 3,3º) y necesita ser refinado.
B
Apto para el consumo
A
Aceite de oliva virgen extra Tiene que tener una acidez inferior a 0,8º y una determinada puntuación en la cata Nuestro de expertos. análisis
Apto para el consumo
Refinado Durante el proceso el aceite pierde su acidez, aroma, sabor y color característicos. Aceite de oliva refinado
B
Aceite de oliva virgen Acidez máxima de 2º y una puntuación en la cata menor que el extra.
Aceite de oliva Es la mezcla de aceite de oliva refinado y aceites de oliva virgen, que le aportan su acidez y su sabor (más intenso cuanto mayor es la proporción de aceite virgen).
OCU-COMPRA MAESTRA 319 OCTUBRE 2007
11
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte II: glúcidos y lípidos
1
ACTIVIDADES TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA. PARTE II: GLÚCIDOS y LÍPIDOS GLÚCIDOS o HIDRATOS DE CARBONO 1. Define químicamente un glúcido e indica con qué otros nombres se conocen. ¿Porqué?. 2. ¿Qué diferencia existe entre osa y ósido?. ¿Y entre holósido y heterósido?. 3. ¿Qué se entiende por hidrólisis de un compuesto?. ¿Porqué los disacáridos y polisacáridos son moléculas hidrolizables?. 4. ¿Cuantos estereoisómeros existen en una aldohexosa?. ¿Y en una aldopentosa?. 5. Construye las fórmulas de los epímeros de la D-Fructosa. 6. Se puede deducir se la D-eritrosa es levógira o dextrógira?. 7. Dibuja todos los pasos de la ciclación de una D-galactosa hasta llegar a la siguiente sustancia: α-DGalactopiranosa. 8. La diabetes es una enfermedad hormonal ocasionada por un mal funcionamiento de páncreas endocrino, que no produce insulina. Esta hormona es responsable, entre otras cosas, de facilitar el paso de glucosa a través de la membrana celular. ¿Qué efectos puede producir la ausencia de glucosa en las células?. 9. Algunos disacáridos de interés biológico son la maltosa, sacarosa y lactosa. Fíjandote en sus fórmulas contesta a las siguientes cuestiones: a) b) c) d) e) f) g)
¿De qué monómeros está formado cada uno de estos disacáridos?. ¿Qué carbonos intervienen en la formación del enlace glucosídico en cada caso?. ¿Son anoméricos o no?. ¿Cuáles son los grupos funcionales implicados en la formación del enlace glucosídico?. ¿Qué se desprende?. ¿Su formación ha liberado o consumido energía?. ¿Cuáles de estos disacáridos son reductores?. ¿Porqué?.
10. ¿Porqué el almidón, celulosa y glucógeno son polisacáridos diferentes si todos están formados por moléculas de D-glucopiranosa?. 11. Porqué la glucosa se almacena en forma de almidón en los vegetales, en vez de estar libre en la célula. 12. ¿Porqué la celulosa no es un nutriente?. ¿Cuál es su importancia en la alimentación?. 13. Habrás visto en anuncios publicitarios papillas infantiles compuestas a base de cereales dextrinados. ¿Qué significa esto?. ¿Qué beneficio ofrece a los bebés?. 14. ¿Cuál es la importancia biológica de los siguientes glúcidos: celulosa, ribulosa, lactosa, galactosa, quitina, gliceraldehido y N-acetil-glucosamina?.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte II: glúcidos y lípidos
2
LÍPIDOS 15. ¿Cuál es característica fundamental de los lípidos, que permite reunirlos en un grupo y cuál es la que diferencia entre los dos grupos principales?. 16. Señala a qué tipo de lípido son estas sustancias: ácido cólico, aceite, gangliósido, aldosterona, xantofila, cera, progesterona, esfingomielina y vitamina A. 17. ¿De qué depende que los ácidos grasos sean sólidos o líquidos?. ¿A qué se denominan ácidos grasos esenciales y qué importancia tienen?. 18. Completa las siguientes reacciones, indicando el tipo de compuesto que se origina: O a) CH3-(CH2)10-C-O-CH2 O I CH3-(CH2)10-C-O-CH O I CH3-(CH2)10-C-O-CH2
+ 3 NaOH →
b) Ácido linoleico + 4 O2 → 19. Cómo forman los jabones emulsiones estables con las grasas. ¿Qué sustancias hay en nuestro organismo que también emulsionan las grasas?. Busca en alguna enciclopedia cómo se fabrica el jabón casero. 20. ¿Porqué las grasas son reservas de energía a largo plazo?. ¿Qué las diferencia de las ceras?. 21. Cuáles de las siguientes moléculas son anfipáticas: Colesterol, vitamina A, ácido lignocérico, triacilglicérido, cefalina. 22. ¿Porqué los lípidos saponificables simples son muy insolubles en agua mientras que los lípidos saponificables complejos son algo solubles?. 23. Las vitaminas liposolubles A, E y K son terpenos compuestos por 5 unidades de isopreno. ¿Porqué crees que las industrias lácteas añaden estas vitaminas a la leche desnatada?. 24. Porqué la aspirina es antipirética, antiinflamatoria y analgésica. Porqué la aspirina y otros antiinflamatorios pueden provocar la aparición de ulceras gastroduodenales. 25. Define los conceptos de: lípido, anfipático, jabón, hidrófobo, esterificación, manteca, micela, emulsión y polar. 26. Lee el artículo “Relación del colesterol con el tipo de dieta”, y responde a las cuestiones que se plantean.
Biología 2º Bachillerato
GLÚCIDOS EJERCICIO TIPO DE ISOMERÍA ESPACIAL EN MONOSACÁRIDOS A partir de las siguientes fórmulas de monosacáridos, se pide: 1. Señalar los carbonos asimétricos presentes. 2. Calcular el número de isómeros espaciales o estereoisómeros posibles de cada uno de ellos. 3. Indicar si pertenecen a la serie D o L 4. Formular y nombrar los enantiómeros de cada uno de ellos. 5. Formular y nombrar un epímero de cada uno de ellos. 6. Formular y nombrar los anómeros de cada uno de ellos.
CHO H C OH HO C H HO C H H C OH CH2OH GALACTOSA
CH2OH C= O H C OH HO C H H C OH CH2OH SORBOSA
Biología 2º Bachillerato
Actividades refuerzo
1
MONOSACÁRIDOS. ACTIVIDADES ISOMERÍA ESPACIAL 1. Señala los CARBONOS ASIMÉTRICOS y calcula el NÚMERO DE ESTEREOISÓMEROS posibles de cada uno de los siguientes monosacáridos.
2. Escribe la fórmula de los ENANTIÓMEROS de los siguientes monosacáridos: D-eritrulosa; D-idosa; L-ribulosa: L-arabinosa y D-sedoheptulosa. 3. Qué monosacáridos del ejercicio 1 son EPÍMEROS de los siguientes:
Biología 2º Bachillerato
Actividades refuerzo
2
4. Señala en las siguientes fórmulas, cuáles son ANOMÉROS y .
5. ¿Existen ANÓMEROS y de los siguientes monosacáridos?. Justifica la respuesta. D-lixosa; D-sicosa; D-ribulosa; D-gliceraldehído; L-idosa. 6. Dibuja las fórmulas de los ANÓMEROS y de cada uno de los siguientes monosacáridos, y nombra cada uno de ellos según su estructura cíclica.
BIOLOGÍA 2º BACHILLERATO LÍPIDOS. ACTIVIDAD TIPO DE REACCIONES QUÍMICAS.
Completa las siguientes reacciones químicas, escribiendo: Fórmulas y tipos de productos resultantes Tipo de reacción química llevada a cabo a)
CH3- (CH2)18-COOH + HO-CH3 → ácido araquídico
b)
metanol
CH3- (CH2)7-CH=CH-(CH2)7-COOH + NaOH → ácido oleico
c)
CH3-(CH2)5-CH=CH-(CH2)7-COOH + 2 O2 → ácido palmitoleico
+
d)
ácidos grasos
e)
→
glicerina
+ NaOH →
triglicérido
f)
+ 3 H2O →
triglicérido
TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA PARTE III. PROTEÍNAS y ÁCIDOS NUCLEICOS 1. PROTEÍNAS y ÁCIDOS NUCLEICOS: BIOPOLÍMEROS PORTADORES DE LA INFORMACIÓN GENÉTICA 2. PROTEÍNAS: CONCEPTO, FUNCIONES y CLASIFICACIÓN 3. LOS AMINOÁCIDOS
▪ ▪
Clasificación
Propiedades de los aminoácidos
4. EL ENLACE PEPTÍDICO 5. ESTRUCTURA DE LAS PROTEÍNAS ▪ ▪ ▪ ▪
Estructura primaria Estructura secundaria Estructura terciaria Estructura cuaternaria
6. PROPIEDADES DE LAS PROTEÍNAS ▪ ▪ ▪
Solubilidad Especificidad Desnaturalización
7. CLASIFICACIÓN DE LAS PROTEÍNAS 8. FUNCIONES BIOLÓGICAS DE LAS PROTEÍNAS 9. LOS ÁCIDOS NUCLEICOS: CONCEPTO, TIPOS y FUNCIONES. 10. LOS NUCLEÓTIDOS: COMPONENTES DE LOS ÁCIDOS NUCLEICOS 11. FUNCIONES DE LOS NUCLEÓTIDOS 12. POLINUCLEÓTIDOS 13. ÁCIDO DESOXIRRIBONUCLEICO (ADN) 13.1. ESTRUCTURA DEL ADN. Modelo de la doble hélice 13.2. TIPOS DE ADN
13.3. DESNATURALIZACIÓN e HIBRIDACIÓN DEL ADN
14. ÁCIDO RIBONUCLEICO (ARN) ▪ ARN mensajero (ARNm) ▪ ARN ribosómico (ARNr) ▪
ARN de transferencia o ARN transferente (ARNt)
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
2
1. PROTEÍNAS y ÁCIDOS NUCLEICOS: BIOPOLÍMEROS PORTADORES DE LA INFORMACIÓN GENÉTICA Las proteínas y los ácidos nucleicos son biomoléculas que presentan una serie de características comunes, que conviene resaltar antes de empezar su estudio por separado. Proteínas y ácidos nucleicos son biopolímeros o macromoléculas, formadas por la unión mediante enlaces covalentes de moléculas más sencillas (monómeros). Las proteínas se forman por la polimerización de aminoácidos y las ácidos nucleicos por la polimerización de nucleótidos. En las proteínas y en los ácidos nucleicos, el ordenamiento o la secuencia de los monómeros (aminoácidos y nucleótidos) es característico y particular de las distintas cadenas moleculares de las proteínas y de los ácidos nucleicos, y es el que determina su función biológica. El ordenamiento de los monómeros no es arbitrario. En los ácidos nucleicos existe unas instrucciones almacenadas en forma de secuencias de nucleótidos que deciden el ordenamiento de los aminoácidos de las proteínas. Por esta razón, los ácidos nucleicos y las proteínas son biopolímeros portadores de la información genética, ya que el ordenamiento de sus monómeros no obedece al azar, sino a instrucciones heredadas de nuestros antecesores a lo largo del proceso evolutivo. En la célula la información genética contenida en los ácidos nucleicos se utiliza para fabricar proteínas.
2. PROTEÍNAS: CONCEPTO, FUNCIONES y CLASIFICACIÓN Las proteínas son biomoléculas orgánicas formadas, al menos, por cuatro bioelementos: C, H, O y N; pero muchas de ellas contienen S, P y otros bioelementos (Fe, Cu, I, Mg, etc.,…). Químicamente las proteínas son polímeros de moléculas relativamente sencillas, no hidrolizables, denominadas aminoácidos (aa). La unión de aminoácidos origina péptidos, que según su tamaño molecular pueden ser: Oligopéptidos: formados por no más de 10 aminoácidos. Polipéptidos: formados por más de 10 aminoácidos. Las proteínas son polipéptidos, formados por más de 50 aminoácidos o con un peso molecular mayor de 5.000 daltons, normalmente entre 6.000 y 106 daltons, por lo que se trata de macromoléculas. Las proteínas se clasifican en dos grandes grupos: ▪ Holoproteínas: formadas exclusivamente por aminoácidos. ▪ Heteroproteínas: formadas por aminoácidos más otros componentes no proteicos. La parte no proteica se la designa como el grupo prostético, y dependiendo de su naturaleza química se pueden diferenciar: Glucoproteínas: el grupo prostético es un glúcido. Lipoproteínas: el grupo prostético es un lípido. Fosfoproteínas: el grupo prostético es un ácido fosfórico. Nucleoproteínas: cuando contienen nucleótidos. Cromoproteínas: si el grupo prostético es un pigmento. Las proteínas son los compuestos orgánicos más abundantes de la materia viva, constituyendo alrededor del 50% de su peso seco. Las funciones que desempeñan son muy variadas: Estructural: las proteínas son el principal material de construcción de los seres vivos, formando parte de casi todas sus estructuras: desde la membrana celular hasta ser el principal componente del tejido conjuntivo (colágeno), el pelo o las uñas (queratina). Enzimática: las reacciones metabólicas están catalizadas y controladas por unas proteínas, denominadas enzimas. Inmunológica: los anticuerpos, que intervienen en la defensa del organismo frente a los agentes patógenos, son proteínas. Hormonal: algunas hormonas, como la insulina y el glucagón, que regulan la concentración de glucosa en sangre, son proteínas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
3
Transporte: pueden transportar gases, como la hemoglobina que transporta el oxígeno, o lípidos, como las lipoproteínas de la sangre. Movimiento: las proteínas son elementos esenciales en el movimiento muscular, ya que la actina y la miosina de las células musculares, son las responsables de la contracción de los músculos. De reserva: algunas proteínas sirve de reserva de aminoácidos durante el desarrollo biológico, como la ovoalbúmina del huevo, la caseína de la leche o la gliadina del trigo. Homeostática: ciertas proteínas mantienen el equilibrio osmótico del medio celular y extracelular.
3. LOS AMINOÁCIDOS Los aminoácidos son los componentes de las proteínas. Químicamente son ácidos orgánicos que presentan un grupo amino (-NH2), un grupo carboxilo (-COOH) y un átomo de hidrógeno (H) unidos covalentemente a un carbono central, que se designa como carbono . El enlace que le queda al carbono está ocupado por un grupo lateral o un grupo R (de radical) que varía en los distintos aminoácidos. Existen 20 aminoácidos proteicos o -aminoácidos, que son los constituyentes básicos de las proteínas. Además, hay otros 150 aminoácidos que se encuentran libres o combinados en las células y en los tejidos, pero que no se encuentran en las proteínas, y se conocen como aminoácidos no proteicos. Algunos de ellos son intermediarios de las reacciones metabólicas (citrulina y ornitina) o forman parte de las paredes bacterianas, como el ácido-D-glutámico.
Clasificación Los aminoácidos se clasifican atendiendo a las características de su grupo radical, según su ionización, polaridad y reactividad, en: ▪ Neutros polares: no tienen carga eléctrica neta, y su grupo R contiene grupos polares (alcohol, tiol o amida), por lo que son solubles en agua. ▪ Neutros apolares: no tienen carga eléctrica neta, y su grupo R está formado por largas cadenas hidrocarbonadas, lo que hace que sean poco solubles en agua. ▪ Ácidos: cuando el grupo R lleva un grupo ácido, de manera que a pH neutro, tienen carga negativa. ▪ Básicos: cuando el grupo R lleva un grupo básico (amino), de tal modo que a pH neutro, tienen carga eléctrica positiva. La mayoría de los aminoácidos pueden sintetizarse unos a partir de otros, pero algunos no pueden ser sintetizados y deben obtenerse de la dieta, son los denominados aminoácidos esenciales. Los aminoácidos esenciales son diferentes para cada especie. En la especie humana los aminoácidos esenciales son diez: Thr, Lys, Arg, His, Val, Leu, Ile, Met, Phe y Trp.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
4
PROPIEDADES DE LOS AMINOÁCIDOS Las propiedades de los aminoácidos están determinadas por el radical, que es distinto en cada aminoácido, y determina sus propiedades físicas y químicas. Los aminoácidos son sólidos, solubles en agua (excepto los hidrófobos), cristalizables, incoloros o poco coloreados y con un punto de fusión alto, por encima de 200 º C. Además de las propiedades mencionadas, hay dos propiedades que conviene destacar: Estereoisomería y actividad óptica: al igual que los monosacáridos, los aminoácidos poseen al menos un carbono asimétrico, que es el carbono , excepto la glicina que no tiene ninguno. Debido a esto, los aminoácidos presentan estereoisomería y actividad óptica. Los aminoácidos pueden presentar dos configuraciones espaciales, D y L, dependiendo de la posición del grupo amino (-NH2), a la derecha e izquierda, respectivamente del carbono . Estas dos configuraciones espaciales se denominan estereoisómeros. Ambos estereisómeros son imágenes especulares y no superponibles. Todos los aminoácidos proteicos son de la serie L, pues las células los sintetizan utilizando enzimas estereoespecíficas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
5
Los aminoácidos muestran, además, actividad óptica, denominándose dextrógiros (+) o levógiros (-), según desvíen la luz polarizada hacia la derecha o hacia la izquierda. De la misma forma que los glúcidos, la disposición D o L es independiente de la actividad óptica: un L-aminoácido puede ser dextrógiro o levógiro. Carácter anfótero: la presencia de los grupos carboxilo y amino confiere a los aminoácidos un comportamiento ácido-base o comportamiento anfótero, que significa que se comportan como ácidos o bases dependiendo el pH del medio acuoso en el que estén disueltos. Cuando los aminoácidos se encuentran disueltos en agua (pH=7) los grupos amino aceptan protones, comportándose como bases, y quedan cargados positivamente (NH3+) y los grupos carboxilo, desprenden protones, comportándose como ácidos, y quedan cargados negativamente (COO-), por lo que los aminoácidos están doblemente ionizados y forman iones híbridos, que se denominan formas dipolares o zwitteriones, y poseen igual número de cargas positivas y negativas. El valor del pH en el que un aminoácido tiende a adoptar la forma dipolar neutra se denomina punto isoeléctrico, y es diferente para cada aminoácido. Cuando el valor del pH del medio se desvía del punto isoeléctrico, el aminoácido se comportará como ácido o base (en medio ácido como base y en medio alcalino como ácido), permitiendo la regulación del pH.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
6
4. EL ENLACE PEPTÍDICO Los aminoácidos se pueden unir entre sí mediante el denominado enlace peptídico (un enlace amida de tipo covalente). El enlace peptídico se establece entre el grupo carboxilo (-COOH) de un aminoácido y el grupo amino (-NH2) de otro, liberándose una molécula de agua. La unión de dos aminoácidos origina un compuesto que denominamos dipéptido.
Los átomos de C, N y O que forman parte del enlace comparten electrones, lo que hace que aparezcan dos formas resonantes. Se puede así afirmar, que el enlace peptídico tiene un carácter parcial de doble enlace. Este hecho impide que se efectúen torsiones alrededor del enlace peptídico, lo que determina que los átomos de C, N y O se sitúen en el mismo plano. Solamente se pueden efectuar torsiones alrededor en los carbonos . El dipéptido presenta un grupo amino y un grupo carboxilo libres, los cuales pueden unirse a otros aminoácidos, y así sucesivamente. De esta forma se originan cadenas de aminoácidos (cadenas peptídicas), de longitud variable, que según el número de aminoácidos se denominan tripéptidos, tetrapéptidos, etc., hasta polipéptidos. El resultado es que la cadena peptídica presenta una forma más o menos en zig-zag. En los enlaces peptídicos no participan los radicales de los aminoácidos, que quedan “colgando” de la cadena peptídica.
Biología 2º Bachillerato
7
Tema 1. La base físico-química de la vida.
Por convenio, el extremo amino se considera el comienzo de la cadena peptídico y el grupo carboxilo el final. amino →
← carboxilo
Como al establecer cada enlace peptídico se libera una molécula de agua, también será posible la reacción contraria; es decir, la ruptura de dichos enlaces por acción de agua; los péptidos son polímeros hidrolizables y su hidrólisis total origina aminoácidos.
5. ESTRUCTURA DE LAS PROTEÍNAS Cada proteína está compuesta por una o varias cadenas polipeptídicas y, aunque solo hay 20 aminoácidos, en cada célula existen miles de proteínas distintas con funciones características. Las cadenas polipeptídicas no son moléculas lineales, sino que se pliegan en el espacio y adquieren una forma característica, que determina su función biológica. La conformación o la estructura de una proteína es la disposición espacial que adoptan las cadenas polipeptídicas. La compleja estructura de las proteínas puede estudiarse en diferentes niveles de complejidad, conocidos como estructura primaria, secundaria, terciaria y cuaternaria. Cada nivel informa de la disposición espacial del nivel anterior. ESTRUCTURA PRIMARIA La estructura primaria de una proteína es la secuencia de aminoácidos de la cadena polipeptídica, es decir, el número, tipo y orden de los aminoácidos que constituyen la proteína. La secuencia de aminoácidos es diferente en cada proteína y determina la conformación tridimensional de la proteína y, por tanto, su función biológica. Siempre existe un extremo con un aminoácido cuyo grupo amino está libre y otro extremo con un aminoácido con un grupo carboxilo libre. Por convenio, lo aminoácidos se numeran comenzando por el que posee el extremo amino libre.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
8
ESTRUCTURA SECUNDARIA La estructura secundaria de una proteína es la forma en que la secuencia de aminoácidos se pliega en el espacio. A medida que los aminoácidos se van uniendo para formar la cadena polipeptídica, giran y adoptan una disposición espacial lo más estable posible, que es la estructura secundaria. Existen dos tipos básicos de estructura secundaria: -hélice y la lámina plegada o lámina . En las proteínas coexisten ambos, aunque uno de ellos puede predominar sobre el otro. Estructura en -hélice: el nombre alude a la -queratina, proteína muy abundante en las células de la epidermis. La estructura en -hélice se produce cuando una cadena polipeptídica gira sobre sí misma, de manera que la molécula adopta una disposición en hélice, donde los radicales se sitúan hacia el exterior. La -hélice se mantiene estable gracias a la formación de puentes de hidrógeno entre los grupos –NH y –CO de los enlaces peptídicos que quedan enfrentados. Si los puentes de hidrógeno se rompen, la estructura secundaria se pierde.
Lámina plegada o lámina : este tipo de estructura está presente en la -queratina, presente en uñas, pelos y plumas. Las cadenas polipeptídicas se disponen en paralelo y se pliegan formando una especie de fuelle o lámina plegada en zigzag, quedando unidas transversalmente mediante puentes de hidrógeno análogos a los que estabilizan la -hélice. Las cadenas laterales de los aminoácidos se disponen alternativamente por encima y debajo de la lámina plegada.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
9
ESTRUCTURA TERCIARIA Las proteínas no se disponen linealmente en el espacio, sino que sufren nuevos plegamientos que hacen que la molécula adopte una disposición espacial tridimensional estable denominada estructura terciaria. La estructura terciaria se mantiene estable gracias a la formación de diferentes enlaces entre los radicales de los aminoácidos, que pueden ser: Puentes disulfuro: son enlaces covalente fuertes entre dos grupos –SH pertenecientes de dos moléculas de cisteina. Fuerzas electrostáticas: son enlaces de tipo iónica entre grupos con cargas eléctricas opuestas. Puentes de hidrógeno: se establecen entre grupos polares no iónicos en los que existen cargas parciales en su cadena lateral. Fuerzas de Van der Waals e interacciones hidrofóbicas: son las uniones más débiles y se producen entre aminoácidos polares. En general, existen dos tipos de estructuras terciarias en las proteínas: Globulares: poseen un alto grado de plegamiento y dan lugar a estructuras con forma de esfera. Las proteínas globulares suelen ser solubles en agua y presentan funciones enzimáticas, de transporte u hormonales. Las proteínas globulares suelen tener diferentes fragmentos con -hélice y láminas , pero las disposiciones suelen disponerse en la periferia y las hélices en el centro de la molécula. Además, las proteínas globulares se doblan de tal manera que, en solución acuosa, los restos hidrófilos quedan hacia el exterior y los hidrófobos hacia el interior y, por el contrario, en un ambiente lipídico, los restos hidrófilos quedan en el interior y los hidrófobos en el exterior. Filamentosas: el plegamiento de la cadena polipeptídica es menor, por lo que estas estructuras presentan formas alargadas. Las proteínas filamentosas son insolubles en agua y disoluciones salinas y suelen tener función estructural, como la queratina, el colágeno o la elastina.
Proteína filamentosa
Proteína globular
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
10
ESTRUCTURA CUATERNARIA Cuando una proteína está formada por varias cadenas polipeptídicas, adquiere un nivel estructural superior, la estructura cuaternaria. Cada cadena polipeptídica es una subunidad de la proteína o protómero, y la estructura cuaternaria es, sencillamente, la disposición relativa de las subunidades proteicas entre sí. La unión entre las subunidades se realiza mediante los mismos enlaces que mantienen la estructura terciaria. Dependiendo del número de subunidades tendremos dímeros, tetrámeros, pentámeros, etc. Un ejemplo de estructura cuaternaria es la hemoglobina, formada por cuatro subunidades de globina (dos y dos ) unidas a una parte no proteica (el grupo hemo).
6. PROPIEDADES DE LAS PROTEÍNAS Las propiedades de las proteínas están determinadas por su composición química y estructura. Solubilidad Normalmente las proteínas fibrilares o filamentosas son insolubles en agua, mientras que las proteínas globulares son solubles. La solubilidad de estas proteínas se debe a que los radicales polares se localizan en la periferia de la proteína en o con las moléculas de agua, formándose una capa de solvatación de agua alrededor de cada proteína que impide la unión entre ellas. Debido a su elevada masa molecular, cuando las proteínas son solubles forman dispersiones coloidales en el agua y no se difunden generalmente a través de las membranas biológicas. La solubilidad se puede ver afectada por diferentes factores, como el pH, la temperatura o la concentración salina. Así por ejemplo, al añadir sales al agua, estas compiten con las cargas de los aminoácidos por las moléculas de agua, se rompe la capa de solvatación que rodea a cada proteína, y estas acaban precipitando. Especificidad A diferencia de las biomoléculas estudiadas hasta ahora, las proteínas son moléculas específicas, es decir, cada especie posee algunas proteínas que otros organismos no tienen. Incluso proteínas que presentan la misma función y una estructura tridimensional muy semejante suelen tener una secuencia de aminoácidos algo diferente en cada especie. Este hecho permite llevar a cabo estudios
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
11
filogenéticos y establecer el grado de parentesco entre especies, analizando las semejanzas que existen entre algunas de sus proteínas. Además, incluso dentro de la misma especie, los individuos se diferencian por las proteínas que tienen. La especificidad de las proteínas es la causa del rechazo en el transplante de órganos y en las transfusiones sanguíneas. Desnaturalización La función biológica de una proteína depende de su estructura tridimensional, también denominada conformación. Cualquier cambio que suponga una alteración de esta conformación, afecta a la funcionalidad de una proteína. Cuando una proteína sufre una alteración en su estructura o conformación y deja de ser funcional, hablamos de desnaturalización. Los factores que pueden producir la desnaturalización de las proteínas son variados: aumento de temperatura, variaciones de pH, cambios en la concentración salina, etc. En la desnaturalización proteica, no se rompen los enlaces peptídicos, pero sí los enlaces que mantienen la estructura terciaria y secundaria, alterándose el plegamiento de las cadenas peptídicas, y adquiriendo la proteína una conformación abierta. La desnaturalización puede ser: Irreversible: cuando los factores responsables han sido tan intensos o tan duraderos que la proteína no puede recuperar su forma original. Un ejemplo es la coagulación por el calor de la clara del huevo, por desnaturalización de la ovoalbúmina. Reversible: si los factores responsables actúan con escasa intensidad y durante poco tiempo, la proteína recupera su conformación original cuando cesa la acción de los factores responsables de la desnaturalización. Un ejemplo sería el moldeado del cabello, debido a la desnaturalización de la queratina.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
12
7. CLASIFICACIÓN DE LAS PROTEÍNAS 1. HOLOPROTEÍNAS: formadas exclusivamente por aminoácidos A) PROTEÍNAS FILAMENTOSAS: insolubles en agua. Aparecen principalmente en animales. Colágeno: tejido conjuntivo, cartílago y hueso Queratina: cabello, uñas, plumas, cuernos, pezuñas,... Elastina: tendones, vasos sanguíneos B) PROTEÍNAS GLOBULARES: solubles en agua o disoluciones polares. Histonas: asociadas al ADN Prolaminas*: semillas vegetales ( zeína del maíz, gliadina del trigo, hordeína de la cebada) Gluteínas*: orizanina del arroz, glutenina del trigo. ( * Insolubles en agua ) Albúminas: seroalbúmina de la sangre, ovoalbúmina del huevo, lactoalbúmina de la leche, globina de la hemoglobina Globulinas: ovoglobulina del huevo, lactoglobulina de la leche, gammaglobulinas o inmunoglobulinas (anticuerpos) 2. HETEROPROTEÍNAS: formadas por una parte proteica de aminoácidos y un grupo prostético (no proteico) A) CROMOPROTEÍNAS: el grupo prostético es una sustancia coloreada. PORFIRINAS: el grupo prostético es un anillo tetrapirrólico o porfirina. En el centro de este anillo aparece un catión metálico: Grupo hemo: catión Fe2+ . Hemoglobina, Mioglobina (transportan O2), Citocromo C (transporta electrones) Grupo hemino: catión Fe3+. Peroxidasas, Catalasas. NO PORFIRINAS: Hemocianina: contiene Cu, aparece en crustáceos y moluscos Hemeritrina: contiene Fe, aparece en anélidos y braquiópodos B) GLUCOPROTEÍNAS: el grupo prostético es un glúcido Hormonas: FSH, LH, TSH Proteoglucanos: liquido sinovial, tendones, huesos y cartílagos Glucoproteínas de las membranas celulares Inmunoglobulinas (anticuerpos) C) LIPOPROTEÍNAS: grupo prostético formado por ácidos grasos Lipoproteínas de las membranas celulares Lipoproteínas de la sangre: transportan lípidos D) FOSFOPROTEÍNAS: el grupo prostético es el ácido fosfórico (H3PO4). Caseína: en la leche Vitelina: en el huevo E) NUCLEOPROTEÍNAS: el grupo prostético es un ácido nucleico. Son nucleoproteínas las asociaciones de histonas o protaminas con ADN.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
8. FUNCIONES BIOLÓGICAS DE LAS PROTEÍNAS
13
Biología 2º Bachillerato
14
Tema 1. La base físico-química de la vida.
9. LOS ÁCIDOS NUCLEICOS: CONCEPTO, TIPOS y FUNCIONES. N y P.
Los ácidos nucleicos son biomoléculas de la mayor importancia biológica, formadas por C, H, O,
Son macromoléculas o polímeros formados por la unión de moléculas hidrolizables denominadas nucleótidos. Todos los seres vivos contienen dos tipos de ácidos nucleicos: - ADN o DNA (ácido desoxirribonucleico). Se encuentra en el núcleo celular y en algunos orgánulos, como las mitocondrias y los cloroplastos. - ARN o RNA (ácido ribonucleico). Se encuentra en el núcleo y en el citoplasma, formando parte de los ribosomas. Los virus poseen solamente un tipo de ácido nucleico, bien ADN o ARN. El ADN es el material genético, portador de los caracteres hereditarios, que cumple dos funciones en los seres vivos: ▪ Almacena la información genética, lo que significa que: ─ El ADN contiene la información para el crecimiento y desarrollo de un ser vivo, con las características típicas de su especie. ─ El ADN contiene las instrucciones para sintetizas proteínas, y por tanto dirige la síntesis de proteínas en la célula. ▪ Transmite la información genética en cada generación, copiándose exactamente antes de que la célula se divida, mediante el proceso de replicación o duplicación del ADN. La función del ARN es expresar la información genética, es decir, ejecutar las órdenes contenidas en el ADN. Por tanto, el ARN es el encargado de sintetizar las proteínas. En la célula la información genética se transmite de ADN a ADN, y fluye del ADN al ARN y de éste a las proteínas. Este flujo de información se conoce como “el dogma central de la biología molecular”. ADN → ARN → Proteínas
10. LOS NUCLEÓTIDOS: NUCLEICOS
COMPONENTES
DE
LOS
ÁCIDOS
Los componentes de los ácidos nucleicos son los NUCLEÓTIDOS. Los nucleótidos están formados por tres componentes: ácido fosfórico, una pentosa y una base nitrogenada, por lo que se trata de moléculas hidrolizables. La pentosa puede ser de dos tipos: ─ Ribosa (-D-ribofuranosa): forma parte de los nucleótidos del ARN denominados ribonucleótidos. ─ Desoxirribosa (-2-desoxi-D-ribofuranosa): forma parte de los nucleótidos del ADN o desoxirribonucleótidos. Las bases nitrogenadas de los nucleótidos son derivadas de dos compuestos heterocíclicos: purina y pirimidina, por lo que se clasifican en: ▪ Bases púricas: derivan de la purina. Las más importantes son: ─ Adenina (A): se encuentra tanto en el ADN como en el ARN. ─ Guanina (G): se encuentra tanto en el ADN como en el ARN. ▪ Bases pirimidínicas: derivan de la pirimidina. Las más importantes son: Citosina (C): se halla tanto en el ADN como en el ARN. ─ Timina (T): se encuentra sólo en el ADN. ─ Uracilo (U): se encuentra sólo en el ARN.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
15
La unión entre una base nitrogenada (púrica o pirimidínica) y una molécula de pentosa, origina un NUCLEÓSIDO. La unión entre ambos componentes se lleva a cabo mediante un enlace de tipo covalente, denominado enlace N-glucosídico, que se establece entre el nitrógeno 1 de las bases pirimidínicas o e 9 de las base púricas y el átomo 1´de la pentosa. Base nitrogenada + Pentosa = Nucleósido Los ribonucleósidos se designan con el nombre de la base nitrogenada, haciéndola termina en –osina si es una base púrica, y en –idina si se trata de una base pirimidínica. Los desoxirribonucleósidos se nombran igual, pero anteponiendo el prefijo desoxi-. La unión entre un nucleósido y un ácido fosfórico origina un NUCLÉOTIDO. Los nucleótidos son ésteres fosfóricos de los nucleósidos, de manera que entre el ácido fosfórico y el grupo –OH del carbono 5´de la pentosa se forma un enlace éster con la liberación de una molécula de agua. Los nucleótidos se nombran habitualmente con el nombre del nucleósido, eliminando la letra -a final y añadiendo el número de fosfatos unidos( monofosfato, difosfato, trifosfato). Frecuentemente se suelen emplear siglas para designarlos, como AMP que significa adenosín monofosfato.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
16
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
17
11. FUNCIONES DE LOS NUCLEÓTIDOS Los nucleótidos son moléculas de gran interés biológico, ya que, además de constituir los ácidos nucleicos, llevan a cabo diferentes funciones en los seres vivos. Algunas de ellas son:
Moléculas acumuladoras y donantes de energía. La energía desprendida en las reacciones metabólicas se utiliza para fabricar nucleótidos que actúan como monedas energéticas en la célula. Los dos principales son el ADP (adenosín difostato) y el ATP (adenosín trifosfato), que almacenan la energía en los enlaces fosfato-fosfato. Este tipo de enlaces son enlaces de alta energía, lo que quiere decir que se requiere una gran cantidad de energía para su formación, y por tanto su rotura libera la misma cantidad de energía (8 kcal/mol). La energía desprendida en las reacciones metabólicas se emplea para fabricar ATP a partir de ADP, y cuando se necesita energía se utiliza la almacenada en el ATP que se convierte de nuevo en ADP. De esta manera, el sistema ADP/ATP constituye una forma eficaz de transferir energía entre reacciones metabólicas.
Mensajeros químicos El adenosín monofosfato cíclico (AMPc) desempeña un papel clave en el desencadenamiento de las respuestas celulares ante estímulos del medio. Las hormonas y los neurotransmisores son moléculas mensajeras que se encuentran en el medio celular y se unen a ciertos receptores de las membranas celulares. Esto favorece la síntesis del AMPc, que actúa como mensajero químico dentro de la célula, permitiendo la ejecución de varios procesos bioquímicos, que en última instancia, originan una respuesta celular.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
18
Coenzimas Existen ciertos nucleótidos que actúan como coenzimas (moléculas necesarias para muchas enzimas) en algunas reacciones metabólicas importantes. Este es el caso de: Nicotínamín-adenín-dinucleótido (NAD+). Es un derivado de la vitamina PP o nicotinamida. Nicotínamín-adenín-dinucleótido fosfato (NADP+) Flavín-adenín-dinucleótido (FAD). Es un derivado de la riboflavina o vitamina B2. Estos tres coenzimas participan en reacciones de deshidrogenación, fundamentales en el metabolismo celular. Captan protones y electrones de moléculas oxidadas y los ceden fácilmente a otras moléculas. Al captar protones y electrones quedan como NADH, NADPH y FADH2 (formas reducidas).
12. POLINUCLEÓTIDOS La unión de un gran número de nucleótidos, mediante enlaces covalentes, formando largas cadenas de nucleótidos, da lugar a los polinucleótidos o ácidos nucleicos. La unión entre nucleótidos se realiza mediante enlaces o puentes fosfodiéster (enlace nucleotídico), que se establecen entre el grupo fosfato unido al carbono 5´ de un nucleótido y el grupo hidroxilo del carbono 3´ de una pentosa. Como la unión de los nucleótidos se produce entre pentosas y fosfatos, las bases nitrogenadas no participan en los enlaces. Se establecen así largas cadenas sin ramificar formadas por la secuencia pentosa-fosfato-pentosa-fosfato,… en las que las bases nitrogenadas quedan “colgando” lateralmente de las pentosas. Así el esqueleto de los polinucleótidos lo constituyen los grupos alternantes de pentosas y fosfatos y la secuencia de bases nitrogenadas es la que proporciona la especificidad a la cadena polipeptídica formada, y por tanto, la que determina la información genética. En todos los polinucleótidos existe un extremo (denomina extremo 3´) con una pentosa con el grupo –OH del carbono 3´ libre, y otro extremo (llamado extremo 5´), donde se localiza un grupo fosfato libre unido al carbono 5´ de otra pentosa. Para indicar la composición del polinucleótido se suele indicar la secuencia de bases nitrogenadas y los extremos 5´y 3´. Ya hemos visto que existen dos tipos de ácidos nucleicos o polinucleótidos: ADN, que es un polinucleótido compuesto de desoxirribonucleótidos de A, G, C y T. ARN, que es un polinucleótido compuesto de ribonucleótidos de A, G, C y U.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
19
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
20
13. ÁCIDO DESOXIRRIBONUCLEICO (ADN) Como ya hemos visto, el ADN está formado por la unión de desoxirribonucleótidos, es decir, nucleótidos que contienen desoxirribosa. En cuanto a las bases nitrogenadas pueden ser adenina, guanina, citosina y timina, pero nunca uracilo. Con excepción de algunos virus (como el X174), el ADN está constituido por dos largas cadenas de nucleótidos unidas entre sí en toda su longitud. Esta doble cadena puede disponerse en forma lineal (ADN del núcleo de las células eucariotas) o en forma circular (ADN de las células procariotas, de ciertos virus y de las mitocondrias y cloroplastos). La molécula de ADN porta la información genética necesaria para el crecimiento y desarrollo biológico de un individuo y contiene los mensajes e instrucciones para que las células realicen sus funciones. Es decir, lleva codificada la información a partir de la cual se forma un organismo vivo, por lo que constituye el material genético. 13.1. ESTRUCTURA DEL ADN El ADN es una molécula altamente estructurada en la que, de manera semejante a las proteínas, se distinguen varios niveles de complejidad: estructura primaria, estructura secundaria y estructura terciaria.
Estructura primaria La estructura primaria viene determinada por la secuencia de nucleótidos de una cadena de polinucleótidos. En uno de los extremos de dicha cadena existe un fosfato libre (extremo 5´) y en el otro un grupo –OH libre del carbono 3´ de una pentosa (extremo 3´). Como todos los nucleótidos contienen desoxirribosa, la diferencia entre las moléculas de ADN radica en el orden de las bases nitrogenadas que cuelgan de las pentosas. Por tanto, la secuencia precisa en la que aparecen los cuatro tipos de bases (A, G, C y T) del ADN es la que determina las características biológicas del individuo.
Estructura secundaria La estructura secundaria del ADN informa de la disposición especial de las dos cadenas de polinucleótidos que forman una molécula de ADN. Basándose en estudios de difracción de rayos X, James Watson y Francis Crick propusieron en 1953 un modelo molecular aceptado en la actualidad, que permite explicar las propiedades físicoquímicas y biológicas del ADN: el modelo de la doble hélice. Previamente al modelo de la doble hélice propuesto por Watson y Crick, hubo varios descubrimientos realizados por otros investigadores, que aportaron datos sobre la estructura del ADN. Entre ellos, destacan: ▪ 1950, E. Chargaff. Después de estudiar gran variedad de muestras de ADN de diferentes especies, observa que siempre existía la misma cantidad de bases nitrogenadas púricas y pirimidínicas. Descubrió que el número de adeninas era igual de al timinas, y el de guaninas al de citosinas. Estos resultados constituyeron la denominada ley de equivalencia de bases de Chargaff. ▪ 1953, Rosalin Franklin y Maurice Wilkins. Aplicando el método de difracción de rayos X al ADN, dedujeron que esta molécula posee una estructura helicoidal con dos periodicidades, una cada 0,34 nm y otra cada 3,4 nm.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
21
Modelo de la doble hélice de ADN. Watson y Crick, 1953 A partir de estos datos, Watson y Crick elaboraron su modelo de estructura tridimensional del ADN (“modelo de la doble hélice”), que presenta las siguientes características: El ADN está constituido por dos cadenas de polinucleótidos unidas entre sí en toda su longitud. Las dos cadenas son antiparalelas, lo que significa que el extremo 3´de una de ellas se enfrenta al 5´de la otra. La unión entre las cadenas se realiza mediante puentes de hidrógeno entre las bases nitrogenadas de ambas: concretamente, la adenina forma dos puentes de hidrógeno con la timina y la guanina tres con la citosina. Resulta evidente que las dos cadenas no son idénticas, sino complementarias, ya que cada una de ellas tiene la secuencia de bases complementaria a la otra. (Si se conoce una secuencia es posible deducir inmediatamente la complementaria). Las dos cadenas están enrolladas en espiral formando una doble hélice alrededor de un eje imaginario. Las bases nitrogenadas quedan en el interior de la doble hélice, mientras que los esqueletos pentosafosfato se sitúan en la parte externa. De esta forma, las cargas negativas de los grupos fosfato se unen a las cargas positivas de otras moléculas o de cationes, estabilizando la estructura. Los planos de las bases nitrogenadas enfrentados son paralelos entre sí y perpendiculares al eje de la hélice. El enrollamiento de la doble hélice es dextrógiro, es decir, giran en el sentido de las agujas del reloj, y además plectonémico, o sea, las cadenas no se pueden separar sin desenrollarlas. La anchura de la doble hélice es de 2 nm, mientras que la longitud de cada vuelta es de 3,4 nm y cada 0,34 nm se encuentra un par de bases complementarias. Puede deducirse, por tanto, que existen 10 pares de nucleótidos por cada vuelta.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
22
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
23
Otros modelos de doble hélice La estructura secundaria del ADN descrita por Watson y Crick se conoce como B-ADN, y es la más abundante en la naturaleza. Pero existen otras estructuras secundarias descubiertas posteriormente: A-ADN: es una doble hélice dextrógira, cuya hélice es más ancha y más corta, mide 2,3 nm y en cada vuelta hay 11 pares de bases. Los pares de bases están inclinados respecto al eje central. Z-ADN: la doble hélice es levógira y cada vuelta mide 3,8 nm y contiene 12 pares de bases. Presenta un aspecto en zig-zag. Este tipo de hélice se debe a que las bases púricas alternan repetidamente con las pirimidínicas, como sucede en las secuencias CGCG o CACA.
Estructura terciaria La estructura en doble hélice del ADN sufre nuevos plegamientos que dan lugar a un tercer nivel estructural: la estructura terciaria. Es necesario por dos razones: Las largas cadenas de ADN deben acoplarse en el reducido espacio disponible en el interior celular. La regulación de la actividad del ADN dependen en gran medida del grado de plegamiento que sufra la molécula. La estructura terciaria es compleja y sabemos que existen proteínas (como las histonas) asociadas al ADN que organizan la estructura y permiten su empaquetamiento en el interior celular. El resultado final es la formación de cromatina y cromosomas, que estudiaremos en el núcleo celular.
13.2. TIPOS DE ADN Dependiendo del número de cadenas de polinucleótidos y su forma de empaquetamiento, el ADN en los organismos puede ser: Células eucariotas: ADN bicatenario (ADN2C ó ADNbc) lineal, dos cadenas dispuestas en línea, como en el núcleo de las células eucariotas. Células procariotas: ADN bicatenario circular y superenrrollado, dos cadenas que se disponen formando un círculo cerrado, como en las bacterias (y también en mitocondrias y cloroplastos). Virus: ADN monocatenario (ADN1C ó ADNmc) o ADN bicatenario lineal o circular.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
24
13.3. DESNATURALIZACIÓN e HIBRIDACIÓN DEL ADN La molécula de ADN es muy estable en condiciones normales, debido a los numerosos puentes de hidrógeno que unen las bases nitrogenadas de las dos cadenas polinucleotídicas. Sin embargo, la estructura en doble hélice se puede perder, separándose las dos cadenas o hebras, cuando se alteran las condiciones de pH (por encima de 13) o se calienta a temperaturas en torno a 100 ºC. Este fenómeno se conoce como desnaturalización del ADN. La desnaturalización se produce al romperse los puentes de hidrógeno que unen las dos cadenas de polinucleótidos, ambas cadenas se separan y se enrollan individualmente al azar. La temperatura a la que el 50% de la doble hélice está separada se denomina temperatura de fusión (Tm). Su valor depende del número de pares guanosina-citosina que haya en la molécula, de tal manera que si este es elevado la Tm será elevada, ya que el número de puentes de hidrógeno que se debe romper es mayor, y por tanto se necesita más energía para hacerlo. La desnaturalización del ADN es un proceso reversible, ya que si las hebras se mantienen a una temperatura en torno a los 65 ºC durante un periodo de tiempo prolongado, forman una nueva doble hélice con total funcionalidad. Este proceso se denomina renaturalización o hibridación del ADN.
Técnicas de hibridación De la misma forma que dos hebras de un mismo ADN se pueden renaturalizar en condiciones de pH y temperatura adecuadas, también se puede conseguir que dos hebras de distinta procedencia lo hagan. Así, se pueden obtener moléculas híbridas a partir de dos hebras de cualquier tipo de ADN, siempre que entre ambas exista una secuencia complementaria. Cuanto más relacionados están los ADN, mayor porcentaje de renaturalización se producirá. En una misma especie, el porcentaje de hibridación será mayor entre individuos emparentados. En diferentes especies, habrá mayor hibridación cuanto más relacionadas evolutivamente estén las especies. Por ejemplo, si se forma un híbrido entre ADN de ratón y ADN humano, el porcentaje de hibridación se encuentra en torno al 25%. Las técnicas de hibridación pueden servir para detectar secuencias complementarias, localizar genes relacionados entre distintas poblaciones o diagnosticar enfermedades genéticas producidas por la alteración en la secuencia de ADN .
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
25
14. ÁCIDO RIBONUCLEICO (ARN) El ARN, al igual que el ADN, es un polinucleótido no ramificado, formados por una serie de nucleótidos unidos por enlaces éster fosfóricos. A diferencia del ADN, el ARN lleva ribosa como pentosa y como bases nitrogenadas adenina, guanina, citosina y uracilo (no leva timina). El uracilo, como sucede con la timina en el ADN, se puede emparejar con la adenina. A excepción de algunos virus (reovirus), el ARN está formado por una única cadena de nucleótidos, aunque en algunos tipos de ARN las bases se pueden emparejar originando tramos de ARN bicatenarios, originados por el plegamiento de la cadena sobre sí misma. Las cadenas de ARN son más cortas que las de ADN y pueden aparecer tanto en el núcleo como en el citoplasma celular. El ARN es la molécula encargada de fabricar las proteínas específicas de un organismo, transmitiendo el mensaje codificado por el ADN. Así, mientras el ADN contiene información, el ARN la utiliza para que se produzcan las proteínas específicas del individuo. Este proceso es sumamente complejo (lo estudiaremos en el tema 5) y requiere la intervención de varios tipos de ARN: ▪ ARN mensajero o ARNm ▪ ARN ribosómico o ARNr ▪ ARN transferente o ARNt
ARN mensajero (ARNm) El ARNm es una copia de parte del ADN (de un gen o un grupo de genes que vayan a expresarse), cuya información será utilizada por los ribosomas para fabricar proteínas con una secuencia concreta de aminoácidos. El ARNm es lineal, sin zonas bicatenarias y constituye del 2 al 5% del ARN. Su función es llevar el mensaje genético del ADN hasta los ribosomas. El ARNm se forma mediante un proceso denominado transcripción, a partir de cualquiera de las dos cadenas del ADN. Cada vez que se necesita fabricar una proteína, la célula fabrica el ARNm correspondiente, ya que esta molécula tiene una vida muy corta (es destruida por ribonucleasas) y si no fuera así habría una superproducción de proteínas. La información contenida en el ARNm se presenta en una secuencia de bases nitrogenadas. Cada grupo de tres bases del ARNm que codifica para un aminoácido se denomina triplete o codón.
5´ ... AUG G C A U G C C G A A U A UAA... 3´ ARN ribosómico (ARNr)
Tripletes o codones
El ARNr forma parte de los ribosomas y participa, por tanto, es el proceso de unión de los aminoácidos para sintetizar las proteínas. La cadena de nucleótidos del ARNr, a diferencia del ARNm, está muy plegada, con muchos tramos bicatenarios. Se encuentra asociado a proteínas y de esta asociación se forman los ribosomas. Constituye entre el 80-85% del ARN celular total. Las células procariotas y eucariotas tienen cadenas de ARNr ligeramente distintas, que se diferencian por su coeficiente de sedimentación, tal como se aprecia en el siguiente cuadro: Subunidad ribosómica menor Subunidad ribosómica mayor
Procariotas
Eucariotas
16 S
18 S
5S 23 S
5S 5,8 S 28 S
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
26
ARN de transferencia o ARN transferente (ARNt) Las moléculas de ARNt están formadas por cadenas muy cortas (entre 70 y 90 nucleótidos). Su estructura secundaria es muy característica, ya que existen tramos de doble cadena, por emparejamiento de bases. Estos tramos se denominan brazos y hay cuatro en cada molécula. En los extremos de los brazos existen zonas sin emparejar que se denominan bucles, y cada uno de ellos desempeña una función particular. El extremo 3´de la cadena siempre tiene la secuencia de bases CCA y es por donde se unen los aminoácidos. En el extremo 5´siempre existe G. La estructura extendida del ARNt tiene forma de hoja de trébol, aunque en realidad los brazos se pliegan formando una estructura acodada que recibe el nombre de “estructura de boomerang”. El ARNt constituye, aproximadamente, el 15% del ARN total. El ARNt se encarga de transportar los aminoácidos presentes en el citoplasma hasta los ribosomas, donde se unirán para formar proteínas. Cada molécula de ARNt transporta un aminoácido concreto. Las diferencias entre las moléculas de ARNt son debidas a una secuela de tres bases nitrogenadas, el anticodón, que varía en los distintos ARNt y es la zona por donde se unen al ARNm. Existen más moléculas de ARNt diferentes que aminoácidos, por lo que un aminoácido puede ser transportado por diferentes moléculas de ARNt.
Expresión de la información genética
original papers
NATURE | VOL 421 | 23 JANUARY 2003 | www.nature.com/nature
© 2003 Nature Publishing Group
397
original papers
398
© 2003 Nature Publishing Group
NATURE | VOL 421 | 23 JANUARY 2003 | www.nature.com/nature
GENÓMICA y PROTEONÓMICA Genómica La Genómica es un área de la Biología cuyo objetivo es el estudio de los genomas. El “Genoma” es el conjunto de genes que especifican todos los caracteres que pueden ser expresados en un organismo. Es el juego completo de instrucciones hereditarias para la construcción y mantenimiento de un organismo en determinadas condiciones medioambientales. El término “Genómica” fue introducido en 1986, considerando el genoma como una unidad funcional y para distinguir el estudio de genomas completos, o de grandes regiones del mismo, de estudios genéticos más tradicionales centrados en un gen o un pequeño grupo de genes relacionados funcional o estructuralmente. A mediados de los años ochenta se disponía de la secuencia completa de algunos virus y orgánulos celulares. Los avances en las técnicas de secuenciación y análisis informático de secuencias permitieron el abordaje de proyectos de secuenciación de organismos más complejos. A partir de 1995 se produjo un incremento exponencial en la aparición de secuencias de genomas completos, iniciado con los de las bacterias Haemophilus influenzae y Mycoplasma genitalium . En 1996 se dio a conocer la primera secuencia de un organismo eucariota, Saccharomyces cerevisiae , y en 1998 se finalizó la secuenciación de un organismo eucariota pluricelular, Caenorhabditis elegans . En 2003 se publicó la secuencia completa del genoma humano, un hito indiscutible por la apertura a nuevas investigaciones y aplicaciones en el área de la Biomedicina. Hasta la fecha se han publicado la secuencia completa de cientos de organismos, incluyendo, además de los mencionados, numerosos microorganismos, animales y plantas modelo como Drosophila melanogaster , Rattus norvegicus o Arabidopsis thaliana . El conocimiento de estas secuencias no es más que el primer paso de lo que se ha dado en llamar “Genómica Funcional”, la posibilidad de caracterizar la función de los genes descubiertos en estos organismos mediante diferentes estrategias globales como el análisis de los perfiles de expresión génica mediante microarrays, análisis fenotípicos de mutantes o el análisis de interacciones proteícas. En paralelo, la caracterización en diferentes poblaciones de microsatélites o polimorfismos de nucleótidos (SNPs) asociados a determinados fenotipos abre enormes expectativas en la investigación biomédica.
Proteonómica La Proteómica es un área de la Biología cuyo objetivo es el estudio de los proteomas. Un proteoma es el conjunto de proteínas expresadas por un genoma, una célula o un tejido. El término Proteoma fue utilizado por primera vez en 1995. Hubo dos factores decisivos para el desarrollo de la proteómica: – Por un lado la secuenciación de los genomas a gran escala (se conoce la secuencia de los genes pero no su función). – Y por otro lado, el desarrollo de técnicas de separación y análisis de proteínas (Electroforesis Bidimensional y Espectrometría de Masas).
La secuenciación del genoma humano ha permitido conocer el número de genes que poseemos y que dicho número no es muy diferente del de otros organismos. La complejidad de los organismos parece radicar en las proteínas ya que un gen puede dar lugar a diferentes formas proteicas. Las proteínas van a sufrir diferentes modificaciones post-traduccionales para realizar su función. Además las proteínas van a interaccionar con otras proteínas formando complejos proteicos. La proteómica proporciona un conjunto de herramientas muy poderosas para el estudio a gran escala de la función de los genes a nivel de proteína. La aplicación de la proteómica tiene un enorme potencial en el área de la biomedicina para el desarrollo de fármacos (anticancerígenos, para el sistema nervioso, aparato cardiovascular, antimicrobianos, etc) métodos de diagnóstico, desarrollo de vacunas, etc.
Genómica, proteonómica y medicina La secuenciación del genoma humano, junto con el desarrollo de nuevas tecnologías “ómicas” de alto rendimiento (genómica, proteonómica, metabolómica), están aumentando de manera esencial el conocimiento de la enfermedad humana y estableciendo unas bases para la medicina personalizada (MP). La medicina personalizada (MP) es una modalidad de la medicina que utiliza la información de los genes, proteínas y metabolitos de cada paciente para prevenir, diagnosticar y tratar la enfermedad. Emplea la información del genoma de un individuo (y los datos que se derivan, expresión de proteínas, presencia de metabolitos) en pruebas de diagnóstico útiles y tratamientos específicos para cada enfermedad y para cada paciente. La medicina genómica hace uso de la información genómica y de las tecnologías complementarias (bioinformática) para determinar el riesgo y la predisposición a la enfermedad, diagnóstico y pronóstico y la selección y priorización de las opciones terapéuticas. Mientras que la farmacogenética se centra en el estudio de cómo un gen (o un número pequeño de genes) afecta al metabolismo, la farmacogenética lo hace en el estudio de cómo la variación genética del genoma afecta al metabolismo y respuesta frente a los fármacos. La medicina personalizada utiliza test moleculares para dividir a los pacientes según su respuesta a un tratamiento y mejora la eficacia del tratamiento seleccionando a los individuos que responden bien o excluyendo a los que van a tener un efecto adverso.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
1
ACTIVIDADES TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA PARTE III: PROTEÍNAS y ÁCIDOS NUCLEICOS PROTEÍNAS 1. a) b) c)
Utilizando como ejemplo la fórmula del aminoácido alanina, indica: ¿Qué es un carbono asimétrico?. ¿Cuántos y qué C asimétricos tiene la molécula de la figura?. ¿Qué propiedades poseen las moléculas que tienen C asimétricos?.
2. Los aminoácidos son compuestos anfóteros, ¿qué significa dicha propiedad?. ¿A qué se debe?. ¿Se podrían separar los distintos aminoácidos de una mezcla en función de su carga eléctrica?. Razona la respuesta. 3. Si el punto isoeléctrico de la alanina es 6, indicar la carga y estructura química de este aminoácido a pH 6, pH 2 y pH 9. 4. Se dispone de una disolución acuosa de alanina y treonina cuyos puntos isoeléctricos son 6,02 y 6,6 respectivamente. Explica razonadamente qué aminoácido se dirigirá hacia el ánodo y cuál hacia el cátodo si el pH de la solución es 6,3. Razona la respuesta. 5. a) b) c)
Con respecto al esquema adjunto: ¿Qué tipo de enlace observas?. ¿Tiene ese enlace capacidad de rotación?. Razónalo. ¿Son esos enlaces responsables de la estructura secundaria de las macromoléculas de las que forman parte?. Razónalo.
6. Escribe la fórmula desarrollada del siguiente péptido: H2N - Phe - Ser - Cis - Lys - COOH 7. La tripsina es un enzima que hidroliza los enlaces peptídicos en los que el grupo carboxílico lo aporta una lisina o una arginina. ¿Cuál será el resultado de la hidrólisis por medio de la tripsina sobre estos péptidos?. a) H2N - Lys - Met - Ala - Arg - Met - Val - COOH b) COOH - Lys - Arg - Met - Cys - Lys - Phe - NH2 8. a) b) c)
Indica qué enlaces mantienen las siguientes estructuras proteicas: Hélices estabilizadas Estructuras globulares Estructura cuaternaria
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
2
9. ¿De qué depende la actividad biológica y la especificidad de una proteína?. 10. ¿Qué enlaces se rompen al someter a una proteína a una temperatura elevada?. ¿Cómo se denomina este proceso?. ¿Qué repercusión tiene en la funcionalidad de la proteína?. 11. ¿Cuál es la causa de que las proteínas filamentosas sean insolubles en agua?. 12. ¿Porqué las proteínas animales tienen mayor valor biológico que las vegetales?. 13. Cita las funciones biológicas de las siguientes proteínas: a) Ovoalbúminas b) Glucoproteínas c) Cromoproteínas d) Actina y miosina e) Queratinas ÁCIDOS NUCLEICOS 14. Observa el modelo molecular de la derecha y responde a las cuestiones: a) ¿A qué molécula corresponde?. b) ¿Cuáles son los monómeros que lo forman?. c) ¿Qué nombre reciben estos?. d) ¿Qué moléculas constituyen estos monómeros?. 15. ¿Qué diferencia existe entre un nucleósido y un nucleótido?. 16. La figura representa una molécula muy importante para los seres vivos. ¿Cómo se denomina?. ¿Qué función desarrolla en la célula?. ¿Qué tipo de enlaces químicos presenta esta molécula que la diferencian de otras similares?. Indícalos en la fórmula.
17. Ácidos nucleicos: a) Nombra las unidades estructurales que los forman y los enlaces que las unen. b) Explica las diferencias químicas y estructurales de los dos tipos de ácidos nucleicos. c) Menciona al menos una localización de cada tipo de ácido nucleico. 18. Dibuja el trinucleótido dAMP-dTMP-dCMP y señala todos los enlaces de tipo éster que hay. Para facilitar el dibujo, simboliza las bases nitrogenadas con las letras A, T y C. Dibuja de la misma forma la hebra complementaria. Recuerda que son antiparalelas. 19. Indica a qué tipo de ácido nucleico corresponden las siguientes secuencias de bases nitrogenadas: a) 5´...CCGATC...3´ b) 3´...GGATCC...5´ c) 3´...UACCGA...5´ d) 5´...ACCGGC...3´
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
3
20. En una ADN bicatenario se ha hallado que en el total de bases nitrogenadas hay un 23 % de adenina. ¿Cuáles son los porcentajes de las demás bases?. 21. En un ácido nucleico se ha encontrado el siguiente porcentaje de bases nitrogenadas: Adenina 22% Guanina 19% Citosina 26% Uracilo 33% ¿Se trata de ADN o ARN?. ¿Es de una sola hebra o de doble hebra?. 22. ¿Cuál es la secuencia de ADN complementaria de 5´ TACCTCAT....3¨?. 23. La secuencia de bases de una molécula de ARNm es: A-A-U-U-U-G-C-C-A … a) Escribe la doble cadena de nucleótidos del ADN de la que se copió. b) Indica cuál de las dos sirvió de molde. c) Escribe los anticodones correspondientes. 24. Observa el esquema: a) ¿A qué estructura corresponde?. b) Explica su función.
I.E.S Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
1
ACTIVIDADES GENÉTICA
1. Escribe qué secuencias de ADN son complementarias a las siguientes: a) b) c) d)
3´ ....T T A G C G G C T A C G C C T A ....5´ 5´ ....A C C G T C G T A C C G T T C G ....3´ 5´ ....C G T A A C G T T C G A C C G T .....5´ 3´ ....A T T C G T T A C C G T A T T C C ...3´
2. Escribe las secuencias de ARN complementarias a las anteriores secuencias de ADN. 3. Escribe las secuencias de ADN que han dado lugar a las siguientes secuencias de ARN (escribe las dos cadenas de ADN, indicando su sentido y cuál es la cadena con sentido). a) 5´... A U C G C G C G G C U U A C G ....3´ b) 3´... C G C U U A A C G C U A A C U ....5´ c) 5´... U A C G C U A C C U U G C A C .....3´ 4. Las siguientes composiciones corresponden a diferentes cadenas de A.D.N.: - Cadena 1: A=30%; G=24%; T=20%; C=26% - Cadena 2: A=15%; G=60%; T=20%; C=5% - Cadena 3: A=45%; G=10%; T=35%; C=10% - Cadena 4: A=20%; G=40%; T=30%; C=10% a) Calcula la composición de las bases nitrogenadas de las cadenas de A.D.N. complementarias. b) Calcula la composición de las bases nitrogenadas de las cadenas de A.R.N. que resulten de la transcripción de las cadenas de A.D.N. complementarias.
5. Escribe las secuencias de aminoácidos que son codificadas por los siguientes fragmentos de ADN: a) 5´... T A A G C T A C G T A C ... 3´ b) 3´... G C C T T A G C C A T C ... 5´ c) 5´... T T A C C G T A T C G G ... 3´ d) 3´... A T A C T G G T T A C C ... 5´ 6. Escribe las secuencias de A.D.N. que codifiquen para la síntesis de los siguientes péptidos: a) H2N...Pro-Asp-Ser-Trp...COOH b) HOOC...Ile-Leu-Val-Tyr...NH2 c) H2N...Tyr-Thr-Ser-Val...COOH
BIOLOGÍA 2º BACHILLERATO ACTIVIDADES SECUENCIACIÓN DEL ADN Se han secuenciado dos muestras de ADN, una mediante el método enzimático de Sanger (muestra A) y otra mediante secuenciación automática (muestra B). Determina en cada caso cuál es la secuencia de bases nitrogenadas de cada una de las muestras, indicando el sentido de la cadena.
Muestra A
Muestra B
SECUENCIACION ADN SOLUCION
BLOQUE II LA CÉLULA, MORFOLOGÍA Y FUNCIÓN
TEMA 2. LA CÉLULA: ORGANIZACIÓN Y ESTRUCTURA TEMA 3. CICLO CELULAR Y DIVISIÓN CELULAR TEMA 4. NUTRICIÓN CELULAR: METABOLISMO
TEMA 2. LA CÉLULA: ORGANIZACIÓN y ESTRUCTURA 1. INTRODUCCIÓN A LA CÉLULA: LA TEORÍA CELULAR 2. LA ORGANIZACIÓN CELULAR 3. LA ORGANIZACIÓN PROCARIOTA 4. LA ORGANIZACIÓN EUCARIOTA 5. LA MEMBRANA PLASMÁTICA • Composición química • Estructura de la membrana: modelo de mosaico fluido. • Funciones de la membrana celular 6. LA PARED CELULAR • Composición y estructura • Funciones de la pared celular 7. CITOPLASMA 7.1. CITOSOL o HIALOPLASMA 7.2. EL CITOESQUELETO 7.3. CENTRIOLOS, CILIOS y FLAGELOS 7.4. RIBOSOMAS 7.5. LOS ORGÁNULOS MEMBRANOSOS 7.5.1. Retículo endoplásmico (RE) 7.5.2. Aparato o complejo de Golgi 7.5.3. Lisosomas 7.5.4. Vacuolas 7.5.5. Peroxisomas 7.5.6. Mitocondrias 7.5.7. Cloroplastos 8. EL NÚCLEO CELULAR 8.1. CARACTERÍSTICAS GENERALES 8.2. ESTRUCTURA y COMPOSICIÓN DEL NÚCLEO INTERFÁSICO • Envoltura nuclear • Nucleoplasma • Nucleolo • Cromatina 8.3. LOS CROMOSOMAS • Estructura y composición • Cariotipo • Células diploides y haploides
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
1
1. INTRODUCCIÓN A LA CÉLULA: LA TEORÍA CELULAR El primero en observar células fue el científico inglés Robert Hooke en 1665 sobre una preparación de corcho y con un microscopio muy rudimentario. El corcho, observado en aumento, parecía estar constituido por pequeñas celdillas rodeadas por una pared rígida. Fue Hooke el primero en acuñar el término célula para referirse a estas estructuras. Sin embargo no llegó a reconocer la verdadera estructura de las células y, en realidad, lo que vio en el corcho no eran células sino sus paredes celulares muertas. El primero que observó células vivas fue Antón van Leeuwenhoek entre finales del s.XVII y principios del XVIII, describió los glóbulos rojos y observó espermatozoides, protozoos e incluso bacterias, todo ello con microscopios muy rudimentarios (en realidad simples lupas) fabricados por él mismo. Los progresos en el estudio de las células (Citología) dependen muy directamente del desarrollo de la microscopía; por ello hubo que esperar casi dos siglos hasta que se empezó a entender la verdadera significación de las células. En 1831 ya se conocía la existencia del núcleo celular; en 1839 se había descrito minuciosamente el proceso mitótico y en ese mismo año nacía la Teoría celular, atribuida a Schleiden y Schwann, que introducía el concepto fundamental de que la célula es la unidad básica de todos los seres vivos. Este principio fue ampliado finalmente por Virchow en 1859 con lo que la Teoría celular quedó definitivamente establecida. Se puede resumir en tres principios: 1.- Todos los organismos vivos están constituidos por una o varias células; la célula es, por tanto, la unidad vital de los seres vivos. 2.- Las células son capaces de una existencia independiente; las células son, por tanto, la unidad anatómica y fisiológica de los seres vivos. 3.- Toda célula proviene de otra célula ya existente; la célula es, por tanto, la unidad genética de los seres vivos. Hasta finales del s.XIX se consideraba que el tejido nervioso constituía una excepción a la teoría celular ya que se creía que no estaba formado por células independientes sino por una red o retículo de fibras y células interconectadas en la que no era posible diferenciar los elementos celulares, las neuronas. Fue Ramón y Cajal quien resolvió este problema al enunciar su teoría de la neurona en la que se demostraba que las neuronas eran elementos independientes y constituían la unidad anatómica y funcional del sistema nervioso. De esta manera, la teoría celular quedó definitivamente generalizada a todas las células, tanto vegetales como animales.
2. LA ORGANIZACIÓN CELULAR En todos los seres vivos , las biomoléculas se encuentran reunidas en conjuntos organizados a los que llamamos células. Las células son las asociaciones más simples de biomoléculas que son capaces de mantenerse estables frente al medio, para lo cual realizan las funciones de nutrición y relación, y además se pueden perpetuar en el tiempo gracias a la capacidad de reproducción. La célula es, por tanto, la unidad básica de un ser vivo, tanto a nivel estructural, como funcional y genético. Todas las células presentan una serie de componentes comunes: • Membrana plasmática: delgada membrana superficial que separa el contenido interno de la célula del exterior, y además regula el intercambio de moléculas entre la célula y el medio. • Citoplasma: es el interior celular, bañado por un liquido viscoso, donde se desarrollan numerosas reacciones metabólicas. En el seno del citoplasma se encuentran dispersos diversas estructuras conocidas como orgánulos celulares. • Material genético: está representado por el ADN, que dirige las actividades celulares y posibilita la transmisión de los caracteres hereditarios a la descendencia. A pesar de estas características “universales”, no todas las células presentan el mismo nivel de complejidad, pudiéndose distinguir dos modelos diferentes de organización celular: células procariotas y células eucariotas. Las células procariotas son las más sencillas y fueron las primeras en aparecer hace 3.600 m.a. Durante más de 1.500 m.a fueron el único tipo de células existentes en el planeta, hasta que por endosimbiosis surgieron hace unos 2.000 m.a las primeras células eucariotas.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
2
3. LA ORGANIZACIÓN PROCARIOTA Las células procariotas son mucho más sencillas que las eucariotas y se sitúan en la base evolutiva. La estructura procariota es característica y exclusiva de las bacterias, que constituyen el Reino Monera. La mayoría de las células procariotas son de pequeño tamaño, desde menos de una micra (μm) hasta unas pocas micras, equivalentes en tamaño a algunos orgánulos celulares eucariotas como mitocondrias o cloroplastos. Básicamente, una célula procariota típica presenta la siguiente estructura: • Una pared celular rígida que rodea a la membrana y responsable de la forma celular. La composición de la pared es diferente a la pared de las células vegetales, abundando los peptidoglucanos. Las únicas células procariotas desprovistas de pared son los micoplasmas, que son los organismos celulares más pequeños (0,1 a 0,8 μm de diámetro). • Una membrana plasmática que delimita el citoplasma celular y que presenta unas invaginaciones denominadas mesosomas, donde se localizan las enzimas respiratorias. • El citoplasma de aspecto granuloso, con ribosomas más pequeños que los eucariotas, con un coeficiente de sedimentación de 70 S, e inclusiones formadas por materiales de reserva (glúcidos, nitrógeno, fósforo, etc.). • La zona del nucleoide, situada en el centro de la célula, que contiene el material genético no rodeado por ninguna membrana, por lo que los procariotas no presentan un verdadero núcleo. El material genético está formado por una molécula de ADN circular, lo que se denomina cromosoma bacteriano, y otras pequeñas moléculas de ADN bicatenario circular denominadas plásmidos. Algunos tipos de bacterias contienen además otros elementos, como flagelos, pelos y fimbrias, cápsula y capas mucosas.
4. LA ORGANIZACIÓN EUCARIOTA A excepción de las bacterias, el resto de los seres vivos (reinos Protoctistas, Hongos, Animales y Plantas), presentan una organización eucariota. Las células eucariotas son más complejas y de mayor tamaño que las procariotas, con un diámetro que oscila entre los 10 y 30 mm, aunque puede variar ampliamente. También presentan una gran variedad de formas, en relación con su modo de vida si se trata de organismos unicelulares o con la función que desempeña el tejido al que pertenecen, si se trata de seres pluricelulares. Una de las características más notables de la célula eucariota es la “compartimentalización”, es decir, la existencia de diversos compartimentos u orgánulos delimitados por membranas que permiten que distintas funciones se lleven a cabo es diferentes partes de la célula. La estructura de una célula eucariota típica consta de los siguientes elementos: • La membrana plasmática, que constituye el límite externo de la célula y regula en transporte e intercambio de sustancias con el medio externo. Además es esencial en el intercambio de señales con otras células, ya que dispone de moléculas receptoras que responden a distintos estímulos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
3
• En ocasiones, rodeando a la membrana existe una pared celular rígida, fundamentalmente de celulosa en las células vegetales y de quitina en el caso de algunos hongos. Las células animales poseen un glicocálix adherido a la membrana que contribuye a la cohesión de los tejidos. • El citoplasma celular contiene los orgánulos celulares y está ocupado por un entramado de filamentos proteícos que constituyen el citoesqueleto o esqueleto celular, implicado también en la formación de cilios y flagelos, los movimientos celulares y la división celular. Las células animales poseen unos orgánulos, los centriolos, formados por filamentos del citoesqueleto. Los ribosomas presentan un coeficiente de sedimentación de 80 S, mayor que en las células procariotas. En el interior del citoplasma existe un sistema interna de membranas complejo constituido por el Retículo Endoplásmico (conectado a la membrana nuclear) y el Complejo de Golgi, orgánulos relacionados con la biosíntesis de moléculas y su distribución en el interior de la célula, así como la secreción de sustancias al exterior. Otros orgánulos membranosos son las vacuolas, muy desarrolladas en las células vegetales, y los lisosomas, que contienen enzimas digestivas para la degradación de sustancias en el interior de las vacuolas digestivas. Presentan dos orgánulos relacionados con la obtención de energía, las mitocondrias y los cloroplastos, estos últimos exclusivos de las células vegetales. En las mitocondrias se realiza la respiración celular y en los cloroplastos la fotosíntesis. • Todas las células eucariotas presentan núcleo delimitado por una doble membrana porosa. En su interior se encuentra la cromatina, constituida por ADN asociado a histonas (proteínas) y el nucleolo donde se fabrican las subunidades de los ribosomas. Así pues, aunque la organización básica de todas las células eucariotas es semejante, se pueden distinguir dos grandes tipos, células animales y vegetales.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
4
5. LA MEMBRANA PLASMÁTICA La membrana plasmática es una delgada envoltura que rodea y limita completamente a la célula, permitiendo que el contenido celular tenga una composición distinta a la del medio. La membrana plasmática separa el interior del exterior celular y controla el intercambio de sustancias entre la célula y su medio. La estructura de la membrana es la misma en todas las células. En cortes ultrafinos visualizados al microscopio electrónico aparece como dos bandas oscuras separadas por una clara, con un espesor de 7,5, nm. Esta organización es común, además, al resto de membranas biológicas limitantes de los orgánulos celulares por lo que se denomina unidad de membrana. COMPOSICIÓN QUÍMICA Las membranas biológicas están constituidas mayoritariamente por lípidos (40%) y proteínas (60%), junto a una pequeña proporción de glúcidos. a) Lípidos de membrana: todos ellos son antipáticos, por lo que se orientan en presencia de agua. • Fosfolípidos: son los lípidos más abundantes. Poseen una zona hidrófila, que constituye las denominadas cabezas polares y otra zona hidrófoba, que forma la cola apolar. • Glucolípidos. Semejantes a los fosofolípidos. Aparecen solo en la cara externa de la membrana. • Colesterol. Abunda en las células animales. b) Proteínas de membrana: también son moléculas antipáticas, de manera que las zonas polares sobresalen en las superficies de las membranas, mientras que las regiones apolares se encuentran en el interior hidrófobo. Según su grado de asociación con los lípidos, se clasifican en: • Integrales: constituyen alrededor del 70% de las proteínas y están íntimamente asociadas a los lípidos. Algunas proteínas presentan hidratos de carbono unidos a ellas (glucoproteínas) y se disponen en la cara externa de la membrana. • Periféricas: están débilmente asociadas a los lípidos. Aparecen principalmente en la cara interna. c) Glúcidos de membrana: están unidos a los lípidos o a las proteínas, en forma de glucolípidos o glucoproteínas, y se encuentran sobresaliendo en la cara externa de la membrana. Forman una capa periférica que recibe el nombra de glucocálix, glicocálix o cubierta celular, que interviene en los procesos de reconocimiento y comunicación celular, y proporciona protección mecánica y química a la superficie celular. En el exterior del glucocálix se sitúa una capa secretada por la célula denominada matriz extracelular, rica en colágeno, elastina y otras proteínas, que permite la adhesión de las células y el mantenimiento de los tejidos. ESTRUCTURA DE LA MEMBRANA: MODELO DE MOSAICO FLUIDO. Después de conocida la composición de las membranas celulares, se propusieron diferentes modelos para explicar cómo están organizados sus componentes. En 1972, Singer y Nicholson, señalaron que la membrana no era una estructura rígida como se pensaba, sino fluida, y permitía el movimiento de las proteínas que podían encontrarse embebidas o asociadas a la bicapa de lípidos. Propusieron así un modelo, conocido como el modelo de mosaico fluido, vigente en la actualidad. Los lípidos de membrana, debido a su carácter antipático, se disponen formando una doble capa o bicapa lipídica, donde la parte polar de la molécula se coloca hacia fuera, en o con el agua, mientras que la parte no polar se orienta hacia el interior de la bicapa, evitando así el o con el agua. La bicapa lipídica es impermeable a las moléculas solubles en agua, de manera que actúa como barrera entre la célula y el medio y además es una estructura fluida, ya que los lípidos se pueden desplazar libremente dentro de la bicapa mediante distintos movimientos (difusión lateral, flexión, rotación y flip-flop).
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
5
La fluidez de la bicapa depende del grado de insaturación de sus cadenas hidrocarburadas (a mayor insaturación mayor fluidez), y a la presencia de colesterol, que inmoviliza parte de las cadenas hidrocarburadas de los fosfolípidos. Las proteínas integrales se encuentran dispersas, atravesando totalmente o parcialmente la doble capa de lípidos, con una disposición en mosaico. Las proteínas periféricas se sitúan sobre la superficie de la bicapa. Debido a la disposición de los lípidos y proteínas, las membranas celulares aparecen al microscopio electrónico con tres bandas: una banda central clara correspondiente a la bicapa lipídica, y otras dos bandas externas oscuras correspondientes a las regiones polares de las proteínas, que sobresalen de la bicapa. Así pues, el armazón básico de las membranas biológicas está formado por la bicapa lipídica, que actúa de barrera, mientras que las proteínas desempeñan funciones específicas actuando como receptoras de mensajes, transportadores de sustancias o enzimas.
Membrana al m.o. FUNCIONES DE LA MEMBRANA CELULAR La función principal de la membrana es actuar de límite celular,, y por tanto, separar el citoplasma y sus orgánulos del medio externo. Este papel no es pasivo, ya que la membrana actúa de barrera selectiva que regula el intercambio y transporte de sustancias entre el interior celular y el medio. La membrana celular además, cumple otras funciones: • Es responsable de la formación y control del gradiente electroquímico (diferencia de carga eléctrica) entre el interior y el exterior celular. • Intercambia señales con el medio externo y con otras células. • Interviene en la división del citoplasma o citocinesis. • Esta relacionada con la inmunidad celular, ya que en la membrana se localizan algunas moléculas con propiedades antigénicas, responsables por ejemplo del rechazo en el transplante de tejidos y órganos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
6
• Está relacionada con la captación de sustancias (endocitosis) y con la secreción de sustancias al exterior (exocitosis). Estos procesos implican la creación y destrucción de membrana celular.
6. LA PARED CELULAR
Las células vegetales poseen una envoltura externa a la membrana plasmática, altamente organizada y rígida, que constituye la pared celular. Composición y estructura La pared celular tiene dos componentes mayoritarios: • Un componente cristalino, constituido por fibras de celulosa. • Un componente amorfo, formado por una matriz de pectinas, hemicelulosa, glucoproteínas, agua, sales minerales y, en algunos casos, ligninas. En las células diferenciadas, la pared celular aparece como una estructura gruesa compuesta por varias capas, que se van depositando a medida que se produce el crecimiento celular: • Lámina media. Es la capa más externa y la primera en formarse después de la división celular, y puede ser compartida por dos células adyacentes. Está formada por pectinas y proteínas, unidas a iones de Ca2+. • Pared primaria. Es una gruesa capa presente en todas las células vegetales situada por debajo de la lámina media. Está formada por largas fibras de celulosa entrecruzadas y cohesionadas por hemicelulosa y pectinas. • Pared secundaria. Aparece en algunas tipos especiales de células vegetales (tejidos de soporte y vasculares) cuando finaliza el crecimiento celular y las células se hacen adultas. Se sitúa por debajo de la pared primaria, y consta de una mayor cantidad de fibras de celulosa que se ordenan paralelamente dando lugar a varias capas con distintas orientaciones. Carece de pectinas, y en ocasiones entran a formar parte de su composición otras polímeros, como la lignina (xilema y esclerénquima), ceras y cutina (haz de las hojas) o suberina (corcho). La pared celular de las células vegetales no es continua , ya que presenta una serie de canales denominados plasmodesmos, que permiten la comunicación y el intercambio de fluidos y moléculas. Los plasmodesmos pueden encontrarse en ocasiones en depresiones de la pared primaria (menos engrosada) y donde está ausente la pared secundaria. En este caso se llaman punteaduras. Funciones de la pared celular -
Confiere rigidez al organismo y contribuye al mantenimiento de la forma celular. Evita la rotura celular por choque osmótico, permitiendo a las células vegetales vivir en un medio hipotónico. Une las células adyacentes, conectando las células de los tejidos vegetales. Posibilita el intercambio de fluidos y la comunicación intercelular.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
-
7
Impermeabiliza la superficie vegetal en algunos tejidos, gracias a la cutina y a la suberina, evitando pérdidas de agua. Sirve de barrera frente al paso de agentes patógenos.
7. CITOPLASMA El citoplasma es todo el contenido celular, comprendido entre la membrana plasmática y la membrana nuclear. Está constituido por tres componentes: citosol o hialoplasma, el citoesqueleto y los diversos orgánulos celulares. 7.1. CITOSOL o HIALOPLASMA Es el líquido acuoso que baña el citoplasma. Contiene gran cantidad de sustancias disueltas: glucosa, aminoácidos, sales minerales, proteínas, etc. y su consistencia puede pasar de fluida (sol) a viscosa (gel). En el citosol se desarrollan ciertas reacciones metabólicas, como la glucolisis, la síntesis de glicógeno y las fermentaciones. Además en el citosol se pueden almacenar sustancias en forma de gránulos, denominadas inclusiones, como por ejemplo los depósitos de glicógeno, las gotas de grasa y algunos pigmentos. En este medio es donde se encuentran inmersos los orgánulos celulares y el citoesqueleto. 7.2. EL CITOESQUELETO El citoesqueleto está formado por una red de filamentos de proteínas, que se extiende por todo el citoplasma, sirviendo de soporte interno celular. El citoesqueleto determina la forma de la célula, su organización interna y su movimiento. Está formado por tres tipos de filamentos: •
Microfilamentos. Son los filamentos más delgados y están compuestos por la proteína actina. Los microfilamentos de actina intervienen en varios procesos, tales como la contracción muscular, la emisión de pseudópodos que posibilitan la fagocitosis y el movimiento ameboide y la formación del anillo contráctil que provoca el estrangulamiento de la célula al final de la división celular. Además mantienen la morfología de las microvellosidades del epitelio intestinal.
•
Filamentos intermedios. Presentan un diámetro intermedio entre los microfilamentos y los microtúbulos, y abundan especialmente en las células animales. Tienen una función estructural, como por ejemplo los filamentos de queratina que proporcionan fuerza mecánica a las células epiteliales y los neurofilamentos que dan resistencia a los axones de las neuronas.
•
Microtúbulos. Son los filamentos más gruesos, de 25 nm. de diámetro, y están formados por la polimerización de la proteína tubulina. Son cilindros huecos y se originan a partir de un punto o centro organizador de los microtúbulos (MTOC) o centrosoma. Los microtúbulos se pueden encontrar dispersos por todo el citoplasma, constituyendo parte del citoesqueleto, o bien formar estructuras estables como los centríolos que estudiaremos más adelante. Los microtúbulos abundan en la mayoría de las células y desempeñan varias funciones: − Contribuyen al mantenimiento de la forma celular y a la organización del citoesqueleto. − Participan en el transporte de orgánulos y partículas en el interior celular, actuando como carriles internos de la célula.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
8
−
Constituyen los elementos del huso acromático durante la división celular que permite el movimiento de los cromosomas. − Son los elementos estructurales de los centríolos y conforman el esqueleto interno de los cilios y flagelos.
7.3. CENTRIOLOS, CILIOS y FLAGELOS Los centríolos, cilios y flagelos son estructuras estables formadas por microtúbulos semejantes a los que constituyen el citoesqueleto, por eso se les considera orgánulos microtubulares.
Centríolos y centrosoma Son dos cilindros que aparecen en el interior del centrosoma o citocentro y no están rodeados por ninguna membrana. No están presentes en las células de los vegetales superiores. Cada centríolo está formado por nueve tripletes de microtúbulos, que se unen mediante una proteína, la nexina. Los centríolos se originan por duplicación de otros preexistentes, de forma que el nuevo centríolo se dispone perpendicular al original. Los centríolos están rodeados por un material denso o material pericentriolar (centrosfera), de donde irradian unos microtúbulos en todas las direcciones, que constituyen el áster. El conjunto formado por los dos centríolos, el material pericentriolar y el áster recibe el nombre de centrosoma o citocentro. En las células vegetales carentes de centríolos, los centrosomas aparecen como zonas densas de material amorfo. Los centríolos intervienen en la organización de los cilios y flagelos y del huso acromático, pero el material pericentriolar es el auténtico centro organizador de los microtúbulos del citoesqueleto.
Centriolos
Centrosoma
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
9
Cilios y flagelos Son apéndices móviles que aparecen en muchas células, que presentan una estructura común formada por tres elementos: el axonema, la placa basal y el corpúsculo basal. El axonema presenta nueve pares de microtúbulos dispuestos alrededor de un par de microtúbulos centrales (9+2), y el corpúsculo basal nueve tripletes (9+0). La diferencias entre los cilios y flagelos reside en la longitud, los flagelos son más largos y menos numerosos en las células. Además el mecanismo de movimiento es distinto, los flagelos se mueven describiendo ondas simples, mientras que los cirios presentan un movimiento más complejo de propulsión y retracción. Su función es la de provocar el desplazamiento de células aisladas (espermatozoides, protozoos), o el movimiento del líquido extracelular sobre la superficie de la célula o el arrastre de partículas (epitelio ciliar de la tráquea)
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
10
7.4. RIBOSOMAS Los ribosomas son pequeños gránulos, que están presentes en todo tipo de células, y en ellos se fabrican las proteínas en la fase de traducción de la información genética. No son orgánulos membranosos, y debido a su tamaño (200 Å de diámetro), solo son observables al microscopio electrónico. Los ribosomas de las células eucariotas (80 S) son mayores que los de las procariotas (70 S). Están compuestos por varias moléculas de ARN ribosómico (ARNr), asociadas a diferentes proteínas. Cada ribosoma está constituido por dos subunidades, una mayor (60 S en eucariotas y 50 S en procariotas) y otra menor (40 S en eucariotas y 30 S en procariotas). Las subunidades se originan por separado en el nucleolo y luego se combinan en el citoplasma cuando van a fabricar proteínas, para ello entre las dos subunidades queda un pequeño espacio donde se coloca el ARN mensajero (ARNm), portador de la información genética para la síntesis de proteínas. Los ribosomas se pueden localizar dispersos en el citosol o unidos a la cara externa del retículo endoplásmico rugoso. También aparecen en el interior de mitocondrias y cloroplastos. Suelen presentarse agrupados, formando polirribosomas o polisomas, donde todos los ribosomas traducen la misma molécula de ARN mensajero.
Polirribosoma
7.5. LOS ORGÁNULOS MEMBRANOSOS En la célula eucariota se pueden distinguir dos tipos de orgánulos con membrana atendiendo a su estructura y función: El retículo endoplásmico, el complejo de Golgi y las vesículas, que están formados por membranas ▪ simples e intervienen en la síntesis, clasificación y empaquetamiento de sustancias, así como en la digestión celular (lisosomas) y en la regulación osmótica (vacuolas). Se denomina sistemas de endomembranas al conjunto de orgánulos que están relacionados entre sí y con la membrana nuclear. Sus principales componentes son el retículo endoplásmico, el complejo de Golgi y la membrana nuclear. Debido a la conexión entre sus componentes, el sistema endomembranoso se podría considerar una red de cavidades que dividen el citoplasma en dos compartimentos: uno encerrado en el interior de las membranas y el otro situado fuera de ellas. Las mitocondrias, peroxisomas y los cloroplastos, implicados en el metabolismo energético, y ▪ constituidos, a excepción de los peroxisomas, por una doble mebrana. Las mitocondrias y los cloroplastos presentan ADN propio y ribosomas 70 S, por lo que se les ha atribuido un origen endosimbiótico y proceden de antiguas bacterias aerobias y cianobacterias respectivamente.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
11
7.5.1. RETÍCULO ENDOPLÁSMICO (RE) Es el componente más desarrollado del sistema de endomembranas celulares, y está formado por una serie de cavidades membranosas irregulares aplastadas y comunicadas entre sí. Se distinguen dos tipos de retículo, aunque están ampliamente intercomunicados: • Retículo endoplásmico rugoso (RER): localizado cerca del núcleo y formado por cavidades membranosas con forma de saco (sáculos), que presentan ribosomas adheridos a su cara externa. • Retículo endoplásmico liso (REL): más alejado del núcleo, y formado por estructuras membranosas tubulares (túbulos). Carece de ribosomas adosados.
Funciones biológicas • • • •
•
Actúa de soporte mecánico, al dividir en compartimentos el contenido acoso del citoplasma. Sirve de sistema de transporte intracelular de diferentes sustancias. Síntesis de lípidos: en el REL se fabrican los lípidos de membrana (fosfolípidos y colesterol) que luego son distribuidos por las diferentes estructuras membranosas de la célula. Síntesis de proteínas: en los ribosomas del RER se fabrican proteínas, que luego penetran en el interior de los sacos del retículo. Algunas de ellas pasan al REL y se transforman en lipoproteínas, y otras son transportadas hasta el Aparato de Golgi para transformarse en glucoproteínas. Detoxificación: el REL es capaz de metabolizar algunas toxinas liposolubles, transformándolas en compuestos menos tóxicos e hidrosolubles, para facilitar su eliminación por el organismo.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
12
7.5.2. APARATO o COMPLEJO DE GOLGI El aparato de Golgi es complejo membranoso que se suele situar cerca del núcleo, próximo al retículo endoplásmico, y en las células animales alrededor de los centríolos. Está formado por un conjunto de unidades, denominadas dictiosomas, en cada una de las cuales se distinguen los siguientes elementos: • Cisternas: vesículas aplanadas y agrupadas en pilas. • Vesículas de transición: pequeñas vesículas íntimamente asociadas a las cisternas, que sirven de vehículo de transporte de sustancias. Se sitúan en la cara del dictiosoma más próxima al RER (cara cis o de formación) • Vesículas de secreción: son vesículas de mayor tamaño que se sitúan en la cara del dictiosoma orientada a la membrana plasmática (cara trans o de maduración).
Función biológica El aparato de Golgi se encarga de dirigir el tráfico de macromoléculas, evitando la mezcla al azar de los centenares de enzimas, lo que produciría un caos metabólico en la célula. Además es el encargado de fabricar los lisosomas primarios, interviene en la secreción celular y participan en la formación de la pared celular vegetal. Su misión fundamental es la de transportar y concentrar las proteínas procedentes del RER, así como la de glucosilar (unir oligosacáridos) las proteínas y lípidos para producir glucoproteínas y glucolípidos. Así a la cara cis o de formación de los dictiosomas van llegando proteínas procedentes del RER encerradas en pequeñas vesículas de transición. Las proteínas van atravesando el dictiosoma de cisterna en cisterna, trnasportadas por otras vesículas, se les van añadiendo nuevos glúcidos y poco a poco maduran. Una vez completada su maduración, son clasificadas por grupos según su destino, y más tarde emitidas por la cara trans o de maduración encerradas en vesículas. Algunas forman vesículas de secreción que expulsan las proteínas al exterior; otras forman los lisosomas· y otras se unen a la membrana sirviendo de material de reparación.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
13
7.5.3. LISOSOMAS Los lisosomas son vesículas membranosas que están presentes en todas las células eucariotas, y en cuyo interior contienen gran cantidad de enzimas hidrolíticas o hidrolasas ácidas (porque actúan a un pH ácido) y que son capaces de digerir la mayoría de las macromoléculas biológicas, por lo que la función de estos orgánulos es digestiva. Una característica de la membrana de los lisosomas es que presentan una gran cantidad de glucoproteínas que les protegen del ataque de sus propias hidrolasas. Según su origen, los lisosomas se clasifican en dos tipos: • LISOSOMAS PRIMARIOS: son los que no han intervenido en el proceso digestivo. Proceden de las cisternas del aparato de Golgi. Estos lisosomas pueden verter su contenido fuera de la célula mediante exocitosis y digerir así material extracelular, lo que se denomina digestión extracelular. Así por ejemplo, los las células óseas van remodelando el hueso, y los espermatozoides pueden penetrar en las envolturas del óvulo gracias a un gran lisosoma primario llamado acrosoma. En otras ocasiones los lisosomas primarios se fusionan con otras vesículas portadoras de materiales exógenos o endógenos y se convierten en lisosomas secundarios. • LISOSOMAS SECUNDARIOS: son vesículas que realizan la digestión intracelular. En función del material sobre el que actúan pueden clasificarse en: − Vacuolas digestivas o heterofágicas. Resultan de la fusión de los lisosomas primarios con vesículas endocíticas que contienen materiales (nutrientes o microorganismos) que han sido incorporados a la célula por endocitosis. En el interior de las vacuolas digestivas las enzimas hidrolíticas ejercen su acción digestiva, y los productos de la digestión son aprovechados por la célula. Cuando la digestión es incompleta, queda una pequeña formación con sustancias no digeridas denominada cuerpo residual, que puede ser eliminada de la célula por exocitosis. Este tipo de digestión colabora en la nutrición celular y en la defensa contra microorganismos patógenos, como virus y bacterias. − Autolisosomas o vacuolas autofágicas. Proceden de la fusión de lisosomas primarios con vesículas originadas en el interior de la célula (autofagosomas) que rodean restos celulares u orgánulos inservibles. Las vacuolas autofágicas eliminan materiales inútiles y destruyen zonas lesionadas de la célula, asegurando el recambio de los componentes celulares y evitando la degeneración celular. Además también degradan el exceso de macromoléculas producidas por la célula. Intervienen también en procesos de metamorfosis, en los que se producen transformaciones de tejidos. Las vacuolas autofágicas aseguran, a su vez, la nutrición celular en condiciones de ayuno, en el que las células consumen sus propios materiales. Si la digestión es incompleta también se originan cuerpos residuales.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
14
7.5.4. VACUOLAS Las vacuolas son orgánulos rodeados de membrana y con un elevado contenido de agua, en los que se acumulan diversas sustancias. Aunque también existen en las células animales, están mucho más desarrolladas en las vegetales, donde el conjunto recibe el nombre de vacuoma. Las vacuolas proceden de vesículas derivadas del RE y del aparato de Golgi. Su membrana recibe el nombre de tonoplasto. El tamaño y forma de las vacuolas varía según el grado de desarrollo de la célula, de manera que a medida que la célula crece y envejece las vacuolas aumentan de tamaño y se unen gradualmente, por lo que muchas células adultas presentan una gran vacuola que ocupa la parte central del citoplasma (en algunos casos hasta el 90% del volumen celular). Las funciones que desarrollan en las células vegetales son muy variadas: − Sirven de almacén de reserva para diversos iones y sustancias, como glúcidos, aminoácidos, proteínas, pigmentos, así como productos tóxicos (alcaloides y compuestos aromáticos que sirven de defensa contra depredadores) y de desecho. − Contribuyen al mantenimiento de la turgencia celular y con ello se consigue aumentar el tamaño de la célula de forma económica acumulando agua. Esto incrementa la superficie celular y por tanto la capacidad de intercambio de sustancias con el medio. − Contienen enzimas lisosómicas. 7.5.5. PEROXISOMAS Inicialmente se los denominó microcuerpos, y se trata de pequeñas vesículas que contienen enzimas de oxidación (peroxidasas y catalasas). Su membrana se origina a partir del REL. Están presentes en todas las células eucariotas. Los peroxisomas están implicados en reacciones de oxidación y desempeñan un papel muy importante en la detoxificación, gracias a las enzimas que contienen. Las oxidasas oxidan una gran variedad de compuestos, como aminoácidos, ácidos grasos y purines, originando como subproducto peróxido de hidrógeno (agua oxigenada). RH2 + O2 → R + H2O2 (peróxido de hidrógeno) Las catalasas posteriormente utilizan el peróxido de hidrógeno para oxidar diversos compuestos tóxicos, como el etanol, los fenoles o el ión superóxido. H2O2 + CH3 – CH2OH → CH3 – CHO + 2 H2O Etanol
Acetaldehido
Este tipo de reacciones son muy importantes en el hígado y en el riñón, de manera que cerca de la mitad del etanol ingerido es oxidado a acetaldehído por las catalasas. Si existe exceso de peróxido de hidrógeno, dañino para la célula, es transformado también por las catalasas en agua y oxigeno. 2 H2O2 → 2 H2O + O2
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
15
7.5.6. MITOCONDRIAS Las mitocondrias son orgánulos rodeados por dos membranas, presentes en todas las células eucariotas. Son capaces de dividirse por sí mismas por estrangulación. En ellas se realiza el metabolismo respiratorio energético, cuya finalidad es la obtención de energía. Presentan un tamaño y forma variables, aunque generalmente son cilíndricas o alargadas, y su diámetro oscila entre 0,5 y 1 μm, y tienen una longitud máxima de 7 μm. El número de mitocondrias varía con el tipo de célula, y abundan en las células que precisan de una elevado cantidad de energía, como las fibras musculares, hepatocitos o los ovocitos. Estructura y composición • • •
•
De fuera hacia dentro, en las mitocondrias se pueden distinguir los siguientes elementos: Membrana mitocondrial externa: es lisa y permeable, gracias a la presencia de porina. Espacio perimitocondrial: se localiza entre las dos membranas y tiene una composición semejante al citosol. Membrana mitocondrial interna: presenta una serie de pliegues, dirigidos hacia el interior, denominados crestas mitocondriales. Es más impermeable a los iones que la membrana externa. En ella se encuentran las cadenas de transporte electrónico y las ATP sintetasas, denominadas partículas elementales F1, que constan de una cabeza dirigida hacia el interior de la mitocondria y un pequeño pedúnculo. Matriz mitocondrial: contiene ADN mitocondrial circular, ARN y ribosomas de coeficiente de sedimentación semejante al de las bacterias. Incluye, además, diversas enzimas que intervienen en el ciclo de Krebs y en la β-oxidación de los ácidos grasos y transportadores de electrones, como el NADH.
Función biológica La función de las mitocondrias es la obtención de energía para la célula, por lo que se pueden considerar como las centrales energéticas celulares. Esta función se halla compartimentada en la matriz mitocondrial y en la membrana mitocondrial interna, donde suceden diversos procesos. • En la matriz mitocondrial tienen lugar: − La β-oxidación de los ácidos grasos y la descarboxilación oxidativa del ácido pirúvico. Ambos procesos generan Acetil-CoA y moléculas reducidas (NADH + H+ y FADH2 ). − El ciclo de Krebs, donde mediante un ciclo de reacciones químicas se oxida el Acetil-CoA a CO2, obteniéndose intermediarios metabólicos y moléculas reducidas (NADH + H+ y FADH2 ). • En la membrana mitocondrial interna se realiza la cadena de transporte electrónico, cuya función es transportar electrones desde las moléculas reducidas anteriores hasta el oxígeno. Este transporte de electrones genera una energía que es utilizada por las ATPasas de las crestas mitocondriales para sintetizar ATP mediante el proceso de fosforilación oxidativa.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
16
7.5.7. CLOROPLASTOS Los cloroplastos forman parte de un conjunto de orgánulos membranosos característicos de las células vegetales que se denominan plastos o plastidios. Los plastos son orgánulos con doble membrana capaces de sintetizar y acumular diferentes sustancias. Pueden ser de tres tipos: • Leucoplastos: son plastos incoloros, que almacenan sustancias de reserva, como almidón grasas, etc. Abundan sobre todo en las raíces y en los rizomas. • Cromoplastos: son plastos coloreados que contienen abundantes pigmentos carotenoides (carotenos y xantofilas), responsables del color característico de frutos como el tomate, zanahoria, limón, etc., y de las flores. • Cloroplastos: son orgánulos verdes que fabrican y acumulan clorofila, que están relacionados con el metabolismo fotosintético. Su forma tamaño y distribución varía de unas células a otras y con las especies: las células de las algas suelen poseer un solo cloroplasto muy voluminoso y las plantas superiores contienen entre 20 y 40 cloroplastos por célula, y su forma más frecuente es ovoide. Los cloroplastos son más grandes que las mitocondrias: su tamaño oscila entre 2 y 10 μm.
Estructura de los cloroplastos La estructura de un cloroplastos consta de tres elementos característicos: • Envoltura. Formada por una membrana plastidial externa, muy permeable, y una membrana plastidial interna menos permeable. Ambas membranas son continuas y delimitan completamente al cloroplasto. Las dos membranas están separadas por un espacio intermembranoso. • Estroma. Es la región rodeada por la membrana plastidial interna. El estroma contiene ADN circular doble, ribosomas 70 S, granos de almidón e inclusiones lipídicas. En él se localizan enzimas implicadas la fijación del CO2 , como la ribulosa 1,5-difosfato-carboxilasa oxidasa (RuBisCo) y otras que participan en el ciclo de Calvin. • Tilacoides y grana. Se encuentran inmersos en el estroma. Son una serie de sacos membranosos que se disponen paralelos al eje mayor del cloroplasto. Se pueden presentar de dos formas: > Tilacoides de los grana: pequeños sacos lenticulares que se apilan formando grupos llamados grana. > Tilacoides del estroma o lamelas: vesículas alargadas que atraviesan el estroma conectando los grana entre sí. Todo el sistema de tilacoides están interconectado y forma un compartimento interno que recibe el nombre de espacio tilacoidal. Las membranas de los tilacoides contienen los pigmentos fotosintéticos, principalmente clorofilas, carotenoides y otros pigmentos asociados. Los pigmentos fotosintéticos se asocian en dichas membranas con proteínas formando los fotosistemas, que actúan como órganos captadores de luz que despreden electrones. Además en las membranas tilacoidales se localizan las cadenas de transporte electrónico y las ATPasas implicadas en el proceso de fotofosforilación.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
17
Función de los cloroplastos Los cloroplastos son los orgánulos donde tiene lugar la fotosíntesis oxigénica. En la fotosíntesis, la célula vegetal utiliza la luz como fuente de energía, el CO2 como fuente de carbono y el H2O como donador de electrones y fabrica materia orgánica desprendiendo oxígeno. La fotosíntesis abarca dos fases: • Fase luminosa: sucede en la membrana de los tilacoides y se producen una serie de reacciones que convierten la luz en energía química (ATP) y poder reductor (NADPH + H+). Para ello es imprescindible la presencia de pigmentos que absorben la luz y de H2O que cede electrones. • Fase oscura: sucede en el estroma y tiene lugar la fijación del CO2 y su reducción a moléculas orgánicas mediante el Ciclo de Calvin, utilizando el ATP y el NADPH obtenidos en la fase anterior. Las moléculas orgánicas obtenidas se almacenan en forma de polisacáridos, principalmente almidón. Todas estas reacciones suceden sin la presencia de luz.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
18
8. EL NÚCLEO CELULAR 8.1. CARACTERÍSTICAS GENERALES El núcleo es una estructura membranosa característica de las células eucariotas, que alberga la información genética (ADN) y fabrica el ARN, antes de su salida al citoplasma, donde se producirá la síntesis de proteínas. Esta separación espacial supuso un acontecimiento de especial importancia en el transcurso de la evolución, ya que dio lugar a la célula eucariota, la unidad funcional de los seres vivos superiores. En las células eucariotas el núcleo actúa como centro de control: interviene activamente en el desarrollo y división de la célula, y regula la organización, diferenciación y especialización celular. La mayoría de las células poseen un solo núcleo, que ocupa por término medio un 10% del volumen celular. Excepcionalmente, existen células plurinucleadas, que según su origen, pueden ser de dos tipos: sincitios, que resultan de la unión de varias células uninucleadas, como las fibras musculares; o plasmodios, originados por sucesivas divisiones del núcleo, sin que se divida el citoplasma, como sucede en los huevos de los insectos. La morfología del núcleo es muy variada; aunque predominan las formas esféricas u ovales, es posible encontrar núcleos fusiformes, aplanados, arrosariados, ramificados e incluso fragmentados. El núcleo se localiza, por lo general, en el centro de la célula. En algunos casos, sin embargo, puede aparecer desplazado por otros orgánulos, como en las células vegetales, que está apartado por la vacuola, o en las células secretoras, que se encuentra en la base. El tamaño del núcleo está en relación directa con el citoplasma, de manera que si el volumen de uno aumenta, también lo hará el otro. La relación entre el volumen del núcleo y del citoplasma es lo que se denomina relación nucleoplasmática (RNP), que se expresa de la siguiente manera:
RNP =
Vn Vc − Vn
Vn = volumen del núcleo
Vc = volumen celular
La relación nucleoplasmática es constante para cada célula y depende de la función celular. Cuando la RNP alcanza un valor mínimo se inicia la división celular. 8.2. ESTRUCTURA y COMPOSICIÓN DEL NÚCLEO DEL NÚCLEO INTERFÁSICO La estructura y composición del núcleo varía a lo largo de la vida de una célula (ciclo celular), diferenciándose dos períodos: período de división o mitosis, durante el que una célula se divida para originar células hijas, y período de interfase o de no división, durante el cual el ADN se transcribe y la célula realiza su actividad normal. A continuación vamos a estudiar la estructura y composición del núcleo en interfase o núcleo interfásico. El núcleo interfásico consta de los siguientes componentes: envoltura nuclear, nucleoplasma, nucleolo y cromatina.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
19
Envoltura nuclear La envoltura nuclear deriva del RE y está formada por dos membranas concéntricas, externa e interna, separadas por un espacio perinuclear. La membrana externa está conectada y se continua con el retículo endoplásmico rugoso. Por debajo de la membrana nuclear interna se observa una lámina nuclear fibrosa formada por filamentos intermedios, que interviene en la organización de la cromatina y en su desaparición y nueva formación durante la mitosis. Ambas membranas se comunican por medio de poros nucleares (80 nm de diámetro), a través de los cuales se produce el intercambio de moléculas grandes, como el ARN y las proteínas, entre el núcleo y el citoplasma. Cada poro está rodeado por un anillo de bloques de proteínas dispuestos en forma octogonal. En el centro del anillo contiene un material amorfo y denso formado por finas fibrillas. Todo el conjunto constituye el complejo del poro, lo que significa que los poros nucleares no son simples aberturas, sino que seleccionan específicamente las moléculas que lo atraviesan. Desde el interior nuclear, a través de los poros, pasan al citoplasma moléculas de ARN mensajero y las subunidades de los ribosomas, mientras que desde el citoplasma pasan al núcleo nucleótidos, proteínas ribosómicas y enzimas implicadas en la duplicación y transcripción.
Nucleoplasma El nucleoplasma, también llamado carioplasma, el es medio interno acuoso donde se encuentran inmersos los demás componentes del núcleo. Está compuesto por proteínas, principalmente enzimas relacionadas con la duplicación del ADN y la transcripción a ARN.
Nucleolo El nucleolo es una estructura esférica visible en el interior del núcleo interfásico, que carece de membrana. Su función principal es la síntesis y ensamblaje de las subunidades de los ribosomas. Algunas células presentan más de un nucleolo. El nucleolo está compuesto de proteínas y ácidos nucleicos, ADN (1- 3%) y ARN (10 – 30%). Estructuralmente, en cada nucleolo se distinguen dos zonas: • Zona fibrilar: ocupa la parte central. Contiene ADN y ARN. El ADN nucleolar que contiene los genes para la síntesis de ARNr y puede formar parte de cromosomas distintos constituye el organizador nucleolar, y contínuamente se está transcribiendo a moléculas de ARNr, originando unas estructuras plumosas. • Zona granular: ocupa la parte periférica. En esta zona las moléculas de ARNr se combinan con proteínas para originar las subunidades ribosómicas 60 S y 40 S, que posteriormente emigrarán al citoplasma atravesando los poros nucleares y se unirán formando ribosomas completos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
20
Nucleolo y formación de ribosomas Estructuras plumosas del organizador nucleolar
Cromatina La cromatina está compuesta por ADN plegado, asociado a proteínas básicas: las histonas. En la cromatina el ADN se asocia a las histonas y forma unos complejos denominados nucleosomas. Cada nucleosoma contiene ocho moléculas de histonas que forman un núcleo central cilíndrico, donde se enrolla la molécula de ADN, que da dos vueltas alrededor de dicho cilindro. Se podría decir que los nucleosomas son las “unidades estructurales” de la cromatina. Al observar una fibra elemental de cromatina al microscopio electrónico se distingue una fibra de “cuentas” ensartadas, semejante a un collar (estructura de collar de perlas). Cada una de las “cuentas” equivale a un nucleosoma (ADN-histonas), y entre cada unidad hay un fragmento de ADN libre que correspondería al “hilo” del collar. La cadena de nucleosomas es la unidad o fibra elemental de cromatina, de unos 10 nm de grosor. Esta fibra elemental se enrolla helicoidalmente hasta formar un solenoide o fibra de 30 nm, que contiene seis nucleosomas por cada vuelta de hélice. La fibra de 30 nm es la cromatina tal como se visualiza al microscopio electrónico. A su vez las fibras de 30 nm se pliegan en el núcleo formando bucles radiales, que se van compactando y enrollando sucesivamente durante la división del núcleo, hasta formar los cromosomas metafásicos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
21
Eucromatina y heterocromatina
Cromatina y collar de perlas
Tipos de cromatina • Eucromatina. De aspecto laxo o difuso, corresponde a zonas de cromatina activas (aproximadamente, el 10% de la cromatina celular), donde se produce la transcripción. • Heterocromatina. De aspecto más denso, son zonas de cromatina condensada (el 90% del total), que corresponde a zonas inactivas que no se transcriben. A su vez se distinguen dos tipos de heterocromatina: constitutiva, que aparece condensada siempre durante todo el ciclo celular, y cuyo ADN no se transcribe nunca; y facultativa, cuya condensación depende del estado de desarrollo del organismo y del tipo de célula, y cuyos genes se inactivan a lo largo de la diferenciación celular. La heterocromatina facultativa es escasa en tejidos embrionarios y aumenta cuando se especializan las células. 8.3. LOS CROMOSOMAS Estructura y composición Cuando una célula se divide por mitosis, la cromatina se condensa, originando los cromosomas. Los cromosomas son estructuras cilíndricas que representan el máximo grado de empaquetamiento del ADN, y por tanto, de la cromatina. Durante la metafase de la mitosis, cada cromosoma está formado por dos partes o cromátidas iguales (que se corresponden con dos filamentos de cromatina idénticos), y unidas por un estrechamiento denominado centrómero. Los extremos de las cromátidas se denominan telómeros, y en ellos se encuentran secuencias repetitivas de ADN cuya función es asegurar la integridad del cromosoma y evitar la pérdida de información genética en la duplicación. El centrómero recibe también el nombre de constricción primaria, y en él se encuentran el cinetocoro, que es una placa de
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
22
proteínas donde se conectan los microtúbulos del huso acromático durante la mitosis. Existen otras zonas de estrechamiento, denominadas constricciones secundarias, algunas de las cuales corresponden a los organizadores nucleolares y por tanto contienen genes para la síntesis de ARN ribosómico. Estas constricciones son constantes en su posición y tamaño, por lo que resultan útiles para identificar los cromosomas. Algunos cromosomas (cromosomas-SAT) presentan zonas esféricas denominadas satélites separadas del resto del cromosoma por una constricción secundaria. El centrómero divide cada cromátida en dos brazos, los brazos cromosómicos. Según la posición del centrómero y la longitud de los brazos, los cromosomas se dividen en cuatro tipos: • Metacéntricos: centrómero central y brazos iguales. Durante la anafase aparecen en forma de V. • Submetacéntricos: un brazo más largo que el otro. Durante la anafase aparecen en forma de L. • Acrocéntricos: cromosomas con forma de bastón, con un brazo muy corto y otro muy largo. Durante la anafase mantienen su forma cilíndrica. • Telocéntricos: cromosomas con el centrómero situado en uno de los extremos, por lo que solo presenta un brazo distinguible. Cariotipo El cariotipo es el conjunto de rasgos característicos de los cromosomas de cada especie (tamaño, forma, número, etc.). Cada cromosoma o pareja de cromosomas se designa con un número, excepto los cromosomas sexuales que se denominan con las letras X e Y. Así pues el cariotipo de una célula presenta dos tipos de cromosomas: • Autosomas: cromosomas ordinarios, iguales en individuos masculinos y femeninos, que no deciden el sexo del individuo. • Heterocromosomas o cromosomas sexuales: son normalmente una pareja de cromosomas, diferente según el sexo. Así en la especie humana, se distinguen dos cromosomas sexuales: el cromosoma X y el cromosoma Y. El primero está presente en los dos sexos, y el segundo es propio del sexo masculino. Así pues en la especie humana el cariotipo femenino esta formado por 44 autosomas + XX, y el masculino es 44 autosomas + XY. La representación gráfica del cariotipo, ordenados los cromosomas de mayor a menor, se denomina idiograma o cariograma.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
23
Células diploides y haploides El número de cromosomas es constante en cada especie, y según esto, las células pertenecientes a una especie determinada pueden ser de dos tipos: • Diploides (2n): presentan dos cromosomas iguales (en forma y tamaño) de cada tipo, denominados cromosomas homólogos, ambos tienen los genes para los mismos caracteres. Estas células presentan por tanto dos series o dotaciones de cromosomas, cada una de ellas heredada de un progenitor. • Haploides (n): presentan solo una serie o dotación de cromosomas, todos diferentes entre sí, por lo que no presentan cromosomas homólogos. Así pues, en una célula diploide, los cromosomas están en parejas y hay dos genes para cada carácter (genes alelos), mientras que en una haploide todos los cromosomas son distintos y hay un solo gen para cada carácter. Por ejemplo, en la especie humana, las células somáticas (no intervienen en la reproducción) tienen 46 cromosomas, pero como son 2n, en realidad se trata de 23 parejas. Los gametos humanos (óvulos y espermatozoides), al ser n, tienen 23 cromosomas todos distintos. Algunos organismos tienen células poliploides, en las que el número de cromosomas de cada tipo es mayor de dos.
CARIOTIPO HUMANO
Los grupos que comprende el cariotipo humano son los siguientes: - Cromosomas grandes Grupo A, (cromosomas 1, 2 y 3), meta y submetacéntricos Grupo B, (cromosomas 4 y 5), submetacéntricos - Cromosomas medianos Grupo C, (cromosomas 7, 8, 9, 10, 11, 12 y además los cromosomas X), submetacéntricos Grupo D, (cromosomas 13, 14 y 15) acrocéntricos - Cromosomas pequeños Grupo E, (cromosomas 16, 17 y 18) submetacéntricos Grupo F, (cromosomas 19 y 20) metacéntricos Grupo G, (cromosomas 21 y 22) acrocéntricos Por acuerdo los cromosomas sexuales X e Y se separan de sus grupos correspondientes y se ponen juntos aparte al final del cariotipo.
I.E.S. Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
1
TEMA 2. LA CÉLULA: ESTRUCTURA y FUNCIÓN 1. ¿Cuántas veces es más grande el volumen de una célula eucariota globosa de 20 μ de diámetro que una bacteria tipo coco de 2 μ de diámetro?. 2. Un hepatocito humano posee un volumen aproximado de 5.000 μm3. Sabiendo que el porcentaje de volumen celular ocupado por el núcleo de esta célula es del 6%, calcula la relación nucleoplasmática (RNP). 3. Qué estructura u orgánulo celular desempeña las siguientes funciones dentro de la célula: a) Fabrica las proteínas b) Dirige el funcionamiento de la célula c) Forma los lisosomas d) Fabrica los lípidos de membrana e) Selecciona las sustancias dentro de la célula f) Da forma a las células animales g) Realiza la fotosíntesis h) Almacena sustancias de reserva y) Forma los cilios y flagelos j) Distribuye las sustancias fabricadas en el retículo endoplásmico k) Almacena granos de almidón l) Fabrica el ARN ribosómico m) Digiere nutrientes que toma la célula del medio externo 4. Identifica la letra entrecomillada de los siguientes ejercicios: 4.1 La “A” es una lámina que separa los medios intra y extracelular. Químicamente está constituida por una bicapa de “B” donde se incrustan las “C”. Esta lámina posee unas terminaciones glucídicas, muy ramificadas que forman el “D”. En las células vegetales, además de la lámina anteriormente citada, hay una envoltura gruesa: la “E”, formada principalmente por “F”. 4.2. Los “A” son orgánulos celulares constituidos por dos “B” de diferente tamaño. Poseen agua, proteínas y “C”. Varios de estos orgánulos se suelen unir una cadena de ARN mensajero, y a este conjunto se le denomina “D”. Los orgánulos en cuestión se encuentran libres en el “E”, o unidos a la membrana externa del “F” que, en este caso, recibe el nombre de “G”. 4.3. Los cilios y flagelos de las células animales derivan de unos orgánulos cilíndricos denominados “A”, y cuando estos se encuentran agrupados se disponen perpendicularmente formando el “B”. Este conjunto está rodeado por la “C”, de la que parten unos filamentos que se disponen radialmente: el “D”. Cada “E” está formado por “F” grupos de 2 ó 3 microtúbulos. Esta disposición contrasta con la de los “G” y “H” que, además tienen “Y” microtúbulos centrales. 4.4. Rodeando al núcleo celular o al centrosoma se suele encontrar un orgánulo celular denominado “A”, que está formado por unos sáculos aplanados que se originan del “B”, y que se agrupan formando los “C”. Este orgánulo forma vesículas cargadas de enzimas, los “D”, que se unen a los fagosomas y, con éstos, constituyen las “E”. 4.5. Las “A” están separadas del “B” por una doble membrana. La interna se invagina formando las “C”. El espacio interno o “D” es rico en enzimas, posee “E” circular y unos ribosomas denominados “F”. 4.6. Los “A” son unos orgánulos que no se encuentran en las células “B”. Presentan una doble membrana y en su interior hay un tercer tipo de membrana que se dispone formando saquitos discoidales llamados “C”. El espacio interno o “D” contiene enzimas, polisacáridos. ADN “F” y pequeños “G” que fabrican proteínas.
I.E.S. Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
2
4.7. El “A” es el que controla y gobierna todas las funciones celulares de la célula. Está constituido por una membrana (prolongación del “B”) que presentan una serie de “C” que comunican el medio interno de este o “D” con el “E”. También posee uno o varios “F”. Dispersas en su interior se encuentran unas masas densas de ADN unidas a proteínas, que son los filamentos de “G”. 4.8. Los “A” son los componentes celulares responsables de la información genética. En metafase se observan formados por dos “B” idénticas unidas por el “C”, que divide a los “A” en dos partes llamadas “E”, si son muy desiguales “F” y si uno de ellos no se aprecia se denomina “G”. 5. Ordena de mayor a menor tamaño las siguientes formas vivas: virus; ribosoma; núcleo; mitocondrias; óvulo humano; glóbulo rojo; bacteria. 6. Por ultracentrifugación es posible separar los diferentes componentes celulares y, generalmente, cuanto mayor sea el tamaño de la estructura celular menor será la fuerza centrífuga necesaria para sedimentarla. ¿En qué orden sedimentarán los siguientes componentes celulares?: mitocondrias, lisosomas, núcleos, proteínas y ribosomas. 7. Responde verdadero o falso a las siguientes cuestiones y explica el por qué: a) Los ribosomas están formados por ADN, ARN y proteínas. b) El retículo endoplásmico siempre tiene adosado ribosomas a su cara externa. c) Las vesículas de Golgi contienen proteínas que provienen del retículo endoplásmico. d) Los lisosomas son orgánulos exclusivos de las células vegetales que contienen enzimas formadas por el ergatoplasma. e) En las mitocondrias hay ADN monocatenario circular. f) La clorofila se encuentra dispersa en el estroma de los cloroplastos. g) La estructura del cilio es similar a la del flagelo. h) El conjunto de centrosoma, centrosfera y áster se llama centriolo. i) Los peroxisomas son orgánulos ricos en una hormona llamada peroxidasa. 8. En el interior de ciertos orgánulos, más pequeños que las mitocondrias, hay gran cantidad de enzimas que utilizan el oxígeno celular como aceptor de electrones y, como consecuencia, se forma una sustancia tóxica que debe ser eliminada. Esta sustancia es rápidamente reducida mediante una enzima cuya actuación produce agua y oxígeno. a) ¿De qué sustancia tóxica se trata?. b) ¿Cómo se llama la enzima que transforma esta sustancia?. c) ¿Cuáles son los orgánulos a los que se refiere el párrafo anterior?. 9. De las estructuras y orgánulos que se citan a continuación, hay algunos que no los poseen las células vegetales, otros de los que carecen, y los hay presentes en ambos tipos de células. Indica dónde aparecen cada uno de ellos: cloroplastos, mitocondrias, granos de glucógeno, ribosomas, pared celular, cilios, cromosomas, vacuolas, granos de almidón, centriolos, aparato de Golgi, peroxisomas, nucleolo.
I.E.S. Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
3
Cuestiones de selectividad • Dibuja, mediante un esquema, la estructura de una mitocondria. Indica sus componentes y explica las funciones biológicas de este orgánulo./ Estructura y función del retículo endoplásmico. • Indica qué orgánulos están delimitados por doble membrana. ¿Todas las células contienen dichos orgánulos?. Razona la respuesta./ A partir de un dibujo del núcleo, se pide identificarlo, identificar sus partes y describir su función. ¿Es posible hallarlo en todas las células?. • Estructura y funciones del citoesqueleto./A partir de un dibujo del Modelo de Mosaico fluido de la membrana plasmática se pide: Identificar las moléculas señaladas y definir su naturaleza química; Señalar las funciones principales de la membrana. • De las siguientes estructuras, indica las que son características de células animales, las que corresponde a células vegetales y las que son comunes a ambas, razonando la respuesta: a) Membrana plasmática, b) Pared celular. c) Cloroplastos. d) Mitocondrias. e) Centrosoma. f) Vacuolas. /Desarrolla la siguiente propuesta: “Cromatina y cromosomas son dos estados del mismo material nucleosómico”. • Indique si las siguientes afirmaciones son verdaderas o falsas, razonando la respuesta: a) Los componentes dominantes de los ribosomas son: agua, fosofolípidos y polisacáridos. b) Solo algunos ribosomas están adheridos a biomembranas. c) Todos los ribosomas tienen el mismo coeficiente de sedimentación. D) Las dos subunidades de los ribosomas son funcionales cuando están separadas. • Clasifica los orgánulos de una célula eucariota según sean membranosos, no membranosos o energéticos. Dibuja un esquema del Aparato de Golgi, denomina sus partes y explica las principales funciones de dicha estructura endomembranosa. • Representa mediante un dibujo, la arquitectura molecular de la membrana plasmática y denomina sus componentes. ¿Estimas que puede establecerse alguna relación entre la membrana plasmática y los lisosomas?. Razona la respuesta. • Describe, con ayuda de un esquema, la estructura y principales características de una célula eucariota animal. Indica un proceso fisiológico celular en el que participe el centrosoma./Dibuje una célula bacteriana y otra vegetal e indique las principales diferencias entre ellas. • Teniendo en cuenta que el retículo endoplasmático (RE) es una estructura membranosa intracelular, contesta a las siguientes cuestiones: a) ¿Qué dos propiedades del RE coexisten en la célula?. Si tuviera que observar una célula al microscopio electrónico, ¿qué característica morfológica le permitiría diferenciar una modalidad de la otra?. ¿Qué funciones básicas desarrolla cada una de los dos tipos de RE?. ¿Estima que el RE es exclusivo de células animales, de vegetales o de ambos tipos de células?. Razone la respuesta.
TEMA 3. LA REPRODUCCIÓN CELULAR 1. EL CICLO CELULAR 1.1. LA INTERFASE. MUERTE CELULAR. 1.2. LA MITOSIS 1.3. LA CITOCINESIS o CITODIÉRESIS 2. LA MEIOSIS 3. MITOSIS, MEIOSIS y REPRODUCCIÓN 4. DIFERENCIAS ENTRE MITOSIS y MEIOSIS 5. MEIOSIS y CICLOS BIOLÓGICOS
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
2
1. EL CICLO CELULAR El aumento en tamaño de los seres vivos superiores sólo es posible por un aumento en el número de células que los forman. Cuando una célula adquiere un tamaño adecuado, se divide para originar dos células hijas. El ciclo celular es el tiempo que transcurre desde que una célula se forma por división de una preexistente hasta que se divide y origina dos células hijas. La duración del ciclo es muy variable, como se expone en el siguiente cuadro:
El ciclo celular se divide en dos fases muy definidas: Interfase y mitosis o fase M.
1.1. LA INTERFASE Es la fase más larga del ciclo celular, ya que ocupa casi el 94 % de él, y transcurre entre dos mitosis, razón por la que también se la denomina intermitosis. En ella la célula aumenta de tamaño, expresa su mensaje genético y realiza una intensa actividad biosintética a todos los niveles. Desde el punto de vista citológico, la interfase se caracteriza por la ausencia de cromosomas visibles, visualizándose solo la cromatina. En la interfase se distinguen tres etapas: FASE G1: este período transcurre entre el final de una mitosis y el inicio de la síntesis o duplicación del ADN. En ella la célula aumenta de volumen hasta alcanzar el tamaño de su forma celular típica, aumenta el número de orgánulos celulares y fabrica y acumula las sustancias necesarias para la división celular. En un cierto momento de esta fase se alcanza el punto de no retorno o punto R, en el cual la célula ya está obligada a realizar todo el proceso. Una vez sobrepasado dicho punto la célula continua el ciclo hacia la fase siguiente. Previamente al punto R hay una fase de reposo o fase G0, y su duración depende de numerosos estímulos externos (nutrientes, cambios de temperatura, alteraciones de la membrana, ...). Hay células que permanecen de por vida en el estado G0, y que han sufrido un importante proceso de diferenciación, como las neuronas y las fibras musculares estriadas. Al final de la etapa G1, se produce una activa síntesis de proteínas (histonas y no histonas) y nucleótidos y enzimas necesarios para la duplicación del ADN. FASE S: en esta etapa se duplica el ADN del núcleo, y como resultado de ello, cada cromosoma que se origine en la mitosis estará formado por dos cromátidas idénticas (cada una con una molécula de ADN) unidas por el centrómero. Primero de replica la eucromatina y después la heterocromatina, más condensada. La duración de esta fase depende del tipo de célula y la temperatura. En los mamíferos dura unas siete horas. FASE G2: tiene una duración muy corta (alrededor de tres horas en mamíferos), y en ella la célula aumenta ligeramente de tamaño. Se transcriben y traducen genes que codifican las proteínas necesarias para la división celular y se duplican los centríolos. Al final de esta fase las células se redondean. La fase G2 finaliza en el momento en que se inicia la condensación de los cromosomas para comenzar la mitosis.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
3
Etapas del ciclo celular y mecanismos de control a lo largo del ciclo celular
FACTORES QUE CONTROLAN EL CICLO CELULAR A lo largo del ciclo celular existen una serie de puntos de control que actúan como frenos, que impiden a la célula continuar el ciclo si no está lo suficientemente preparada. Los tres principales puntos de control se encuentran: Al final de la etapa G1. El punto R o de no retorno es el primer punto de control del ciclo celular, donde la célula evalúa si está preparada para dividirse o no. Al final de la etapa G2. La célula evalúa si está preparada para entrar en mitosis. Este punto de control actúa como mecanismo de seguridad que garantiza que solamente entren en mitosis aquellas células que hayan completado la duplicación de todo su material genético. Durante la mitosis, en la metafase, existe un tercer punto de control, en el que la célula no continuará la mitosis si los cromosomas no están perfectamente alineados en el huso acromático, antes de empezar a separarse por sus cromátidas. En el control del ciclo celular intervienen diferentes factores que interactúan entre sí, que pueden hacer que la célula detenga su crecimiento y división. Algunos de los principales factores que controlan el ciclo celular son: 1. ENZIMAS: intervienen dos proteínas clave, las ciclinas y las proteínas quinasas dependientes de ciclinas (Cdk). Las proteínas quinasas (Cdk) se asocian con distintas ciclinas en las diferentes etapas del ciclo celular, formando el complejo CdK-ciclina. La activación de este complejo dispara procesos que conducen a la célula a través de las distintas etapas del ciclo. La degradación de las ciclinas inactiva el complejo. 2. FACTORES DE CRECIMIENTO (GF): son diferentes proteínas que actúan como hormonas, que activan los genes que intervienen en la proliferación celular, entre ellos los protooncogenes, que inducen a la célula a entrar en la Fase S y en división.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
4
3. FACTORES GENÉTICOS: existen diferentes genes que controlan el ciclo celular, entre ellos: Protooncogenes: intervienen en el crecimiento y la división celular. Genes supresores de tumores: detienen el ciclo celular, impidiendo la proliferación celular y por tanto las formación de tumores. Gen p53: paraliza el ciclo celular ante cualquier alteración del ADN. (leer artículo sobre gen p53) Gen p27 Una mutación en estos genes provocarían una división incontrolada de las células y la formación de tumores cancerosos. En muchos casos la presencia de genes alterados conduce a la proliferación descontrolada de las células que se encuentra en el origen de todo cáncer. 4. OTROS FACTORES: Tamaño celular: el crecimiento estimula a la célula a dividirse. o con otras células: el o con otras células impide el crecimiento celular y por tanto inhibe la división. Edad: a mayor edad, menor será el número de veces que las células se dividan en un cultivo. Oxigenación: la falta de oxigenación puede producir la muerte celular por necrosis. LA MUERTE CELULAR Las células no se multiplican indefinidamente, dependiendo del tipo celular se da un número limitado de divisiones. Cuando esto sucede la célula entra en una fase de senescencia (Fase G0) hasta que muere de forma programada, mediante un mecanismo denominado apoptosis celular. La apoptosis es un proceso necesario, ya que permite la renovación celular, de manera que las células muertas son reemplazadas por nuevas células jóvenes. Dicho proceso ha de estar controlado, tanto por factores externos del medio, como por factores internos de la propia célula. Si este control deja de producirse origina un descontrol en el ciclo celular que conduce a algunas patologías, como el Cáncer, Alzheimer, Parkinson y la Cardiopatía isquémica. Cuando las células mueren por un daño irreparable (infección, falta de O 2, lesión grave, presencia de toxinas,...) hablamos de necrosis celular, que provoca inflamación en la zona y esta acaba cicatrizando. Las dos formas de muerte celular, apoptosis y necrosis, originan diferentes fenómenos en la célula, tal y como muestra la figura:
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
5
1.2. MITOSIS La Mitosis o Fase M es una período de gran actividad celular. En él se produce la división nuclear o cariocinesis, y los cromosomas duplicados se distribuyen de manera idéntica en cada una de las células hijas mediante un estructura formada por microtúbulos denominada huso acromático. Al final de la mitosis se originan dos células hijas idénticas genéticamente y con la misma dotación cromosómica que la célula madre.
Etapas de la mitosis (cambios que se producen) PROFASE: Condensación de las fibras de cromatina y formación de los cromosomas. Cada cromosoma se formará a partir de dos fibras de cromatina idénticas genéticamente, generando cada una de ellas las dos cromátidas del cromosoma. Desaparición progresiva del nucleolo Formación de una nueva pareja de centríolos, de manera que las dos parejas de centríolos se desplazan a ambos polos de la célula quedando unidas por los filamentos del HUSO ACROMÁTICO o HUSO MITÓTICO. Entre las fibras del huso acromático se pueden diferenciar dos tipos: Fibras polares: van de un polo a otro de la célula Fibras cromosómicas: se unen a los cromosomas por el cinetocoro Entrada de agua en el núcleo celular, lo que provoca que se hinche y la membrana nuclear acabe rompiéndose, de manera que al final de la profase el núcleo ha desaparecido como estructura. METAFASE: Las fibras cromosómicas del huso acromático se alargan y provocan que los cromosomas se dispongan en el centro del huso acromático, formando la PLACA ECUATORIAL. Durante la metafase los cromosomas alcanzan su máximo grado de condensación, denominándose cromosomas metafásicos, cada uno de ellos con dos cromátidas, tal y como hemos estudiado. ANAFASE: Las fibras del huso acromático se acortan, provocando la separación de las dos cromátidas de cada cromosoma (cromátidas hermanas). Al final de la anafase existen dos grupos de cromátidas hermanas, uno a cada lado de la célula. Estas cromátidas, constituyen en sí cromosomas de una sola cromátida (cromosomas anafásicos). Los dos grupos de cromátidas son genéticamente idénticos. TELOFASE: Cada grupo de cromátidas o cromosomas anafásicos se va rodeando de fragmentos de membrana nuclear procedentes del retículo endoplásmico. Los cromosomas se van estirando y poco a poco se vuelven a convertir en filamentos de cromatina. Progresivamente se va formando un nuevo nucleolo, alrededor de cada nuevo núcleo. El huso acromático desaparece. Al final de la telofase la célula presentará dos núcleos claramente diferenciados, pero genéticamente idénticos.
1.3. CITOCINESIS o CITODIÉRESIS La división celular no termina con la mitosis, con ella se ha repartido la dotación genética de la célula, pero aún es necesario que el citoplasma se divida entre las dos células hijas y se repartan los orgánulos celulares de la manera más equitativa posible. Este proceso es la citocinesis o citodiéresis, y ocurre de forma diferente en las células animales y vegetales. Está sincronizada con la mitosis y se realiza al final de la telofase.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
6
a) Células animales: la división del citoplasma se realiza por estrangulamiento. En el centro de la célula se origina una especie de anillo contráctil que estrangula a la célula hasta que se cierra y provoca la separación de las células hijas. b) Células vegetales: la división de citoplasma se produce por tabicación. Entre los dos núcleos formados se origina una especie de tabique (fragmoplasto) a partir de vesículas del Aparato de Golgi, que separará las dos células hijas.
2. MEIOSIS ( R! ) La meiosis es una forma de división o reproducción celular mediante la cual, una célula madre se divide dos veces consecutivamente originando cuatro células hijas, con la mitad de cromosomas que la célula madre de la que proceden y genéticamente distintas entre sí. La meiosis solamente se produce en células diploides (células 2N), originando células hijas haploides (células N). En nuestro organismo las únicas células que se dividen por meiosis son las células madre de los gametos, espermatogonias y ovogonias, (células2N), generando así los espermatozoides y óvulos (células N). Fases de la meiosis MEIOSIS I o Fase reduccional (1ª división). Se generan dos células con la mitad de cromosomas que la célula madre PROFASE I: es la etapa más larga de la meiosis. Se distinguen los siguientes períodos: Leptotene: las cromátidas se condensan para formar cromosomas. Zigotene: los cromosomas homólogos se disponen por parejas (apareamiento de cromosomas homólogos) y se unen en determinadas zonas denominadas sinapsis. Paquitene: es cuando se produce la máxima condensación de los cromosomas. Se produce el intercambio de información genética (RECOMBINACIÓN GENÉTICA) entre cromátidas NO hermanas de cromosomas homológos, mediante un fenómeno físico denominada SOBRECRUZAMIENTO o ENTRECRUZAMIENTO. Diplotene: los cromosomas homólogos de cada pareja comienzan a separarse. Cada cromosoma tendrá cromátidas genéticamente distintas debido a la recombinación genética. Diacinesis: los cromosomas homólogos de cada pareja han completado su separación. Se rompe la membrana nuclear y se forma el huso acromático.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
7
METAFASE I: los cromosomas homólogos se colocan por parejas en el centro de la célula formando la PLACA ECUATORIAL. ANAFASE I: se separan los cromosomas homólogos de cada pareja, se forman dos grupos de cromosomas, cada uno con DOS cromátidas, y genéticamente distintos, uno a cada lado de la célula. Recuerda que las dos cromátidas de cada cromosoma son genéticamente distintas. TELOFASE I: al final de esta etapa se originan dos células hijas con la mitad de cromosomas que la célula madre de la que proceden y genéticamente distintas. Además son células N, ya que NO presentan parejas de cromosomas homólogos. MEIOSIS II (2ª división). Se trata de una mitosis normal, con sus correspondientes etapas (PROFASE II, METAFASE II,...). Al final de esta segunda división se originarán cuatro células, dos por cada una de las que se formaron en la 1ª división, todas ellas haploides (células N), con la mitad de cromosomas que la célula madre original y genéticamente diferentes.
3. MITOSIS, MEIOSIS y REPRODUCCIÓN Tanto la mitosis como la meiosis son dos tipos de división celular, sin embargo tienen una función diferente: La mitosis interviene en el crecimiento, la renovación celular y la regeneración de tejidos dañados en los organismos pluricelulares, y en la reproducción asexual de los organismos. La meiosis es imprescindible en la reproducción sexual, ya que gracias a ella se originan las células reproductoras o gametos. Además permite mantener el número de cromosomas generación tras generación y aporta un aumento de la variabilidad genética gracias a la recombinación genética entre cromosomas homólogos y a la distribución al azar de los cromosomas entre los gamitos (la fecundación al azar de los gamitos sería el tercer factor que aumenta la variabilidad genética).
4. DIFERENCIAS ENTRE MITOSIS y MEIOSIS MITOSIS Se produce UNA DIVISION celular
MEIOSIS Se producen DOS DIVISONES celulares consecutivas, sin interfase por medio. La célula madre origina DOS células hijas idénticas La célula madre origina CUATRO células hijas entre sí, y con igual número de cromosomas que la diferentes genéticamente y con la mitad de célula madre cromosomas que la célula madre En la PROFASE I se produce el La PROFASE se realiza SIN SOBRECRUZAMIENTO. SOBRECRUZAMIENTO de cromosomas homólogos NO hay RECOMBINACIÓN GENÉTICA. y la RECOMBINACIÓN GENÉTICA En METAFASE NO se emparejan los cromosomas En METAFASE I se EMPAREJAN los cromosomas homólgos homólogos En ANAFASE I se separan los cromosomas En ANAFASE se dividen los cromosomas por sus homólogos de cada pareja, formándose grupos de cromátidas, generando cromosomas con una sola cromosomas con dos cromátidas a cada lado de la cromátida célula La mitosis es la forma de división de las CÉLULAS La meiosis es la forma de división que origina las SOMÁTICAS CÉLULAS REPRODUCTORAS o GAMETOS Afecta a células 2N y N Afecta solamente a células 2N, originando células N
Biología y Geología 2º Bachillerato
8
Tema 3. La reproducción celular
5. MEIOSIS y CICLOS BIOLÓGICOS
CICLO DIPLONTE: Meiosis GAMETOGÉNICA Formación gametos ADULTO (2N)
R!
Gametos (N) Fecundación ZIGOTO (2N)
CICLO HAPLONTE: Meiosis ZIGÓTICA Sucede después de la formación del zigoto ADULTO (N)
Gametos (N) Fecundación
R!
ZIGOTO (2N)
CICLO DIPLOHAPLONTE: Meiosis ESPOROGÉNICA Formación de esporas ESPOROFITO (2N)
R!
Esporas (N)
ZIGOTO (2N) Fecundación
Gametos (N)
GAMETOFITO (N)
Mitosis y citocinesis vegetal
Mitosis y citocinesis animal
Las dos cromátidas del cromosoma profásico
Fibras (microtúbulos) del áster
Nuevo centríolo en formación
Fibras polares o continuas
Envoltura nuclear fragmentada PRINCIPIO DE LA PROFASE
PROFASE Cromosomas dispuestos en la placa ecuatorial
Fibras cromosómicas constituidas por microtúbulos cinetocóricos
PROFASE Semihuso Interzona
Cromosomas orientados por las fibras del huso
Semihuso
FINAL DE LA PROFASE
METAFASE Complejo centriolar
Fibras (microtúbulos) interzonales
Semihuso acortado
PRINCIPIO DE LA ANAFASE
Inicio de la nueva envoltura nuclear Interzona alargada
Surco de división Cilindros de sustancia densa
Semihuso acortado FINAL DE LA ANAFASE
INICIO DE LA TELOFASE
Cilindros de sustancia densa
Anillo contráctil
FINAL DE LA TELOFASE
Mitosis y citocinesis por estrangulación de una célula 2 n en que n 5 2.
Cromosomas homólogos
Inicio de la sinapsis
Nódulo de recombinación produciendo un entrecruzamiento Bivalente
Centrómero
PROFASE I
Bivalente (5 tétrada) Paquiteno
Zigoteno
Leptoteno
METAFASE I
Diacinesis
Diploteno
ANAFASE I
Quiasma: unión temporal resultante de un entrecruzamiento. Aparece en la desinapsis.
TELOFASE I
Las dos cromátidas hermanas de un solo cromosoma Bivalente: las cuatro cromátidas de los dos cromosomas homólogos unidos Citocinesis e intercinesis PROFASE II
METAFASE II
ANAFASE II
n
n
n TELOFASE II
Meiosis de una célula 2 n en que n 5 2.
n
Gen P53, asesino y policía MALÉN AZNÁREZ 27/01/2008 Es la estrella de los genes, un supergén temido y amado al tiempo, porque de su actuación depende que se desarrollen, o no, algunos de los cánceres más frecuentes. Policía y asesino, a p53 le persiguen médicos, investigadores y grandes laboratorios. Ahora se ha descubierto que también puede influir en el envejecimiento. Es una historia fascinante. Una historia en la que un malo, malísimo, un perfecto asesino, se convierte de repente en bueno, buenísimo, en un magistral guardián del bien. Pero, como el famoso protagonista de Stevenson, sigue siendo al mismo tiempo Dr. Jekyll y Mr. Hyde, a ratos asesino, a ratos policía. También es una historia con un toque calvinista de la que, en algún momento, se desprende la idea de que todo lo bueno esconde su parte de maldad. Y es una historia con suspense, porque en el aire flota un posible premio Nobel difícil de adjudicar. Por si fuera poco, en-globa bajo el mismo techo a dos de los ogros del siglo: el cáncer y el envejecimiento. Aunque lo parezca, no es un relato policiaco. Es sólo la trayectoria apasionante de un gen, el más famoso de todos los genes, un supergén. Porque p53, que así se llama el protagonista, ha conseguido traspasar la barrera investigadora de genetistas, bioquímicos, biólogos moleculares y médicos, para saltar a los medios de comunicación no especializados. Se le conoce como el guardián del genoma, el policía de los oncogenes, el gen asesino, el gen protagonista y muchas cosas más. Todavía es joven, no ha cumplido aún 30 años, lo que en investigación es una nadería, y por eso sorprende su rápida fama. En 1993 fue declarado “el gen más importante del año” y, desde entonces, no ha hecho más que ganar terreno. Es el único gen al que se dedica en exclusiva un congreso internacional cada dos años. Se le ha estudiado, y se le estudia, en todos los aspectos que puedan imaginarse, y su posible manipulación es una diana codiciada por los grandes laboratorios farmacéuticos del mundo que buscan contrarreloj un fármaco que se perfila cercano. ¿Qué le hace tan fascinante? El investigador Manuel Serrano, jefe del grupo de Supresión Tumoral del Centro Nacional de Investigaciones Oncológicas (CNIO), que lleva años trabajando en p53, lo tiene clarísimo. “Es un gen clave; por eso es la estrella de los genes”. La explicación de Serrano, como la de tantos investigadores que en todo el mundo se dedican al “gen estrella”, es sencilla: p53 es clave, porque es el gen que con más frecuencia se encuentra mutado en el cáncer. Para que haya un cáncer p53 tiene que estar inactivado, y lo está en el 55% de los cánceres más comunes: mama, colon, pulmón, vejiga, linfoma. “P53 es un gen que se activa sólo en situación de estrés, cuando hay daño en una célula. Es un detector de situaciones peligrosas, un sensor; por eso se le llama “guardián” o “policía”, porque cualquier alteración que haya en la célula, y hay muchas asociadas al cáncer, lo activa. Entonces, p53 bloquea o mata la célula alterada, impide su proliferación o división celular. En definitiva, imposibilita la propagación de la célula dañada por apoptosis (suicidio celular) o porque la mantiene bloqueada sin dejarla reproducirse”, explica Serrano. Crucial a la hora de prevenir el cáncer, p53 es un gen anticanceroso que en circunstancias normales nos defiende de la enfermedad. Cuando fue descubierto, en 1979 (su nombre se debe a que la proteína que lo codifica tiene un peso molecular aproximado de 53.000), entró enseguida a formar parte de la lista de los genes malos, los oncogenes o genes causantes del cáncer. Pero, en 1989, pasó a integrar el grupo de los buenos, el de los supresores tumorales que inhiben o detienen la división celular —el cáncer se produce por una acumulación de daños genéticos originados por células que se multiplican sin control—. Pasó que su primera identificación se hizo con una de sus formas mutadas, y nocivas, no con su estado natural. Esta curiosa doble función puede tener la culpa de que aún no se haya concedido el Nobel a los supresores tumorales, como se hizo en su día con los oncogenes. Quizá porque, como se pregunta Serrano, “¿a quién se lo dan?, ¿a los tres investigadores que descubrieron una versión mutada y pensaron que era un oncogén, o a quien, una década después, se dio cuenta de que era un gen supresor?
¿P53 es igual en todos los humanos? “Sí, en general, pero no es idéntico; hay minúsculas variaciones que tienen un pequeño impacto en su función”, dice Serrano, que añade: “Una cosa es clara: un cáncer no puede existir con p53 funcionando a tope”. Y el investigador señala un hecho importante recientemente descubierto que viene a añadir brillo al gen estrella. “Sabíamos que p53 está relacionado con el cáncer, y ahora se ha demostrado que también lo está con el envejecimiento”. Y es en esta faceta en la que el grupo de Serrano, junto con el de María Blasco, también del CNIO, investiga con notables resultados publicados en Nature. Su laboratorio ha fabricado unos superratones modificados genéticamente, con más p53, que son más resistentes al cáncer. “Eso era lo esperado, pero la novedad fue ver que esos animales envejecían más lentamente, vivían un poco más. Eso nos hizo pensar que p53 también podía estar protegiendo del envejecimiento. Una forma de explicarlo sencillamente es decir que el daño causado en la célula, del tipo que sea —de alta intensidad, asociado al cáncer, o de baja intensidad, asociado al envejecimiento—, es el responsable de que haya cáncer y haya envejecimiento. Y p53 estaría noqueando ese daño, disminuyéndolo”. En resumen: p53 protege del cáncer, pero también hace que el envejecimiento se retrase. Así que el famoso gen no sólo es vital para que, haciendo de policía o asesino, nuestro organismo desarrolle, o no, alguno de los cánceres más habituales, sino que, además, si pudiéramos aumentarlo sin contrapartidas perversas, podría ralentizar nuestro envejecimiento. Dos pájaros de un tiro. ¿Se puede hacer? Manuel Serrano sonríe: “¡Es el sueño! Y pensamos que manipulando unos pocos genes podría aumentarse muchísimo la longevidad”. Hasta llegar a los superratones del laboratorio de Serrano, se había demostrado que ratones manipulados genéticamente con p53 por investigadores estadounidenses estaban protegidos del cáncer, pero envejecían prematuramente. Eso hizo pensar que el beneficio anticanceroso de p53 tenía su contrapartida perversa obligada: más envejecimiento. Pero el equipo de Serrano demostró que sus ratones, además de estar protegidos del cáncer, vivían más tiempo. “De alguna manera”, dice el investigador, “la resistencia al cáncer y al envejecimiento tienen que estar sincronizada. Los ratones, en su entorno natural, para el que han sido seleccionados por la evolución, viven muy poco tiempo: seis meses. Los humanos somos de los mamíferos más longevos, tenemos una de las mejores resistencias al cáncer y al envejecimiento, pero la maquinaria molecular de un ratón y un humano es la misma. Eso quiere decir que en esta maquinaria tiene que haber alguna manera de sincronizar ambas cosas, y p53 podría ser el medio. Si se aumenta la potencia de p53, se está luchando contra el envejecimiento y aumentando la resistencia al cáncer simultáneamente”. En esta línea, Serrano recuerda que los genomas de un chimpancé y un humano son prácticamente idénticos en el 99,8%. Sin embargo, la vida máxima de un chimpancé es de 60 años y el humano rara vez sobrepasa los 110. La media de un chimpancé es de 40 años, y la de un humano, de 80. “Debe de haber algo muy sutil en nuestros genes que cambia el hecho de vivir 50 años a vivir 100. Entonces, junto con el equipo de María Blasco, nos disponemos a hacer unas manipulaciones genéticas para ver si somos capaces de aumentar la longevidad en los ratones mucho más. Ése es nuestro desafío. Si conseguimos que un ratón que en el entorno privilegiado de un laboratorio llega a vivir tres años pase a vivir seis, sería una prueba de que la longevidad es algo flexible y sabríamos cómo aumentarla”. ¿Manipular el p53 para estar más jóvenes? “Ésa sería otra posibilidad, prevenir o ralentizar el envejecimiento, pero por ahora es sólo una simple posibilidad, aunque se intuye cercana”, dice Serrano. “Nosotros usamos p53, que es la estrella del cáncer, pero la estrella de la longevidad es la telomerasa, y ahora, combinando ambos genes, hemos visto que los ratones viven mucho más tiempo. Pero éste es un proyecto que dirige María Blasco”. María Blasco, jefa del grupo de Telómeros y Telomerasa del CNIO, lo sabe casi todo sobre el llamado “gen de la inmortalidad”. No en balde, ha sido una de las investigadoras pioneras en el panorama internacional de la telomerasa, una enzima que, cuando se le pone a una célula normal, la convierte en inmortal, ya que se encarga de mantener los telómeros, unas estructuras que están al final de los cromosomas y que con la edad se van perdiendo. Y cuando alguien se queda sin telómeros en las células, no hay división posible de éstas. “No existe vida sin telómeros; si a una especie se le quita la telomerasa, desaparece. Es algo fundamental para la vida y también para la célula tumoral”, apostilla Blasco.
Así que parece obligado preguntar a la bióloga molecular si en esta batalla que tienen emprendida, conjuntamente contra el cáncer y el envejecimiento, es sólo cuestión de ponerle telomerasa a un ratón para hacerlo inmortal. “La respuesta es no, porque la telomerasa hace que haya más cáncer. Para que haya un tumor, tiene que activarse la telomerasa, y si un ratón tiene más telomerasa de lo normal, por ejemplo, haciendo ratones transgénicos, sabemos que tendrá más tumores. Lo que hemos hecho es utilizar los superratones de Manuel, porque el p53 protege del cáncer y alarga en un 18% la vida de los ratones, y si a eso le añadimos el gen de la inmortalidad, la telomerasa, conseguimos que estos ratones multitransgénicos vivan una media de un 50% más, sin cáncer, lo que son palabras mayores. Eso es lo que hemos descubierto ahora”. Palabras mayores. Porque esta prolongación de vida, de un 50%, en los superratones es la más larga que se ha descrito en mamíferos. Más de lo que se consigue con la restricción calórica, que es uno de los mecanismos más importantes para alargar la vida. “No hemos conseguido todavía hacer ratones inmortales, lo que quiere decir que probablemente haya más cosas, y ése es el siguiente paso. Ésta es la primera vez que se revela un efecto de la telomerasa en la longevidad. En ningún organismo, ni gusano, ni levadura, se había visto; sólo en células”, asegura Blasco, sin ocultar su satisfacción. Se sabía que la telomerasa es un gen que tiene que ver con el envejecimiento y que, cuando se quita, el organismo envejece antes. “Pero lo que no se sabía, al menos nadie lo había demostrado hasta ahora, es que, cuando se aumenta, también aumenta de forma notable la vida del ratón, que es un mamífero. Y hemos visto que si eliminamos el cáncer y a la vez aumentamos la telomerasa, conseguimos alargar mucho más su vida”, dice Blasco, que añade que en humanos, muy probablemente pasaría lo mismo. “Con seguridad, los dos procesos, cáncer y envejecimiento, han coevolucionado. Nos hace mucha ilusión ir extendiendo la vida en ratones, porque probablemente haya que tocar pocas cosas para cambiarla. Esto no es un mero juego genético; si conseguimos identificar la combinación de genes que alargan la vida de un ratón, podremos pensar en diseñar nuevos fármacos que hagan lo mismo en humanos”. Los deseos de Blasco son en estos momentos el sueño de cientos de investigadores en todo el mundo, pero sus trabajos pueden parecer todavía muy básicos y alejados de resultados, a corto o medio plazo, para tratamientos oncológicos. Pero no es así. P53 se ha convertido en una de las más perseguidas dianas de los grandes laboratorios farmacéuticos que buscan aceleradamente un fármaco inteligente capaz de actuar en la curación del cáncer. Y ya se perfilan resultados. En este terreno se hallaría Nutlin, un compuesto activador de p53 (fabricado por Roche) que se está probando en humanos y que entra en el apartado de las llamadas “drogas inteligentes”—está diseñada específicamente, se conoce su estructura tridimensional y cómo activa p53 con todo tipo de detalles—. Pero por el momento es todavía una droga, con problemas pendientes de solución para llegar a la categoría de fármaco, y no se utiliza en tratamientos oncológicos, pero los expertos confían en que podrá hacerse pronto. “La idea al utilizar esta droga, u otras similares, es activar p53 en los tumores donde es funcional pero está dormido”, dice Manuel Serrano, que se declara optimista en cuanto al tiempo que falta para poder usar estos nuevos fármacos. Un poco más cauto, Miguel Ángel Piris, director del programa de Patología Molecular del CNIO, reconoce que hay diversos compuestos como Nutlin que buscan activar p53 y se encuentran ya en ensayos clínicos para testar su utilidad en pacientes. “Pero una cosa es que en el laboratorio sean útiles para las células, e incluso tumores inducidos en ratones, y otra que tengamos un protocolo razonable para tratar pacientes. Además, los ensayos clínicos con drogas nuevas están muy regulados y requiere bastante tiempo alcanzar datos sólidos que justifiquen su uso clínico”. Todavía es pronto para hablar de fármacos, pero donde ya se utiliza habitualmente p53 es en el diagnóstico de algunos tumores como el de mama, donde cerca de un 20% o 30% de casos han perdido p53 frente a otros que no. ¿Cuál es el interés de identificar mutaciones de p53? “En muchos casos, porque identifican formas de cáncer que son más agresivas y que posiblemente requieran una terapia distinta, dado que el cáncer progresa más rápidamente y son pacientes que van a tener una respuesta más pobre a la terapia”, afirma Piris, que trabaja en linfomas. “Es un factor de pronóstico, pero no es un factor predictivo. Nos permite identificar a pacientes
que van a tener una evolución clínica más agresiva, pero, en la mayoría de los casos, lo que no sabemos todavía es cómo tratar adecuadamente a estos enfermos”. Los tipos de tumores en los que la mutación de p53 es más frecuente son los de ovario, esófago, colorrectal, cabeza y cuello, y pulmón. Y los pronósticos más desfavorables están asociados a los de pulmón, vejiga, linfomas y sarcomas. Pero Piris, que forma parte de un grupo internacional que acumula datos sobre mutaciones de p53 desde hace casi veinte años (en 500 casos de linfoma han visto que la mutación estaba presente en el 20% de los casos, y eso se correlacionaba con un pronóstico desfavorable), es optimista. “Hasta hace poco, no sabíamos siquiera que existieran mutaciones frecuentes en este gen o qué función tenía en las células normales o neoplásicas. Ahora conocemos más acerca de su función y cómo se inactiva, bastante acerca de la frecuencia de las mutaciones, y experimentalmente cómo se puede bloquear el efecto de esas mutaciones. Espero que en un futuro seamos capaces de recorrer de forma rápida el camino que va del conocimiento a la terapia”. Dado que el organismo humano está siempre expuesto a daños exógenos, además de los endógenos —en nuestras células hay a veces errores accidentales—, es bueno saber si se conocen agentes externos, como el alcohol, el tabaco, los insecticidas o la contaminación industrial, que faciliten la mutación de p53. “Lo cierto es que tanto el tabaco como la radiación ultravioleta han sido incriminados como potenciales mutágenos de p53. El cáncer de pulmón en los fumadores tiene un patrón característico de mutaciones de p53 que sugiere daño al ADN debido a los efectos de los carcinógenos del tabaco. Un fenómeno parecido se observa en las mutaciones de p53 en los tumores cutáneos atribuidos a la radiación solar”, afirma Piris, que añade sonriente: “Pero si pudiéramos inducir la activación de p53 nativo —no el mutado que ejerce como oncogén—, desaparecería el problema”. Doble juego, asesino y guardián. © Diario EL PAÍS S.L. - Miguel Yuste 40 - 28037 Madrid [España] - Tel. 91 337 8200 © Prisacom S.A. - Ribera del Sena, S/N - Edificio APOT - Madrid [España] - Tel. 91 353 7900
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
1
ACTIVIDADES UNIDAD 3. LA REPRODUCCIÓN CELULAR 1. Desde que una célula se origina hasta que se divide en dos células hijas, hay dos etapas claramente diferenciadas en el ciclo celular. a) ¿Qué nombre recibe cada una de esas etapas?. b) ¿En qué fases se divide cada etapa?. c) ¿En qué momentos del ciclo celular hay cambos en la cantidad de ADN?. d) Pon un ejemplo de célula que no experimente división celular una vez que ha alcanzado la diferenciación. 2. Relaciona los conceptos de ambas columnas: Célula somática Célula haploide Fase M Duplicación del ADN Cromosoma anafásico Célula diploide Gameto División celular Fase Go Una cromátida Cromosoma metafásico Dos cromátidas Fase S Diferenciación celular 3. La colchicina es una droga que inhibe la polimerización de la tubulina y, por tanto, la formación de microtúbulos. ¿Qué efectos tendrá sobre la mitosis?. 4. ¿Cuántas células se formarán después de 30 mitosis consecutivas, sufridas por todas y cada una de las células resultantes de una célula inicial?. 5. Las células hepáticas de cierta especie animal poseen dos cromosomas metacéntricos y dos telocéntricos. a) ¿Pueden tener los óvulos de las hembras de esta especie, solamente dos cromosomas metacéntricos? b) ¿Y las células renales? 6. Se sabe que, en los eucariotas, cada cromátida está constituida por una sola molécula de ADN. Indica el número de estas moléculas de ADN en las siguientes células de una especie con 2n = 6. a) Un espermatozoide. b) Una célula en metafase mitótica. c) Una célula en periodo G1. d) Una célula en periodo G2. e) Una célula en profase de la segunda división meiótica. 7. ¿Cómo se genera la variabilidad genética en la reproducción sexual?.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
2
DIBUJOS y ESQUEMAS 8. Dibuja una célula 2n = 4 en anafase mitótica. 9. Dibuja una célula 2n = 6 en estado de profase y anafase mitóticas y en profase I y anafase I meióticas.
10. En qué etapa de la mitosis se encuentran las siguientes células: A
B
C
11. La célula representada se encuentra en una etapa de la Meiosis. Indica de qué etapa se trata. ¿Qué diferencia encuentras entre esta misma etapa en Mitosis y Meiosis?.
12. La gráfica representa la variación en el contenido de ADN durante el ciclo celular. Responde: a) ¿Qué ocurre en el intervalo de tiempo 2 a 3?. ¿Cómo se denomina la fase que transcurre en ese intervalo?. b) ¿La gráfica corresponde a un ciclo mitótico o meiótico?. ¿Porqué?.
Biología 2º Bachillerato
ACTIVIDADES DE REFUERZO TEMA 3. REPRODUCCIÓN CELULAR 1. Observa la grafica y contesta: a) ¿Qué representa la gráfica?. Explica cómo cambia el contenido de ADN desde la fase A hasta la G. b) ¿Qué función tiene el cambio de contenido de ADN?. Suponiendo que los cromosomas se vieran visibles a lo largo de todo el ciclo, ¿en qué fases desde la C a la G, de la gráfica 1 encontrarías las estructuras cromosómicas (1 a 4) que se muestran en la figura 2?.
2. Las figuras (A-O) representan diferentes etapas de la meiosis masculina de una planta 2n = 6. Establece el orden correcto en que suceden.
3. El esquema representa de forma muy simplificada varios aspectos del comportamiento cromosómico en la primera división meiótica en un organismo 2n = 8. Identifica los procesos numerados 1, 2 y 3.
Biología 2º Bachillerato 4. En la figura aparecen tres células anafásicas (A, B y C) de una especie animal 2n = 6. ¿En qué división se encuentran cada una de ellas (mitosis, 1º división meiótica, 2ª división meiótica)?. Razona la respuesta.
5. En la figura aparecen tres células (A, B y C) de una especie animal 2n = 6. ¿En qué fase de la mitosis o de la meiosis está cada una de ellas?. Razona la respuesta.
6. En siguiente esquema representan una fase concreta del proceso meiótico. Explica razonadamente de qué fase y de qué división se trata. ¿Cuántos quiasmas se han producido como mínimo en este meiosis?. ¿Cuántos cromosomas tendrá el organismo adulto al que pertenece esta célula?.
TEMA 4. LA NUTRICIÓN CELULAR: EL METABOLISMO 1. VISIÓN GLOBAL DE LA NUTRICIÓN CELULAR 2. CAPTURA e INGESTIÓN DEL ALIMENTO: EL INTERCAMBIO DE SUSTANCIAS ENTRE EL INTERIOR y EL EXTERIOR DE LA CÉLULA 2.1. INTERCAMBIO DE PEQUEÑAS MOLÉCULAS e IONES A TRAVÉS DE LA MEMBRANA
• •
Transporte pasivo Transporte activo
2.2. INTERCAMBIO DE MACROMOLÉCULAS y PARTÍCULAS
• •
Endocitosis Exocitosis
3. INTRODUCCIÓN AL METABOLISMO CELULAR 3.1. CARACTERÍSTICAS DE LAS REACCIONES METABÓLICAS 3.2. CATABOLISMO Y ANABOLISMO 3.3. TIPOS DE METABOLISMO 3.4. LA ENERGÍA EN LAS REACCIONES METABÓLICAS: LA IMPORTANCIA DEL ATP
4. REGULACIÓN DE LAS REACCIONES METABÓLICAS: LAS ENZIMAS 4.1. CONCEPTO DE CATÁLISIS y DE ENZIMA 4.2. ACCIÓN ENZIMÁTICA 4.3. CINÉTICA ENZIMÁTICA 4.4. FACTORES QUE INFLUYEN EN LA VELOCIDAD DE LAS REACCIONES ENZIMÁTICAS 4.5. MECANISMOS PARA AUMENTAR LA EFICACIA ENZIMÁTICA 4.6. REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA 4.7. CLASIFICACIÓN DE LAS ENZIMAS
5. CATABOLISMO 5.1. INTRODUCCIÓN AL CATABOLISMO: LA OXIDACIÓN 5.2. CATABOLISMO DE LOS GLÚCIDOS 5.2.1. LA GLUCÓLISIS 5.2.2. LA RESPIRACIÓN AEROBIA
• • • •
Formación del acetil-CoA El ciclo de Krebs La cadena respiratoria Balance energético de la oxidación completa de la glucosa
5.2.3. LA FERMENTACIÓN
• •
Fermentación láctica Fermentación alcohólica
5.3. CATABOLISMO DE LÍPIDOS
•
β-oxidación de los ácidos grasos
5.4. CATABOLISMO DE PROTEÍNAS 5.5. CATABOLISMO DE ÁCIDOS NUCLEICOS
6. ANABOLISMO
6.1. LA FOTOSÍNTESIS 6.1.1. LOS PIGMENTOS FOTOSINTÉTICOS Y LOS FOTOSISTEMAS 6.1.2. MECANISMO GENERAL DE LA FOTOSÍNTESIS
• •
Fase luminosa Fase oscura
6.1.3. BALANCE GLOBAL DE LA FOTOSÍNTESIS 6.1.4. FOTOSÍNTESIS BACTERIANA 6.1.5. FACTORES QUE INFLUYEN EN LA FOTOSÍNTESIS 6.1.6. IMPORTANCIA DE LA FOTOSÍNTESIS 6.2. LA QUIMIOSÍNTESIS 6.3. OTRAS RUTAS ANABÓLICAS
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
1
1. VISIÓN GLOBAL DE LA NUTRICIÓN CELULAR Mediante las funciones de nutrición, la célula toma materia y energía del medio, y las transforma con dos objetivos: fabricación de nuevos materiales celulares y obtención de energía para realizar diferentes trabajos. En consecuencia, la nutrición celular comprende los siguientes procesos: entrada de materiales (ingestión y digestión), transformación de los mismos (metabolismo) y eliminación de productos (excreción y secreción). Ingestión y digestión. La ingestión es la entrada de nutrientes en la célula por diferentes mecanismos que veremos más adelante. Las moléculas de gran tamaño y las partículas, e incluso restos celulares y células enteras quedan englobadas en vesículas endocíticas y son digeridas, tal y como hemos visto en el tema anterior, por los lisosomas. Las moléculas pequeñas no precisan de digestión. Metabolismo. El metabolismo es el conjunto de reacciones químicas enzimáticas que sufren los nutrientes en el interior de las células, con los dos objetivos antes indicados. Las moléculas de las diferentes sustancias contienen energía química, almacenada en forma de enlaces, de modo que las reacciones metabólicas implica, conjuntamente, transformaciones de materia y energía, y cada una de ellas está catalizada por un enzima específica. Excreción y secreción. En ambos procesos, la célula elimina al exterior productos del metabolismo, por diferentes mecanismos. Se habla de excreción cuando se trata de productos de desecho y de secreción cuando las sustancias eliminadas tienen utilidad para otras células.
2. CAPTURA e INGESTIÓN DEL ALIMENTO: EL INTERCAMBIO DE SUSTANCIAS ENTRE EL INTERIOR y EL EXTERIOR DE LA CÉLULA Gracias a la membrana, la célula mantiene una composición diferente en su citosol, y en cada uno de sus orgánulos, a la que existe en el exterior. Pero la membrana no puede ser una barrera completamente impermeable, por lo que las células han tenido que desarrollar sistemas de permeabilidad selectiva para transportar nutrientes esenciales, excretar productos residuales del metabolismo y regular las concentraciones intracelulares de iones. 2.1. INTERCAMBIO DE PEQUEÑAS MOLÉCULAS e IONES A TRAVÉS DE LA MEMBRANA PLASMÁTICA De forma general, la membrana celular, debido a la presencia de la doble capa de fosfolípidos, permite el paso de moléculas hidrofóbicas por simple difusión. Sin embargo, es impermeable a iones y moléculas orgánicas polares, que pasan al interior por mecanismos de transporte específicos en los que intervienen proteínas. Las membranas de cada orgánulo tienen sus propias proteínas de membrana que determinan qué tipo de sustancias pueden entrar o salir. El intercambio de pequeñas moléculas e iones a través de la membrana puede ser por transporte pasivo o activo.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
2
Transporte pasivo El transporte pasivo es un proceso de difusión que ocurre espontáneamente y sin gasto de energía. Siempre sucede a favor de gradiente de concentración (de la zona de mayor a la de menor concentración) o a favor de un gradiente eléctrico (las cargas de distinto signo se atraen). La combinación de ambos gradientes constituye el gradiente electroquímico. El transporte pasivo puede tener lugar por difusión simple o difusión facilitada. • Difusión simple. Algunas moléculas se difunden libremente a través de la doble capa de fosfolípidos, sin la intervención de las proteínas. Pasan así moléculas pequeñas y solubles en lípidos. Concretamente moléculas no polares, como el O2 y el CO2, y moléculas polares sin carga, como el H2O, etanol y la urea. • Difusión facilitada. La bicapa lipídica es impermeable a los iones y a las moléculas polares más o menos grandes, como la glucosa o los aminoácidos. El transporte de dichas moléculas solo es posible mediante unas proteínas transmembrana, que pueden ser de dos tipos: proteínas de canal y proteínas transportadoras o permeasas. • Proteínas de canal. Son proteínas que forman canales o poros que atraviesan la membrana, permitiendo el paso de iones (Na+, K+, Cl-, Ca2+), por lo que también se denominan canales iónicos. La mayoría de estos canales son muy estrechos y solo permiten el paso de iones de manera selectiva, es decir, cada canal deja pasar un tipo de ión. Muchos de ellos no permanecen continuamente abiertos, y su apertura y cierre están regulados por diferentes mecanismos: algunos se abren por la interacción de una molécula señal o ligando (canales regulados por ligando) y otros, como los responsables de la excitación eléctrica de las células nerviosas y musculares, se abren en respuesta a un cambio en el potencial de membrana (canales regulados por voltaje). • Proteínas transportadoras o permeasas. Este tipo de proteínas se unen a la molécula que van a transportar en una parte de la membrana y la liberan en la otra, mediante un cambio conformacional reversible (modelo ping-pong). Cada transportador se encarga de transportar específicamente una determinada molécula o ión, de modo semejante a como la hace un enzima con un sustrato específico.
Transporte activo Se realiza en contra de gradiente electroquímico, y por tanto, lleva un consumo de energía. En todos los casos, el transporte activo tiene lugar mediante proteínas transportadoras que están acopladas a una fuente de energía metabólica, como es la hidrólisis del ATP, actuando como una bomba direccional. Las más importantes transportan cationes de Na+, K+, Ca2+ o H+. En las células animales destaca especialmente la llamada bomba de Na+-K+. Bomba de Na+-K+ La bomba de Na+-K+ es un sistema de transporte que acopla el transporte de Na+ hacia el exterior de la membrana con el tranporte de K+ hacia el interior, ambos en contra de su gradiente. El proceso de transporte se realiza con consumo de ATP, de manera que por cada molécula de ATP consumida se bombean tres Na+ hacia el exterior y dos K+ hacia el interior. Con ello se consigue, que al bombear tres
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
3
cargas positivas hacia fuera y dos hacia dentro, se genera una diferencia de potencial eléctrico a ambos lados de la membrana, de manera que el interior está cargado negativamente respecto al exterior. Esta diferencia de potencial permite mantener el potencial de membrana de las células musculares y nerviosas, lo que hace que sean eléctricamente excitables. La bomba de Na+-K + consume, aproximadamente, el 30 por 100 del ATP de la célula.
2.2. INTERCAMBIO DE MACROLÉCULAS Y PARTÍCULAS Muchas macromoléculas, así como partículas, no pueden pasar a través de las membranas plasmáticas por los mecanismos que hemos visto. La entrada de estos materiales se realiza mediante endocitosis y su salida por exocitosis.
Endocitosis Mediante la endocitosis, las células eucariotas pueden captar continuamente fluidos y moléculas, así como grandes partículas y células enteras. Para ello, el material que se ha de capturar es rodeado progresivamente por una pequeña porción de membrana plasmática, donde se produce un hundimiento o depresión. Después se formará una vesícula endocítica, que quedará en el citoplasma para su posterior utilización, y serán los lisosomas los encargados de digerir su contenido. Existen dos tipos de endocitosis: pinocitosis y fagocitosis. La mayoría de las células eucarióticas ingieren continuamente líquidos y solutos por pinocitosis, mientras que la fagocitosis queda restringida a los protozoos y a células especializadas como los macráfagos y algunos leucocitos, que eliminan microbios, células deterioradas y células cancerosas. • Pinocitosis. Consiste en la ingestión de fluidos y sustancias disueltas mediante la formación de vesículas pinocíticas. Se realiza continuamente en las células eucarióticas e implica pérdidas de membrana plasmática (a veces hasta el 100% en una hora). Normalmente tiene lugar en regiones especializadas de la membrana, que están revestidas por una proteína denominada clatrina. En algunos casos existen, además, receptores específicos en la membrana a los que se unen de forma específica las moléculas que van a ser capturadas. Tiene la ventaja de que así se pueden capturar y concentrar, de forma selectiva, ciertas moléculas específicas, como hormonas, factores de crecimiento, colesterol y otros componentes. • Fagocitosis. Es la ingestión de grandes partículas de tipo variado, incluso, restos celulares o células enteras y microorganismos, utilizando grandes vesículas llamadas fagosomas. Este proceso lo utilizan los protozoos para ingerir grandes cantidades de partículas variadas. En los organismos pluricelulares superiores realizan la fagocitosis unas pocas células especializadas con fines distintos a la nutrición: las células fagocitarias. Entre ellos se encuentran los macrófagos y los neutrófilos, que ingieren y destruyen microorganismos invasores y eliminan células viejas o lesionadas y restos celulares. Para ello proyectan hacia el exterior zonas de la membrana plasmática (pseudópodos) que rodean al microorganismo y terminan englobándolo, formando un fagosoma.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
4
Exocitosis Es un proceso, en cierto modo, contrario a la endocitosis. Se lleva a cabo mediante la fusión de vesículas del interior de la célula con la membrana plasmática. De este modo, las vesículas de exocitosis aportan los componentes de su membrana (fundamentalmente proteínas y lípidos) a la membrana plasmática, compensando las pérdidas de fragmentos de membrana por endocitosis. Mediante la exocitosis, las células eliminan al exterior productos de desecho o secretan moléculas, como hormonas o compuestos que forman la matriz extracelular.
3. INTRODUCCIÓN AL METABOLISMO CELULAR 3.1. CARACTERÍSTICAS DE LAS REACCIONES METABÓLICAS El metabolismo es el conjunto de reacciones químicas que ocurren en el organismo en el interior de las células. En todo momento en una célula suceden miles de reacciones químicas, de manera muy rápida y ordenada, ajustadas a las necesidades que tenga la célula en cada instante. Estas reacciones solo son posibles a temperatura ambiente gracias a las enzimas. El número de reacciones químicas es tan elevado que parece imposible su comprensión. Sin embargo, existen una serie de características generales, aplicables a todas ellas, que permiten clarificar los procesos metabólicos. • Los compuestos que penetran en la célula experimenta una serie de reacciones químicas sucesivas, cada una controlada por una enzima diferente. Estas secuencias ordenadas de reacciones son las rutas metabólicas. Las moléculas que participan en dichas rutas reciben el nombre de metabolitos. En estas rutas el producto final de una reacción constituye la molécula de partida de la siguiente. Las rutas metabólicas son variadas, ramificándose y conectándose una con otras. • Existen rutas metabólicas convergentes y divergentes. En las primeras se obtiene el mismo producto final a partir de distintas moléculas de partida. En las segundas, una única molécula origina diferentes productos. Una misma molécula puede formar parte de una ruta convergente y de otra divergente, originándose itinerarios metabólicos, en ocasiones, muy complicados. Algunas rutas son cíclicas, de manera que los productos de la última reacción son también sustratos de la reacción inicial. • Pese a la enorme variedad de seres vivos existentes, las rutas metabólicas más importantes, como las empleadas en la obtención de energía o para la síntesis de los grandes grupos de moléculas, son comunes en la mayoría de los organismos. Esto constituye un apoyo a la hipótesis del origen único de los seres vivos. • Todas las reacciones metabólicas son catalizadas, es decir, precisan de la presencia de ciertas moléculas, denominadas enzimas, para llevarse a cabo. Para cada una de las reacciones existe una enzima diferente que permite su realización. • Las reacciones metabólicas pueden clasificarse en dos grandes grupos: catabólicas y anabólicas. Las primeras son degradativas, es decir, en ellas se pasa de moléculas más complejas a otras más sencillas. Su
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
5
finalidad es la obtención de energía. Las reacciones anabólicas son, por el contrario, constructivas y, por tanto, sirven para la síntesis de nuevas moléculas. En ellas es necesario un aporte de energía.
3.2. CATABOLISMO y ANABOLISMO El metabolismo, tal como acabamos de ver, puede estudiarse como la suma de dos conjuntos de reacciones: catabólicas y anabólicas.
Catabolismo El catabolismo es el conjunto de reacciones metabólicas en las que los compuestos orgánicos se degradan en moléculas más sencillas y menos energéticas, lo que conlleva una liberación de energía. Se trata pues de reacciones exergónicas. Se pasa de polímeros a monómeros y de monómeros a compuestos orgánicos más pequeños o inorgánicos. En general, estas reacciones implican la rotura de enlaces covalentes y la oxidación de compuestos. La energía que se desprende es utilizada por la célula para fabricar intermediarios ricos en energía, principalmente en forma de ATP o de mediadores reducidos (NADH, NADPH, FADH2, etc.). Cada tipo de molécula (glúcido, lípido, proteína) será degradada en una ruta catabólica específica, y dichas rutas desembocan en rutas catabólicas centrales, por lo que las rutas catabólicas son convergentes. Así, en el catabolismo aerobio se pueden distinguir tres fases principales: ▪ Fase I. Los polímeros o macromoléculas se descomponen, por hidrólisis, en sus respectivos monómeros. ▪ Fase II. Los productos de la fase anterior se degradan en moléculas más simples, las cuales se transforman, mediante una serie de reacciones en una molécula denominada acetil-CoA. Así pues el acetil Co-A puede ser considerado como una encrucijada metabólica, donde confluye el catabolismo de glúcidos, proteínas y ácidos nucleicos. ▪ Fase III. El acetil Co-A se oxida totalmente a CO2 y H2O.
Anabolismo
El anabolismo es el conjunto de procesos de biosíntesis, por los cuales a partir de moléculas sencillas se originan compuestos más complejos y más energéticos. Se trata pues, de reacciones de síntesis, que son endergónicas y por lo tanto, hay un consumo de energía procedente de las rutas catabólicas o de procesos de captación de energía luminosa (como en la fotosíntesis).
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
6
Las reacciones anabólicas incluyen la formación de enlaces covalentes y la reducción de moléculas. A partir de moléculas inorgánicas o moléculas orgánicas sencillas, se sintetizan monómeros y a partir de ellos, los polímeros. El objetivo final del anabolismo es la fabricación de materiales de construcción y de sustancias de reserva. Las rutas anabólicas son divergentes, ya que a partir de unas pocas moléculas precursoras sencillas se sintetiza una gran variedad de macromoléculas. En el anabolismo también se podrían distinguir tres fases: una primera fase, de síntesis de moléculas precursoras pequeñas; una segunda fase, donde dichas moléculas se utilizan para formar monómeros; y una tercera fase, en la que los monómeros se emplean para la síntesis de polímeros (polisacáridos, grasas, proteínas). El anabolismo y el catabolismo, aunque son procesos opuestos, están interconectados y suceden de forma simultánea. Aunque sus caminos no son idénticos, existen rutas metabólicas comunes a ambos, y se denominan rutas anfibólicas, como el ciclo de Krebs, que puede utilizarse con fines anabólicos y catabólicos. 3.3. TIPOS DE METABOLISMO Toda célula necesita tomar del exterior alguna forma de energía que pueda aprovechar, así como alguna forma de materia a partir de la cual fabrique su propia materia. Existen diferentes tipos de metabolismo atendiendo a estas necesidades:
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
7
3.4. LA ENERGÍA EN LAS REACCIONES METABÓLICAS: IMPORTANCIA DEL ATP Las células obtienen la energía, tal y como hemos visto, degradando los compuestos orgánicos mediante reacciones de oxidación y en otras ocasiones (como las células fotosintéticas) a partir de la luz. En estos procesos exergónicos, la energía liberada se utilizara en procesos endergónicos o trabajos que precisen energía, como la síntesis de nuevas moléculas, el transporte activo de sustancias a través de la membrana y los movimientos celulares. Así pues, la energía desprendida en las reacciones exergónicas se puede aprovechar para que ocurran otras reacciones, que en el mismo sentido son energéticamente desfavorables. Esta propiedad se conoce con el nombre de acoplamiento energético entre reacciones. Es tan fundamental, que sin ella, el metabolismo celular sería imposible. En general, por cada reacción endergónica que se produce en la célula existe otra exergónica que, acoplada a la primera, sirve de fuente de energía. La molécula que va a actuar como “moneda de cambio energético” en las células para que se produzca el acoplamiento energético es el ATP.
El ATP El ATP o adenosín trifosfato es un nucleótido que actúa como moneda de energía dentro de la célula. Está formado por una adenina y una cadena de tres grupos fosfato, entre los cuales se establecen “enlaces de alta energía”. El ATP almacena grandes cantidades de energía en los enlaces P~P, pero durante muy poco tiempo, ya que es una molécula que no puede almacenarse (una persona consume unos 45 kg de ATP al día, pero en cada instante la cantidad de ATP es menor de 1 g.). Cuando una célula obtiene energía, bien a partir de la luz o bien por oxidación de moléculas que toma del exterior, utiliza parte de esa energía para fabricar ATP a partir del ADP y fosfato inorgánico. ADP + Pi + energía → ATP + H2O Cuando la célula necesita realizar algún proceso endergónico, lo acopla a la hidrólisis del ATP para dar ADP y fosfato inorgánico, liberándose unas 7 kcal por mol de ATP. ATP + H2O → ADP + Pi + energía (7,3 kcal/mol) Así el sistema ATP/ADP sirve como sistema universal de intercambio de energía, haciendo de intermediario entre los procesos exergónicos o productores de energía y los endergónicos o consumidores de energía. Las enzimas que catalizan la hidrólisis del ATP reciben el nombre general de ATPasas y participan en procesos como movimientos celulares o intercambios de sustancias a través de la membrana. Para activar un compuesto y que aumente su energía útil y pueda hacer reacciones que, por sí solo, serían endergónicas, se le suele transferir un grupo fosfato procedente de la hidrólisis del ATP. Este proceso se denomina fosforilación. El compuesto, al resultar fosforilado, recibe parte de la energía almacenada en el ATP y queda más reactivo. Este mecanismo es típico de reacciones de condensación, que resultarían muy endergónicas si tuvieran que juntarse las moléculas en su estado normal. Mecanismos de síntesis de ATP Como el ATP no puede acumularse en grandes cantidades, no sirve de reserva de energía. Las reservas celulares son sustancias orgánicas, como glúcidos y grasas, de donde ha de ser liberada para “recargar” el ADP en ATP. En otras ocasiones el ATP se forma a partir de compuestos fosfatados los que ceden un grupo fosfato directamente al ADP. En el caso de las células fotosintéticas, la energía de la luz se
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
8
emplea para fabricar ATP. Así pues, son varios los mecanismos de formación de ATP, que se pueden englobar en dos categorías: ▪
Fosforilación a nivel de sustrato: cuando un grupo fosfato procedente de una molécula fosfatada es transferido al ADP para formar ATP en una única reacción química.
▪
Fosforilación asociada a una cadena de electrones: cuando la energía liberada por el transporte electrónico, realizado a favor de gradiente de potenciales de oxido-reducción, es acoplada a la fosforilación del ADP. Existen dos fosforilaciones de este tipo: > Fosforilación oxidativa: que se lleva a cabo en la respiración aerobia al oxidar compuestos orgánicos, y es el principal mecanismo de síntesis de ATP en las células aerobias. > Fotofosforilación: que se lleva a cabo en la fase luminosa de la fotosíntesis y en ella se sintetiza ATP aprovechando la energía luminosa.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
9
4. LA REGULACIÓN DE LAS REACCIONES METABÓLICAS: LAS ENZIMAS. 4.1. CONCEPTO DE CATÁLISIS y DE ENZIMA Las células desarrollan su actividad por medio de un complejo entramado de reacciones químicas orgánicas. Si estas reacciones se produjeran sin catalizadores, serían tan lentas que prácticamente no se llevarían a cabo. Los catalizadores son sustancias que aceleran una reacción química hasta hacerla instantánea o casi instantánea. Los catalizadores biológicos o biocatalizadores son las enzimas. Las enzimas actúan disminuyendo la energía de activación necesaria para que se produzca la reacción, uniéndose temporalmente con las moléculas que están reaccionando. Para comprender el funcionamiento de las enzimas, vamos a estudiar algunos conceptos sobre catálisis química. Cualquier reacción química se inicia con la rotura de ciertos enlaces entre átomos que constituyen las moléculas de los reactivos, para formar, posteriormente, los nuevos enlaces que originan las moléculas de los productos. Este estado en que los enlaces de los reactivos están debilitados, pero en el que aún no se han formado los nuevos, se conoce como estado de transición o estado activado. Para alcanzar dicho estado, es preciso comunicar a los reactivos cierta energía, denominada energía de activación. Dicha energía añadida hace aumentar la energía cinética de las moléculas, o sea, las activa, y tiene dos efectos importantes: ▪ Vencer las fuerzas de repulsión entre los electrones que envuelven a las moléculas que van a reaccionar. ▪ Romper los enlaces químicos de las moléculas que reaccionan y hacer posible la formación de nuevos enlaces. Así pues, solamente las moléculas activadas podrán reaccionar, y por tanto cuanto mayor sea la proporción de moléculas activadas en una reacción, más rápida se desarrollará esta. En las reacciones espontáneas, la energía de activación es tan baja que se obtiene de la propia energía cinética de las moléculas o de la luz que incide en el lugar de la reacción. En las reacciones no espontáneas, esta energía es tan alta que no se produce si no se aplica calor. En química, existen dos formas de conseguir que una reacción transcurra más rápidamente: aplicando calor o utilizando un catalizador. Los catalizadores actúan disminuyendo la energía de activación necesaria para que las moléculas reaccionen, y para ello se unen temporalmente a dichas moléculas, o sea, a los reactivos o sustratos. Esa unión temporal se traduce en un acercamiento íntimo de las moléculas que reaccionan y puede debilitar sus enlaces químicos, con lo que se facilita la formación de otros nuevos enlaces. Como consecuencia de todo ello, los catalizadores al combinarse con los reactivos producen un estado de transición de menor energía de activación que la reacción no catalizada, así pues, es menor la energía inicial que debe usarse para empezar la reacción y, por ello, habrá una mayor proporción de moléculas activadas y la reacción transcurrirá más deprisa. Como el catalizador no se modifica durante el proceso, puede reutilizarse continuamente. Para entender todo este proceso, vamos a considerar una reacción química tal que S
P
S representa la molécula o moléculas reaccionantes (sustratos o reactivos), que constituyen el estado inicial y P representa el o los productos de la reacción, que constituyen el estado final. Pero hay una barrera de energía que los separa, la energía de activación (Ea), que corresponde al estado de transición. Sin la energía de activación, A no existiría, pues no sería estable y se habría transformado en P. S → [ Estado de transición ]→ P
Sustratos
Productos
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
10
Aunque en el laboratorio la energía de activación se puede conseguir con calor, las reacciones en las células se llevan a cabo a baja temperatura, de manera que solucionan el problema mediante el uso de unos catalizadores especiales o biocatalizadores, que denominamos enzimas (E). Las enzimas se combinan con los sustratos de forma reversible, formando el complejo enzima-sustrato (ES), que representa el estado de transición con menor energía de activación que la reacción no catalizada. Posteriormente el complejo enzima-sustrato se escinde, liberando la enzima (E) sin alterar y los productos (P) de la reacción.
E+S
[ ES ]
E+P
4.2. ACCIÓN ENZIMÁTICA Las enzimas son catalizadores muy potentes y eficaces. Las reacciones orgánicas son muy complejas y es habitual que en el laboratorio se formen subproductos. Las reacciones enzimáticas son tan específicas que no se forman productos secundarios y su velocidad es más de una millón de veces superior a la de la reacción sin catalizar. Para entender la catálisis enzimática, conviene resumir las características de las enzimas y de su actividad: • Todos los enzimas son proteínas, a excepción de ciertas moléculas de ARN con actividad catalítica, denominadas ribozimas. • Como catalizadores, las enzimas actúan en pequeñas cantidades y se recuperan después de la reacción. • La característica más sobresaliente de las enzimas es su elevada especificidad. Esta es doble y explica que no se formen subproductos: ─ Especificidad de sustrato. Sustrato es la molécula sobre la que el enzima ejerce su acción catalítica. ─ Especificidad de acción. Cada reacción está catalizada por un enzima específico. • La acción enzimática se caracteriza por la formación de un complejo enzima-sustrato que representa el estado de transición. • El enzima y el sustrato se unen mediante fuerzas débiles (puentes de hidrógeno, interacciones electrostáticas, interacciones hidrofóbicas, etc.) en un lugar específico del enzima denominado centro activo. El centro activo es una pequeña región del enzima que contiene los componentes moleculares
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
11
por los que se une al sustrato. Generalmente se trata de una pequeña depresión situada sobre la superficie de la enzima. La unión entre el enzima y el sustrato para formar el complejo ES se ha explicado tradicionalmente mediante el modelo de la “llave y la cerradura”: el sustrato se une al centro activo y encaja como la llave y la cerradura. Sin embargo, se ha observado que los centros activos de algunos enzimas cambian su forma como respuesta a la presencia del sustrato, hasta que encajan. Así pues, el sustrato induce la forma del enzima para que se produzca el ajuste, por lo que ha este modelo se le ha denominado de ajuste inducido. El proceso sería comparable a cómo se adapta un guante de goma a la mano. El guante vacío tiene una forma parecida a la mano, pero no la forma exacta de la persona que lo va a usar, la cual solo se adquiere una vez puesto en la mano. La complementariedad entre el centro activo del enzima y el sustrato explica la especificidad de la unión entre el enzima y el sustrato.
•
Los enzimas presentan las características de estructura y propiedades expuestas para las proteínas. Pueden ser holoproteínas y heteroproteínas. Algunos enzimas actúan con la ayuda de moléculas no proteicas, denominadas cofactores. En estos casos la proteína enzimática recibe el nombre de apoenzima y el conjunto apoenzima y cofactor se denomina holoenzima. Los cofactores pueden ser: − Inorgánicos: como iones metálicos (Mg2+, Fe2+, Zn2+, Ca2+, etc). − Orgánicos: en este caso se denominan coenzimas. Las coenzimas son moléculas orgánicas complejas, y no suelen ser específicos de una sola apoenzima, es decir, un mismo coenzima puede actuar como cofactor de muchas enzimas diferentes. Los coenzimas suelen unirse débilmente con la proteína enzimática, pero en otros casos se hallan unidos estrechamente, en cuyo caso se habla de grupo prostético. La naturaleza de los coenzimas es muy variada. Pueden actuar como coenzimas: ▪ Vitaminas: como las derivadas del complejo vitamínico B. ▪ Adenosín fosfatos: ATP y ADP. ▪ Piridín nucleótidos: NAD y NADP. ▪ Flavín nucleótidos: FMN y FAD. ▪ Coenzima A.
4.3. CINÉTICA ENZIMÁTICA La cinética enzimática estudia la velocidad de las reacciones catalizadas por enzimas. La velocidad de una reacción (cinética) se define como la cantidad de materia transformada en función del tiempo, y se mide por la desaparición del sustrato o por la aparición del producto, en función del tiempo y por métodos muy variables. En una reacción, la velocidad depende, entre otros factores, de la concentración del sustrato. En 1913, Michaelis y Menten propusieron una ecuación que relaciona la velocidad de reacción con la concentración del sustrato. Según ellos, la reacción enzimática se realiza, tal y como hemos visto, de la siguiente manera:
E+S
[ ES ]
E+P
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
12
Según esto, la enzima (E) se puede encontrar bajo dos formas: libre y combinada con el sustrato. La velocidad de la reacción será máxima cuando todo el enzima esté en la forma ES y la cantidad de enzima libre sea muy pequeña. Estas condiciones se dan cuando la concentración de sustrato es muy alta, ya que los enzimas libres que van apareciendo están intactos y se combinan de nuevo inmediatamente con otra molécula de sustrato, formándose nuevos complejos ES. Si representáramos gráficamente la velocidad (V) de la reacción enzimática respecto a la concentración de sustrato (S), se obtiene una curva hiperbólica típica. Al principio, la velocidad aumenta mucho según aumente la concentración de sustrato, pero llega un punto en que ya no aumenta más por mucho que aumente la [S], es cuando el enzima está saturada de sustrato, y por tanto no quedan enzimas libres. La ecuación de dicha curva es la ecuación de Michaelis-Menten:
v=
Vmax ⋅ [S] K M + [S]
Este dato experimental corrobora la hipótesis de Michaelis-Menten: si realmente se forma el complejo ES, cuando la [S] es suficientemente grande, todo el enzima disponible se encuentra en forma de complejo ES y la velocidad de la reacción es máxima. Uno de los valores que más se utilizan para caracterizar a los enzimas es la denominada constante de Michaelis (KM), que se define como la concentración de sustrato a la cual se alcanza la mitad de la velocidad máxima (Vmax). La KM se mide en moles/l, oscilando entre 10-2 y 10-5 moles/l. El valor de KM se puede determinar gráficamente y cada enzima posee una KM característica para cada sustrato. Por tanto, esta constante indica la afinidad del enzima por el sustrato, de forma que una KM baja indica que con una baja concentración de sustrato se consigue la mitad de la velocidad máxima y por tanto el enzima tiene una gran afinidad por el sustrato. 4.4. FACTORES QUE INFLUYEN EN LA VELOCIDAD DE LAS REACCIONES ENZIMÁTICAS Entre los factores que pueden modificar la velocidad de las reacciones enzimáticas se pueden citar los siguientes: X Concentración de sustrato. Como hemos visto, al aumentar la concentración de sustrato aumenta la velocidad de la reacción hasta un máximo, a partir de ese momento, un aumento de la concentración de sustrato no supone un aumento en la velocidad de la reacción, ya que no quedan enzimas libres al estar saturadas de sustrato. X El pH. Cada enzima tiene un pH óptimo. Los valores por encima o por debajo de este valor óptimo provocan un descenso de la velocidad enzimática, debido a cambios en los radicales que forman el centro activo. Por debajo de un pH mínimo y por encima de un pH máximo, se produce la desnaturalización de la enzima y su actividad se anula por completo. El pH óptimo suele ser bastante próximo al fisiológico, aunque hay enzimas que actúan a pH con valores extremos, como las enzimas digestivas: la pepsina a pH ácido (1,5.2,5) y la tripsina a pH básico (8-11).
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
13
La temperatura. Como en el caso anterior, existe también una temperatura óptima en la que la actividad enzimática es máxima. Las temperaturas inferiores a este valor óptimo provocan una disminución de la vibración molecular que hace más lento el proceso, mientras que temperaturas superiores a la óptima pueden provocar la desnaturalización de la enzima y la pérdida total de funcionalidad. En la especie humana la temperatura óptima es la temperatura corporal.
X
4.5. MECANISMOS PARA AUMENTAR LA EFICACIA ENZIMÁTICA Los procesos metabólicos que tienen lugar en las células se llevan a cabo mediante reacciones encadenadas a través de rutas metabólicas, de forma que el producto final de una reacción es el sustrato de la siguiente. Estas rutas pueden ser largas, por lo que el tiempo para llevarlas a cabo sería elevado. Para que las reacciones se produzcan de forma óptima, existen mecanismos que permiten aumentar la eficacia de la acción enzimática. Algunos de estos mecanismos son los siguientes: • Compartimentación celular. Las enzimas implicadas en algunos procesos metabólicos importantes se localizan juntas dentro del mismo orgánulo celular, y así se encuentran en mayor concentración que dispersas por el citoplasma, y además se asegura que se encuentran en las condiciones ambientales (pH, concentración de iones, etc) adecuadas para su actividad enzimática. • Reacciones en cascada. En este caso el producto de una reacción actúa como enzima de otra reacción, cuyo producto, a su vez, es la enzima de una nueva reacción, y así sucesivamente. Estas reacciones en cascada aumentan la eficacia de la actividad enzimática, ya que el número de moléculas obtenidas aumenta en cada paso de forma considerable. Esto es lo que sucede, por ejemplo, en la coagulación sanguínea, en la que la red de fibrina debe formarse rápidamente para evitar la pérdida de sangre. • Complejos multienzimáticos. Los complejos multienzimáticos son agrupaciones de enzimas que llevan a cabo reacciones consecutivas de una ruta metabólica, lo que permite realizar el proceso completo con gran rapidez, ya que nada más obtener un producto, este puede actuar como sustrato de una nueva reacción al estar en o con la enzima correspondiente. Un ejemplo es el de la piruvatodeshidrogenasa que descarboxila, oxida y activa el ácido pirúvico para formar acetil-CoA que ingresará en el ciclo de Krebs.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
14
4.6. REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Las miles de reacciones que ocurren en el interior de las células están rigurosamente controladas ya que las necesidades celulares son cambiantes, y por tanto, la velocidad de las reacciones enzimáticas debe variar de acuerdo con ellas. La regulación de la actividad enzimática se basa en el principio de economía celular por el que solamente permanecen activas las enzimas precisas en cada momento, evitando así la fabricación innecesaria de productos, cuya acumulación, además, puede tener efectos negativos. Los mecanismos de regulación empleados son la activación y la inhibición enzimática y el alosterismo. X Activación enzimática. Se basa en la presencia de ciertos iones y moléculas que actúan como activadores y permiten que ciertas enzimas que se mantenían inactivas lleven a cabo su acción, es decir, se activen. Como activadores pueden actuar algunos cationes, como el Mg2+ o Ca2+, y en otras ocasiones, el propio sustrato es el que activa la enzima, de manera que el sustrato activa su propia metabolización.
X Inhibición enzimática. Los inhibidores enzimáticos son sustancias que disminuyen o anulan la actividad de un enzima. La enzima, previamente activa, deja de actuar en presencia del inhibidor, el cual puede ser algún ión o alguna molécula orgánica y, muy frecuentemente, el producto final de la reacción. En este último caso, en el que la enzima se inhibe cuando ya no es necesario obtener más cantidad de producto y la señal es el propio producto, se habla de inhibición feed-back o retroinhibición.
La inhibición puede ser irreversible, cuando el inhibidor, que se denomina en este caso “veneno metabólico”, se une covalentemente a la enzima, alterando su estructura e inutilizándola permanentemente. Un ejemplo es el cianuro, que actúa sobre la citocromo-oxidasa que interviene en la respiración aerobia, razón por la que este compuesto es un potente veneno. La inhibición reversible, mucho más común, tiene lugar cuando la enzima vuelve a tener actividad una vez eliminada la sustancia inhibidora. En este caso, la unión del inhibidor con la enzima se realiza mediante enlaces no covalentes más fáciles de romper. Si el inhibidor se une al centro activo de la enzima impidiendo, por tanto, la unión del sustrato, se habla de inhibición competitiva ya que el inhibidor y el
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
15
sustrato compiten por el centro activo. Si el inhibidor se une a otra zona de la enzima distinta del centro activo y modifica la estructura del enzima dificultando la unión del sustrato, se habla de inhibición no competitiva. X Alosterismo. El alosterismo es un sistema de regulación enzimática muy preciso. Las enzimas alostéricas catalizan algunas reacciones importantes como, por ejemplo, el primer paso de una ruta metabólica o un punto de ramificación de diferentes rutas metabólicas. Estas enzimas están formadas por varias subunidades (tienen estructura cuaternaria) y poseen varios centros de regulación, es decir, tienen varios sitios para la unión de activadores e inhibidores. Además adoptan dos conformaciones distintas, la forma R (de alta afinidad por el sustrato) y la forma T (de baja afinidad por el sustrato). La forma R se estabiliza cuando los centros reguladores están ocupados por activadores y por el contrario, los inhibidores alostéricos estabilizan la forma T. Entre las subunidades de un mismo enzima existe una cooperación, de manera que la activación o inhibición de una de ellas provoca el mismo efecto en las demás. Esto permite una regulación más rápida y con menor cantidad de activadores e inhibidores. La cinética de estas enzimas es distinta al resto, como puede observarse en la gráfica de la velocidad de reacción frente a la concentración de sustrato, que es una curva sigmoidea.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
16
4.7. CLASIFICACIÓN DE LAS ENZIMAS Se conocen alrededor de 2000 enzimas. En la nomenclatura tradicional, se nombran mediante términos que aluden al sustrato y al tipo de reacción catalizada, añadiendo el sufijo –asa. La nomenclatura recomendada por la Comisión Internacional de Enzimas (IEC) se basa en un código de cuatro números que hace referencia a la clase en que está incluida, a la subclase, a la subdivisión y a la enzima concreta de que se trate. Esta nomenclatura no resulta cómoda y se utiliza con menos frecuencia que la tradicional. Según el tipo de reacción que catalizan, las enzimas se clasifican en seis clases, según el cuadro:
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
17
5. CATABOLISMO 5.1. INTRODUCCIÓN AL CATABOLISMO: LA OXIDACIÓN El catabolismo es el conjunto de reacciones de degradación de moléculas orgánicas complejas. Las reacciones catabólicas tienen lugar en todos los seres vivos, autótrofos y heterótrofos, y su finalidad es proporcionar energía utilizable por la célula, poder reductor y precursores metabólicos. Las reacciones catabólicas más importantes consisten en la oxidación de moléculas orgánicas no hidrolizables, como monosacáridos, ácidos grasos, glicerina, etc. Así el catabolismo se puede considerar como un proceso de degradación oxidativa de moléculas orgánicas, cuya finalidad es la obtención de energía contenida en los enlaces químicos de dichas moléculas. Reacciones REDOX La oxidación es una pérdida de electrones y en las células, las sustancias orgánicas suelen oxidarse por deshidrogenación (pérdida de átomos de hidrógeno, o sea, de e- y H+), lo que implica la existencia de alguna sustancia que capte dichos electrones y protones y que, por tanto se reduzca, por lo que estas reacciones son del tipo oxidación-reducción o reacciones REDOX. Así, las oxidaciones se dan siempre simultáneamente con reacciones de reducción. El compuesto (A-H) que se oxida cede el hidrógeno y/o los electrones a otro que se reduce (B) captándolos. En el catabolismo, los átomos de hidrógeno perdidos por una molécula al oxidarse son captados por los transportadores de hidrógeno (nucleótidos como el NAD+, el NADP+ o el FAD+). Posteriormente estos los cederán al compuesto que se reduce.
Formas de oxidación ▪ ▪
La oxidación de los compuestos biológicos se puede realizar de dos formas distintas: Mediante la fermentación. Consiste en una oxidación incompleta de los compuestos orgánicos en la que el aceptor final de los electrones es otro compuesto orgánico. El ATP se forma por fosforilación a nivel de sustrato. Tiene lugar en el citoplasma. Mediante la respiración celular. Es un proceso de oxidación completa de compuestos orgánicos en el que el aceptor final de electrones es un compuesto inorgánico. Según cuál sea el aceptor, puede ser: > Respiración aerobia: si el aceptor final de electrones es el oxígeno. El ATP se forma por fosforilación asociada a una cadena de electrones (fosforilación oxidativa). En las células eucariotas tiene lugar en las mitocondrias. > Respiración anaerobia: si el aceptor final de electrones es otro compuesto inorgánico, distinto del oxígeno, como el NO3-, SO42-, etc. El ATP se origina por fosforilación oxidativa. La realizan algunas bacterias.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
18
5.2. EL CATABOLISMO DE LOS GLÚCIDOS Tanto si la oxidación se realiza por respiración como por fermentación, la degradación inicial de la glucosa se produce mediante un proceso denominado glucólisis. La glucólisis tiene lugar en el citosol y consiste en una serie de reacciones que conforman una ruta catabólica en la que una molécula de glucosa (seis carbonos) se transforma en dos moléculas de ácido pirúvico (tres carbonos). La glucólisis es, por tanto, una ruta central del catabolismo de la glucosa, común a todo tipo de organismos, tanto aerobios como fermentadores. La diferencia entre unos y otros radica en el destino posterior del ácido pirúvico formado: ▪ En condiciones aerobias, el ácido pirúvico se oxida hasta CO2 y H2O. ▪ En condiciones anaerobias, el ácido pirúvico sigue otros caminos que conducen a las diferentes fermentaciones. 5.2.1. LA GLUCÓLISIS La glucólisis es, probablemente una de las rutas metabólicas más antiguas, ya que se pudo dar en un ambiente anaerobio como el de la atmósfera primitiva y servir de mecanismo de obtención de energía. Consiste en una ruta metabólica que degrada cada molécula de glucosa en dos molécula de ácido pirúvico, obteniéndose como balance energético dos moléculas de NADH y dos moléculas de ATP. Tiene lugar en el citosol Las diez reacciones que componen la glucólisis se pueden agrupar para su estudio en dos etapas o fases: • Fase preparatoria: se activa la glucosa mediante fosforilación y posteriormente se descomponen en dos moléculas de gliceraldehido-3-fosfato (de 3 carbonos). En esta fase, por cada molécula inicial de glucosa se consumen dos ATP. • Fase de producción de energía: consiste en la transformación del gliceraldehido-3-fosfato en ácido pirúvico, mediante una serie de reacciones en las que destacan los siguientes hechos: − Oxidación del gliceraldehido-3-fosfato, liberándose dos átomos de hidrógeno por cada molécula consumida. Los protones y electrones de los átomos de hidrógeno son captados por el NAD+, reduciéndose a NADH + H+ (cada NAD+ capta dos electrones y un protón). − Transferencia del grupo fosfato, desde metabolitos intermediarios a moléculas de ADP, dando lugar a la síntesis de dos moléculas de ATP por gliceraldehido mediante fosforilación a nivel de sustrato. Como por cada molécula de glucosa se forman dos de gliceraldehido-3-fosfato, en conjunto se obtienen 4 ATP y 2 (NADH + H+). Pero al haberse gastado 2 ATP en la primera fase, el balance global es la ganancia de 2 ATP y 2 (NADH + H+) por molécula de glucosa consumida.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
19
5.2.2. LA RESPIRACIÓN AEROBIA Mediante la respiración celular, el ácido pirúvico formado durante la glucólisis se oxida completamente a CO2 y H2O, en presencia de oxígeno. Las etapas de la respiración aerobia son tres: 1. Formación de acetil Co A 2. Ciclo de Krebs 3. Cadena respiratoria
1. Formación de acetil- CoA El ácido pirúvico formado en la glucólisis en el citoplasma celular pasa a la matriz mitocondrial, atravesando las membranas mitocondriales externa e interna. En el interior de la matriz, el ácido pirúvico experimenta una descarboxilación oxidativa, catalizada por un complejo enzimático llamado piruvato-deshidrogenasa. Este oxidación se produce en dos etapas: − El grupo carboxilo se elimina en forma de CO2. − Oxidación del grupo ceto a grupo carboxilo. La energía liberada en este oxidación queda “atrapada” en el enlace de alta energía entre el resto acetilo y la coenzima A (CoA) que interviene en la reacción, y se origina acetil-CoA. Esta oxidación proporciona la formación de una molécula de NADH + H+. Así, por cada molécula de glucosa inicial se producen 2 acetil-CoA, 2 CO2 y 2 (NADH + H+). Los ácidos grasos y los aminoácidos también pueden transformarse en acetil-CoA, por rutas metabólicas distintas que veremos más adelante, y así se incorporan a la respiración aerobia.
2. El ciclo de Krebs El ciclo de Krebs o de los ácidos tricarboxílicos (CAT) es una conjunto cíclico de reacciones que produce la oxidación completa del acetil-CoA hasta CO2. Los electrones cedidos en esta oxidación son captados por las coenzimas FAD y NAD+, liberándose las correspondientes moléculas reducidas, FADH2 y NADH + H+. El ciclo de Krebs se lleva a cabo en la matriz mitocondrial y tiene distintos objetivos: − Obtención de poder reductor: NADH y FADH2. − Obtención de precursores metabólicos. − Obtención de energía en forma de GTP por fosforilación a nivel de sustrato. El acetil-CoA se incorpora al ciclo de Krebs al unirse con una molécula de ácido oxalacético (4 carbonos), separándose el CoA y obteniéndose una molécula de ácido cítrico (6 carbonos). A continuación tiene lugar una serie de reacciones encadenadas, en las que unos ácidos orgánicos se transforman en otros, regenerándose al final el ácido oxalacético con lo que el proceso puede continuar. Por cada vuelta completa del ciclo de Krebs (molécula de acetil-CoA que ingresa en el ciclo) se obtiene como balance: − Una molécula de GTP (convertible en ATP). − Tres moléculas de (NADH + H+) y una de FADH2, que permiten, posteriormente, la formación de moléculas de ATP en la cadena respiratoria. − Dos moléculas de CO2, que corresponde a los carbonos de una molécula de acetil-CoA completamente oxidados. Como se necesitan dos vueltas al ciclo de Krebs para terminar la oxidación de una molécula de glucosa, el rendimiento energético del ciclo de Krebs será: 2 ATP, 6 (NADH+ + H+) y 2 FADH2.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
20
3. La cadena respiratoria La molécula de glucosa que inició la glucólisis se encuentra completamente oxidada. Parte de su energía se ha utilizado en la síntesis de ATP. Sin embargo, la mayor parte de la energía se encuentra en los electrones que fueron aceptados por el NAD+ y el FAD. Estos electrones, procedentes de la glucólisis, la oxidación del ácido pirúvico y el ciclo de Krebs, se encuentran aún en un nivel energético alto. Las formas reducidas del NAD+ y el FAD (NADH y FADH2) tienen un elevado poder reductor y transfieren sus electrones al oxígeno molecular (O2) a través de una cadena de transporte de electrones o cadena respiratoria. Este proceso de transporte de electrones libera gran cantidad de energía libre que se emplea en la formación del ATP a partir de ADP + Pi, en la llamada fosforilación oxidativa. Transporte electrónico En este proceso, los electrones presentes en las moléculas de NADH y FADH2, son cedidos a moléculas transportadoras y pasan de unas a otras a favor de un gradiente de potenciales de oxidorreducción hasta el O2, que actúa como compuesto aceptor final de electrones. La cadena transportadora de electrones o cadena respiratoria que interviene en la respiración mitocondrial está formada por un conjunto de moléculas, asociadas a la membrana interna, capaces de oxidarse y reducirse, es decir, de aceptar electrones de una molécula anterior y cedérselos a la siguiente. Para que este proceso tenga lugar espontáneamente, las moléculas transportadoras deben estar situadas según un gradiente de potenciales de oxidorreducción, de manera que, al pasar de una molécula de la cadena a la siguiente, los electrones “descienden” a niveles energéticos inferiores. Este descenso a niveles energéticos más bajos libera energía, que será empleada posteriormente en la síntesis de ATP por fosforilación oxidativa. Los transportadores de electrones de la cadena respiratoria se agrupan en cuatro grandes complejos supramoleculares que están insertos en la membrana mitocondiral interna: ▪ Complejo I o Complejo NADH-deshidrogena ▪ Complejo II o Ubiquinona o Coenzima Q ▪ Complejo III o Complejo citocromo b-c1 ▪ Complejo IV o Complejo citocromo-oxidasa
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
21
Fosforilación oxidativa: hipótesis quimiosmótica Como hemos visto, la energía liberada en la cadena de transporte de electrones se emplea para fabricar ATP a partir de ADP + Pi, en un proceso denominado fosforilación oxidativa. El mecanismo por el que se sintetiza ATP mediante este proceso se explica por la hipótesis quimiosmótica o teoría del acoplamiento quimiosmótico, y fue propuesto por Peter Mitchell en 1961. Según la hipótesis quimiosmótica, la energía que los electrones van perdiendo al pasar por los complejos transportadores se emplea en bombear protones (H+) a través de la membrana mitocondrial interna, que se acumulan en el espacio intermembranal de la mitocondria. La acumulación de protones entre las dos membranas mitocondriales origina una diferencia de concentración de protones, y también una separación de cargas eléctricas, entre la matriz mitocondrial y el espacio intermembrana, lo que se denomina gradiente electroquímico. Este gradiente electroquímico es capaz de generar una fuerza protón-motriz de unos 230 mV que proporciona energía aprovechable para hacer funcionar cualquier proceso que esté acoplado a un canal por el que puedan circular los protones a favor de gradiente hacia la matriz. La fuerza protón motriz constituye el motor energético de la fosforilación del ADP en la síntesis de ATP. En la membrana mitocondrial interna se encuentran situadas las enzimas ATP sintetasas que contienen un canal en su interior, a través del cual los protones pueden volver a entrar en la matriz mitocondrial. El paso de los protones permite que las ATP sintetasas actúen para formar ATP. Por cada tres protones que pasan por las ATP sintetasas se forma una molécula de ATP a partir de ADP y Pi. Como el flujo de protones es impulsado por el gradiente electroquímico, este proceso tiene carácter quimiosmótico.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
22
Balance energético de la cadena respiratoria En la fosforilación oxidativa, cada par de electrones que son cedidos desde el NADH hasta la molécula de oxígeno proporciona energía para formar tres moléculas de ATP. Cuando los electrones proceden del FADH2, se obtienen dos moléculas de ATP, ya que las moléculas de FADH2 entran en la cadena en un nivel energético menor. BALANCE ENERGÉTICO GLOBAL de la OXIDACIÓN COMPLETA DE LA GLUCOSA Si se considera la producción neta de ATP en las etapas de la glucólisis hasta su conversión en acetil-CoA y su posterior oxidación, la oxidación completa de la molécula produce 36 moléculas de ATP. Esta producción de ATP representa un rendimiento del 40% de la energía contenida en una molécula de glucosa, y equivale a 266 kilocalorías obtenidas por la célula por mol de glucosa consumida. La célula viva es por lo tanto, considerablemente más eficaz que cualquier motor, que puede perder hasta el 75 % de la energía que se le proporciona. La mayor eficacia de la célula se debe principalmente a que la liberación de energía se produce en una serie de reacciones en cadena, en cada una de las cuales tiene lugar un cambio de energía pequeño. De los 36 ATP producidos, solamente dos moléculas de ATP y dos de GTP, se producen por fosforilación a nivel de sustrato. Los 32 ATP restantes se originan por fosforilación oxidativa, a partir del NADH y FADH2. Los NADH formados fuera de la mitocondria (producidos en la glucólisis), no pueden atravesar directamente la membrana mitocondrial interna, pero sus electrones se pueden incorporar a la cadena respiratoria gracias al funcionamiento de las llamadas lanzaderas de sustrato. Se conocen dos tipos: • Lanzadera del glicerol-fosfato: se encuentra en las células del cerebro y músculo esquelético. Los electrones del NADH pasan al FADH2 mitocondrial, con lo que la cadena respiratoria sólo rendirán 2 ATP. • Lanzadera del malato-aspartato: predomina en el hígado y en el corazón. Los electrones del NADH del citosol se transfieren al NADH mitocondrial y rendirán 3 ATP en la cadena respiratoria.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
23
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
24
5.2.3. LA FERMENTACIÓN La fermentación es un proceso de oxidación incompleta de los compuestos orgánicos, ya que no se libera toda la energía química que contienen. El objetivo final de la fermentación es la obtención de energía en forma de ATP, mediante la fosforilación a nivel de sustrato, por lo que no interviene la cadena respiratoria. La fermentación es un proceso anaerobio, por lo que el aceptor final de electrones es un compuesto orgánico, de manera que como productos finales se obtienen diversas sustancias orgánicas más sencillas. El rendimiento energético de las fermentaciones es muy bajo comparado con la respiración aerobia, ya que al tratarse de una oxidación incompleta, los productos orgánicos obtenidos aún conservan un contenido energético considerable. Además la obtención de ATP es por fosforilación a nivel de sustrato, lo que implica el consumo previo de ATP en las reacciones iniciales de activación. La fermentación es realiza principalmente por diversos microorganismos (levaduras y bacterias) que pueden vivir en condiciones anaerobias, pero también en las plantas y animales cuando escasea el oxígeno las células pueden utilizar la fermentación para producir energía. Los sustratos de la fermentación son, generalmente glúcidos, en particular glucosa. No obstante, las bacterias responsables de la putrefacción de la materia orgánica son capaces de llevar a cabo una fermentación de proteínas y aminoácidos, en cuyo caso se habla de fermentación pútrida o putrefacción y se obtienen como productos indol, cadaverina o escatol, responsables del olor de la materia orgánica en descomposición. Las fermentaciones de los glúcidos comienzan con la glucólisis y a continuación en una segunda fase el ácido pirúvico es transformado en diferentes productos finales, variables según el tipo de fermentación. Por lo tanto tienen lugar dos etapas: ▪ Etapa de oxidación de la glucosa hasta ácido pirúvico (glucólisis). Se consume NAD+ y se produce NADH. ▪ Etapa de reducción del ácido pirúvico para dar los productos finales. Se genera el NAD+, necesario para proseguir la glucolisis. La reducción del ácido pirúvico da lugar a los productos finales. Si se origina ácido láctico tiene lugar la fermentación láctica, mientras que si se produce etanol y CO2 se trata de la fermentación alcohólica.
Fermentación láctica Consiste en la degradación anaerobia de la glucosa a ácido láctico. En una primera etapa la glucosa se oxida a dos moléculas de ácido pirúvico, generándose NADH. Posteriormente el ácido pirúvico, al aceptar los electrones del NADH, se reduce a ácido láctico. El rendimiento energético es de 2 moléculas de ATP, obtenidas por fosforilación a nivel de sustrato.
Son muchas las bacterias que realizan este tipo de fermentación, entre las cuales destacan los lactobacilos (Lactobacillus), que se encuentran en la leche y también en el intestino. El queso, yogur y otras leches acidificadas son productos obtenidos por fermentación láctica. También se emplea esta fermentación como método de conservación de ciertos productos vegetales o cárnicos como algunos embutidos.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
25
La fermentación láctica descrita es lo que se conoce como fermentación homoláctica, ya que el ácido láctico es el único producto final. Pero hay bacterias (Lactobacillus bifidus, Lecuonostoc) que hacen una fermentación ligeramente diferente, denominada heteroláctica, en que se además de ácido láctico se producen otras sustancias. La fermentación láctica es un proceso que sucede en las fibras musculares cuando no reciben suficientemente aporte de oxígeno. El ácido láctico al precipitar en las fibras musculares contraídas provoca el dolor característico de las “agujetas”. Cuando el aporte de oxígeno vuelve a ser abundante, el ácido láctico se reconvierte en pirúvico.
Fermentación alcohólica o etílica Consiste en la degradación anaerobia de glucosa a etanol, originándose CO2 como subproducto. La glucosa se oxida a ácido pirúvico, generando NADH. Posteriormente suceden dos procesos: ▪ Descarboxilación del ácido pirúvico, que origina acetaldehído y se libera CO2. ▪ Reducción del acetaldehído a etanol, gracias al enzima alcohol-deshidrogenasa, y consumiendo los NADH producidos en la glucolisis. El rendimiento energético es de 2 ATP, como en la fermentación láctica.
La fermentación alcohólica es realizada principalmente por las levaduras y entre ellos la más conocida y utilizada es Saccharomyces cerevisiae. Ciertas cepas seleccionadas de esta levadura son utilizadas en la producción de vino y cerveza y otras en la fabricación del pan. Saccharomyces cerevisiae sigue un metabolismo fermentativo en condiciones anaerobias, pero cuando hay oxígeno realiza la respiración aerobia, y no produce alcohol. Este fenómeno se conoce como efecto Pasteur, y es importante en la industria de bebidas alcohólicas, pues para que la producción de alcohol sea correcta las levaduras deben desarrollarse en ausencia de oxígeno.
5.3. CATABOLISMO DE LÍPIDOS Por su importancia como reservas energéticas, nos vamos a centrar en el catabolismo de las grasas o triglicéridos. Las grasas son moléculas muy adecuadas como combustible de reserva, pues su catabolismo libera mucha energía, son insolubles en agua y, como tienen poca reactividad química, no provocan reacciones indeseadas en la célula. Muchas células almacenan en su citoplasma moléculas de grasa en forma de pequeñas gotitas, como en los tejidos adiposos. No obstante, estas mismas características hacen que su degradación no sea tan fácil, por lo que cuando la célula necesita un aporte energético utiliza los glúcidos como combustibles, y solamente si necesita un mayor aporte de lo habitual, degrada las grasas. La movilización de las grasas es más lenta que las reservas glucídicas, y además el transporte de las mismas, desde el tejido adiposo a otros lugares, requiere la utilización de moléculas especiales. El catabolismo de las grasas empieza por su hidrólisis, realizada por las enzimas lipasas, obteniéndose glicerina y ácidos grasos. triglicérido + agua → glicerina + ácidos grasos La glicerina se convierte fácilmente en gliceraldehido-3-fosfato y continúan la ruta de la glucólisis. Los ácidos grasas siguen una ruta catabólica especial denominada β- oxidación.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
26
β-oxidación de los ácidos grasos Los ácidos grasos constituyen una fuente de carbono y energía muy importante, ya que su degradación proporciona a la célula muchas más moléculas de ATP por unidad de peso que la glucosa. La β-oxidación consiste en un proceso de oxidación que da lugar a moléculas de acetil-CoA. Esta oxidación se produce en la matriz mitocondrial. El acetil-CoA generado se incorporará al ciclo de Krebs y, posteriormente se llevará a cabo la fosforilación oxidativa. La degradación de los ácidos grasos implica realmente dos procesos: 1. Activación del ácido graso en el citosol. El ácido graso se une a la CoA mediante un enlace éster para formar acil-CoA, que es la forma activa del ácido graso. En esta reacción se consume una molécula de ATP. El acil-CoA penetra en el interior de la mitocondria atravesando las membranas mitocondriales, ayudado por una molécula transportadora llamada carnitina. 2. β-oxidación propiamente dicha. En el interior de la matriz mitocondrial el acil-CoA experimenta un ciclo de reacciones que va escindiendo dos átomos de carbono a partir del extremo carboxilo. La β-oxidación se desarrolla en cuatro etapas: 1. Deshidrogenación. El acil-CoA se oxida por deshidrogenación, originándose una molécula con doble enlace y los átomos de hidrógeno se utilizan para formar FADH2 a partir del FAD. 2. Hidratación. Se añade una molécula de agua al doble enlace generado antes, originándose una grupo alcohol. 3. Oxidación. El grupo alcohol se oxida a cetona y los átomos de hidrógeno se utilizan para formar NADH + H+ a partir del NAD+. 4. Tiólisis. Se rompe el enlace que une los carbonos α y β por la incorporación de una molécula de CoA y se origina una molécula de acil-CoA con dos carbonos menos y otra de acetil-CoA. La nueva molécula de ácil-CoA experimentará un nuevo proceso de β-oxidación. Así en cada β-oxidación, el acil-CoA (ácido graso activado) perderá dos carbonos, por lo que para oxidar completamente un ácido graso activado (acil-CoA) serán necesarias varias β-oxidaciones, o lo que es lo mismo, varias vueltas en este ciclo de reacciones, por lo que el proceso de oxidación total de un ácido graso se suele representar mediante una hélice, denominada hélice de Lynen. En cada vuelta de dicha hélice, es decir, en cada β-oxidación, se obtienen los siguientes productos: − 1 acil-CoA con dos carbonos menos − 1 acetil-CoA, que se incorpora al ciclo de Krebs para su degradación aerobia. − 1 FADH2 y 1 NADH + H, que se oxidan en la cadena respiratoria, de forma que los protones y electrones son finalmente captados por el O2, originándose agua. El proceso genera ATP por fosforilación oxidativa. En consecuencia, los productos finales del catabolismo de los ácidos grasos son CO2, H2O y ATP.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
27
5.4. CATABOLISMO DE PROTEÍNAS Las proteínas y los aminoácidos, no son buenos carburantes metabólicos, ya desempeñan otras funciones (estructural, reguladora, transportadora, etc.). Sin embargo, si no hay suficiente aporte de glúcidos y lípidos (dieta de ayuno), los aminoácidos se pueden utilizar para obtener energía. Asimismo en las dietas excesivamente ricas en proteínas, en las que hay un excedente de aminoácidos o en la degradación normal de proteínas para su renovación, si hay exceso de algún aminoácido. El catabolismo de las proteínas empieza por la hidrólisis de los enlaces peptídicos, liberando los aminoácidos constituyentes. Posteriormente los aminoácidos sufren una degradación, que consiste en dos etapas: 1. Eliminación del grupo amino. El grupo amino se transfiere (transaminación) desde el aminoácido hasta una molécula aceptora, que generalmente es el α-cetoglutarato (a-KG), que se transforma en glutamato. Estas reacciones están catalizadas por las transaminasas y suceden en el hígado. Posteriormente se elimina el grupo amino del glutamato (desaminación oxidativa) en forma de amoníaco o ión amonio. Dicha reacción se lleva a cabo en el hígado y en los riñones, y está catalizada por la enzima glutamatodeshidrogenasa. El amoníaco posteriormente es eliminado en diversas formar: urea en los animales ureotélicos (mamíferos, anfibios, peces de agua salada): ácido úrico en los animales uricotélicos (insectos, aves y reptiles); y directamente como amoníaco en los animales amoniotélicos (invertebrados acuáticos y peces de agua dulce). 2. Oxidación e la cadena carbonada. La molécula carbonada que se origina tras la eliminación del grupo amino, se incorpora a otras rutas metabólicas, tanto catabólicas como anabólicas, distinguiéndose los aminoácidos glucogénicos, que se degradan a ácido pirúvico y otros compuesto y se pueden utilizar para fabricar glucosa) y los cetogénicos, que se utilizan para formar acetil-CoA, que en el hígado se puede transformar en unos compuestos llamados cuerpos cetónicos.
5.5. CATABOLISMO DE ÁCIDOS NUCLEICOS Los ácidos nucleicos, ADN y ARN, son hidrolizados por enzimas nucleasas, liberándose nucleótidos. Estos, a su vez, se descomponen en la pentosa, el fosfato y la base nitrogenada que los constituyen, y pueden ser reutilizados en la síntesis de nuevos nucleótidos o sino son catabolizados. En la degradación de las bases pirimidínas (C, U y T) se origina CO2 y NH3, y en la de las bases púricas (A y G) se origina ácido úrico y alantoína o ácido alantoico, según el animal que se trate.
6. ANABOLISMO El anabolismo es el conjunto de procesos bioquímicos mediante los cuales las células sintetizan la mayoría de las sustancias que las constituyen. Se pueden considerar dos grandes grupos de procesos anabólicos. Unos permiten la obtención de moléculas orgánicas a partir de moléculas inorgánicas y son, por tanto, exclusivos de organismos autótrofos. Según empleen como fuente primaria de energía la luz o la energía desprendida de de la oxidación de ciertas moléculas, se diferencian la fotosíntesis y la quimiosíntesis, respectivamente. Otros procesos anabólicos consisten en la síntesis de moléculas orgánicas a partir de otras, también orgánicas, y los realizan todos los seres vivos, tanto autótrofos como heterótrofos. 6.1. LA FOTOSÍNTESIS La fotosíntesis es un proceso anabólico por el cual las plantas, las algas y algunas bacterias pueden transformar la energía de la luz en energía química, almacenarla en forma de ATP y poder reductor, y luego utilizarla para sintetizar moléculas orgánicas. La vida en el planeta depende de los organismos fotosintéticos pues estos pueden sintetizar materia orgánica de novo. Por ello, constituyen la base fundamental de las cadenas tróficas, es decir, son los productores primarios de los ecosistemas.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
28
Las plantas verdes, algas y cianobacterias llevan a cabo la fotosíntesis mediante un proceso que libera oxígeno como producto final, y por esta razón se llama oxigénica. El oxígeno molecular liberado procede de la fotólisis del agua, que actúa como donador de electrones. Por en contrario, en la fotosínteis anoxigénica, proceso llevado a cabo por el resto de bacterias fotosintéticas, no se utiliza el agua como donador de electrones y, como consecuencia, no se libera oxígeno como producto final. Primeramente, vamos a estudiar la fotosíntesis oxigénica, que se realiza en el interior de los cloroplastos de las células vegetales. 6.1.1. LOS PIGMENTOS FOTOSINTÉTICOS Y LOS FOTOSISTEMAS Para que los organismos fotosintéticos pueden utilizar la energía de la luz, primero tienen que absorberla. Para ello, cuentan con unas sustancias, los pigmentos fotosintéticos. En las plantas verdes, los pigmentos son la clorofila y los carotenoides. En las cianobacterias se encuentran también las ficobilinas, y en algunas algas aparecen entre otros, la ficocianina y la ficoeritrina. La clorofila es un compuesto que contiene un anillo tetrapirrólico, en cuyo interior hay un átomo de magnesio, y una cadena lateral de un alcohol llamado fitol. Las más importantes son la clorofila a y la clorofila b. Los carotenoides, llamados también pigmentos rios, son lípidos de tipo isoprenoide, y absorben la luz a diferente longitud de onda que las clorofilas. Los más importantes son el β-caroteno y la xantofila. Las clorofilas y los carotenoides se encuentran asociados a proteínas, en las membranas tilacoidales de los cloroplastos, formando unas estructuras denominadas fotosistemas. En el interior de cada fotosistema se pueden diferenciar dos zonas: el complejo antena, formado por cientos de clorofilas y carotenoides, que se encargar de absorber la luz. Al hacerlo se excitan y transmiten la energía se excitación a una zona denominada centro de reacción, formado por una molécula especial de clorofila, que al recibir dicha energía libera electrones. Existen dos tipos de moléculas especiales de clorofila, conocidas como P700 y P680, y cada una presenta una máxima eficacia a diferente longitud de onda. Debido a esto, en las membranas de los tilacoides se pueden diferenciar dos tipos de fotosistemas: ▪ Fotosistema I (PSI): se localiza preferentemente en los tilacoides del estroma. El centro de reacción contiene dos moléculas de clorofila a del tipo P700, ya que su máxima absorción de produce a una longitud de onda de 700 nm. ▪ Fotosistema II (PSII): se localiza en los tilacoides de los grana. Su centro de reacción contiene dos moléculas de clorofila a del tipo P680, ya que su máxima absorción es a una longitud de onda de 680 nm. 6.1.2. MECANISMO GENERAL DE LA FOTOSÍNTESIS La fotosíntesis consta de dos fases, cada una de ellas sucede en un lugar diferente de los cloroplastos. ▪ Fase luminosa o lumínica. Se lleva a cabo en los tilacoides. Comprende un conjunto de reacciones dependientes de la luz, cuyo objetivo es absorción y transformación de la energía luminosa en energía química, en forma de ATP y NADPH. ▪ Fase oscura o biosintética. No necesita luz y se lleva a cabo en el estroma. En esta etapa se produce la biosíntesis de compuestos orgánicos a partir de CO2, utilizando el ATP y el NADPH obtenidos en la fase anterior.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
29
FASE LUMINOSA DE LA FOTOSÍNTESIS En la fase luminosa, la energía luminosa se convierte en energía química, originándose dos tipos de moléculas: el transportador de energía, ATP y el transportador de electrones, NADPH. La fase luminosa tiene lugar en la membrana de los tilacoides, que es donde se encuentran las estructuras moleculares que intervienen: − Los fotosistemas, PSI y PSII. Son los que absorben la energía luminosa y desprenden electrones hacia la cadena de transporte de electrones. − La cadena de transporte de electrones, semejante a la de las mitocondrias. Los transportadores de electrones que participan en la cadena son: la Plastoquinona (PQ), el complejo citocromo b6-f y la Plastocianina (PC). Existen dos formas de transporte de electrones: − Transporte no cíclico o acíclico − Transporte cíclico − La ATP sintasa, que genera ATP con la energía liberada en el transporte de electrones por la membrana tilacoidal.
Transporte no cíclico de electrones y fotofosforilación no cíclica (fase luminosa acíclica) El transporte no cíclico de electrones permite utilizar la energía luminosa para producir ATP y NADPH. En este transporte intervienen los dos fotosistemas (PSI y PSII), de manera que se produce un flujo lineal de electrones desde el agua hasta el NADPH. El esquema que representa el transporte no cíclico de electrones es lo que se conoce como esquema Z. Básicamente lo que sucede es que los dos fotosistemas al absorber la luz (fotones) emiten electrones, que pasan del PSII al PSI a lo largo de una cadena de transporte de electrones. El paso de los electrones desde un fotosistema a otro a lo largo de la cadena de transporte libera energía, que se utiliza para sintetizar ATP a partir de ADP y P, en un proceso conocido como FOTOFOSFORILACIÓN. Todo este proceso sucede de la forma siguiente: − El PSII al recibir dos fotones libera dos electrones que son recogidos por la plastoquinona (PQ). Los dos electrones que pierde el PSII son repuestos por el agua, para ello las moléculas de agua que se encuentran en el interior del tilacoide son destruidas por acción de la luz, liberándose O2, protones y electrones. Este proceso se denomina FOTÓLISIS del AGUA. Por cada molécula de H2O destruida: H2O −
½ O2 + 2 H+ + 2 e-
La plastoquinona (PQ) al recibir los dos electrones del PSII se activa y capta dos protones del estroma, reduciéndose de PQ a PQH2. Los dos electrones recogidos por la PQ los transfiere al citocromo b6-f y los protones captados se introducen hacia el interior del tilacoide. Esto provoca que el sistema formado por la Plastoquinona y el Citocromo b6-f actúe como una bomba de protones, que bombea protones del estroma hacia el interior del tilacoide. − Si tenemos en cuenta que las moléculas de H2O al destruirse liberan H+ hacia el interior del tilacoide, y que la Plastoquinona bombea también H+ hacia el interior del tilacoide desde el estroma, esto produce un gradiente electroquímico entre el interior del tilacoide y el estroma, de manera que la [H+] aumenta dentro del tilacoide respecto al estroma, lo que provoca un flujo de H+ desde el interior de los tilacoides hacia el estroma, esos H+ salen de los tilacoides a través de las ATP sintasas, activándolas y provocando la síntesis de ATP a partir de ADP y P. Este proceso se conoce como FOTOFOSFORILACIÓN. Como media, por cada tres H+ que atraviesan las ATP sintasas se genera una molécula de ATP. − Los electrones recogidos por la citocromo b6-f son recogidos por la plastocianina (PC), y esta hace llegar a los electrones al PSI. El PSI al igual que el PSII absorbe fotones, cada dos fotones que absorbe libera dos electrones, esos electrones que pierde son los repuestos por la Plastocianina. Los electrones liberados por el PSI son recogidos por la enzima ferredoxina NADP-reductasa, que se activa, capta dos H+ del estroma y reduce el NADP a NADPH + H+. A este proceso se le conoce como FOTORREDUCCIÓN del NADP.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
30
Esquema del transporte acíclico de lectrones y la fotofosforilación acíclica
Transporte cíclico de electrones y fotofosforilación cíclica (fase luminosa cíclica) En esta fase solamente interviene el fotosistema I (PSI), y se genera un transporte de electrones cíclico. Al no intervenir el PSII no hay fotólisis del agua, por lo que no se desprende oxígeno. Tampoco hay reducción del NADP, y solo se obtiene ATP. El PSI puede funcionar independientemente del PSII, cuando la longitud de onda de la luz es superior de 680 nm. Al absorber la luz, libera electrones, estos son recogidos por la ferredoxina que los pasa al citocromo b6-f por medio de la plastoquinona. Del citocromo b6-f los electrones vuelven al PSI por medio de la plastocianina. Al igual que en el transporte acíclico, la plastoquinona bombea protones hacia el interior del tilacoide, que salen al estroma atravesando las ATP sintasas, generandose así ATP. La finalidad de la fase cíclica es subsanar el déficit de ATP que se produce en la fase acíclica. La reducción de una molécula de CO2 en la fase oscura requiere de dos moléculas de NADPH y tres de ATP. En la fase acíclica se forma algo más de una molécula de ATP por cada molécula de agua destruida, por lo que es necesaria una síntesis adicional de ATP, que se consigue mediante el transporte acíclico. Este transporte permite utilizar la energía luminosa para generar ATP sin formar NADPH.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
31
FASE OSCURA DE LA FOTOSÍNTESIS En la fase oscura o biosintética, se utiliza el ATP y el NADPH obtenidos en la fase luminosa, para sintetizar materia orgánica a partir de compuestos inorgánicos. Como fuente de carbono se utiliza el CO2, como fuente de nitrógeno se utilizan los nitratos y como fuente de azufre los sulfatos. Como todas las moléculas tienen un esqueleto carbonado, es importante conocer el mecanismo que permite la incorporación de CO2 a los compuestos orgánicos. Este proceso se llama asimilación o fijación del CO2. El CO2 es asimilado mediante una ruta cíclica, que fue descubierta por Melvin Calvin en la década de 1950, denominada, por ello, ciclo de Calvin.
Ciclo de Calvin o ciclo de las pentosas El Ciclo de Calvin consta de tres fases: 1. Fijación del CO2. 2. Reducción del átomo de carbono procedente del CO2. 3. Regeneración de la ribulosa-1-5-difosfato.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
32
1. Fijación del CO2. El CO2 se incorpora al ciclo, uniéndose a una pentosa, la ribulosa-1-5-difosfato. Esta reacción está catalizada por la enzima ribulosa-1-5-difosfato carboxilasa oxidasa, también llamada rubisco, considerada la enzima más abundante del planeta. La unión entre ambas origina un compuesto inestable, que se disocia en dos moléculas de tres carbonos, el ácido- 3-fosfoglicérico. 2. Reducción del átomo de carbono procedente del CO2. La reducción del átomo de carbono incorporado tiene lugar en dos reacciones diferentes, una fosforilación y la reducción propiamente dicha, etapas que requieren la acción del ATP y el NADPH respectivamente. El resultado de estas dos reacciones es la transformación del ácido-3-fosfoglicérico en la molécula de gliceraldehido-3-fosfato. Como son dos ácidos fosfoglicéricos los que se transforman, se originan dos moléculas de gliceraldehido-3-fosfato. El gliceraldehido-3-fosfato puede tener tres destinos distintos: − Utilizarse para la síntesis de glucosa y otras hexosas. − Seguir la ruta de la glucólisis para formar ácido pirúvico. − Utilizarse en la regeneración de la ribulosa-1-5-difosfato para cerrar el ciclo de Calvin. 3. Regeneración de la ribulosa-1-5-difosfato. Para que el ciclo de Calvin pueda seguir funcionando y continúe fijando CO2 es preciso recuperar la ribulosa-1-5-difosfato. En esta etapa, a partir del gliceraldehido-3-fostato se originan una serie de intermediarios de tres, cuatro, cinco, seis y siete carbonos, y al final se obtiene ribulosa-5-fosfato, que por fosforilación con ATP, se convierte en ribulosa-1-5difosfato, y será la aceptora de nuevas moléculas de CO2.
Estequiometría del ciclo de Calvin En cada “vuelta” del ciclo de Calvin, se fija 1 átomo de carbono procedente del CO2. Vamos a calcular el gasto de ATP y NADPH que tiene que realizar un organismos autótrofo para fabricar una molécula de glucosa de seis carbonos. Para fabricar una molécula de glucosa se han de incorporar 6 moléculas de CO2, y se necesitan otras 6 de ribulosa y por tanto esto implicaría dar 6 vueltas al ciclo de Calvin.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
33
En esquema, sería necesario lo siguiente:
Por tanto, para obtener 1 molécula de glucosa a partir de CO2, los organismos fotosintéticos gastan 12 moléculas de NADPH y 18 moléculas de ATP. 6.1.3. BALANCE GLOBAL DE LA FOTOSÍNTESIS ¿Cuantas moléculas de CO2, H2O, ATP, NADPH y fotones (hν) hacen faltan para fabricar una molécula de glucosa?. ¿cuantas moléculas de O2 se desprenden? 1. ¿Cuántas moléculas CO2 son necesarias? Por cada molécula de GLUCOSA (C6H12O6) son necesarias 6 moléculas de CO2. Esas 6 moléculas se utilizan de la forma siguiente: • los 6 C son utilizados para fabricar una molécula de GLUCOSA (ya que tiene 6 C) • los 6 O2, que equivalen a 12 O, se utilizan así: ¬ 6 O se utilizan para fabricar una molécula de GLUCOSA (ya que tiene 6 O) ¬ 6 O se reducen y generan H2O. Como son 6 O se producirán 6 moléculas de H2O 2. ¿Cuántas moléculas de ATP y NADPH + H+ se necesitan? Según el ciclo de Calvin, cada CO2 fijado y reducido consume 3 ATP y 2 (NADPH + H+). Como se consumen 6 CO2, el total de ATP y NADPH consumidos serán 6 CO2
18 ATP + 12 (NADPH + H+)
3. ¿Cuántas moléculas de H2O se necesitan?. Los átomos de H del (NADPH + H+) que se forma en la fase luminosa proceden del H2O. Como se necesitan 12 (NADPH + H+) para formar una molécula de GLUCOSA, eso quiere decir que se consumen 12 moléculas de H2O, una por cada NADPH + H+. En resumen, hasta ahora tenemos que, para fabricar una molécula de GLUCOSA se consumen 6 CO2 + 12 H2O + 18 ATP + 12 (NADPH + H+) y se obtiene 1 GLUCOSA, se desprenden 6 O2 y se forman 6 H2O. BALANCE GLOBAL 18 ATP
18 (ADP + P)
6 CO2 + 12 H2O
C6H12O6 + 6 O2 + 6 H2O (GLUCOSA) 12 (NADPH + H+)
12 NADP+
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
34
4. ¿Cuantos fotones (hν) son necesarios?. Los fotones se absorben en la FASE LUMINOSA, por cada molécula de H2O que se descompone (FOTÓLISIS del AGUA) hacen falta 4 FOTONES (dos por cada FOTOSISTEMA). Como se consumen y descomponen 12 H2O, se necesitan en total 48 FOTONES.
6.1.4. FOTOSÍNTESIS BACTERIANA Las bacterias fotosintéticas, al no contener cloroplastos, los pigmentos fotosintéticos y los transportadores de electrones se localizan en invaginaciones de la membrana. Los pigmentos fotosintéticos, salvo en las cianobacterias, son las bacterioclorofilas, ligeramente diferentes a las clorofilas. La mayoría de las bacterias fotosintéticas tienen exclusivamente un fotosistema y obtienen el ATP por fotosfosforilación cíclica. La obtención de poder reductor no está ligada al proceso fotosintético. Al carecer de fotosistema II, estos microorganismos no pueden utilizar el agua como donador de electrones y, en consecuencia, no se desprende oxígeno en la fotosíntesis, por lo que es anoxigénica. Solamente las cianobacterias realizan una fotosíntesis prácticamente idéntica a la de las plantas verdes, la fotosíntesis oxigénica. 6.1.5. FACTORES QUE INFLUYEN EN LA FOTOSÍNTESIS La actividad fotosintética constituye un pilar básico en la fisiología de los organismos que la llevan a cabo. Su adecuada realización es fundamental para su supervivencia y por ello es un proceso muy bien regulado. En esta regulación intervienen varios factores. 1. La luz. Por lo general, al aumentar la intensidad luminosa, aumenta la actividad fotosintética. No obstante, las distintas especies de plantas están adoptadas a intensidades de luz diferentes; por eso hay plantas adaptadas a zonas de penumbra y otras que precisan una luz muy intensa. Si la intensidad luminosa supera ciertos límites, se produce el fenómenos de la fotooxidación, y los pigmentos fotosintéticos se oxidan de forma irreversible. Para la misma intensidad, las adaptadas a climas tropicales presentan mayor rendimiento que las plantas de climas templados, y nunca llegan a la saturación lumínica. 2. La concentración de CO2. La eficacia de la fotosíntesis aumenta al aumentar la concentración de CO2, hasta un valor máximo en que se estabiliza, debido a la saturación de la enzima rubisco en el ciclo de Calvin. 3. La temperatura. Todas las reacciones metabólicas, y por tanto la fotosíntesis, se aceleran al aumentar la temperatura, hasta un valor determinado. A partir de este se desnaturalizan las enzimas y el proceso se detiene. Cada especie tiene una temperatura óptima en la que la eficacia de la fotosíntesis es máxima. 4. La humedad. El grado de humedad en el suelo y en el aire son factores que condicionan el rendimiento fotosintético. Si el aire tiene poca humedad, las plastas cierran los estomas para evitar pérdidas de agua y esto dificulta la captación del CO2.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
35
5. La concentración de oxígeno. Cuando la concentración de O2 es muy elevada la eficacia de la fotosíntesis disminuye debido a un proceso denominado fotorrespiración. La fotorrespiración es un fenómeno que afecta a las plantas de climas templados (como España), denominadas también plantas C3, y sucede cuando el clima se vuelve más cálido y las plantas cierran sus estomas para evitar la desecación, aumentando así los niveles de O2 en el interior de la hoja. La enzima rubisco, además de catalizar la fijación del CO2, tiene actividad oxidasa, oxida a la ribulosa-difosfato incorporándole el O2, lo que tras varias reacciones, origina CO2 y H2O, lo que representan un saldo negativo para la economía de la planta. Se piensa que la fotorrespiración es un proceso que protege a las plantas de la fotooxidación.
Fotorrespiración y plantas C4 Las plantas de climas tropicales, donde el clima es mucho más cálido han resuelto este problema porque captan el CO2 de forma distinta. En sus hojas tienen dos tipos de células cargadas de cloroplastos donde realizan la fotosíntesis, las células del mesófilo y las células perivasculares (están alrededor de los nervios de las hojas). El CO2 que entra por los estomas de las hojas es fijado en las células del mesófilo por una molécula de tres carbonos, el ácido fosfoenolpirúvico (PEPA) y se convierte en una molécula de cuatro carbonos (por eso las plantas a las tropicales se las designa como C4), el oxalacetato. Este se transforma en otra sustancia, el ácido málico que sale de las células del mesófilo, se introduce en las células perivasculares y desprende CO2 que es fijado por la ribulosa, convirtiéndose el málico en ácido pirúvico, que regresa a las células del mesófilo y se transforma de nuevo en PEPA. Así pues el ácido málico se convierte en una sustancia que está continuamente bombeando CO2 y por lo tanto los niveles de CO2 en las células perivasculares se mantienen más elevados que los de oxígeno, evitando así la fotorrespiración. Esta vía C4 de fijación del carbono, llamada ciclo de Hatch-Slack, tiene un mayor consumo de ATP y NADPH que la fijación del CO2 de la forma habitual, pero compensa con creces las pérdidas que produciría la fotorrespiración.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
36
6.1.6. IMPORTANCIA DE LA FOTOSÍNTESIS La fotosíntesis es un proceso de enorme importancia hay en día en la Biosfera, pero a lo largo de la evolución ha sido crucial en la transformación de la atmósfera primitiva. A nivel de la Biosfera, es fundamental porque: ▪ Es el principal mecanismo de BIOSÍNTESIS de materia orgánica a partir de compuestos inorgánicos. La materia orgánica fabricada por los organismos fotosintéticos pasa de unos seres vivos a otros mediante las cadenas tróficas. ▪ Permite el equilibrio ecológico entre los organismos autótrofos y heterótrofos. ▪ Transforma la energía luminosa en energía química, que es la utilizada por los seres vivos. ▪ Libera oxígeno, utilizada en la respiración aerobia para oxidar la materia orgánica. A nivel evolutivo, la fotosíntesis fue el proceso responsable del cambio de la atmósfera primitiva reductora a una atmósfera oxidante, a medida que las cianobacterias, hace 2.000 millones años, liberaban oxígeno al realizar una fotosíntesis oxigénica. La aparición del oxígeno atmosférico supuso el fin de la síntesis abiótica de materia orgánica, la aparición de organismos aerobios y la formación de la capa de ozono protectora de la radiación ultravioleta. 6.2. QUIMIOSÍNTESIS La quimiosíntesis es un tipo de metabolismo exclusivo de procariotas, en concreto de las bacterias quimiosintéticas o quimilitotrofas. Estas bacterias son autótrofas, por lo que fabrican compuestos orgánicas a partir de la materia inorgánica que toman del medio, y para ello utilizan la energía que se desprende de la oxidación de compuestos inorgánicos (amoníaco, nitritos, sulfuros, ión ferroso, hidrógeno, etc.). Según esto, la quimiosíntesis se puede dividir en dos fases: > Obtención de energía. La energía desprendida en la oxidación de compuestos inorgánicos se utiliza para fabricar ATP y NADH. > Producción de materia orgánica. EL ATP y NADH obtenidos en la fase anterior se utilizan para la síntesis de materia orgánica por medio del ciclo de Calvin.
▪ ▪ ▪ ▪
Las bacterias quimiosintéticas se clasifican por el tipo de oxidación que realizan: Bacterias nitrificantes: oxidan compuestos de nitrógeno. Se distinguen dos géneros, Nitrosomas y Nitrobacter, que se complementan y comparten el mismo hábitat y están ampliamente distribuidas en el agua y en el suelo. Sulfobacterias: oxidan azufre o compuestos reducidos de azufre, como H2S o el tiosulfato. Ferrobacterias: oxidan el hierro ferroso a hierro férrico. Abundan en ciertas charcas de agua dulce con sales reducidas de hierro. Bacterias del hidrógeno: oxidan el H2, produciendo agua. Son frecuentes en hábitats donde se producen fermentaciones que liberan hidrógeno como producto final.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
37
6.3. OTRAS RUTAS ANABÓLICAS
Gluconeogénesis La gluconeogénesis es una ruta metabólica por la que tiene lugar la síntesis de glucosa a partir de precursores más sencillos, y es una ruta inversa a la glucólisis. La célula utiliza esta ruta metabólica cuando necesita glucosa y no dispone de ella, de manera que los metabolitos intermedios que se producen en la glucólisis se utilizan para fabricar glucosa. La gluconeogénesis es un proceso energéticamente desfavorable, y consume unos 6 ATP por molécula de glucosa que se fabrica. Esta ruta tiene lugar preferentemente en el hígado y en parte en el riñón, y mediante ella es posible sintetizar glucosa a partir de ácido láctico, aminoácidos o algún metabolito del ciclo de Krebs. Así pues, evita un excesiva acumulación de ácido láctico en el músculo cuando no hay suficiente oxigenación.
Biosíntesis de ácidos grasos y triglicéridos Los ácidos grasos son el componente fundamente de todos los lípidos saponificables, por ello su formación es una etapa importante en la síntesis de lípidos. Los ácidos grasos se sintetizan a partir del acetil-CoA que se fabrica en la mitocondria. El acetilCoA sale al citosol y sufre unas reacciones de condensación, deshidratación y reducción que conducen a la síntesis de ácidos grasos. El complejo enzimático que lleva a cabo todo el proceso es el ácido grasosintetasa. Las grasas o triglicéridos posteriormente se formarán por esterificación de tres moléculas de ácidos grasos con una de glicerina. Para que se produzca ambos compuestos deben estar activados, los ácidos grasos se activan uniéndose a la coenzima A (CoA) y la glicerina a un grupo fosfato. Los triglicéridos se fabrican en el citoplasma de las células hepáticas y en los adipocitos.
Biosíntesis de aminoácidos Los aminoácidos son indispensables para cualquier ser vivo, ya que son los componentes de las proteínas y además son importantes precursores en la síntesis de otras moléculas, como hormonas, neurotransmisores, pigmentos, etc. La biosíntesis de aminoácidos tiene lugar en el citoplasma, y en ella intervienen dos procesos: la síntesis del esqueleto carbonado, a partir de precursores metabólicos; y la incorporación del grupo amino mediante reacciones de transaminación. Los aminoácidos suelen agruparse por familias según el precursor metabólico del que parte la síntesis del esqueleto carbonado, así se habla de aminoácidos de la familia del aspartato, de la familia del glutamato, de la familia del ácido pirúvico, etc. Las plantas y las bacterias quimiosintéticas pueden fabricar el grupo amino a partir de compuestos inorgánicos, como el nitrato, amoníaco, etc. Pero los animales y otros organismos heterótrofos, solo podemos sintetizar nuevos aminoácidos a partir de los aminoácidos adquiridos en la dieta, por medio de transaminaciones. Las reacciones de transaminación están catalizadas por las transaminasas del hígado. Aquellos aminoácidos que no se pueden fabricar a partir de otros se denominan aminoácidos esenciales, y en el ser humano son nueve.
Esquema de la nutrición celular
BIOLOGÍA 2º METABOLISMO CELULAR
FOTOFOSFORILACIÓN ACÍCLICA FOTORREDUCCIÓN DEL NADP
Estroma
PC Interior tilacoide
FOTÓLISIS DEL AGUA
FOTOFOSFORILACIÓN
Biología 2º Bachillerato
Tema 4: La nutrición celular. El metabolismo
ACTIVIDADES TEMA 4. LA NUTRICIÓN CELULAR: EL METABOLISMO TRANSPORTE, ATP y METABOLISMO 1. ¿Qué quiere decir que la permeabilidad de la membrana es selectiva y cuál es la causa de ello?. 2. ¿Qué tipos de proteínas de transporte hay en la membrana plasmática?. En qué proceso interviene cada una de ellas. 3. Si una célula se encuentra rodeada por un líquido cuya concentración de O2 y de aminoácidos es inferior a la del contenido celular, ¿podrían entrar dichas sustancias en la célula?. Razona la respuesta. 4. Si en una célula se impide la síntesis de ATP, ¿podría quedar afectada alguna de las funciones de la membrana plasmática?. ¿Porqué?. 5. Completa el cuadro: CATABOLISMO
ANABOLISMO
Energía: Consume/Desprende Materia: Degrada/Sintetiza Reacciones: Oxidación/Reducción 6. ¿Qué diferencias y semejanzas existen, respecto a los procesos metabólicos que realizan, entre las células autótrofas y heterótrofas?. ¿Y entre las fotosintéticas y quimiosintéticas?. 7. ¿Qué quiere decir que el acetil-CoA es una encrucijada metabólica?. 8. ¿Por qué una determinada via catabólica no es exactamente la inversa de su correspondiente anabólica?. 9. Considerando que la energía es el dinero con que se pagan los trabajos celulares, establece la relación entre las siguientes moléculas energéticas y sus equivalentes en términos monetarios, razonando la respuesta: Almidón, glucógeno, grasas Glucosa ATP
Dinero de bolsillo Libreta a plazo fijo Cuenta corriente
10. ¿Cómo se puede aumentar la velocidad de cualquier reacción y cómo se realiza en los seres vivos?.
Biología 2º Bachillerato
Tema 4: La nutrición celular. El metabolismo
11. Tanto en la respiración mitocondrial como en la fase luminosa de la fotosíntesis hay enzimas que trabajan con NADH o NADPH, una cadena de transporte de electrones y ATP-sintetasas, pero hay ciertas diferencias. Responde a las cuestiones del siguiente cuadro: RESPIRACIÓN
FOTOSÍNTESIS
a) La cadena transportadora de electrones está en: b) El transportador de hidrógenos es: c) ¿Se produce oxidación del NADH o reducción del NADP+?. d) Los protones (H+) son aportados por: e) Los protones (H+) son introducidos en: f) Los protones (H+) se unen a ......... para producir: g) La parte globosa de la ATP-sintetasa está dirigida hacia: h) La síntesis de ATP se denomina:
CUESTIONES DE SELECTIVIDAD Respecto al metabolismo intermediario: a) Indique los posibles orígenes del acetil-CoA que entra en el ciclo de Krebs para condensarse con el oxalacetato b) ¿A qué molécula da lugar dicha condensación?. c) Indique el compartimento subcelular en el que ocurre esta reacción Comenta brevemente y calcula el balance energético de la degradación total a CO 2 y H2O de una molécula de glucosa. Explica en los siguientes procesos metabólicos: a) Glucólisis; b) Ciclo de Krebs; c) Fosforilación oxidativa; cuáles son los productos finales que se obtienen en ellos e indica en qué compartimentos celulares y en que subestructuras de los mismos tienen lugar. Explique los factores que modulan la actividad de la fotosíntesis vegetal. Referido a la fotosíntesis: a) ¿Cuál es la ecuación global que la describe?. b) ¿Dónde se localiza la cadena de transportadores de electrones?. c) ¿Cuál es el dador final de electrones en la fotofosforilación cíclica?. ¿Y en la acíclica?. d) ¿Cuál es el compuesto aceptor del CO2 en el ciclo de Calvin?. La incubación de células con cianuro interrumpe el consumo respiratorio de oxígeno. Al respecto, contestar las preguntas siguientes, razonando la respuesta: a) ¿Qué proceso metabólico se inhibe por el cianuro?. b) ¿Cuál es la función principal del proceso inhibido?. c) ¿En qué orgánulo celular y en qué estructura de dicho orgánulo ocurre?.
Biología 2º Bachillerato
Tema 4: La nutrición celular. El metabolismo
ENZIMAS y CINÉTICA ENZIMÁTICA
Biología 2º Bachillerato CATABOLISMO
Tema 4: La nutrición celular. El metabolismo
Biología 2º Bachillerato
FOTOSÍNTESIS
Tema 4: La nutrición celular. El metabolismo
BIOLOGÍA 2º BACHILLERATO ACTIVIDADES REFUERZO TEMA 4. METABOLISMO Las siguientes figuras representan diversos procesos metabólicos estudiados en clase. representada, averigua: • ¿Qué representa?. • ¿En qué estructura y subestructura celular tiene lugar?. • Nombra los procesos o fases indicados con números (Fig. 1, 4) o letras (Fig. 2, 3). • Nombra los compuestos señalados con números (Fig 3, 5, 6).
De cada figura
Fig. 2
Fig. 4
Fig. 3
Fig. 5 Fig. 5
Fig. 6
BLOQUE III HERENCIA Y GENÉTICA MOLECULAR
TEMA 5. LA HERENCIA Y GENÉTICA MOLECULAR
TEMA 5. LA HERENCIA y GENÉTICA MOLECULAR 1. GENÉTICA: CONCEPTOS BÁSICOS 2. EXPERIMENTOS y LEYES DE MENDEL 3. TEORÍA CROMOSÓMICA DE LA HERENCIA 4. MODIFICACIONES A LAS PROPORCIONES DE LAS LEYES DE MENDEL 5. DETERMINACIÓN GENÉTICA DEL SEXO 6. HERENCIA LIGADA AL SEXO 7. EL ADN COMO PORTADOR DE LA INFORMACIÓN GENÉTICA 8. LA DUPLICACIÓN DEL ADN 8.1. 8.2. 8.3.
HIPÓTESIS PROPUESTAS PARA LA DUPLICACIÓN MECANISMO DE DUPLICACIÓN DEL ADN SISTEMAS DE REPARACIÓN DEL ADN
9. LA EXPRESIÓN DEL MENSAJE GENÉTICO 9.1. 9.2.
LA TRANSCRIPCIÓN TRADUCCIÓN o BIOSÍNTESIS DE PROTEÍNAS
10. EL CÓDIGO GENÉTICO 11. REGULACIÓN DE LA EXPRESIÓN DE LOS GENES 12. MUTACIONES 13. INGENIERÍA GENÉTICA
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
1
1. GENÉTICA: CONCEPTOS BÁSICOS Genética: es la ciencia que estudia la herencia biológica, es decir, la transmisión de los caracteres morfológicos y fisiológicos que pasan de un individuo a sus descendientes. Existen dos grandes vías de investigación para explicar todos estos fenómenos relacionados con la herencia biológica: Genética clásica o mendeliana: estudia la herencia a través de experimentos de reproducción, partiendo de los caracteres observables (fenotipo), comprueba su transmisión por herencia a los descendientes, y a partir de proporciones matemáticas intenta averiguar cuál es la información biológica de los individuos (genotipo). Genética molecular: estudia las moléculas que contienen la información biológica (ADN) y los procesos bioquímicos de transmisión y manifestación. El sentido de su estudio es inverso a la Genética clásica, partiendo de la información (genotipo), se deduce cómo serán los caracteres (fenotipo). Gen: es la unidad de material hereditario. Es un fragmento de ácido nucleico, generalmente ADN (salvo en algunos virus, en los que es ARN), que lleva la información para un carácter. Mendel desconocía su naturaleza, y los denominó caracteres hereditarios. Se encuentran localizados en los cromosomas, y la posición que ocupan se denomina locus. A los genes se les designa con símbolos, generalmente con letra cursiva. La letra que se utiliza suele ser la inicial del carácter. Otro tipo de notación es el uso de superíndices, que permite simbolizar más de dos genes que informan sobre el mismo carácter. Alelos: cada uno de los genes que informa sobre el mismo carácter. En los individuos diploides, cada caracteristica hereditaria viene determinada por dos copias del mismo gen, a cada copia se le denomina alelo, y cada uno se hereda de un progenitor. Los alelos se localizan en cada miembro de la pareja de cromosomas homólogos. Homocigótico o raza pura: son los individuos que para un carácter poseen los alelos iguales. Heterocigótico o raza híbrida: individuo que poseen para una carácter los alelos diferentes. Genotipo: conjunto de genes que presenta un individuo para una o varias características, y que ha heredado de sus progenitores. Fenotipo: es la manifestación externa del genotipo, es decir, la suma de los caracteres observables en un individuo. El fenotipo depende del genotipo y de la influencia del ambiente: Fenotipo = Genotipo + Ambiente Por ejemplo, dos plantas con igual genotipo se desarrollan de forma diferente, si una está al sol y otra a la sombra. Herencia dominante: se dice que un carácter tiene herencia dominante cuando en los individuos híbridos, solo se manifiesta uno de los dos alelos que rigen sobre ese carácter. El alelo que se manifiesta se denomina alelo dominante, y el que queda oculto alelo recesivo. Los alelos recesivos solamente se manifiestan en los individuos que son de raza pura para esa característica.
2. EXPERIMENTOS Y LEYES DE MENDEL Gregor Johann Mendel nació en 1822 en Heinzendorf (Austria) e ingresó en el monasterio agustino de Brno en 1843 para continuar su educación. Asistió durante dos años a la Universidad de Viena, donde se formó sólidamente en Matemáticas, Física y Ciencias Naturales. De vuelta al monasterio, emprendió sus experimentos con plantas de guisante (Pisum sativum). Realizó miles de cruzamientos, recogiendo una cantidad ingente de datos sobre las frecuencias con se transmitía cada una de las características de la planta. A partir de estos datos postuló una serie de leyes sobre la herencia de los caracteres biológicos. Mendel publicó sus descubrimientos en 1866, en una revista de poca difusión y en un momento en que el interés científico estaba muy polarizado sobre la teorías evolucionista de Darwin. La constancia de los factores hereditarios de Mendel no parecía compatible con la evolución de las especies, y lo que en realidad constituía su explicación científica fue ignorada. Pasaron treinta y cuatro años, en una de las coincidencias más sorprendentes de la investigación científica, tres autores por separado, el holandés De Vries, el alemán Correns, y el austríaco Tschermak, redescubrieron en el mismo año (1900) los hallazgos de Mendel.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
2
Primer experimento y Primera Ley de Mendel Mendel trabajó fijándose en siete caracteres, cada uno de los cuales podía tener dos manifestaciones o características diferentes: Forma de la semilla Color de los cotiledones Color de la cubierta Forma de la legumbre Color de la legumbre no madura Posición de la flor Longitud del tallo En su primer tipo de experimentos se fijó cómo se transmitían cada una de estas características por separado en la descendencia. Escogió plantas de guisantes con semillas amarillas y plantas con semillas verdes, y se cercioró de que se trataban de razas puras. Como la planta de guisante se reproduce normalmente por autofecundación, lo primero que comprobó es que siempre que se autofecundaban plantas nacidas de semillas amarillas, daban semillas amarillas, y si se trataba de la variedad de semillas verdes, siempre daban frutos con semillas verdes. Cruzó ambas variedades, cortando los estambres de las flores de una de las variedades antes de que maduraran y las fecundaba artificialmente con el polen recogido de las flores de otra variedad. Esperaba que aparecieran los nuevos frutos con sus semillas y anotaba sus características. Recogidas todas las semillas del cruzamiento, observó que todas ellas eran de color amarillo. De este experimento se deduce la primera ley de Mendel, llamada Ley de la uniformidad: “Todos los descendientes del cruce entre dos razas puras son iguales entre sí”. Segundo experimento y Segunda Ley de Mendel Surgió entonces la dificultad de encontrar una explicación científica al resultado anterior. Había que dar explicación a una interesante pregunta: ¿había desaparecido el otro carácter?. Para comprobarlo, plantó los guisantes del cruzamiento anterior, y dejó las plantas resultantes se autofecundaran, y el resultado fue la aparición de las dos clases de semillas, amarillas y verdes, en una proporción de 3 a 1 a favor de la variedad amarilla, que es la que había aparecido en todos los individuos de la primera generación. El hecho de que aparecieran variedades de semilla verde indicaba que las plantas que se habían autofecundado tenían información para esa característica. Si en ellas no se manifestaba, debía ser porque la otra información (semilla amarilla) era dominante. A la característica que se manifiesta, Mendel la denominó carácter dominante, y la que no se manifiesta carácter recesivo. A las partículas o sustancias responsables de transmitir dichas características las denominó factores hereditarios (lo que hoy llamamos genes). A partir de este segundo experimento, dedujo la segunda ley, llamada Ley de la segregación: “Los dos factores hereditarios que informan para un mismo carácter, no se fusionan o mezclan, sino que permanecen diferenciados durante toda la vida del individuo y se segregan, es decir, se separan y reparten en el momento de la formación de los gametos”.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
3
Tercer experimento y Tercera Ley de Mendel En su tercer tipo de experimento Mendel estudió la descendencia entre plantas que diferían en dos caracteres independientes, para estudiar si existían interrelaciones entre ellos, es decir, si uno influyen en la manifestación de otro. Realizó cruces entre plantas de guisante que siempre daban semillas amarillas y lisas y plantas de raza pura que daban semillas verdes y rugosas. Obtuvo una descendencia homogénea amarilla y lisa. Luego permitió la autofecundación de estas plantas, y de las 566 semillas recogidas, encontró que 3l5 eran semillas amarillas y lisas, 108 verdes y lisas, 101 amarillas y rugosas y 32 verdes y rugosas. Dividiendo todos estos resultados por el menor se obtiene: Amarillas lisas 315/32= 9/16 Amarillas rugosas 108/32 = 3/16 Verdes lisas 101/32 = 3/16 Verdes rugosas 32/32 = 1/16 La proporción entre ellas es de 9:3:3:1, la misma proporción que se obtiene si se combinan al azar cuatro tipo de factores hereditarios totalmente independientes entre sí, y de forma que haya dos que inhiban la manifestación de otros dos, que son sus antagónicos. Basándose en sus experimentos, se deduce la tercera ley de Mendel, llamada Ley de la independencia de los factores hereditarios: ”Cada uno de los factores hereditarios no antagónicos se transmiten a la descendencia con absoluta independencia de los demás”.
Aciertos de los experimentos de Mendel:
Utilizar una especie autógama, lo que permite obtener fácilmente razas puras para algunos caracteres Elegir caracteres cualitativos fácilmente visibles Iniciar sus experimentos fijándose en un solo carácter Dar un tratamiento estadístico a los datos Tener la suerte de seleccionar para su tercer experimento caracteres no ligados
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
4
3. TEORÍA CROMOSÓMICA DE LA HERENCIA Cuando se redescubrieron los trabajos de Mendel en 1900, dos investigadores por separado, W. S. Sutton en estados Unidos, y T. Boveri en Alemania observaron que el comportamiento de los cromosomas durante la meiosis era equivalente al de los genes de Mendel. Por ello, desde 1902 se estableció la teoría de que los genes estaban localizados en los cromosomas. Esta afirmación constituye la base de la Teoría cromosómica de la herencia. En poco tiempo, algunos experimentos confirmaron esta hipótesis. En 1.910, Thomas H. Morgan, de la Universidad de Columbia (EE.UU), trabajando con Drosophila melanogaster, descubrió que había algunos genes que se heredaban juntos, lo que contrastaba con la tercer ley de Mendel. Concluyó que debían estar en el mismo cromosoma y próximos entre sí, denominándose por ello genes ligados. En otros experimentos descubrió que dichos genes se heredan de forma independiente, pero aparecía en la descendencia con una frecuencia que no se ajustaba a los resultados de Mendel, lo que le hizo suponer que los genes se disponen linealmente en los cromosomas, y éstos se pueden entrecruzar e intercambiarse fragmentos. Así pues el contenido de la Teoría cromosómica de la herencia se resume en estas afirmaciones: 1.Los factores hereditarios o genes se encuentran situados en los cromosomas. 2.Cada gen ocupa un lugar determinado en un cromosoma concreto. Este lugar se denomina locus (en plural loci). Los alelos se encuentran en los loci de los cromosomas homólogos, por esta razón existe un par de alelos para cada carácter 3.La ordenación de los genes es lineal, de forma que aquellos que se encuentren próximos tienden a heredarse juntos, y se denominan genes ligados. 4.Los genes de un mismo cromosoma se pueden heredar de forma independiente por recombinación debido a un intercambio de material entre cromosomas o sobrecruzamiento.
4. MODIFICACIONES A LAS PROPORCIONES DE LAS LEYES DE MENDEL Existen algunos casos en los que las Leyes de Mendel parecen no cumplirse. En realidad, esto no es así, sino que las relaciones entre genes o el propio efecto génico alteran los resultados. Entre estos casos se pueden citar los siguientes: EPISTASIA. Consiste en la influencia que existe entre genes diferentes que afectan a la expresión del mismo fenotipo. En ella, un gen (epistático) suprime la acción de otro gen no alélico (hipostático). Así la proporción 9:3:3:1 se ve alterada. HERENCIA INTERMEDIA. Se produce cuando en un híbrido, los dos alelos tienen la misma “fuerza” para manifestarse, por lo que aparece un fenotipo intermedio entre las dos razas puras.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
5
CODOMINANCIA. Se da cuando dos alelos son equipotentes, de manera que en los híbridos se manifiestan los dos caracteres. Por ejemplo la herencia de los grupos sanguíneos, los individuos IAIA son del grupo A, los individuos IBIB son del grupo B, y los individuos IAIB son del grupo AB. GENES LETALES. Un gen letal es aquel que produce la muerte de un individuo antes de que alcance su madurez sexual. Lógicamente, los individuos que mueren no son incluidos en la descendencia y, por tanto las frecuencias se ven alteradas. ALELISMO MULTIPLE. Se produce cuando para un mismo carácter existen varios alelos (más de dos) que constituyen una serie alélica. Estos múltiples alelos siguen las leyes mendelianas, pero al existir más de dos alternativas, los fenotipos que aparecen son más variados. Un ejemplo son los grupos sanguíneos ABO en el ser humano. HERENCIA CUANTITATIVA, CONTÍNUA o POLIGÉNICA. Los caracteres habitualmente estudiados sonde tipo cualitativo, es decir, presentan pocas alternativas, y estas son claras y fáciles de observar. Los caracteres cuantitativos son los que presentan diferentes graduaciones entre dos valores extremos. Por ejemplo, la altura, el peso, el coeficiente de inteligencia,... El carácter cuantitativo depende de varios genes que contribuyen en determinada proporción. A estos genes se les denomina poligenes (Herencia poligénica), cada uno de ellos produce un efecto pequeño. Un ejemplo es el color de la piel, que depende de tres o cuatro pares de genes, además el ambiente ayuda a que se dé una serie de tonalidades.
5. DETERMINACIÓN GENÉTICA DEL SEXO Un aspecto importante del fenotipo de un organismo es su sexo, que en la mayoría de los casos se halla controlado por genes, situados en cromosomas específicos (cromosomas sexuales), aunque también existen organismos en los que el sexo depende de factores ambientales. Determinación cromosómica En numerosos organismos, entre ellos la especie humana, la determinación del sexo se realiza por la presencia de cromosomas especiales, llamados cromosomas sexuales o heterocromosomas, que se diferencian del resto, que son los autosomas o cromosomas autosómicos. Existen tres sistemas distintos de determinación cromosómica: Sistema XX/XY. El sexo femenino presenta dos cromosomas iguales (XX) y todos los gametos que producen llevan el cromosoma X (sexo homogamético), y el masculino presenta un cromosoma de cada tipo (XY) y por tanto la mitad de sus gametos llevan el cromosoma X y la otra mitad el cromosoma Y (sexo heterogamético). Es el tipo de determinación de la especie humana y de otros muchos animales (mamíferos, equinodermos, moluscos y gran número de artrópodos).
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
6
Sistema ZZ/ZW. Las hembras son el sexo heterogamético (ZW) y los machos el homogamético (ZZ). Es propia de las aves, algunos anfibios y reptiles y de las mariposas. Sistema XX/XO o ZZ/ZO. Se caracteriza por que uno de los dos sexos solo tiene un cromosoma sexual. Se da en muchos insectos.
Determinación por haplodiploidía En algunos insectos sociales (abejas, avispas, hormigas) no existen cromosomas sexuales, y el sexo está determinado por el número de dotaciones cromosómicas. Así los individuos diploides (2n) son hembras y los haploides (n) son machos. Las hembras se desarrollan a partir de óvulos fecundados y los machos a partir de óvulos sin fecundar por partenogénesis. Determinación génica En algunas plantas, y también en algunos animales, el sexo depende de una o varias parejas de genes. Un ejemplo muy estudiado es el de la planta Ecballium elaterium (pepinillo del diablo), en la que el sexo depende de una serie alélica (a0>a+>ad), en donde el alelo a0 determina el sexo masculino, el alelo a+ determina característica hermafroditas y el alelo ad determina características femeninas. Determinación ambiental En algunos animales, la determinación del sexo depende de circunstancias ambientales, como la temperatura. Así entre los grandes saurios (cocodrilos, caimanes y aligátores) el sexo está determinado por la temperatura a la que se incuban los huevos, si es superior a 27 ºC se obtendrán machos y si es inferior nacerán hembras.
6. HERENCIA LIGADA AL SEXO Hay características que no se expresan en la misma proporción en los dos sexos. Esto se debe a que los genes responsables de ellas se encuentran localizados en uno de los dos cromosomas sexuales. Los caracteres cuyo alelos están localizados en los cromosomas sexuales se dice que están ligados al sexo. El cromosoma X y el cromosoma Y, a pesar de ser distintos, tiene regiones que se aparean y entrecruzan durante la meiosis (segmento homólogo) y otras que no lo hacen (segmento diferencial). Los alelos localizados en el segmento homólogo o apareante están parcialmente ligados al sexo, y los que se localizan en el segmento diferencial están totalmente ligados al sexo.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
7
Los casos más llamativos de herencia ligada al sexo son: Herencia ligada al cromosoma Y. Todos los genes que se encuentren en el segmento diferencial del cromosoma Y son heredados únicamente por los hijos varones. Se llama herencia holándrica, ya que se manifiesta solo en los varones, como la presencia de pelos en las orejas o la ictiosis (piel gruesa, oscura y áspera). Herencia ligada al cromosoma X. Se debe a genes localizados en el segmento diferencial del cromosoma X. La condición aparece generalmente en los varones, mientras que en las mujeres, que lleven el gen, aunque son fenotípicamente normales, pueden transmitir el carácter a sus hijos. Dos ejemplos bien conocidos son el daltonismo y la hemofilia, enfermedades provocadas por un gen recesito localizado en el segmento diferencial del cromosoma X. Para que una mujer padezca la enfermedad debe ser homocigótica recesiva, mientras que los hombres, que son hemicigóticos, basta para que la padezcan que el gen se encuentre en el único cromosoma X. El daltonismo es un defecto visual que hace que la persona afectada tenga dificultades para distinguir con claridad el color rojo del verde. La hemofilia es una enfermedad que provoca problemas en la coagulación de la sangre debido a la falta de alguno de los factores de coagulación (factor VIII). Herencia influida por el sexo Hay ciertas características que se expresan dependiendo del sexo del individuo. Generalmente se comportan así los caracteres influidos por el ambiente hormonal del individuo. Así, la calvicie en la especie humana y la presencia o ausencia de cuernos en algunas razas ovinas, están determinadas por genes localizados en la región homóloga de las cromosomas sexuales o bien en autosomas, y cuya manifestación depende del sexo.
GENOTIPO: AaBb
PARENTALES
Más frecuencia
Igual frecuencia Menos frecuencia
RECOMBINANTES
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
8
7. EL ADN COMO PORTADOR DE LA INFORMACIÓN GENÉTICA A principios del siglo XX se produjeron grandes avances en genética, una vez, que se redescubrieron los trabajos de Mendel. Así fue a principios de este siglo cuando se formularon la teoría cromosómica de la herencia, que postulaba que las características hereditarias debían localizarse en los cromosomas, y la teoría neodarvinista que reformaba la teoría de la evolución de Darwin a partir de los conocimientos de genética. Pues bien, a pesar de todos estos avances, aún no se tenía claro cuál era la naturaleza de los genes. Se sabía que los cromosomas, que contenían los genes, estaban formados por proteínas y ADN, y parecía que eran las proteínas, debido a su compleja organización y a sus propiedades catalíticas, las que podían contener la información genética. Algunos datos a favor del ADN como portador del mensaje genético podrían ser:
La presencia de ADN en núcleo y en los cromosomas La cantidad de ADN en las células de los individuos de una misma especie es constante Al aumentar la complejidad de un organismo, aumenta su contenido de ADN El ADN absorbe la luz UV de 360 nm, causante de las mutaciones.
Tres experimentos cruciales en toda esta historia fueron los que despejaron las dudas: Griffith (1.928), Avery y col. (1.944) y Hersey y Chase (1.952). (Figuran como apéndice del tema) Fueron los experimentos de Avery y sus colaboradores los que identificaron al ADN como la molécula portadora de la información genética. Años después los experimentos de Chargaff y Watson y Crick demostraron la composición y estructura del ADN. El nacimiento de la Genética molecular comenzaría a partir de entonces, al conocer la estructura del ADN y su papel biológico.
8. LA DUPLICACIÓN DEL ADN Todos los seres vivos somos temporales, tarde o temprano nos llega la muerte. Para que la especie no se extinga, es preciso que nos reproduzcamos, dando lugar a nuevos individuos que continúen viviendo. Para originar estos nuevos individuos es necesario formar nuevas copias de ADN, a partir del ADN progenitor, que pasarán a los nuevos individuos. Cuando una célula se divide transmite su información genética a las células hijas, para lo cual duplica previamente su ADN mediante el mecanismo denominado replicación o duplicación. La estructura del ADN es idónea para este proceso, al estar formado por dos hebras, la replicación del ADN implicaría la separación de las mismas, actuando cada una de molde para la construcción de nuevas cadenas, según la complementariedad de las bases. Así la secuencia de nucleótidos se duplica con exactitud y la información genética permanece constante. 8.1. HIPÓTESIS PROPUESTAS PARA LA DUPLICACIÓN Se han propuesto tres hipótesis para explicar como se produciría la replicación del ADN: Conservativa: la doble hélice original permanecería intacta, originándose una doble hélice completamente nueva. Semiconservativa: cada nueva molécula de ADN está formada por una cadena vieja y otra nueva (fue la propuesta por Watson y Crick). Dispersiva: cada nueva molécula de ADN estaría formada por fragmentos de cadenas viejas y nuevas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
9
Para comprobar cuál de las tres hipótesis era correcta, dos investigadores, Meselson y Stahl (1.958) realizaron varios experimentos. Cultivaron E.coli (la bacteria más utilizada en Genética) en un medio con nitrógeno pesado (N15). Después lo pasaron a un medio con nitrógeno normal (N14) y compararon la densidad de los ADN aparecidos en sucesivas generaciones. Tras sus experimentos y otros similares realizados en otros organismos, los resultados apoyan la hipótesis semiconservativa. A continuación figura la interpretación de los resultados.
8.2. MECANISMO DE DUPLICACIÓN DEL ADN Conocer el mecanismo de replicación de¡ ADN ha supuesto multitud de estudios y experimentos. Algunos de los investigadores más importantes que han participado en ellos, han sido: Kornberg (1.956). Fue discípulo de Severo Ochoa. Aisló de Escherichia coli la enzima ADNpolimerasa. Esta enzima es capaz de fabricar ADN in vitro. Actúan añadiendo nucleótidos al extremo de una cadena de nucleótidos, llamada ADN cebador. Cairns (1.963). Descubrió la existencia de un punto origen de la replicación del ADN en bacterias, y confirmó mediante sus estudios la hipótesis semiconservativa. Okazaki (1.968). Fue el primero en explicar la duplicación bidireccional, como a partir de un determinado punto la replicación progresa en dos direcciones. FASES DE LA DUPLICACIÓN. La duplicación presentan ciertas diferencias en procariotas (bacterias) y eucariotas. Vamos a estudiar el proceso en procariotas, que en sus aspectos básicos es común a eucariotas, y luego hablaremos de las diferencias entre ambos. Duplicación en Procariotas 1. INICIACIÓN. La replicación comienza en un punto concreto de la molécula de ADN, una secuencia de nucleótidos denominada OriC o Punto de iniciación. En este punto se abre la doble hélice, para ello actúa un enzima, denominada HELICASA, que rompe los puentes de hidrógeno que unen las dos cadenas de nucleótidos. Debido a este desenrollamiento de ADN, se producen superenrollamientos en el resto de la molécula, capaces de detener la duplicación, lo que hace preciso el concurso de unas enzimas, denominadas TOPOISOMERASAS, que eliminan las tensiones de las cadenas (actúan por un mecanismo de corte y empalme).
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
10
Una vez que han comenzado a separarse las cadenas de nucleótidos es necesario mantenerlas separadas, para ello actúan unas proteínas que estabilizan la separación de las dos hebras, se denominan PROTEÍNAS SSB. Se inicia así la formación de la horquilla de replicación, actuando las helicasas en ambos sentidos, de manera que el proceso es bidireccional. Las dos horquillas se replicación originadas forman una BURBUJA DE REPLICACION. Para que actúen las ADN-polimerasas necesitan de un cebador, es decir, un pequeño fragmento de nucleótidos a los que poder unir los nuevos nucleótidos que van a constituir las nuevas cadenas de ADN. Esos fragmentos de nucleótidos que actúan de cebadores son pequeños fragmentos de ARN (de 10 nucleótidos) denominados PRIMER, y que son sintetizados por una ARN-polimerasa, denominada PRIMASA. 2. ELONGACIÓN. Una vez sintetizados los primer, actúan la ADN-polimerasa lII, que comienza a fabricar una hebra de ADN a partir del cebador, en sentido S’- 3’, a partir de nucleótidos 3 P. La energía necesaria para la síntesis es proporcionada por los propios nucleótidos, que pierden dos grupos fosfato. Esta nueva hebra es de crecimiento continuo, y se denomina hebra conductora. A medida que las helicasas actúen y sigan abriendo la horquilla de replicación, esta hebra irá creciendo, por la acción de la ADN-pol III que irá añadiendo nuevos nucleótidos, complementarios a los de la cadena molde. En la otra hebra, al estar orientada en sentido contrario, la replicación se produce de forma discontinua, a base de pequeños fragmentos formados por cientos de nucleótidos de ADN, denominados fragmentos de Okazaki. En la síntesis de esta hebra, denominada hebra retardada, porque tarda más en crecer que la hebra conductora, intervienen varias enzimas: ARN-pol: fabrica cebadores ADN-pol lII: fabrica los fragmentos nuevos de ADN (fragmentos de Okazaki) ADN-pol I: retira los fragmentos de ARN y rellena los huecos con fragmentos de ADN ADN-ligasa: empalma los fragmentos de ADN (fragmentos de Okazaki), para formar la hebra retardada, que crece por lo tanto de forma discontinuo. 3. TERMINACIÓN. El proceso de replicación termina cuando la ADN-pol llega hasta la secuencia de terminación (Ter C). Las nuevas hélices terminan de formarse y se separan, originándose dos moléculas de ADN.
Duplicación en Eucariotas La duplicación en eucariotas es diez veces más lento que en procariotas, debido al mayor tamaño de las moléculas de ADN y a la presencia de histonas. Para que el proceso sea más rápido, existen varios puntos de iniciación, de manera que se originan varias unidades de replicación (REPLICONES) que actúan de forma coordinada, progresando la síntesis de nuevas cadenas de ADN hasta que se ponen en o unas con otras. Las histonas sobre las que está enrollado el ADN se quedan con la hebra patrón de la hebra conductora, de manera que la hebra que sirve de molde a la retardada y esta misma se enrollan sobre nuevas histonas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
11
SISTEMAS DE REPARACIÓN DEL ADN Es muy importante que en el proceso de replicación del ADN, el ADN formado no tenga errores de copia, ya que podría dar lugar a mutaciones importantes, como las que provocan la formación de tumores. En los procariotas se ha calculado que aproximadamente cada 107 nucleótidos se produce un error, y en eucariotas la probabilidad es más pequeña, cada 1010 nucleótidos. Para que el ADN conserve escrupulosamente la información genética a través de inmunerables divisiones celulares existen tres procesos que cooperan para asegurar la alta fidelidad de la replicación. Dos de ellos se encargan de prevenir errores: seleccionar nucleótidos y corregir pruebas, y un tercero se encarga de la corrección de posibles errores. La selección de nucleótidos es llevada a cabo por la ADN polimerasa III La corrección de pruebas la lleva a cabo la ADN polimerasa I. La existencia de un nucleótido desemparejado detiene la adición del siguiente, y la ADN-pol I retira dicho nucleótido y busca la pareja adecuada. La corrección de errores es más complicada. Las enzimas recorren las hebras de ADN y reconocen los nucleótidos mal emparejados, los eliminan y sustituyen por otros correctos. Hay que tener en cuenta, que no todos los errores de la replicación de los mensajes genéticos son perjudiciales. Algunos no tienen consecuencias para el organismo y otros son ventajosos, y constituyen una fuente importante de la variación genética necesaria para que tenga lugar la evolución.
9. LA EXPRESION DEL MENSAJE GENETICO Francis Crick, en 1970, enunció el dogma central de la Biología molecular: la información genética contenida en el ADN es transcrita en forma de ARN y traducida a proteínas. En ADN contiene la información genética en forma de una determinada secuencia de nucleótidos, es decir, contiene las instrucciones sobre cómo debe funcionar la célula. Las proteínas ejecutan tales instrucciones. Para ello la información contenida en el ADN se copia a una secuencia de ARN (transcripción) denominada ARN mensajero (ARNm), que en los ribosomas al ser leído se traduce a proteínas (traducción). 9.1.LA TRANSCRIPCIÓN La transcripción es la síntesis de ARN a partir de fragmentos de ADN. La llevan a cabo unas enzimas, las ARN polímerasas (ARN-pol), que utilizan como molde una hebra de ADN. Las ARN polimerasas recorren el ADN en sentido 3’- 5’y añaden nucleótidos con bases complementadas a las de la hebra del ADN que se transcribe. La molécula de ARN crece en sentido 5’ 3’. Así pues en la transcripción intervienen: ADN: que actúa de molde Ribonucleótidos trifosfato (ATP,GTP,CTP,UTP) ARN-polimerasas Fases de la transcripción 1. INICIACIÓN. La transcripción comienza cuando la ARN-pol se asocia con el cofactor sigma (), que permite a esta enzima reconocer y unirse a una secuencia concreta del ADN, denominada promotor, que actúa se señal de inicio. A continuación la ARN-polimerasa, abre la doble hélice y comienza a añadir nucleótidos complementarios a una de las hebras de ADN, que actuará de patrón. 2. ELONGACIÓN. La ARN-pol avanza a lo largo de cadena patrón de ADN, hacia su extremo 5’, añadiendo nucleótidos (unos 40 por segundo), y sintetiza una hebra de ARN en dirección 5’ 3’. 3. FINALIZACIÓN. La finalización se produce al llegar a una secuencia rica en G y C, que actúa se señal de terminación. Se cierra el bucle de ADN y se separa la ARN polimerasa.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
12
Transcripción en eucariotas (Maduración del ARN) En procariotas el ARNm transcrito no precisa de maduración, pero en eucariotas, los genes están fragmentados, es decir, tienen fragmentos que no se transcriben (intrones) y fragmentos que sí lo hacen (exones). Así en el proceso de maduración es necesario eliminar las secuencias sin sentido o intrones y empalmar las secuencias con sentido o exones. En la transcripcion en eucariotas intervienen tres tipos de ARN-pol, cada una de ellas transcribe un tipo de ARN distinto. Las fases de la transcripción son similares a procariotas, primero la ARN-pol se une a la región promotora y empieza a añadir nucleótidos. Cuando se llevan transcritos unos 30 nucleótidos, al extremo 5’ se le añade una caperuza (Gppp). Al finalizar la síntesis al extremo final se le añade un segmento de 200 nucleótidos de adenina (cola poli A). Este ARN transcrito se denomina pre-ARN o ARN heterogéneo nuclear (ARNhn). Ahora tiene que madurar, para ello, un enzima provoca que se curven los intrones y se desprendan, y otra actúa empalmando los exones, para formar un ARNm maduro.
Transcripción
Maduracion del ARN en eucariotas
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
13
9.2. TRADUCCIÓN o SÍNTESIS DE PROTEÍNAS En la biosíntesis de proteínas se pueden distinguir las siguientes etapas: 1. Activación de los aminoácidos. 2. Traducción: iniciación de la síntesis, elongación o alargamiento de la cadena polipeptídica y finalización de la síntesis. 1. Activación de los aminoácidos: Los aminoácidos en presencia de la enzima aminoacil-ARNt sintetasa y de ATP, se unen a un ARNt específico y da lugar a un aminoacil-ARNt. Después de la unión de¡ aminoácido al ARNt, se libera la enzima, AMP y PPi (Pirofosfato inorgánico). 2. Traducción: INICIACIÓN: el ARNm, se une a la subunidad menor de los ribosomas gracias a una secuencia inicial llamada región líder (esta secuencia no se va a traducir). A éstos se asocia el aminoacil ARNt (o sea, una molécula de ARNt que lleva un aminoácido en uno de sus extremos). Los ARNt tienen en una de sus asas un triplete de nucleótidos, llamado anticodón, que se asociará al primer triplete o codón del ARNm, según la complementariedad de las bases (o sea, si el primer codón es AUG, el ARNt que se asocia es el que lleva UAC, que se corresponde según la clave genética con la metionina). A este grupo de moléculas se une la subunidad mayor de los ribosomas, formándose el complejo ribosomal. Este complejo posee dos sitios de unión: Centro P (centro peptidil): donde se sitúa el primer aminoacil-ARNt. Centro A (centro aceptor): donde se sitúan los nuevos aminoacil-ARNt que vayan llegando. Esta fase está catalizada por proteínas llamadas factores de iniciación (IF). ELONGACIÓN: al centro A llega el segundo aminoacil-ARNt. El primer aminoácido que se encontraba en centro P se va a unir a ese segundo amínoácido mediante un enlace peptídica. Esta unión es catalizada por el enzima peptidil-transferasa. El centro P queda, pues, ocupado por un ARNt sin aminoácido, este ARNt saldrá de¡ ribosoma. Se produce entonces la translocación ribosomal, que quiere decir que el ribosoma avanza tres nucleótidos del ARNm, (o sea, un codón), y el ARNt con dos aminoácidos que está en el ribosoma queda en el centro P, y por lo tanto el centro A queda libre para la llegada de otro aminoacil-ARNt. Así poco a poco, a medida que los ribosomas avanzan por el ARNm se va formando una cadena polipeptídica (o sea, una cadena de varios aminoácidos). Esta fase está catalizada por los factores de elongación (EF). FINALIZACIÓN DE LA SÍNTESIS: después de que los ribosomas hayan recorrido la secuencia de nucleótidos del ARNm, el final de la síntesis tiene lugar cuando el sitio A del ribosoma llega a un codón de terminación para el que no existe ningún ARNt complementario. Esos codones o tripletes sin sentido son tres: UAA, UAG y UGA. Ahora sobre el sitio A se sitúan unas proteínas llamadas factores de liberación que catalizan la separación de la cadena polipeptídica del ribosoma. A continuación se separan el ARNm, y las dos subunidades de los ribosomas.
BIOLOGÍA 2º BACHILLERATO. ESQUEMAS GENÉTICA MOLECULAR DUPLICACIÓN o REPLICACION ADN
Horquillas de replicación
Burbuja de replicación y duplicación bidireccional
BIOLOGÍA 2º BACHILLERATO. ESQUEMAS GENÉTICA MOLECULAR TRANSCRIPCIÓN Y TRADUCCIÓN
Maduración ARN eucariota
Síntesis de cadena de ARN
Etapas transcripción
Traducción
NH
|
ELONGACIÓN
3' NH2
NH2
Met
Met
|
|
UG A
INICIACIÓN
5'
UGA
AUG P
UCA A
NH2
Met
Met
Met
Ser
Ser
Ser
5'
AUG P
AUG 5'
UCA A
UCA P
CCG A
2
H
FINALIZACIÓN
3' 5'
UAU
etc.
AUA
NH2 HOOC
UAU
UGA
CGG CCG A
AUG
Primera translocación
Pro
UCA P
CCG A
2
5' AUG
UCA P
|
Pro
|
|
N
CAU
5'
CAU
3'
Ser
UGA
|
Me t Se r
5'
3' 5'
3'
NH2
UCA A
NH2
|
Met
AUG P
NH2
UGA
UCA A NH
5'
UGA
F
2
UCA A
UGA
NH2 | Ser
|
3'
AUG P
5' 3'
CGG
AUG P
NH
Enlace peptídico
A
CAU
AUG
NH2 | Met
5'
P
CGG
5'
A
CAU
P
AUG
5'
CAU
1
UAA
3'
G AU
5'
2
Ser
UAA
3'
Biosíntesis de las proteínas. En el nombre de los diferentes aminoácidos se ha señalado el lugar que ocupa el grupo amino, para resaltar que la unión con el ARNt o con el siguiente aminoácido se realiza mediante el grupo carboxilo.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
14
10. EL CÓDIGO GENÉTICO El código o la clave genética es el que establece la relación entre la secuencia de nucleótidos y la secuencia de aminoácidos de una proteína. Severo Ochoa recibió el premio Nobel de medicina por su contribución al desciframiento de¡ código genético. Consiguió una enzima (polinucleótido fosforilasa) capaz de fabricar ARN ín vitro sin necesidad de molde. Gracias a esta enzima, fabricó distintos ARN constituidos por un solo nucleótido (poliA, poliU .... ). Años después otros investigadores (Niremberg y Khorana), fabricando ARN sintéticos de secuencias conocidas y utilizando extractos de E. coli y distintos aminoácidos dedujeron las relaciones entre nucleótidos y aminoácidos. Dado que existen 20 aminoácidos diferentes y sólo hay cuatro tipos de nucleótidos, la relación (colinearidad) entre ambos no se podía establecer uno a uno, ni tampoco entre dupletes de nucleótidos (4 x 2 = 16), sino como mínimo, entre tripletes de nucleótidos (4 x 3 = 64) y aminoácidos. CARACTERÍSTICAS DEL CÓDIGO GENÉTICO
Es universal, pues es el mismo en todos los seres vivos, y no es ambiguo, ya que cada codón o triplete, especifica para el mismo aminoácido. Está degenerado, lo que quiere decir que un mismo aminoácido puede ser codificado por varios tripletes, ya que existen 64 tripletes distintos para los 20 aminoácidos. La tercera base suele ser variable para codificar un mismo aminoácido. Esto representa una ventaja, ya que aunque se produzca un error en la copia de un nucleótido, seguiría la colinearidad entre el triplete y el nucleótido. Por otro lado, si sólo hubiera veinte tripletes traducibles, habría 44 tripletes sin sentido (64 - 20 = 44) y un simple error en un nucleótido lo convertiría probablemente en un triplete sin sentido, interrumpiéndose así la biosíntesis de la proteína. Carece de solapamiento, lo que significa que los tripletes se disponen en el ARN, uno a continuación de otro y no comparten ninguna base.
11. REGULACIÓN DE LA EXPRESIÓN DE LOS GENES CONCEPTO DE GEN Los genes son las unidades de herencia de los cromosomas, al ser el material genético que se transmite de padres a hijos. Cada gen está formado por una secuencia de nucleótidos que codifica para una molécula de ARN o una cadena polipeptídica. Los genes presentan una triple capacidad: 1. Capacidad de mutar. Puede cambiar la secuencia de nucleótidos de un gen, apareciendo estados alternativos, que son los alelos (genes que informan sobre la misma característica, pero no llevan la misma información). 2. Capacidad de intercambiar secuencias de ADN con otros genes, mediante recombinación. 3. Capacidad de expresarse, es decir, poseen la información necesaria para la codificación de una proteína. EXPRESIÓN GÉNICA Las células no están continuamente sintetizando todos los tipos de proteínas sobre las cuales tienen información. Si así fuera, se produciría un caos metabólico. Es evidentemente, que debe existir un sistema de regulación. Como la cantidad de proteínas depende directamente de la cantidad de ARN, presente en el citoplasma, y como la vida media de este es muy corta (minutos), la cantidad de ARNm, regula los niveles enzimáticos del medio. Así pues, es suficiente con regular la síntesis de ARNm. En procariotas, como bacterias, la síntesis de ARN, depende de la cantidad de sustrato disponible, mientras que en eucariotas, depende fundamentalmente de hormonas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
15
12. MUTACIONES
Son alteraciones del material genético (ADN o ARN en algunos virus). Se puede alterar la secuencia de nucleótidos, el orden de los genes en un cromosoma o el número de cromosomas. Se producen al azar, durante la duplicación del ADN o la división celular Pueden ser beneficiosas para una población, ya que aumentan la variabilidad, y en caso de cambios en las condiciones del medio, aquellos individuos mutantes que presentaran características que les permitieran adaptarse mejor a las nuevas condiciones tendrían más posibilidades de sobrevivir (selección natural) y transmitir sus características a las descendencia. Así pues las mutaciones a lo largo de la historia biológica han permitido la evolución de las especies y con ello la continuidad de la vida. Ahora bien, hay que tener en cuenta que las mutación tienen más probabilidades de ser perjudiciales que beneficiosas para los organismos, ya que las variantes que existen en una población han sido escogidas por la selección natural. Son perjudiciales para la salud del individuo en la mayor parte de las ocasiones ya que producen deficiencias, como el Síndrome de Down, algunos tipos de cánceres y leucemias, trastornos metabólicos,...
TIPOS DE MUTACIONES En general de suele hablar de tres tipos: 1. Génicas o puntuales: afectan a la secuencia de nucleótidos de un gen. 2. Cromosómicas: si alteran el orden de los genes de un cromosoma. 3. Genómicas: si modifican el número de cromosomas de un individuo. Ejemplos 1. Génicas: La sustitución de un nucleótido por otro en el ADN, que puede provocar un cambio de aminoácido en la proteína correspondiente. Muchas veces la proteína no se ve afectada, pero en otros casos se ve alterada su función biológica, como en la anemia falciforme, donde debido a una mutación se fabrica una hemoglobina anormal, afectando a los glóbulos rojos y al desarrollo del individuo. La adición o deleción (pérdida) de un nucléotido, suele provocar grandes cambios en la proteína codificada. 2. Cromosómicas: La deleción cromosómica implica la pérdida de un fragmento de un cromosoma, con la pérdida de genes correspondiente, por lo que puede ser letal (provoca la muerte). La duplicación cromosómica, o aumento de un fragmento de cromosoma y por lo tanto un aumento del número de genes. Ambas se producen por apareamientos desiguales de cromosomas homólogos en la meiosis. Las translocaciones son cambios en la posición de los genes dentro de un cromosoma. 3. Genómicas: La aneuploidía es una alteración en el número normal de uno o más tipos de cromosomas, sin llegar al juego completo. Como ejemplo está el Síndrome de Down o Mongolismo, que es una trisomía del cromosoma 21 (las personas con Síndrome de Down tienen 3 ejemplares del cromosoma 21). La poliploidía es el aumento de dotaciones cromosómicas. Los individuos pueden ser triploides (3N), como en el plátano, tetraploides (4N) como en la patata,... Por último, si la mutación aparece de forma natural se dice que es una mutación espontánea, si es provocada por agentes mutágenos (como radiaciones o productos químicos) se dice que es inducida. Las mutaciones pueden afectar a las células somáticas y no se transmiten a la descendencia, como en el caso del cáncer, o a las células reproductoras o germinales, en cuyo caso se transmiten a la descendencia.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
16
13. EL ADN, BIOTECNOLOGÍA e INGENIERÍA GENÉTICA La Biotecnología es todo el conjunto de técnicas que emplea seres vivos o compuestos procedentes de ellos (como las enzimas) para la obtención de productos, bienes y servicios de distinto tipo para la humanidad. La Biotecnología abarca: Biotecnología tradicional: utilizada desde hace cientos de años y que emplea, por ejemplo, procesos de fermentación microbiana para la elaboración del pan, bebidas alcohólicas o yogur. Biotecnología moderna: nacida en los últimos 30 años, gracias a los progresos de la biología celular, bioquímica, microbiología, inmunología e ingeniería genética.
INGENIERÍA GENÉTICA Comprende todo el conjunto de métodos y técnicas que permiten el y manipulación del ADN y la transferencia de genes de un organismo a otro. De este modo se han podido obtener organismos transgénicos u Organismos Modificados Genéticamente (OMG). Existen varias técnicas de ingeniería genética, entre las que destacan: Obtención de ADN recombinante. Técnica que permite cortar el ADN de un organismo en múltiples fragmentos, aislar alguno de ellos, e introducirlo, mediante un vector, en otro organismo, originando un organismo transgénico. Clonación del ADN. Permite la producción de múltiples copias de un gen específico o de un fragmento de ADN. Reacción en cadena de la polimerasa (PCR). Técnica in Vitro, que permite obtener de forma muy rápido un elevado número de copias de un fragmento de ADN. Secuenciación del ADN. Técnica que permite conocer el orden de los nucleótidos que forman parte de un gen, o incluso del genoma completo de un organismo. (ya vista en el tema de ácidos nucleicos)
Tecnología del ADN recombinante El ADN formado por la unión de fragmentos de ADN procedente de organismos distintos se denomina ADN recombinante. Por eso todo el conjunto de técnicas que utiliza la ingeniería genética para conseguirlo recibe el nombre de tecnología del ADN recombinante. Los pasos que implica esta tecnología son, en esencia, estos: 1. Las moléculas de ADN de dos organismos diferentes se cortan en fragmentos con ENDONUCLEASAS DE RESTRICCIÓN. Las endonucleasas de restricción son enzimas fabricadas por bacterias y son capaces de cortar el ADN de cualquier organismo por secuencias específicas, dando lugar a fragmentos con extremos de una sola cadena, llamadas extremos cohesivos. Actualmente se conocen más de 1200 endonucleasas de restricción que reconocen y cortan el ADN por distintas secuencias. Una de ellas de la endonucleasa EcoRI, que reconoce la secuencia GAATTC y corta entre los nucleótidos G y A de cada una de las cadenas de las moléculas de ADN.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
17
2. Una vez obtenidos los fragmentos de ADN con extremos cohesivos complementarios, se ponen en o y se someten a la acción de la enzima ADN LIGASA, que une los extremos cohesivos, y forma una molécula de ADN recombinante, que contiene ADN de los dos organismos.
Clonación del ADN La clonación de un gen consiste en introducirlo en una célula, de manera que pueda ser copiada. Para ello se inserta en una molécula de ADN, llamado vector de clonación, capaz de entrar y replicarse independientemente en una célula huésped. El resultado es la formación de ADN recombinante y el vector de clonación actúa como medio de transporte. Para clonar genes se utilizar diferentes vectores de clonación, como los plásmidos bacterianos, pequeñas moléculas de ADN circular que se pueden replicar independientemente en las bacterias. El proceso de clonación de un gen en bacterias incluiría las siguientes etapas: 1. Obtención del plásmido recombinante formado por un plásmido que contenga un gen de resistencia a un antibiótico y el gen que se desea clonar. 2. Transformación de las bacterias incorporándoles el plásmido recombinante. 3. Selección de las bacterias transformadas, añadiendo al medio el antibiótico que 4. Crecimiento de las bacterias en medio de cultivo. 5. Aislamiento de los plásmidos recombinantes y de las copias del gen de interés.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
18
Reacción en cadena de la polimerasa (PCR) La reacción en cadena de la polimerasa (PCR) es un método que permite obtener múltiples copias de un fragmento de ADN en muy poco tiempo, lo que se denominan amplificación del ADN. Es una técnica in vitro, donde se reproduce la duplicación del ADN. Para amplificar el ADN se añaden en un tubo de ensayo los siguientes componentes: La muestra de ADN a amplificar Cebadores: pequeñas cadenas de nucleótidos complementarias a las secuencias de ADN que flanquean al gen que queremos copiar. Los cuatro tipos de desoxirribonucleótidos trifosfato (ATP. GTP, CTP, TTP). Una ADN polimerasa resistente al calor, obtenida a partir de la bacteria termófila Thermus aquaticus (Taq-polimerasa).
Biología 2º Bachillerato
19
Tema 5. Herencia y Genética Molecular
Para conseguirlo se utilizan varios ciclos, y en cada uno de ellos el ADN se duplica, siguiendo estas etapas:
1. Desnaturalización. Se calienta la muestra de ADN a 95 ºC, para desnaturalizar el ADN y separar las cadenas de nucleótidos.
2. Hibridación. Se enfría a 55 ºC la muestra, para que los cebadores hibriden con las secuencias complementarias en cada una de las cadenas del ADN.
3. Síntesis de ADN. Se calienta la muestra a 72 ºC para que la Taq-polimerasa fabrique las nuevas cadenas de ADN.
Las aplicaciones de la PCR son varias: Amplificaciones de ADN antiguos para estudios evolutivos o, paleontológicos. La obtención de la huella genética de ADN en medicina forense. Detección de ADN de genes de virus en etapas tempranas de infección, como por ejemplo el VIH, en pruebas de diagnóstico.
Primer ciclo Segundo ciclo
Tercer ciclo
100
T e m pe ra tu ra (C )
80
Ciclo 1
Ciclo 2
Desnaturalización
Ciclo 3
Síntesis
60
Apareamiento Tiempo
Técnica de PCR
APLICACIONES DE LA INGENIERÍA GENÉTICA Algunas de las aplicaciones de la ingeniería genética son: Agricultura y ganadería: Clonación de plantas o animales con características interesantes (que produzcan frutos de mejor calidad, mayor producción de leche, carne o lana, por ejemplo). Obtención de plantas y animales transgénicos, que al poseer genes de otro organismo adquieren características nuevas, como la resistencia a plagas o heladas, crecimiento más rápido, alimentos animales con menos colesterol, etc,… Control de plagas: algunos microorganismos, como bacterias, han sido utilizados como bioinsecticidas para controlar algunas plagas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
20
Medicina: Obtención de medicamentos, como la insulina, los factores de coagulación, interferón, hormona de crecimiento,…, o como en Farmacogenética, tratar de obtener medicamentos personalizados. Terapia génica, que se basa en la introducción de genes sanos en personas con genes defectuosos causantes de enfermedades, lo que permitiría la curación de la enfermedad. Para introducir el gen en el paciente se pueden emplear virus no patógenos que hayan sido modificados genéticamente y que porten el gen sano. Diagnóstico de enfermedades genéticas mediante el empleo de Biochips, que son pequeñas placas que contienen cientos de genes colocados en diminutas casillas, sobre las que se colocan gotas de sangre o saliva y que permiten detectar la presencia de genes causantes de enfermedades. Utilización de transgénicos para elaborar vacunas.
Medio ambiente (Biorremediación) Obtención de bacterias que degradan hidrocarburos como el petróleo para combatir las mareas negras o plantas transgénicas que permitan convertir algunos contaminantes en sustancias menos tóxicas.
Obtención de planta transgénica
Transposones Los descubre Barbara Mc Clintock en la década de los 40-50, en el genoma del maíz. Son elementos del genoma del maíz que tenían la capacidad de movilizarse favoreciendo la aparición de determinados fenotipos. Los transposones son fragmentos de DNA que pueden pasar de un cromosoma a otro sin una etapa de existencia independiente. En algunos casos se escinden del cromosoma y se insertan en otro lugar; otras veces, el fragmento original permanece en su sitio y una copia se inserta en otro lugar. Otras veces, se copian primero en RNA y, a través de una transcriptasa inversa, producen DNA que se inserta en un cromosoma. Cuando cambian de posición y abandonan el lugar en el que estaban, en ese sitio, se produce un deleción o pérdida de bases. Si el elemento transponible estaba insertado en el interior de un gen, puede que se recupere la función de dicho gen. De igual forma, si el elemento genético móvil al cambiar de posición se inserta dentro de un gen se produce una adición de una gran cantidad de nucleótidos que tendrá como consecuencia la pérdida de la función de dicho gen. Por consiguiente, los elementos genéticos transponibles producen mutaciones. En bacterias existen dos tipos de elementos genéticos móviles: – Transposón Simple, Secuencia de Inserción o Elemento de Inserción (IS): los transposones simples contienen una secuencia central con información para la proteína transposasa – Transposón Compuesto (Tn): contienen un elemento de inserción (IS) en cada extremo en y una región central que además suele contener información de otro tipo. Por ejemplo, los Factores de transferencia de resistencia (RTF), poseen información en la zona central para resistencia a antibióticos (cloranfenicol, kanamicina, tetraciclina, etc.). Transposones en mamíferos. En mamíferos se conocen tres clases de secuencias que son capaces de transponerse o cambiar de posición a través de un ARN intermediario: – Retrovirus endógenos: semejantes a los retrovirus, no pueden infectar nuevas células y están restringidos a un genoma, pero pueden transponerse dentro de la célula. Poseen largas secuencias repetidas en los extremos (LTR), genes env (con información para la proteína de la cubierta) y genes que codifican para la trasnrciptasa inversa, como los presentes en retrovirus. – Retrotransposones o retroposones: sólo contienen genes para la transcriptasa inversa y pueden transponerse. – Retropseudogenes: carecen de genes para la transcriptasa inversa y por consiguiente son incapaces de transponerse de forma independiente, aunque si pueden cambiar de posición en presencia de otros elementos móviles que posean información para la trasncriptasa inversa.
1
Problemas de Genética Biología 2º
GENÉTICA MENDELIANA
Problemas de uno y dos caracteres 1. En el hombre el color pardo de los ojos "A" domina sobre el color azul "a". Una pareja en la que el hombre tiene los ojos pardos y la mujer ojos azules tienen dos hijos, uno de ellos de ojos pardos y otro de ojos azules . Averiguar: a) El genotipo del padre b) La probabilidad de que el tercer hijo sea de ojos azules. 2. La acondroplasia es una anomalía determinada por un gen autosómico que da lugar a un tipo de enanismo en la especie humana. Dos enanos acondroplásicos tienen dos hijos, un acondroplásico y otro normal. a) La acondroplasia, ¿es un carácter dominante o recesivo?. ¿Por qué?. b) ¿Cuál es el genotipo de cada uno de los progenitores?. ¿Porqué?. c) ¿Cuál es la probabilidad de que el próximo descendiente de la pareja sea normal?. ¿Y de que sea acondroplásico?. Realizar un esquema del cruzamiento. 3. Una vaca de pelo retinto (rojizo), cuyos padres son de pelo negro, se cruza con un toro de pelo negro, cuyos padres tienen pelo negro, uno de ellos y pelo retinto el otro. a) ¿Cuál es el genotipo de los animales que se cruzan?. b) ¿Y el fenotipo de la descendencia?. 4. El gen R que rige el pelo rizado domina sobre el gen recesivo (r) del pelo liso. Una mujer con el pelo rizado se casa con un varón con el pelo liso y tienen una hija con el pelo rizado. El padre de la mujer tenía el pelo liso, el de la madre no lo recuerdan, pero sí saben que la abuela materna lo tenía liso y el abuelo materno lo tenía rizado, aunque el de la madre de éste era liso. ¿Cuál es el genotipo de todos ellos?. 5. Razona la veracidad o falsedad de la siguiente afirmación: El color de tipo común del cuerpo de la Drosophila está determinado por el gen dominante "N", su alelo recesivo "n" produce cuerpo de color negro. Cuando una mosca tipo común de raza pura se cruza con otra de cuerpo negro, la fracción de la segunda generación que se espera sea heterocigótica es 1/2 ?. 6. En el pollo las plumas sedosas están determinadas por un gen cuyo efecto es recesivo respecto al que rige las plumas normales. Si de un cruzamiento entre individuos heterocigóticos para dicho gen, se criasen 98 aves, ¿cuántas cabría esperar que fuesen sedosas y cuántas normales?. 7. El pelo rizado en los perros domina sobre el pelo liso. Una pareja de pelo rizado tuvo un cachorro
de pelo también rizado y del que se quiere saber si es híbrido o heterocigótico. ¿Con qué tipo de hembras tendrá que cruzarse?.
8. Como Mendel descubrió, las semillas de color amarillo en los guisantes son dominantes sobre los de color verde. En los experimentos siguientes, padres con fenotipos conocidos pero genotipos desconocidos produjeron la siguiente descendencia: a) Dar los genotipos más probables de cada parental b) En los cruces B, D, E, indíquese qué proporción de la descendencia amarilla producida en cada uno de ellos se esperaría que produjera descendientes verdes por autopolinización.
Parentales A. amarillo x verde
Amarillo Verde 82
78
B. amarillo x amarillo 118
39
C. verde x verde
0
50
D. amarillo x verde
74
0
E. amarillo x amarillo 90
0
Problemas de Genética Biología 2º
2
9. La fenilcetonuria (FCU) es un desorden metabólico que se hereda con carácter autosómico recesivo. Dos progenitores sanos tienen un hijo con FCU. Indica los fenotipos y genotipos de todos los apareamientos que teóricamente pueden dar un descendiente afectado de FCU. a) ¿A cuál de estos tipos de apareamiento pertenece el caso descrito ?. b) ¿Cuál es la probabilidad de que el siguiente hijo padezca también la enfermedad ?. c) ¿Cuál será la probabilidad de qué un hijo normal (sano) de estos padres sea portador heterocigótico para FCU ?. 10. En el conejo, la piel manchada (S) es dominante sobre la piel uniforme (s); y el negro (B) es dominante sobre el pardo (b). Un conejo manchado pardo se cruza con un ejemplar negro uniforme, todos los descendientes son negros manchados. ¿Cuáles son los genotipos de los padres?. ¿Cuál sería el aspecto de la F2 si dos de estos animales de la F1 se cruzan entre sí?. 11. En un cruce entre dos moscas Drosophila melanogaster normales se obtienen los siguientes descendientes con los fenotipos:
¿Cuáles de esos caracteres son dominantes y cuáles recesivos?. ¿Cuál es el genotipo de cada uno de los individuos de la descendencia?. ¿Cuál es el genotipo de los padres?. 12. En el guisante la altura del tallo está determinada por un gen con dos alelos, T (tallo largo) y t (tallo corto). La textura de la semilla está controlada por otro gen cuyo alelo L produce semillas lisas, mientras que el alelo l produce semillas rugosas. Estas dos parejas de genes se transmiten independientemente. Se cruza una variedad pura lisa de tallo alto con otra variedad pura de semillas rugosas y tallo corto. Indicar: a) El genotipo y fenotipo de la F1 b) Los fenotipos de la F2 y la proporción de cada uno de ellos que resultan de la autofecundación de las plantas de la F1. c) Si en la generación parental P, una de las variedades fuera lisa y corta y la otra rugosa y alta, ambas de raza pura, ¿variarán las proporciones fenotípicas en la F1?. Razone la respuesta. 13. En el guisante, el alelo dominante de un gen (T) determina que las flores crezcan en el eje del tallo, mientras que su alelo recesivo (t) determina que crezca sólo el extremo del tallo. Por otra parte, el alelo dominante de otro gen C, determina que las flores sean de color rojo, en tanto que las flores blancas están determinadas por su alelo recesivo c. Si una planta híbrida para las dos características, se cruza con otra de raza pura de flores rojas y localizadas en el eje del tallo, ¿qué proporciones genotípicas y fenotípicas podemos esperar en la generación F1?. 14. Los pollos con alas y patas recortadas reciben el nombre de trepadores. El apareamiento de este tipo de pollos con aves normales da lugar a una descendencia equilibrada entre pollos normales y trepadores. El apareamiento de pollos trepadores entre sí produce una descendencia formada por dos pollos trepadores y uno normal. El cruzamiento entre pollos normales da lugar a una progenie uniforme formada exclusivamente por aves normales. Explicar el fenómeno de forma razonada.
3
Problemas de Genética Biología 2º
15. En el tomate, el color púrpura del tallo está determinado por un alelo autosómico dominante "A". El alelo recesivo "a" determina tallo de color verde. Otro gen autosómico independiente controla la forma de la hoja: el alelo dominante "C" determina hoja con borde recortado y el alelo recesivo "c" determina hoja con borde entero. En la siguiente tabla se indican los resultados en tres cruces entre plantas de fenotipos diferentes. En cada caso, indique cuáles son los genotipos de los progenitores y por qué. Fenotipos de los progenitores
púrpura/recortada púrpura/entera verde/recortada verde/entera
púrpura, recortada x verde, recortada
321
101
310
107
púrpura, recortada x púrpura recortada
144
48
50
18
púrpura, recortada x verde, recortada
722
231
0
0
16. Los ratones gordos se pueden producir por dos genes independientes. El genotipo "oo" genera un ratón gordo y estéril, llamado obeso; su alelo dominante "O" da lugar a crecimiento normal. El genotipo recesivo "aa" también produce un ratón gordo y estéril llamado adiposo, mientras que su alelo dominante ocasiona crecimiento normal. ? Qué proporciones fenotípicas de ratones gordos frente a normales podemos esperar en F1, siendo los padres de genotipo OoAa. 17. La miopía es debida a un gen dominante, al igual que el fenotipo Rh+. Una mujer de visión normal Rh+, hija de un hombre Rh-, tiene descendencia con un varón miope heterocigótico y Rh-. Establece los posibles genotipos y fenotipos de esta pareja, y su frecuencia. 18. Dos condiciones anormales en la especie humana: las cataratas y la fragilidad de los huesos, parecen depender de alelos dominantes, que se heredan independientemente. Un hombre con cataratas y huesos frágiles, cuyo padre era normal para las dos características, tuvo un hijo con un mujer sin cataratas pero con huesos frágiles, cuya madre era de huesos normales. a) Cuál es la probabilidad de que su hijo: b) No tenga ninguna enfermedad c) Tenga cataratas y huesos normales d) Tenga huesos frágiles y ojos normales e) Padezca ambas enfermedades 19. En el ser humano, la presencia de uno de los antígenos Rh de la superficie de los eritrocitos y la forma ovalada de estos (eliptocitosis) son causadas por la existencia de sendos alelos dominantes situados en la misma pareja autosómica. Un hombre con eliptocitosis, cuya madre tenía glóbulos rojos normales y genotipos homocigótico Rh positivo, y cuyo padre era Rh negativo y heterocigótico para la eliptocitosis, se casa con una mujer normal y Rh negativa. a) ¿Cuál es la probabilidad de que su primer hijo sea Rh negativo y tenga eliptocitosis?. b) Si su primer hijo es Rh positivo, ¿cuál es la probabilidad de que tenga eliptocitosis?. ¿Y si es el segundo hijo?. 20. En el cruzamiento AaBbDDFf x AABbddFF, todos los genes segregan independientemente y muestran dominancia. c) ¿Cuántos gametos genéticamente diferentes puede formar cada parental?. d) ¿Cuántos cigotos genéticamente diferentes se podrían formar en este cruzamiento?. e) ¿Qué proporción de la descendencia será heterocigótica para todos los loci?.
Problemas de Genética Biología 2º
4
MODIFICACIONES A LAS PROPORCIONES DE LAS LEYES DE MENDEL Herencia intermedia (codominancia) 21. Una mariposa de alas grises se cruza con una de alas negras y se obtiene una descendencia formada por 115 mariposas de alas grises y 115 mariposas de alas negras. Si la mariposa de alas grises se cruza con una de alas blancas se obtienen 94 mariposas de alas blancas y 94 de alas grises. Razonar ambos cruzamientos, indicando cómo son los genotipos y fenotipos de las mariposas que se cruzan y la descendencia. 22. Dos plantas de dondiego (Mirabilis jalapa) son homocigóticas para el color de las flores. Una de ellas produce flores de color blanco marfil y la otra, flores rojas. Señale los genotipos y fenotipos de los dondiegos originados del cruce de ambas plantas, sabiendo que "B" es el gen responsable del color marfil, "R" es el gen que condiciona el color rojo y que los genes R y B son equipotentes ( herencia intermedia). 23. Las cobayas de pelaje color amarillo son homocigotos (CACA), el color crema se debe a un genotipo heterocigótico (CACB), y el blanco es debido al genotipo homocigótico (CBCB). ¿Qué proporciones genotípicas y fenotípicas se obtienen de un cruzamiento entre dos cabayas de color crema?. 24. En las plantas del género Antirrhinum, las flores rojas y las blancas presentan herencia intermedia. Lo mismo ocurre con las hojas estrechas y las hojas anchas. Suponiendo que las parejas alélicas correspondientes segregan de forma independiente, indicar las proporciones genotípicas y fenotípicas esperadas en: a) La autofecundación de una planta de flores rosas y hojas de anchura intermedia. b) El cruzamiento entre una planta igual a la anterior y otra de flores blancas y hojas estrechas. Genes letales 25. La ausencia de patas en las reses se debe a un gen letal recesivo. Del apareamiento entre un toro y una vaca, ambos híbridos, ? qué proporciones genotípicas se esperan en la F2 adulta?. Los becerros amputados mueren al nacer. 26. La enfermedad de Tay-Sachs es una enfermedad hereditaria recesiva que causa la muerte en los primeros años de vida cuando se encuentra en condición homocigótica. Se piensa que los dedos anormalmente cortos, braquifalangia,se deben al genotipo heterocigótico para un gen letal, siendo normal el individuo BB. ? Cuáles son los fenotipos esperados entre niños adolescentes hijos de padres braquifalángicos y heterocigóticos para la enfermedad de Tay-Sachs ?. 27. Una mujer lleva en uno de sus cromosomas X un gen letal recesivo, y en el otro, el alelo dominante normal. ¿Cuál será la proporción de sexos en la descendencia de esta mujer con un hombre normal?. 28. En los ratones de campo existe un gen que determina el color pelo amarillo y que es dominante sobre el que determina el color normal o de tipo salvaje. El tamaño de la cola está determinada por una pareja alélica, de tal manera que el gen dominante determina tamaño de cola corta mientras que el recesivo determina tamaño normal o de tipo salvaje. Ambas parejas de genes se transmiten a la descendencia independientemente la una de la otra. Aquellos embriones que son homocigóticos para uno o para los dos genes dominantes mueren antes de nacer. ¿En qué proporción y como serán los fenotipos de la descendencia de un cruzamiento entre un macho de color amarillo y cola corta con una hembra de las mismas características?.
Problemas de Genética Biología 2º
5
Alelismo multiple. Series alélicas. 29. Un hombre acusa a su esposa de infidelidad alegando que el cuarto de sus hijos no es suyo. Los dos primeros hijos tienen el grupo sanguíneo AB y el tercero es del grupo A. El hijo motivo de la demanda es del grupo B y los esposos son de los grupos sanguíneos A y AB. Con estos datos, ¿se puede probar la infidelidad de la esposa?. 30. Si un hombre del grupo sanguíneo AB se casa con una mujer del grupo A, cuyo padre era del grupo 0. ¿Qué grupos sanguíneos se puede esperar entre sus hijos y con qué frecuencia?. 31. En una determinada raza de ratones el color del pelo está controlado por una serie alélica: A1 determina el pelaje negro, A2 blanco, A3 rayado y A4 grisáceo. El alelo A1 domina sobre el A2, éste sobre el A3 y éste sobre el A4. Al cruzar un ratón negro y otro rayado se obtuvo una camada formada por dos ratones blancos y cuatro negros. a) ¿Cuáles serán los fenotipos de los ratones que se cruzan?. b) De los ratones de la camada, ¿cuántos se esperaba que fueran blancos?. 32. La herencia del color de la piel en las reses, está determinada por una serie de alelos múltiples, con la siguiente jerarquía de dominancia: S > sh > sc > s El alelo “S” determina una banda de color blanco alrededor del cuerpo que se denomina cinturón holandes. El alelo “sh” produce manchas de tipo Hereford, el color sólido es el resultado del alelo “sc” y las manchas tipo Holstein, están producidas por el alelo “s”. Machos con cinturón holandés homocigóticos son cruzados con hembras tipo Holstein. Las hembras de la F1 son cruzadas con machos tipo Hereford de genotipo “sh sc”. Predecir las frecuencias genotípicas y fenotípicas de la descendencia. 33. Una serie de alelos múltiples gobierna la intensidad de la pigmentación en el ratón. D = color completo; d = color diluido y dl = letal. El orden de dominancia es: D > d > dl Un ratón de color completo portador del gen letal es apareado con un individuo color diluido también portador del gen letal. a) ¿Qué proporción fenotípica puede esperarse de la descendencia viable?. b) ¿Qué porcentaje de la descendencia con color completo es portadora del gen letal?. c) ¿Qué porcentaje de la descendencia con color diluido lleva el gen letal?. Epistasia o interacción génica 34. El color del pelaje de una determinada raza canina es debido a dos parejas de genes independientes. El pelo negro es controlado por un gen dominante respecto a su alelo que determina el color café. En otro locus, un alelo dominante inhibe la pigmentación del pelo produciendo, por tanto, perros de pelo blanco; su alelo recesivo permite la coloración del pelaje. Calcular: a) El porcentaje de perros blancos que se espera obtener del cruzamiento de un perro diheterocigótico con otro de color café. b) La probabilidad de obtener una camada de seis, cinco perros de color café y uno negro. 35. En Salvia horminum el color de la flor está determinada por un par de loci independientes, cada uno con dos formas alélicas (dominante y recesiva). Al cruzar individuos doble heterocigóticos de flor color violeta se obtuvo la siguiente descendencia: 9 de flores violetas, 3 de flores rosas y 4 de flores blancas. ¿Cómo podría explicarse esta segregación?.
Problemas de Genética Biología 2º
6
HERENCIA LIGADA AL SEXO 36. El daltonismo es un carácter ligado al sexo en la especie humana. En un matrimonio, la mujer posee visión normal para los colores, mientras que su padre era daltónico; y su marido posee visión normal, siendo el padre de este también daltónico. ¿Qué descendencia cabe esperar de este matrimonio para dicho carácter?. 37. En la especie humana, la hemofilia es debida a un gen recesivo localizado en el segmento diferencial del cromosoma X. Su alelo dominante no origina esta enfermedad. Un hombre normal se empareja con una mujer normal cuyo padre sí lo era. Calcula la probabilidad de que la pareja tenga: a) Un varón hemofílico b) Un varón hemofílico y una mujer portadora c) Un niño y una niña normales 38. En la especie humana, la aparición de vello en los pabellones auriculares es debida a la existencia de un gen situado en el segmento no homólogo del cromosoma Y. De la descendencia de un hombre con pelo en las orejas y una mujer sin pelos. a) ¿Qué proporción de descendientes varones poseerán pelos en los pabellones auriculares?. b) ¿Cuál es la probabilidad de tener un varón sin pelos en las orejas?. c) ¿Con qué frecuencia las hijas tendrán pelos en los pabellones auriculares?. 39. En la especie humana el color azul de los ojos se debe a un gen autosómico, recesivo frente a su alelo dominante para el color pardo, y el daltonismo es controlado por un gen recesivo situado en el segmento diferencial del cromosoma X. Una mujer de ojos azules y portadora del daltonismo procrea con un varón daltónico y de ojos pardos (hijo de una mujer de ojos azules). Determinar, utilizando el cálculo de frecuencias, cuál es la probabilidad de la pareja de tener una niña daltónica y de ojos azules. 40. Una mujer de grupo sanguíneo A y de visión normal tiene cuatro hijos con dos hombres distintos. Uno de ellos es daltónico y de grupo sanguíneo AB. El otro es normal y de grupo sanguíneo A. Los hijos son: Varón daltónico de grupo sanguíneo O; Hembra normal de grupo sanguíneo B; Hembra normal de grupo sanguíneo O; Hembra daltónica de grupo sanguíneo A. a) ¿Cuál es el padre de cada niño?. b) ¿Son portadoras del daltonismo las dos niñas normales, es decir, no daltónicas?. HERENCIA INFLUIDA POR EL SEXO 41. El tipo mocho (sin cuernos) de las ovejas es producido por un gen que es dominante en las hembras, pero recesivo en los machos. Un macho homocigótico con cuernos se cruza con una hembra también homocigótica, pero mocha. Realiza la segregación respecto al sexo y al carácter mocho en F1 y F2. 42. Consideramos simultáneamente dos rasgos influidos por el sexo, la calvicie y la cortedad del dedo índice, ambos dominantes en el hombre y recesivos en la mujer. Un hombre calvo heterocigótico, con dedo índice largo, se casa con una mujer de dedo índice largo, heterocigótica y calva. Determinar las frecuencias genotípicas de sus hijos/as. 43. En ovinos la lana blanca (W) es dominante sobre la negra (w), y la presencia de cuernos (H) es dominante sobre la ausencia de cuernos (h) en machos, pero recesiva en hembras. Si un macho blanco con cuernos y homocigótico se cruza con una hembra negra sin cuernos y homocigoto, ¿qué descendencia obtendremos en la F1 y en la F2?.
Problemas de Genética Biología 2º
PROBLEMAS DE ÁRBOLES GENEALÓGICOS 44. En la siguiente figura se indica la transmisión de un carácter (individuos en negro) en una familia. a) Se trata de un carácter dominante o recesivo. b) Indica el genotipo más probable de cada uno de los individuos (utiliza las letras A y a). c) ¿El gen que determina este carácter es autonómico o está situado en el cromosoma X?.
45. En la figura se indica la transmisión de un carácter en una familia. El carácter representa las dos alternativas (blanco y negro) y está determinado por un solo gen. a) Indica si el alelo que determina la característica representada en negro es dominante o recesivo. b) Indica si el gen que determina ese carácter es autosómico o está ligado al sexo. c) Indica los posibles genotipos de todos los individuos (utiliza las letras a y a).
46. En la siguiente figura se indica la transmisión de un tipo de cataratas (individuos en negro) en una familia. Se sabe que esa enfermedad está producida por un gen ligado al sexo situado en el cromosoma X. a) Indica si ese tipo de cataratas es dominante o recesivo. b) Indica los posibles genotipos de los de la familia (utiliza los símbolos XA y Xa ). c) Indica la probabilidad de que la mujer señalada con la flecha tenga un hijo con cataratas.
7
Problemas de Genética Biología 2º
8
PROBLEMAS DE PAU CASTILLA y LEÓN
En una experiencia de laboratorio en la que se empleaban ratones negros, se obtuvo una variedad genética con pigmentación de color blanco, comprobándose que eran heterocigóticos respecto al carácter “pigmentación” (Pp), mientras que los ratones normales sin pigmentación eran homocigóticos (PP). Asimismo, pudo comprobarse que los embriones que tenían un genotipo recesivo homocigótico (pp) morían antes del nacimiento. Si los ratones pigmentados se aparean entre sí: ¿Qué genotipo y qué fenotipo y en qué proporción puede esperarse en la generación F1?. Y si dicha generación F1 se aparea libremente entre si, ¿qué fenotipos se obtendrían?
En el tomate el color rojo del fruto es dominante (R) sobre el color amarillo (r) y la forma biloculada (B) domina sobre la multiloculada (b). Si se desea obtener una línea de plantas de frutos rojos y multiloculados a partir del cruzamiento entre razas puras rojas y biloculadas con razas amarilla y multiloculadas. ¿Qué proporciones de la F2 tendrá el fenotipo deseado? ¿Qué proporciones de esta será homozigótica para los dos caracteres?.
Una mujer (cuyo padre era daltónico y su madre normal para la visión de los colores) tiene hijos con un hombre daltónico. ¿Cuales serán los genotipos de los progenitores y de su descendencia?. ¿Cuáles serán los fenotipos y en que proporciones?
Si suponemos que el color de ojos en humanos está controlado por un gen con dos alelos: b responsable de ojos azules y B que produce ojos marrones y es dominante sobre b: ¿Cuál es el genotipo de un hombre de ojos marrones que tiene un hijo de ojos azules con una mujer de ojos azules? Considerando el mismo apareamiento anterior ¿Que proporción de los dos colores de ojos cabría esperar en los descendientes? ¿Que proporción cabría esperar en cuanto al color de los ojos en la progenie de un apareamiento entre dos individuos de ojos marrones, cada uno de los cuales tenía un progenitor con ojos azules? ¿Cuál de las leyes de Mendel se supone se aplica en el cruzamiento propuesto en la cuestión c)? Razone la respuesta.
Dado el siguiente cruzamiento: SsYy x ssyy ¿Qué genotipos y en qué proporciones esperaría encontrar en la generación filial F1? Explique en que consiste el cruzamiento prueba y que utilidades tiene.
Una hembra Drosophila de genotipo desconocido respecto al color de ojos es cruzada con un macho de ojos color blanco (W) [ el color blanco de los ojos es un carácter ligado al cromosoma X y recesivo respecto al color de ojos rojo silvestre (W+)]. En la descendencia obtenida, la mitad de los machos y la mitad de las hembras pertenecen al fenotipo ojos rojos y la mitad de los machos y la mitad de las hembras pertenecen al fenotipo ojos blancos. Deduzca razonadamente: ¿Cuáles son los genotipo y fenotipo de la Drosophila hembra parental?. ¿Cuáles son los genotipos de los posibles individuos de la generación filial F1 obtenidos a partir del cruzamiento indicado?. Explique brevemente que se entiende por herencia ligada al sexo. Cite un ejemplo en la especie humana.
Los colores de las flores de una angiosperma pueden ser rojo, rosa o blanco. Se sabe que este carácter está determinado por dos genes alelos codominantes: rojo (R) y blanco (B). Haga un esquema del cruzamiento, indicando de qué color serán las flores de los descendientes del cruce entre plantas de flores rosa y en qué proporciones se encontrarán. Defina los conceptos de dominancia, recesividad y codominancia.
BIOLOGIA 2º BACHILLERATO SOLUCIONES PROBLEMAS GENETICA
1
a) Aa b) 1/2
24
2
a) Dominante b) Aa x Aa c) Normal: 1/4 Acondroplasia: 3/4
25
a) Roja estrecha (RRAA)=1/16; Roja intermedia (RRAa)=2/16; Roja ancha (RRaa)=1/16; Rosa estrecha(RrAA)=2/16; Rosa intermedia (RrAa)=4/16; Rosa ancha (Rraa)=2/16; Blanca estrecha (rrAA)=1/16; Blanca intermedia (rrAa)=2/16; Blanca ancha (rraa)=1/16. b) Rosa estrecha; rosa intermedia; blanca estrecha y blanca intermedia 1/4 de cada una. 2/3 Aa y 1/3 AA
3
a) rr (retinto) x Rr (negro) b) ½ retinto ½ negro
26
BbTt x BbTt → 3 Normales y 6 con Braquifalangia
4
Dominante: rizado Recesivo: liso. Todos los rizados heterocigóticos
27
2 mujeres y 1 hombre
5
Verdadero
28
6
3/4 normales y 1/4 sedosas
29
4/8 amarillo corta (AaCc); 1/4 amarillo normal (aacc); 1/4 normal corta; 1/4 normal normal No se puede probar.
7
Con hembras homocigóticas recesivas
30
1/2 grupo A; 1/4 grupo AB y 1/4 grupo B
8
a) Aa x aa b) Aa x Aa c) aa x aa d) AA x aa e) AA x AA ó AA x Aa
31
A1A2 x A3A3/A3A4 → 2 Blancos y 4 Negros
9
A: normal a: FCU
32
1/2 cinturón holandés (Ssh/Ssc); 1/4 hereford (shs); 1/4 sólido (scs)
a) Aa x Aa ; Aa x aa ; aa x aa
10
a) bbSS x BBss b) 9: 3 : 3 : 1
33
Ddl x ddl → F1: Dd; Ddl; ddl; dldl a) 2/3 completo y 1/3 diluido; b) 50%; c) 100%
11
a) Alas y cuerpo normal dominantes, alas cortas y cuerpo marrón recesivos. b) Padres AaBb x AaBb c) Descendencia 9 A_B_/ 3 A_bb / 3 aaB_ / 1 aabb
34
a) 2/4 b) (1/4)6
12
P) LLTT x lltt F1) LlTl F2) 9 L_T_/ 3 L_tt /3 llT_ / 1 lltt c) No varían
35
Epistasia simple recesiva. A: color; B: violeta; b: rosa; a: sin color (blanca). a>B,b
13
P) TcCc x TTCC F1) TTCC/TTCc/TtCC/TtCc 1/4 de cada
36
Las hijas normales (la mitad portadoras) y los hijos normales y daltónicos
14
A: trepador a: normal a) Aa x aa b) Aa x Aa c) aa x aa
37
a) 1/4 b) 1/16 c) 1/8
15
a) AaCc x aaCc b) AaCc x AaCc c) AACc x aaCc
38
XYi x XX → XYi XX a) 100% b) 0% c) 0%
16
9:3:3:1
39
aaXDXd x AaXdY → aaXdXd frecuencia 1/8
40
a) Los hijos del grupo 0 del padre del grupo A, la hija daltónica del padre del grupo AB y la hija del grupo B del padre del grupo AB. b) La hija del grupo B sí y la otra puede serlo si lo hereda de la madre
41
F1 Aa (macho con cuernos); F2 3/4 AA,Aa (con cuernos) 1/4 aa (mochos)
17
M aaRh+Rh- x H Aa Rh- Rh-
18
A:Cataratas; B: fragilidad ósea
19
a) 1/4; b) 50%; c) 25%
42
1/4 CCLl; 1/4 CcLl; 1/4 CCll; ¼ Ccll. C: calvo; c: normal; L: corto; l: largo
20
a) 8 y 2; b) 16; c) 2/16
43
F1: HhWw; F2: 9 H_W_; 3 H_ww; 3 hhW_; 3 hhww
21
a) AA (negras) x Aa (grises) b) aa (blancas) x Aa (grises)
44
a) Recesivo; b) ….; c) Autosómico
22
BB x RR → BR (rosa)
45
a) Recesivo; b) Autosómico; c) ….
23
1/4 amarillo (CACA); 1/2 crema (CACB); 1/4 blanco (CBCB)
46
a) Dominante; b) …. ; c) 1/4 (la mitad de los varones con cataratas)
AaBb x aaBb → a) 1/8 b) 1/8 c) 3/8 d) 3/8
BIOLOGÍA 2º BACHILLERATO ACTIVIDADES GENÉTICA. LIGAMIENTO y RECOMBINACIÓN 1. Dibuja todos los posibles gametos resultantes de una meiosis en cada una de las siguientes células. (Donde no se indica recombinación NO existe)
A b
c
b c A a b C
a
b
C
A
B B
A a
B B
a
C C c c
A
B B
A a
a
b b C C c c
PROBLEMAS DE RECOMBINACIÓN 2. Los genes “a” y “b” están situados en el mismo cromosoma. Escribe el genotipo de los descendientes del cruce entre un individuo diheterocigótico (aB/Ab) y un doble homicogótico recesivo en los siguientes casos: a) Sin recombinación entre a y b b) Con recombinación entre a y b ¿Se cumplen las proporciones mendelianas en alguno de los casos?. 3. Al cruzar un individuo doble heterocigótico con un doble homocigótico recesivo se obtuvo la siguiente proporción de descendientes: 1 Aabb: 1 aaBb ¿Cómo son posibles estos resultados?. Razona la respuesta.
4. El cuerpo negro (b) y los ojos púrpura (p) son mutaciones recesivas en Drosophila, frente al cuerpo (P) y ojos (b) silvestres o normales. En una serie de cruces de obtuvieron los siguientes resultados: Cruces
Descendientes
PpBb x ppbb
Normales 1/2- Negros púrpuras 1/2
PpBb x ppBb
Normales 1/4 - Púrpura normales 1/2 - Normal negras 1/4
PpBb x ppbb
Normales 1/3- Púrpura negras 1/3 -Normal negras -1/6 Púrpura normales 1/6
Explica dichos resultados 5. En un individuo triple heterocigótico (AaBbCc) en fase de acoplamiento, ¿cuáles son los tipos de gametos que puede transmitir a la descendencia?. Ordénalos de más a menos frecuentes.
ACTIVIDADES P.A.U. BIOLOGÍA
GENÉTICA MOLECULAR
1. La siguiente secuencia polinucleotídica corresponde a un fragmento de inicio de un gen bacteriano: 5’ ATGCGAGGGCCCTGCGTGCTG 3’ 3´ TACGCTCCCGGGACGCACGAC 5´ a) Escriba la secuencia de bases del ARNm que se pueda transcribir a partir de dicho fragmento (5) y señale su polaridad (1). b) Indique el número máximo de aminoácidos que puede codificar el ARNm transcrito (2) y el criterio en que se basa para dar su respuesta (2). 2. La siguiente secuencia de una monohebra de ADN corresponde al inicio de un gen bacteriano: 5’- ATGTTAAGGGCCCGTTGTGTG – 3’ 3’- TACAATTCCCGGGCAACACAC – 5’ a) Escriba la secuencia del ARNm correspondiente, indicando su polaridad. (2) b) ¿Cuántos aminoácidos puede codificar este fragmento? (2) c) ¿Qué características del código genético hay que aplicar para calcular el número de aminoácidos? (3) d) ¿Qué tipo de variación/es debería suceder en este fragmento de ADN para que produjera un polipéptido de 5 aminoácidos? Razone la respuesta. (3) 3. Dadas las secuencias de polinucleótidos siguientes: I) 5´- AGGCTACCTAAG – 3’ II) 5´- AGCGAUCAUGACA – 3’ III) 5´- CACCGACAAACGAA – 3’ a) Indique razonadamente, en cada caso, si se trata de ADN ó ARN (1) b) ¿Son iguales las dos cadenas que componen la doble hélice del ADN? Razone la respuesta (3) c) Dado el siguiente fragmento de ADN 5´- CGATATAGCCGTTAA - 3´, escriba cuál será su ARN mensajero y la secuencia peptídica sintetizada a partir de él, señalando con claridad cual será el extremo N- y C-terminal del péptido producido (6) (se incluye el código genético en hoja aparte) 4. Si la hebra codificante de un oligonucleótido de DNA es la siguiente: 5’ – ATTAGCCGAATGATT – 3’ a) b) c) d)
Escriba la secuencia de la hebra molde del DNA. Escriba la secuencia del mRNA. ¿Cuántos aminoácidos codifica dicha hebra? Si AUG codifica Met; CGA Arg; AGC Ser; AUU Ile y UGA stop (finalización), escriba la secuencia del oligopéptido codificado por dicha hebra. e) Si se produce una mutación por delección del 10º nucleótido, ¿cuál sería la secuencia del oligopéptido formado?
EXPRESIÓN DEL MENSAJE GENÉTICO
ADN cadena con sentido
3´... T A C C G T A C G G C T T A T A T T ... 5´ 5´... A T G G C A T G C C G A A T A T A A ... 3´ TRANSCRIPCIÓN
ARN 5´ ... A U G G C A U G C C G A A U A U A A ... 3´ codón inicial
CODONES
codón sin sentido
TRADUCCIÓN
PÉPTIDO NH2 -
Met - Ala - Cys - Arg - Ile - COOH
BLOQUE IV MICROORGANISMOS, INMUNOLOGÍA Y SUS APLICACIONES
TEMA 6. MICROBIOLOGÍA Y BIOTECNOLOGÍA TEMA 7. INMUNOLOGÍA TEMA 3. LAS NUEVAS TECNOLOGÍAS EN LA INVESTIGACIÓN DEL MEDIO AMBIENTE
TEMA 6. MICROBIOLOGÍA y BIOTECNOLOGÍA 1. CONCEPTO y PROPIEDADES DE LOS MICROORGANISMOS 2. ORIGEN y CLASIFICACIÓN DE LOS MICROORGANISMOS 3. VIRUS Estructura y clasificación de los virus Ciclos vitales 4. BACTERIAS Arqueobacterias Bacterias verdaderas (eubacterias) Morfología bacteriana Reproducción y genética bacteriana 5. MICROORGANISMOS EUCARIOTAS Algas microscópicas Hongos microscópicos Protozoos 6. BIOTECNOLOGÍA o MICROBIOLOGÍA INDUSTRIAL Aplicaciones de la biotecnología: Industrias alimentarias Industrias químicas Industria farmaceútica y medicina Agricultura Medio ambiente Minería
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
1
1. CONCEPTO Y PROPIEDADES DE LOS MICROORGANISMOS Los microorganismos son un conjunto de seres vivos de gran sencillez estructural y organizativa y que, debido a su reducido tamaño, sólo son visibles al microscopio. En cuanto a su diversidad, caben apuntes que dentro de los microorganismos encontramos toda gama de tipos nutricionales (vistos en el tema 4) y están representados cinco grupos de seres vivos: virus, bacterias, protozoos, hongos y algas, cuyas principales características figuran en esta tabla. Organización
Tamaño
Carácter distintivo
Grupo
Acelular
0,1 µm
Parásitos obligados
Virus
Procariota
10 µm
Anaerobios (la gran mayoría)
Arqueobacterias
Aerobios y anaerobios
Eubacterias
Eucariotas
>250 µm
Con pared celular
Algas
Con clorofila, autótrofos Sin clorofila, heterótrofos
Sin pared celular, heterótrofos
Hongos Protozoos
A pesar de esta variedad hay algunas características derivadas de su pequeño tamaño, comunes a la mayoría: a) Rápido intercambio de sustancias con el medio externo, dado que la disminución del tamaño celular supone un aumento en la relación superficie/volumen. b) Metabolismo muy rápido, pues los compartimentos celulares están muy próximos a los metebolitos y a los nutrientes. Por ello pueden alterar rápidamente el medio en el que viven, agotando los nutrientes e inundándolo de residuos. Esta propiedad la utiliza la industria biotecnológica, que se aprovecha de los microorganismos para la fabricación de diferentes productos (derivados lácteos, antibióticos, licores,...). c) Rápida multiplicación, basada en su eficaz metabolismo. Esta propiedad les otorga a los microorganismos patógenos una gran capacidad invasora.
2. ORIGEN y CLASIFICACIÓN DE LOS MICROORGANISMOS Los microorganismos son seres vivos muy poco evolucionados, de manera que fueron los primeros seres vivos en aparecer en el planeta, tanto es así que durante más de 2.000 millones de años han sido los únicos seres que poblaban en planeta. A partir de estudios de ARN, se ha establecido que el origen de los microorganismos actuales deriva de tres líneas evolutivas que derivaron de un ancestro común (progenote) : Línea Bacteria: que dio lugar a las bacterias y cianobacterias. Línea Archaea: que dio lugar a las arqueobacterias. Línea Eukarya: que originó protozoos, hongos, y algas unicelulares. A partir de esta línea evolutiva evolucionaron el resto de seres vivos actuales. La enorme cantidad de microorganismos ha hecho necesaria una clasificación. De los cinco reinos en que se clasifican a los seres vivos (Whittaker, 1969), los microorganismos se hallan en tres: Reino Monera: engloba a organismos unicelulares y procariotas. Dentro de este grupo se encuentran las ARQUEOBACTERIAS, y EUBACTERIAS o BACTERIAS verdaderas. Reino Protista: engloba a organismos unicelulares y pluricelulares sencillos. Incluye las ALGAS MICROSCÓPICAS y PROTOZOOS. Reino de los Hongos: Engloba organismos unicelulares y pluricelulares, heterótrofos y descomponedores de materia orgánica. En este reino se incluyen los HONGOS FILAMENTOSOS (Mohos) y las LEVADURAS.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
2
Además de todos estos seres vivos, un grupo aparte, dentro de los microorganismos lo constituyen los VIRUS, que son organismos acelulares, que aunque carecen de metabolismo y son parásitos obligados, su importancia como agentes transmisores de enfermedades hace que tienda a estudiárselos como microorganismos. Otras formas acelulares descubiertas en los últimos años son los viroides y priones, estos últimos causantes de la enfermedad de las vacas locas.
3. VIRUS Los virus son organismos sin estructura celular, carecen de metabolismo propio y para multiplicarse necesitan obligatoriamente parasitar un organismo. Su estructura es muy sencilla, presentan un ácido nucleico (genoma vírico), rodeado de una cubierta de proteínas (cápsida) y en algunos casos una envoltura membranosa. Son capaces de adherirse a la superficie de las células, introduciendo en ellas su genoma, y utilizarlas para multiplicarse y generar las envolturas de nuevos virus, utilizando para ello la materia, energía y el sistema enzimático de la célula que parasita, son por tanto, parásitos intracelulares obligados. En general, los virus se caracterizan por su pequeño tamaño (entre 0,02 y 0,03 m de diámetro) y su simplicidad estructural. Estructura de los virus Una partícula vírica o virión está formado por un fragmento de ácido nucleico (genoma vírico) encerrado en una cubierta proteíca o cápsida. Algunos virus presentan además, una envoltura membranosa procedente de la célula hospedadora. Estos virus se denominan virus con envoltura, en contraposición a los virus desnudos, que carecen de ella. Genoma vírico. Contienen un ácido nucleico, ADN en unos casos o ARN en otros, pero nunca los dos a la vez. Este ácido nucleico puede ser lineal, circular, simple o doble. Debido a su pequeño tamaño, evidentemente contienen muy pocos genes. Cápsida. Es una cubierta de proteínas que envuelve al virus. Le sirve de protección al ácido nucleico, y en aquellos que carecen de envoltura membranosa, es la que reconoce a las células que parasita. Las proteínas de la cápsida se denominan capsómeros, y se disponen de forma regular, dando lugar a diferentes tipos de cápsidas: icosaédricas (virus de la polio, hepatitis), helicoidales (virus de la rabia o del mosaico del tabaco) y complejas. Estas últimas son típicas de virus parásitos de bacterias, llamados BACTERIÓFAGOS, y constan de una cabeza y una cola. Envoltura membranosa. Algunos virus presentan una envoltura que rodea a la cápsida, que consta de una doble capa de fosfolípidos y glucoproteínas. Suelen proceder de las células que parasitan. Ejemplos son el virus de la hepatitis, gripe, viruela y el virus del SIDA.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
3
Clasificación a) b) c) d)
Los virus se pueden clasificar según varios criterios: Por la célula que parasitan: virus animales, vegetales o bacteriófagos. Por su forma: helicoidales, poliédricos o complejos. Por tener o no envoltura: virus envueltos o desnudos. Por su ácido nucleico: ADNmc; ADNbc; ARNmc o ARNbc.
CICLO DE LOS VIRUS Aunque los virus no se nutren, ni se relacionan, ya que an con las células de forma fortuita, presentan interesantes mecanismos que les permiten reproducirse dentro de la célula huésped. Los virus realizan las siguientes fases en su ciclo de multiplicación: a) Entrada en el citoplasma de la célula huésped. b) Reproducción de las partículas víricas (viriones). c) Salida de los virus al exterior de la célula infectada. Presentan una característica muy peculiar en su reproducción: la síntesis de cada uno de sus componentes se da por separado y, posteriormente, se produce el ensamblaje entre ellos. Su ciclo vital se ha podido descifrar, gracias al estudio de los bacteriófagos (o fagos), que parasitan a las bacterias, descubriéndose que pueden seguir dos tipos de ciclos, en unos casos se multiplican rápidamente dentro de las células (ciclo lítico) y las destruyen y en otros permanecen un tiempo dentro de ellas de forma latente (ciclo lisogénico).
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
4
Ciclo de un bacteriófago 1) Fase de fijación o adsorción: el virus se une a un receptor específico situado sobre la cubierta de la cápsula de la bacteria. 2) Fase de penetración: es esta fase, únicamente es inyectado el ácido nucleico del virus (ADN) en el interior de la bacteria. A partir de este momento pueden seguir dos ciclos diferentes: a) Ciclo lítico: el ADN del virus utiliza la maquinaria de la bacteria para multiplicarse, fabricar múltiples moléculas ARNm y a partir de estos fabricar las proteínas de la cápsida. Cuando se han sintetizado cantidades suficientes, comienza el ensamblaje de las partículas víricas, de tal forma que el ácido nucleico se rodea de las proteínas de la cápsida y la bacteria se lisa, liberando gran cantidad de bacteriófagos. b) Ciclo lisogénico: este caso, los virus una vez que infectan a la célula, en vez de destruirla, incorporan su ADN al ADN de la célula, de tal forma que no expresa sus genes y se replica junto al de la bacteria, permaneciendo en estado de vida latente. Cuando están en este estado, se les denomina virus atenuados o profagos. Pueden permanecer de esta forma varias generaciones de la célula huésped, de forma que las nuevas células hijas también estarán infectadas, hasta que se produzca un estímulo que haga que el profago se convierta en un virus activo, y se múltiple en el interior de la célula igual que en el ciclo lítico, hasta destruirla. Mientras la célula está infectada, y posea el ADN profago, será inmune frente a infecciones de otros virus del mismo tipo.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
5
4. MICROORGANISMOS PROCARIOTAS: ARQUEOBACTERIAS y BACTERIAS (EUBACTERIAS o BACTERIAS VERDADERAS). ARQUEOBACTERIAS
Es el grupo más antiguo de bacterias. Presentan una membrana plasmática cuyos lípidos carecen de ácidos grasos. Las paredes celulares carecen de peptidoglucanos. Su genoma está formado por una sola molécula de ADN circular, más pequeña que la de las eubacterias. Hay especies autótrofas, aunque la mayoría son heterótrofas. Son capaces de vivir en ambientes de condiciones extremas de temperatura, salinidad, pH y anaerobiosis. Dependiendo de las mismas, a las que han adaptado su metabolismo, se distinguen tres grupos: ▪ Halofíticas: en ambientes de elevada salinidad. ▪ Metanógenas: anaerobias, en ambientes pantanosos y cenagosos. ▪ Hipertermófilas: de ambientes geotérmicos (volcánicos), incluso submarinos, donde las temperaturas superan los 80-100ºC. BACTERIAS
Actualmente se piensa que existen unas 2.000 especies, que pueblan todos los hábitats terrestres. Tienen un tamaño comprendido entre 1 y 10 micras. Su forma puede responder a cuatro tipos: bacilos (forma de bastón), cocos (forma esférica), espirilos (alargadas y enrolladas espiralmente) y vibrios (con forma de coma ortográfica), pudiendo agruparse en colonias de forma específica.
MORFOLOGÍA Y ESTRUCTURA BACTERIANA Desde el exterior al interior presentan las siguientes estructuras: 1. CÁPSULA Es una capa gruesa (100-400 A) que no está presente en todas las bacterias y sin estructura definida. Confiere a la bacteria resistencia a la desecación y al ataque por células fagocíticas, pudiendo servir también como elemento de fijación al sustrato.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
6
2. LA PARED BACTERIANA La pared celular es una cubierta rígida, de 50-100 A, adosada a la cara externa de la membrana plasmática, que rodea totalmente a la célula. Le da forma a la célula y resistencia a las fuertes presiones osmóticas de su interior. Composición y estructura de la pared Esta compuesta por peptidoglicano o mureína (polisacáridos unidos a cortas cadenas peptídicas). El peptidoglicano o mureína, común a todas las paredes celulares de eubacterias está formado por cadenas de polisacáridos de dos glúcidos: N-acetilglucosamina (NAG) y ácido N-acetilmurámico (NAM), unidos por enlaces (1 4); una corta cadena de cuatro aminoácidos se une, a su vez, a los restos de NAM. Se pueden establecer enlaces peptídicos entre los aminoácidos de cadenas de polisacáridos adyacentes.
Dentro de las eubacterias, se distinguen dos tipos de pared celular: Tipo grampositivo (Gram +): tienen paredes anchas, con numerosas capas de muerína reforzadas con ácido teicoico. Las Gram + se tiñen de color violeta en la tinción de Gram Tipo gramnegativo (Gram -): tienen la pared más estrecha, con una capa de mureína interna y una membrana lipídica externa, permeable gracias a canales de porina. Las bacterias Gram – se tiñen de color rosado con la tinción de Gram
Funciones de la pared celular Mantiene la forma de la célula y previene la lisis osmótica Regula el intercambio de sustancia con el medio externo Proporciona carga negativa a la superficie celular Posee componentes con capacidad antigénica
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
7
3. EL CITOPLASMA El citoplasma bacteriano está formado por una matriz gelatinosa, el protoplasma, con alto contenido en agua y de aspecto granuloso, que contiene proteínas y enzimas y alberga los ribosomas 70 S característicos de los procariotas, así como diversas inclusiones de naturaleza muy variada, según el tipo de bacterias.
4. EL NUCLEOIDE En la célula procariota, el material genético se encuentra en el nucleoide, zona de aspecto fibrilar situada en la región central del citoplasma, que no está protegida por una membrana nuclear. En las bacterias, el material genético esta constituido por: ▪ Un único cromosoma formado por ADN bicatenario, circular y superenrrollado. ▪ Uno o varios plásmidos,, pequeñas moléculas de ADN circular extracromosómico que se replican de forma independiente. Pueden unirse temporalmente al cromosoma bacteriano, en ese caso se llaman episomas. 6. APÉNDICES EXTERNOS Flagelos. Son prolongaciones finas cuya longitud es varias veces la bacteria, y que aparecen en un número que oscila entre 1 y 100. Intervienen en el movimiento bacteriano. Dependiendo de la situación de los flagelos las bacterias pueden ser: monotricas, lofotricas, anfitricas y peritricas. Pelos y fimbrias. Son filamentos huecos y tubulares formados por proteínas, y no intervienen en el movimiento. Las fimbrias con cortas y numerosas, mientras que los pelos son largos y suele haber uno o dos por bacteria. Las fimbrias les permiten a las bacterias fijarse al sustrato (actuarían como raíces) y los pelos participan en el intercambio de material genético entre bacterias (CONJUGACIÓN BACTERIANA). REPRODUCCIÓN y GENÉTICA BACTERIANA La reproducción de las bacterias es asexual, por lo que las bacterias hijas son idénticamente iguales a sus madres. Esto hace que en una colonia donde existen miles de ellas, todas sean clónicas. La reproducción se realiza mediante bipartición, a la que precede la duplicación del ADN. Una vez que el ADN se duplica se forma un tabique entre las dos moléculas de ADN, que divide a la bacteria en dos, separándose posteriormente las células hijas. Las bacterias poseen, además, unos mecanismos definidos como parasexuales, mediante los cuales intercambian información genética con otras bacterias, sean o no de su misma especie. Existen tres tipos de mecanismos parasexuales: a) Conjugación. Es un proceso por el cual una bacteria, considerada donadora, transmite ADN, a través de las fimbrias, a otra bacteria receptora. Las bacterias donadoras poseen pequeñas moléculas de ADN, los plásmidos, que pueden ser transmitidos durante la conjugación.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
8
Existen dos tipos de bacterias donadoras: ▪ Bacterias F+: poseen plásmidos (factores F) no integrados en el genoma bacteriano. Las bacterias F+ suelen transferir únicamente el plásmido a la bacteria receptora, denominada F - y que queda convertida en F+. ▪ Bacterias Hfr: poseen plásmidos integrados en el genoma bacteriano (se llaman episomas). Antes de la conjugación, duplican su ADN, incluido e factor F. Transfieren un fragmento de ADN a la bacteria receptora F-, que se recombina con su ADN y se transforma en Hfr.
b) Transducción. Es un fenómeno de intercambio genético que requiere un agente transmisor, que generalmente es un virus, el cual transporta fragmentos de ADN procedentes de la última bacteria parasitada.
c) Transformación. Es un proceso por el que una bacteria introduce en su interior fragmentos de ADN, que aparecen libres en el medio procedentes de la lisis de otras bacterias. Este mecanismo es el responsable de la transformación de cepas bacterianas no virulentas (cepas R) en virulentas (cepas S), cuando se cultivan en medios que contienen fragmentos de ADN procedentes de la cepa S destruida previamente (por ejemplo, por calor). Los mecanismos de intercambio genético explican la variabilidad que pueden presentar algunas bacterias al habitar junto a otras distintas. Un ejemplo de este proceso es la resistencia a antibióticos que presentan ciertas bacterias patógenas al convivir en el intestino con bacterias simbiontes que resisten bien la acción de estos productos farmaceúticos.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
9
5. MICROORGANISMOS EUCARIOTAS ALGAS MICROSCÓPICAS -Las algas son protoctistas, es decir unicelulares o pluricelulares, talofíticas (sin vascularizar), que carecen de tejidos y autótrofas fotosintéticas. -Las algas microscópicas son en su mayoría unicelulares, viven en medios acuáticos formando el fitoplacton. Realizan la mayor parte de la fotosíntesis de la Tierra siendo el primer eslabón de las cadenas tróficas de los ecosistemas acuáticos, liberando grandes cantidades de oxígeno a la atmósfera. -Todas tienen clorofila pero el color verde puede estar enmascarado por otros pigmentos que provocaran el color final y su hábitat. Pueden acumular los excedentes de su metabolismo tanto en forma de almidón como en otras sustancias de reserva. -Su pared celular es de celulosa, (las más sencillas carecen de pared celular), pero pueden tener también otras sustancias que modifican su aspecto. -Se reproducen tanto asexualmente como sexualmente, presentando todo tipo de ciclos biológicos. -Los principales grupos de algas microscópicas unicelulares son: Euglenófitos: Algas de agua dulce que carecen de pared celular. Se mueven mediante dos flagelos. Pueden enquistarse en casos de sequía. Diatomeas: Contienen fucoxantina, pigmento amarillo que les da su color típico. La pared celular está cubierta por dos piezas de sílice que encajan entre sí como una caja y su tapadera. Cuando se acumulan forman la tierra de diatomeas que, además de su interés paleontológico, se usa en la fabricación de pasta de dientes. Dinoflagelados: Son básicamente marinas, con una cubierta o teca muy consistente y de formas caprichosas. Suelen ser de color rojo, pudiendo producir toxinas que en grandes cantidades forman las mareas rojas, contaminantes de los criaderos de moluscos. Los otros grupos de algas, predominantemente pluricelulares, Clorófitos (algas verdes), Feófitos (algas pardas) y Rodófitos (algas rojas), también tiene representantes unicelulares. HONGOS MICROSCÓPICOS -El heterogéneo reino de los hongos agrupa a organismos eucariotas, con pared celular rígida formada por quitina y otros compuestos, pero sin celulosa, heterótrofos y con digestión externa que realizan mediante enzimas secretadas al medio. Tras esta digestión absorben los nutrientes. -Su ecología es muy diversa. Aunque hay representantes acuáticos, principalmente son terrestres. En función de cómo consiguen la materia orgánica que necesitan, encontramos: hongos parásitos, tanto de plantas como de animales causando enfermedades conocidas como micosis. Ejemplo son las tiñas, royas, el cornezuelo, pie de atleta, candidiasis, etc... hongos saprofitos, ocupan en los ecosistemas el nivel trófico de los descomponedores siendo responsables de la mineralización de los bioelementos. hongos simbióticos, con los algas formando los líquenes, o con raíces de plantas en las microrrizas. -En los hongos pluricelulares las células se disponen linealmente formando unos filamentos o hifas. Las hifas pueden formar un entramado conocido como micelio, que en los hongos macroscópicos se hace observable formando el cuerpo fructífero o seta. -Se reproducen por esporas, que pueden ser asexuales, formadas en el extremo de hifas especiales o conidios, o sexuales, con dos tipos, internas (ascosporas) y externas (basidiosporas). Según este criterio taxonómico se originan dos grupos de hongos, los Ascomicetos y Basidiomicetos. -Los principales hongos microscópicos son las levaduras y los mohos, sin valor taxonómico.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
10
Levaduras Son hongos unicelulares que se reproducen asexualmente por gemación. Pertenecen al grupo de los ascomicetos. Viven en medios ricos en azúcares. Tienen una gran importancia económica, pues las fermentaciones del vino, cerveza y pan las realizan levaduras del género Saccharomyces. El género Cándida es una levadura patógena. Mohos Reúne hongos microscópicos, pluricelulares filamentosos. El moho es una fina capa pulverulenta, de diverso color, que forman estos hongos sobre materia orgánica como pan, fruta, queso, carne etc.. Los antibióticos son producidos principalmente por mohos para impedir el desarrollo de las bacterias que competirían con ellos por los nutrientes del medio.
PROTOZOOS -Los protozoos son microorganismos eucariotas unicelulares heterótrofos sin pared celular. La mayoría son de vida libre en medios acuáticos o húmedos, aunque algunos se han adaptado al parasitismo, pudiendo producir enfermedades en el hombre. -Toman la materia orgánica en disolución por pinocitosis o en estado sólido por fagocitosis. Predominan las formas móviles, mediante cilios, flagelos o seudópodos. -Se reproducen asexualmente y sexualmente, normalmente por conjugación. Pueden originar estructuras muy resistentes, llamadas quistes, con las que sobreviven en condiciones adversas. -Hay unas 30.000 especies que se encuentran en todo tipo de las charcas y que se pueden agrupar en cuatro clases Grupo
Locomoción
Hábitat
Ejemplos
Flagelados
Flagelos
Aguas dulces
Tripanosoma, enfermedad del sueño
Sarcodinos
Pseudópodos
Aguas dulces y marinas
Amebas y Foraminíferos
Ciliados
Cilios
Aguas dulces y marinas
Paramecios. Tienen dos núcleos
Esporozoos
Por contracciones
Parásitos
Plasmodium causa la malaria
DIFERENCIAS ENTRE TIPOS DE MICROORGANISMOS – VIRUS: Formas acelulares, parásitos obligados, sin metabolismo propio. – BACTERIAS, PROTOZOOS, ALGAS MICROSCÓPICAS, LEVADURAS y MOHOS: Seres vivos celulares, con metabolismo propio
DIFERENCIAS
1) ORGANIZACIÓN CÉLULAR:
PROCARIOTA: BACTERIAS EUCARIOTA: PROTOZOOS, ALGAS, LEVADURAS, MOHOS
UNICELULARES: BACTERIAS, PROTOZOOS, ALGAS UNICELULARES, LEVADURAS PLURICELULARES: algunas CIANOBACTERIAS (filamentosas), ALGAS FILAMENTOSAS, MOHOS
2) PARED CELULAR
SIN PARED CELULAR: PROTOZOOS CON PARED CELULAR: – De PEPTIDOGLUCANOS: BACTERIAS (excepto ARQUEOBACTERIAS) – De CELULOSA: ALGAS – De QUITINA: MOHOS y LEVADURAS
3) METABOLISMO
AUTÓTROFO FOTOSINTÉTICO: – ALGAS – BACTERIAS FOTOSINTÉTICAS: CIANOBACTERIAS (Fotosíntesis oxigénica), BACTERIAS VERDES Y PURPÚREAS (Fotosíntesis anoxigénica).
HETERÓTROFO TÍPICO: – PROTOZOOS – LEVADURAS y MOHOS (Saprófitos) – BACTERIAS HETERÓTROFAS (Parásitas, Saprófitas y Simbiontes)
AUTÓTROFO QUIMICOSINTÉTICO: – BACTERIAS QUIMIOSINTÉTICAS o QUIMIOLITOTROFAS
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
11
6. BIOTECNOLOGÍA La Biotecnología es la aplicación de procedimientos científicos y técnicas a la transformación de ciertas materias por agentes biológicos para producir bienes y servicios. Estos agentes biológicos son esencialmente microorganismos, y en otros casos enzimas o células vegetales y animales. Los bienes y servicios tienen que ver con la agricultura, pesca, así como con las industrias alimentarias y farmacéutica. El empleo de diferentes microorganismos con fines industriales para la obtención de diferentes productos, por lo que recibe el nombre de biotecnología microbiana o microbiología industrial. La biotecnología microbiana tradicional utiliza los microorganismos tal y como se encuentran en la naturaleza, pero recientemente se están utilizando microorganismos alterados genéticamente mediante métodos de ingeniería genética. Los microorganismos utilizados en la biotecnología proceden de la naturaleza, pero se han seleccionado a partir de sus capacidades para producir determinados productos o con determinados fines. Lo primordial es que el microbio sea capaz de crecer rápidamente, resista al ser cultivado a gran escala y pueda producir la sustancia útil en una cantidad apreciable y en el menor tiempo posible. APLICACIONES DE LA BIOTECNOLOGÍA 1. INDUSTRIAS ALIMENTARIAS Obtención de productos por fermentación: algunos microorganismos no patógenos son muy interesantes al ser capaces de transformar ciertas sustancias en productos de gran importancia para el hombre, mediante procesos de fermentación. La mayoría de estas fermentaciones se producen en condiciones anaerobias, no obstante algunas se llevan a cabo de forma aerobia, tratándose más bien de respiraciones aerobias con oxidación incompleta. Las fermentaciones a escala industrial se llevan a cabo en fermentadores. Se trata de depósitos de diferente capacidad en los que existe un líquido que actúa como medio de cultivo del microorganismo. El medio de cultivo y los microbios industriales se mezclan mediante un sistema de palas y estos van transformando por fermentación sustratos de ese medio y originan los productos de interés. Ejemplos de fermentaciones son: Fermentación alcohólica: llevada a cabo por levaduras del género Saccharomyces. Se utiliza para la obtención de bebidas alcohólicas como el vino y la cerveza, y algunas bebidas destiladas (whisky, ron). Fermentación láctica: llevada a cabo por las bacterias de la leche, como Lactobacillus bulgaricus. Degradan la lactosa y producen ácido láctico. Este proceso se utiliza para la elaboración de productos derivados de la leche, como el queso, yogur, o requesón. También las sales de ácido láctico pueden tener algunos fines, como el tratamiento de anemias (lactato de hierro) y deficiencias de calcio (lactato de calcio) o por ejemplo los lactatos de socio empleados como sustancias plastificantes. 45 Fermentación acética: se trata de un proceso aerobio, por el que diferentes bacterias del género Acetobacter y Gluconobacter degradan el etanol a ácido acético. Se utiliza industrialmente para la obtención de vinagre, utilizando como sustrato vino o sidra. Producción de vitaminas, aminoácidos: algunas vitaminas que se añaden a los alimentos y que su síntesis química resulta complicada, se obtienen por procedimientos de biotecnología. Ejemplos son la vitamina B12 y la riboflavina. Muchos microorganismos pueden sintetizar aminoácidos a partir de compuestos nitrogenados en mayor cantidad de la que necesitan. Estos aminoácidos producidos industrialmente se utilizan como aditivos alimentarios, para potenciar el sabor, como edulcorantes o antioxidantes. Son ejemplos el ácido glutámico, lisina, metionina, alanina y glicina. Fabricación de proteínas para pienso: se utilizan bacterias y levaduras que son ricas en proteínas y que consuman medios de cultivo baratos.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
12
2. INDUSTRIAS QUÍMICAS Producción de enzimas: diversos hongos y bacterias producen enzimas en grandes cantidades que son utilizadas en panadería, pastelería, farmacia, medicina, lavandería y en la industria textil. Producción de disolventes, como acetona y butanol 3. INDUSTRIA FARMACÉUTICA y MEDICINA (SECTOR BIOMÉDICO) Producción de antibióticos: los antibióticos son productos de síntesis, fabricados por algunos microorganismos. Hasta el momento se conocen cerca de 800 antibióticos producidos por hongos del género Penicillium y bacterias de los géneros Bacillus y Streptomyces. La producción industrial de antibióticos ha crecido espectacularmente desde los años 50 debido al descubrimiento de especies con mayor capacidad de producción, mejora de medios de cultivo y de extracción del antibiótico de la mezcla del cultivo. La ingeniería genética ha hecho posible el aislamiento de genes de cepas productoras de antibióticos y su por tranformación bacteriana obtener microorganismos capaces de producirlos a escala industrial. Obtención de hormonas como la insulina y la hormona de crecimiento a partir de bacterias transformadas con los genes responsables de estas moléculas. Otros medicamentos: mediante técnicas de ingeniería genética, empleando microbios como productores se han obtenido eritropoyetina, interferón, factor VIII plaquetario,... Elaboración de vacunas y sueros Empleo de virus para tratamiento de enfermedades infecciosas. Utilización de virus como vectores para introducir genes mediante métodos de terapia génica. 4. AGRICULTURA Control de plagas: Algunos microorganimos han sido utilizados como bioinsecticidas para controlar algunas plagas. Infectan a los insectos en estado adulto o larvario y los matan o bien fabrican alguna sustancia tóxica. Se han utilizado algunos virus y ciertas especies de bacterias y hongos. 5. MEDIO AMBIENTE Depuración de aguas residuales: en las plantas depuradoras de aguas residuales, el tratamiento secundario permite eliminar sustancias orgánicas indeseables mediante diferentes microorganismos, que las oxidan produciendo como desecho CO2 y metano. Limpieza mareas negras: ciertas bacterias, levaduras y algas transformar los hidrocarburos en compuestos más solubles e inestables, que son atacados por otros microorganismos hasta dar como productos finales CO2 y H2O. 6. MINERÍA En el lavado de ciertos minerales se emplean bacterias, así como en la recuperación de escombros mineros.
APLICACIONES BIOTECNOLOGÍA 1. SECTOR ALIMENTARIO
Fabricación de PRODUCTOS FERMENTADOS: – Por FERMENTACIÓN ALCOHÓLICA (realizada por levaduras del gen. Saccharomyces): PAN, BEBIDAS ALCOHÓLICAS FERMENTADAS (vino, cerveza). – Por FERMENTACIÓN LÁCTICA (realizada por bacterias lácticas del gen. Lactobacillus): QUESOS, YOGURES, LECHES FERMENTADAS (tipo Bífidus o similares). – Por FERMENTACIÓN ACÉTICA (realizada por bacterias del gen. Acetobacter): VINAGRE.
Otros: proteínas para pienso animal, algunas vitaminas y algunos aminoácidos como aditivos.
2. SECTOR BIOMÉDICO
Fabricación de ANTIBIÓTICOS por Actinomicetos (Bacterias gram + aerobias) y mohos del genero Penicillium.
Fabricación de HORMONAS: insulina, hormona de crecimiento.
Fabricación de MEDICAMENTOS: Proteínas sanguíneas (factores plaquetarios, EPO), inmunomoduladores (interferón, interleucina).
Fabricación de VACUNAS y SUEROS (tratado en tema 7).
Técnicas de TERAPIA GÉNICA que empleen virus como vectores de transmisión de genes sanos en personas con enfermedades genéticas.
3. MEDIO AMBIENTE
DEPURACIÓN de AGUAS RESIDUALES LIMPIEZA MAREAS NEGRAS (Biorremediación) CONTROL de PLAGAS con BIOINSECTICIDAS
1
ESTUDIO Y CONTROL DE MICROORGANISMOS Medios de cultivo Un cultivo es un conjunto de células microbianas que crecen en un medio con nutrientes. Los medios pueden ser de dos tipos, según su estado:
Medios líquidos o caldos de cultivo. Se elaboran con varios nutrientes líquidos, los cuales se introducen en un tubo de ensayo o en un matraz Errlenmeyer, tapados con algodón. Se utilizan para controlar el crecimiento de las poblaciones. Medios sólidos. Se preparan mezclando una solución con varios nutrientes líquidos con un agente gelificante, como agar-agar.
Los medios pueden tener distintos componentes que favorezcan o inhiban el crecimiento de algunos microorganismos, pudiéndose diferenciar tres tipos:
Medios de enriquecimiento. Incluyen sustancias que permiten el crecimiento de algunos microorganismos sobre otros. Medios selectivos. Contienen una o más sustancias que inhiben el crecimiento de algunos microorganismos. Medios indicadores. Presentan un indicador que permite que ciertas colonias de un microorganismo se diferencien claramente de otras.
Crecimiento de un cultivo microbiano Para representar el crecimiento en un cultivo microbiano se utiliza el logaritmo en base diez del número de células para construir la curva de crecimiento del cultivo a lo largo del tiempo.
2
Control de microorganismos Los agentes que actúan contra los microorganismos pueden ser físicos o químicos, y según el efecto que produzcan pueden ser: Microbicidas: si los matan (bactericida en caso de bacterias). Microbiostáticos: si inhiben su crecimiento (bacteriostático en caso de bacterias).
Agentes físicos a) Esterilización. Es uno de los métodos más utilizados. Se basa en la exposición de los microorganismos a altas temperaturas durante cierto tiempo. Con ello se destruyen las cubiertas bacterianas o se inactivan las enzimas. Dependiendo de los tipos de calor, se diferencian:
Calor húmedo. Produce la desnaturalización y coagulación de las proteínas de los microorganismos. Se diferencia entre: Esterilización clásica. Consiste en un calentamiento a 120 ºC durante 30 minutos. Se utiliza para esterilizar latas y frascos de vidrio con conservas. Esterilización tipo UHT. Es un calentamiento a 140 ºC durante tres segundos. Mantiene mejor las vitaminas de los alimentos, pero no proporciona tanto tiempo de conservación. Calor seco. Produce la oxidación de los componentes celulares.
b) Pasteurización. Se utiliza para eliminar la mayoría de los microorganismos de los alimentos, sin que estos pierdan sus principales características de sabor o aroma. En la pasteurización de la leche se eleva rápidamente su temperatura a 71,7ºC durante quince a veinte segundos. c) Congelación. Es un tratamiento bacteriostático, que permite conservar los alimentos. d) Radiaciones electromagnéticas. Pueden ser: Radiaciones ionizantes. Rayos X o rayos gamma que ionizan las moléculas orgánicas, como el ADN y las proteínas, modificando su composición. Radiaciones no ionizantes. Las radiaciones UV que provocan mutaciones en el ADN o alteran o inhiben su duplicación. d) Filtración. Se utilizan filtros de microporos para retener los microorganismos presentes en el aire o en líquidos.
Agentes químicos a) Esterilizantes. Destruyen toda forma de vida microbiana de las superficies que son tratadas. Se utiliza el formaldehído o glutaraldehído. b) Desinfectantes. Eliminan los microorganismos que producen enfermedades infecciosas, pero no las esporas microbianas. Se utilizan como desinfectantes la lejía (hipoclorito sódico), fenoles, sulfato de cobre, etc. c) Antisépticos. Se utilizan contra microorganismos presentes en heridas, como el alcohol al 70%, la solución de yodo, agua oxigenada, el jabón o los detergentes. d) Agentes quimioterapeúticos. Atacan a los microorganismos causantes de la enfermedad sin dañar las células del hospedador. Se pueden diferenciar dos tipos: Antibióticos. Son de origen natural, ya que son producidos por bacterias del grupo actinomicetales u ciertos hongos filamentosos. Se utilizan para el tratamiento de enfermedades infecciosas. (desarrollado en hoja aparte). Agentes quimioterapeúticos sintéticos, como las sulfamidas que inhiben el crecimiento bacteriano, el AZT que disminuye los efectos infecciosos del virus del SIDA, o la cloroquina que se utiliza contra la malaria.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
1
TEMA 6. MICROBIOLOGÍA y BIOTECNOLOGÍA CUESTIONES DE SELECTIVIDAD Cuestiones sobre clasificación y diversidad de microorganismos. 1. Mencione los grandes grupos de microorganismos e indique sus principales características diferenciales relativas a la organización y al modo de obtener energía. 2. Diga si las siguientes afirmaciones son verdaderas o falsas, justificando la respuesta: a) En la estructura celular de un virus se encuentran siempre presentes: ácidos nucleicos, proteínas y lípidos. b) Las bacterias tienen mitocondrias y carecen de cloroplastos. c) Las levaduras son organismos procariotas autótrofos. d) Los protozoos y las cianobacterias son organismos procariotas heterótrofos. e) Las bacterias obtienen materia y energía por diferentes mecanismos. 3. Indique si las afirmaciones siguientes son verdaderas o falsas, justificando la respuesta: a) Las bacterias son responsables de la transformación de la materia orgánica de los cadáveres en materia mineral. b) Las levaduras son hongos de organización procariota que producen fermentación alcohólica. c) Los virus son capaces de parasitar a los seres vivos, pero existen también formas de vida libre. d) Las algas microscópicas, al igual que los mohos, son microorganismos autótrofos y fotosintéticos. e) Los estreptococos son bacterias esféricas que forman cadenas. 4. ¿Cuáles son los principales grupos de microorganismos eucariotas?. Indique las principales diferencias entre ellos. 5. ¿Qué grupos principales de microorganismos conoce?. ¿Cuáles son principales características? 6. Explique las diferencias estructurales y funcionales que conozca entre virus y bacterias. 7. Indique las principales diferencias entre las algas eucariotas microscópicas y los hongos filamentosos microscópicos. 8. Enumere y explique brevemente las diferencias más importantes entre Cianobacterias y Protozoos. 9. Indique los principales mecanismos de nutrición bacteriana. Cuestiones sobre virus 10. Explique el ciclo lítico de un bacteriófago 11. Indique los diferentes tipos de ácidos nucleicos que contienen los virus y explique esquemáticamente su modo de replicación. 12. Explique el ciclo vital de un retrovirus
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
2
13. Respecto a los virus y, utilizando dibujos esquemáticos: a) Describa el ciclo lítico de un bacteriófago. b) Describa un ciclo lisogénico. c) Indique las diferencias entre uno y otro. 14. En un laboratorio se obtuvo un bacteriófago que tiene la cápside del fago T2 y el ADN del fago T4. Con el bacteriófago obtenido en dicho laboratorio se infecta una bacteria. Conteste a las siguientes preguntas, razonando la respuesta: a) ¿Los fagos descendientes tendrán la cápside de T2 o de T4?. b) ¿Los fagos descendientes tendrán el ADN de T2 o de T4?. Cuestiones sobre Biotecnología y técnicas en microbiología 15. Explique una aplicación de la ingeniería genética a la industria farmacéutica, biomédica o alimentaria. 16. ¿Qué es la Biotecnología?. ¿Qué es un organismo transgénico?. Cite tres ejemplos de aplicación de la Biotecnología. 17. ¿Cuáles son los grupos de microorganismos de interés industrial?. ¿En qué condiciones pueden actuar?. Cite una aplicación industrial de estos microorganismos. 18. Explique el concepto de Biotecnología. Describa una aplicación de la biotecnología a un sector industrial alimentario. 19. Explique que es un antibiótico. ¿Qué tipo de organismos lo producen?. Describa brevemente un proceso tecnológico de producción de antibióticos. 20. Enumere las técnicas que conozca utilizadas para el estudio y la identificación de los microorganismos y explique una de ellas.
TEMA 7. INMUNOLOGÍA 1. MECANISMOS DE DEFENSA 2. EL SISTEMA INMUNITARIO. LOS ÓRGANOS LINFOIDES. LINFOCITOS y MACRÓFAGOS 3. ANTÍGENOS y ANTICUERPOS. REACCIÓN ANTÍGENO-ANTICUERPO 4. RESPUESTAS INMUNITARIAS
Respuesta inmune humoral y celular Respuesta inmune primaria y secundaria
5. INMUNIDAD. VACUNAS y SUEROS 6. ALTERACIONES DEL SISTEMA INMUNE
Alergia o Hipersensibilidad Anafilaxia Autoinmunidad Rechazo Cáncer Inmunodeficiencias: SIDA
Biología 2º Bachillerato Tema 7. Inmunología
1
1. MECANISMOS DE DEFENSA Los mecanismos de defensa son sistemas que han desarrollado los animales y el hombre frente a la invasión de microorganismos patógenos o sustancias extrañas. Pueden ser: ▪ Inespecíficos: impiden la entrada de cualquier gérmen o lo destruyen rápìdamente. La respuesta defensiva es la misma independientemente del tipo de gérmen. Existen tres barreras defensivas inespecíficas: piel y mucosas, microflora normal del organismo y la respuesta inflamatoria.
▪
Específicos: en este caso la respuesta defensiva es específica contra cada tipo de gérmen. Es llevada a cabo por el sistema inmunitario y se la conoce como respuesta inmunitaria.
2. EL SISTEMA INMUNITARIO. LOS ÓRGANOS LINFOIDES. LINFOCITOS y MACRÓFAGOS El Sistema inmunitario es el formado por todo el conjunto de órganos linfoides, que son los encargados de la formación, maduración y acumulación de los linfocitos. Los linfocitos se originan por diferenciación de células madre de la médula ósea y se transforman en uno u otro tipo según el lugar donde maduren. Así, los órganos linfoides se clasifican en: Órganos linfoides primarios: donde maduran los linfocitos. Son el timo, que produce linfocitos T y la médula ósea, que produce linfocitos B. Órganos linfoides secundarios: donde se acumulan los linfocitos que circulan por la sangre y por la linfa. Son los ganglios linfáticos, el bazo, amígdalas, apéndice, placas de Peyer y adenoides. El sistema inmunitario es el responsable de la respuesta inmunitaria, en la que participan dos tipos de células, los linfocitos y macrógafos y los anticuerpos.
Biología 2º Bachillerato Tema 7. Inmunología
2
Linfocitos: son un tipo de glóbulos blancos que presentan un gran núcleo redondeado. Reconocen a los gérmenes, gracias a la presencia de receptores de antígenos en sus membranas, y los atacan. Existen dos tipos: ▪ Linfocitos B: son los que fabrican los anticuerpos. Reconocen a los gérmenes extraños y se transforman en un tipo de células, denominadas células plasmáticas, que producen anticuerpos específicos contra el gérmen. Responsables de la respuesta inmune humoral.
▪
Linfocitos T: no producen anticuerpos. Responsables de la respuesta inmune celular. Existen diferentes tipos (Linfocitos CD4 o colaboradores, Linfocitos CD8 o citotóxicos, Linfocitos T supresores, Linfocitos T destructores), cada uno de los cuales interviene de forma distinta en la respuesta inmune, como veremos más adelante.
Macrófagos: células de gran tamaño que se desplazan con movimiento ameboide entre las células de los tejidos fagocitando a los microorganismos. Además, alertan al sistema inmunitario de la presencia de gérmenes o sustancias extrañas, al exponer moléculas de los gérmenes fagocitados o fragmentos de éstas en su superficie, presentando así el antígeno a los linfocitos para su reconocimiento.
La respuesta inmune es la respuesta específica que lleva a cabo el sistema inmunológico ante la presencia de gérmenes o moléculas extrañas. Puede ser de dos tipos: ▪ Respuesta inmune HUMORAL (mediada por anticuerpos): los linfocitos B fabrican anticuerpos específicos contra el agente infeccioso. ▪ Respuesta inmune CELULAR (mediada por células): los linfocitos T y los macrófagos destruyen al agente infeccioso.
Biología 2º Bachillerato Tema 7. Inmunología
3
3. ANTÍGENOS Y ANTICUERPOS. REACCIÓN ANTÍGENO-ANTICUERPO. Antígeno: toda sustancia extraña capaz de inducir en el organismo una respuesta inmunitaria, que provoca la formación de anticuerpos para destruirlos. En resumen los antígenos, son sustancias con las siguientes características: Son exógenas, es decir, extraños al organismo. Son de naturaleza química muy variada (proteínas, polisacáridos, lipoproteínas,...). Se localizan en la superficie de un agente patógeno o son producidas y liberadas por este. Son inmunológicas, es decir, capaces de inducir la formación de anticuerpos. Presentan una zona, denominada determinante antigénico o epítopo, que se une de forma específica al anticuerpo. Los epítopos son los responsables de la especificidad del antígeno por el anticuerpo. Cada antígeno puede poseer varios epítopos (antígenos polivalentes), que provocan la formación de anticuerpos distintos.
Anticuerpos: son las sustancias que fabrica el sistema inmunológico ante la presencia de un antígeno. Tienen naturaleza de glucoproteína. Están formados por cuatro cadenas polipeptídicas, dos ligeras (L) y dos pesadas (H). En cada anticuerpo existe una región variable que es la que se une al antígeno, y otra región constante, común a muchos anticuerpos.
Reacción antígeno-anticuerpo Es la unión del anticuerpo con el antígeno. Se produce mediante enlaces débiles (nunca covalentes). Es una unión tremendamente específica, cada anticuerpo es capaz de reconocer entre miles de antígenos, aquel que le es complementario. Existen cuatro formas de reacción antígeno-anticuerpo: ▪ Neutralización: el anticuerpo al unirse al antígeno lo anula y pierde su capacidad infectiva. ▪ Aglutinación: los anticuerpos se unen a los antígenos presentes en la superficie de gérmenes y forman agregados que precipitan fácilmente. ▪ Precipitación: parecido a lo anterior, pero en este caso se trata de antígenos solubles en agua (no unidos a la superficie bacteriana) ▪ Opsonización: los anticuerpo se unen a la superficie de los gérmenes (gérmenes opsonizados) y se facilita que sean fagocitados.
Biología 2º Bachillerato Tema 7. Inmunología
4
4. RESPUESTAS INMUNITARIAS Respuesta humoral También se conoce como “inmunidad mediada por anticuerpos”, ya que básicamente consiste en la síntesis de anticuerpos por los linfocitos B. Cuando un antígeno penetra en el organismo, acaba encontrando un linfocito B que posee el anticuerpo específico capaz de reaccionar con él. La unión del linfocito al antígeno estimula la división de los linfocitos y su diferenciación en dos tipos de células: Células plasmáticas: se consideran linfocitos B maduros y poseen un extenso RER, donde fabrican y exportan gran cantidad de anticuerpos (más de 10 millones de moléculas por hora). Estas células no salen de los órganos linfoides, sino que lo hacen los anticuerpos y viajan por la sangre hasta la zona infectada. Células de memoria: algunos linfocitos B se convierten en células de memoria, que permanecen en la sangre fabricando anticuerpos específicos, como si guardaran el recuerdo del antígeno, y ante una segunda infección se multiplican generando células plasmáticas que producen grandes cantidades de anticuerpos que acaban más rápidamente con el antígeno extraño. Respuesta celular También se conoce como “inmunidad mediada por células”, y se basa en la actividad de los linfocitos T y los macrófagos. Cuando un antígeno invade el organismo, los macrófagos lo fagocitan y digieren en pequeños péptidos. Los macrófagos fabrican el complejo proteíco MCH (complejo principal de histocompatibilidad) que reconoce los fragmentos del antígeno y los transporta hasta la superficie del macrófago, permaneciendo allí hasta que son reconocidos por un linfocito T. Al reconocerlos, el linfocito T se activa y se divide, diferenciándose en distintos tipos de linfocitos T que salen de los nódulos linfáticos y se dirigen a la zona afectada. Los diferentes tipos de linfocitos T son los siguientes: Linfocitos T CD4 o Cooperadores: colaboran con los linfocitos B en el reconocimiento de antígenos específicos. Linfocitos T CD8 o Citotóxicos: se unen a células que poseen antígenos extraños en su superficie y las destruyen. Linfocitos T Supresores: inducen el cese de la actividad de los linfocitos B, y por lo tanto, se interrumpe la producción de anticuerpos. Linfocitos T memoria: son linfocitos T activados que permanecen en el tejido linfático como células de memoria y que continúan dividiéndose durante años.
Biología 2º Bachillerato Tema 7. Inmunología
5
Respuestas inmune primaria y secundaria Respuesta inmune primaria: es la respuesta inmunitaria tras un primer o con el antígeno. El sistema inmune tarda tiempo en identificar el antígeno (periodo de latencia) y posteriormente empieza a fabricar anticuerpos. Respuesta inmune secundaria: es la respuesta inmunitaria ante un segundo o con el antígeno. Como el sistema inmunológico lo ha memorizado, la respuesta es más rápida, se tarda menos en fabricar anticuerpos y se producen más rápidamente. A esta capacidad de respuesta inmunológica a un antígeno, más rápida y eficaz, tras un primer o con él se la conoce como memoria inmunológica. Las vacunas aprovechan esta propiedad, al estimular al organismo a que produzca anticuerpos y células memoria. 5. INMUNIDAD. VACUNAS y SUEROS Inmunidad es la capacidad de un individuo para ser invulnerable a una enfermedad infecciosa. Se puede adquirir de forma natural, al haber contraído antes la enfermedad o durante el desarrollo embrionario y la lactancia (a través de la placenta y de la leche materna una mujer transmite anticuerpos al hijo) quedando protegido el recién nacido durante algunos meses. Otra manera de adquirir inmunidad es de forma artificial mediante: Sueros o antisueros: soluciones que contienen anticuerpos específicos (inmonoglobulinas) contra determinada enfermedad. Sus efectos son inmediatos, pero no duraderos (hasta que el organismo consuma los anticuerpos inyectados) Vacunas: soluciones que contienen gérmenes muertos o debilitados. La vacunación es una medida preventiva que persigue que el propio organismo fabrique anticuerpos y células memoria contra una determinada enfermedad, de manera que ante una posible infección la respuesta inmunitaria sea rápida y eficaz.
Biología 2º Bachillerato Tema 7. Inmunología
6
6. ALTERACIONES DEL SISTEMA INMUNE Alergia o hipersensibilidad: es una reacción inmunitaria perjudicial para el organismo, ya que el sistema defensivo reacciona de forma excesiva ante sustancias extrañas inocuas o poco peligrosas. En los procesos alérgicos a los antígenos se les denomina alérgenos, se producen un tipo de anticuerpos especiales (IgE) que se unen a la superficie de unas células denominadas mastocitos. Cuando se produce un segundo o con el alérgeno, los mastocitos segregan histamina y otras sustancias que dilatan y aumentan la permebalidad de los capilares sanguíneos provocando un enrojecimiento e hinchazón de la zona o estimulan la mucosidad. De ahí que para tratar ciertas alergias se empleen antihistamínicos.
Anafilaxia: es un proceso alérgico que afecta a todo el organismo debido a que el alérgeno se introduce en el sistema sanguíneo, llegando incluso a producir la muerte. Ejemplos claros son las personas sensibles a la penicilina o a la picadura de abejas. Autoinmunidad: es un proceso en el que el propio sistema inmunológico ataca determinados órganos o tejidos del cuerpo. Provoca una serie de infermedades denominadas genéricamente enfermedades autoinmunes (anemia perniciosa, diabetes mellitus insulinodependiente, artritis reumatoide, esclerosis múltiple,...).
Rechazo: casos en que el sistema inmunitario reconoce como extraño un órgano o tejido implantado y reacciona destruyéndolo. Esto es debido a que todos nuestros tejidos presentan en la superficie de las células sustancias que actúan como antígenos (antígenos de histocompatibilidad o HLA) que son diferentes en cada uno de nosotros. Por eso a la hora de realizar transplantes hay que hacer un estudio previo de los tejidos del donante y receptor (Test de histocompatibilidad) para conocer las probabilidades de éxito.
Biología 2º Bachillerato Tema 7. Inmunología
7
Cáncer: enfermedad que consiste en la aparición tumores malignos, formados por células cancerígenas, que se dividen sin control y destruyen los tejidos sanos. Cada tumor es una masa de células cancerígenas. Si algunas de esas células se desprenden del tumor y pasan al torrente circulatorio invaden otras zonas, es lo que denominamos metástasis, provocando que la enfermedad se extienda a otras zonas del cuerpo. El sistema inmunitario nos protege de la aparición de tumores, ya que las células cancerígenas presentan antígenos especiales en su superficie que pueden ser detectados como extraños y ser así atacadas por los linfocitos, de ahí que una de las terapias más modernas en la lucha contra el cáncer sea la inmunoterapia, que se basa en potenciar las propias defensas del paciente. Inmunodeficiencia: enfermedad que afecta al sistema inmunitario debilitándolo. Como ejemplo significativo está el SIDA. SIDA (Síndrome de Inmunodeficiencia Adquirida): enfermedad producida por un virus (VIH) que ataca fundamentalmente a los linfocitos CD4 (un tipo de linfocitos T). Algunos conceptos importantes en la enfermedad son: Seropositivo: persona que ha desarrollado anticuerpos anti VIH contra la enfermedad, por haber sido infectada. Puede transmitir la enfermedad. Portador del virus VIH: persona con el virus VIH en su organismo, pero que no ha desarrollado la enfermedad. Puede transmitir la enfermedad. Enfermo o caso de SIDA: persona que sufre la enfermedad y por lo tanto la puede transmitir. Microorganismos oportunistas: gérmenes presentes en el organismo o en el ambiente que aprovechan la oportunidad de que el sistema inmunitario está debilitado para infectar y dañar órganos, que en condiciones normales no podrían. Provocan infecciones oportunistas que acaban con la vida del enfermo, como meningitis, tuberculosis, candidiasis, micosis cutáneas, herpes,... Carga viral: cantidad de virus VIH que circula por la sangre. Se utiliza para controlar la enfermedad. AZT: medicamento para tratar el SIDA que impide su multiplicación al inhibir la transcriptasa inversa. Vías de transmisión: vía sanguínea y sexual, debido a relaciones sexuales, compartir jeringuillas u objetos cortantes infectados, transmisión madre-hijo. CICLO VIH
El VIH comienza su infección de una célula huésped susceptible mediante su unión a los receptores CD4 de la célula huésped. Los receptores CD4 están presentes en la superficie de muchos linfocitos, células que constituyen una parte crítica del sistema inmunológico del organismo. Algunos datos recientes indican que para que el VIH entre en la célula es necesario un correceptor. Este conocimiento del correceptor del VIH y los progresos llevados a cabo en los mecanismos de fusión del VIH con la célula han abierto nuevas posibilidades para el desarrollo de fármacos antivirales. En la actualidad se están diseñando diferentes fármacos nuevos que pretenden prevenir la infección mediante el bloqueo de la fusión del VIH con su célula huésped. Después de la fusión del virus con la célula huésped, el VIH entra en la célula. El material genético del virus, que está formado por ARN, se libera y sufre una transcripción inversa hasta ADN. Para catalizar esta conversión del virus del ARN a ADN es preciso que entre en funcionamiento una enzima del VIH, denominada transcriptasa inversa. Los inhibidores de la transcriptasa inversa, como AZT, han sido los primeros medicamentos anti-VIH y todavía desempeñan una función fundamental en el tratamiento de los pacientes VIH+. Los inhibidores de la transcriptasa inversa se dividen, en función de su estructura y el mecanismo de inhibición de la enzima, en 2 clases: inhibidores análogos nucleósidos e inhibidores análogos no nucleósidos de la transcriptasa inversa. Después del cambio del material genético del VIH en ADN, el ADN viral entra en el núcleo de la célula huésped donde puede integrarse en su material genético. Este proceso está catalizado por la enzima integrasa; actualmente se están estudiando los inhibidores de la integrasa como una nueva forma de bloquear la replicación del VIH. Después de que el ADN viral se haya integrado en el material genético del huésped, es posible que el VIH pueda persistir en un estado latente durante muchos años. Esta capacidad del VIH de permanecer de forma latente en ciertas células constituye la principal barrera para la erradicación o curación del VIH. Por dicho motivo, fundamentado en nuestros conocimientos, los pacientes deben seguir recibiendo tratamiento antiviral durante toda la vida.
8
Biología 2º Bachillerato Tema 7. Inmunología
La activación de las células huésped da la lugar a la transcripción del ADN viral en ARN mensajero (ARNm), que posteriormente se traduce en proteínas virales. El nuevo ARN viral forma el material genético de la siguiente generación de virus. El ARN viral y las proteínas virales se agrupan y forman en la membrana celular un virus nuevo. Dentro de las proteínas virales se encuentra la proteasa del VIH, que es necesaria para procesar otras proteínas del VIH hasta sus formas funcionales. Los inhibidores de la proteasa, uno de los tipos más potentes de fármacos antivirales, actúan bloqueando esta etapa crítica de la maduración. Después de su reunión en la superficie celular, el virus sale de la célula mediante gemación y se libera para infectar otra célula. A menos que el tratamiento interrumpa el ciclo de vida del VIH, esta infección se disemina por todo el organismo y origina la destrucción del sistema inmunológico. Los fármacos antivirales actuales, como los inhibidores de la transcriptasa inversa y los inhibidores de la proteasa, permiten controlar la infección. No obstante, deben conseguirse todavía muchos objetivos antes de poder pensar que la epidemia del SIDA está controlada. Un objetivo importante e inmediato es el diseño de nuevos fármacos más potentes, que sean más fáciles de tomar y que originen un número menor de efectos secundarios. Inhibidores de la transcriptasa inversa actualmente disponibles: zidovudina (AZT, ZDV); didanosina (ddI); zalcitabina (ddC); estavudina (d4T); lamivudina (3TC); abacavir (ABC) Inhibidores no nucleósidos de la transcriptasa inversa: nevirapina; efavirenz Inhibidores de la proteasa: indinavir; ritonavir; saquinavir; nelfinavir ESQUEMA CICLO VIH y TIPOS DE FÁRMACOS QUE INTERRUMPEN EL CICLO
Fármacos que inhiben la proteasa (indinavir; ritonavir; saquinavir; nelfiravir)
Fármacos que impiden la entrada del virus
Fármacos que inhiben la transcripción inversa (AZT;ddI;ddC;d4T;3ct; nevirapina;efavirenz...)
INMUNZACIÓN ACTIVA. VACUNACIÓN La inmunización activa se basa en la estimulación del propio sistema inmunológico, mediante el suministro de los antígenos necesarios para que el organismo pueda fabricar por sí mismo los anticuerpos contra ellos. La vacunación es una forma de inmunización activa, ya que estimula las defensas inmunitarias frente a determinados agentes patógenos o sustancias dañinas, sin desarrollar la enfermedad. La persona vacunada fabrica linfocitos de memoria que permiten producir una respuesta inmunitaria secundaria más rápida y mucho más intensa que la respuesta primaria.
Para que una vacuna pueda ser suministrada debe cumplir dos requisitos: Capacidad inmunogénica. Debe ser capaz de provocar una respuesta inmunitaria eficaz. Ser segura y no producir efectos secundarios.
Tipos de vacunas a) Atenuadas. Contienen microorganismos vivos, pero debilitados, que se reproducen en el individuo vacunado y originan una infección muy limitada. Los microorganismos atenuados se obtienen a partir de cepas virulentas que se cultivan en determinadas condiciones (como altas temperaturas) hasta que disminuye su virulencia. Son ejemplos la vacuna contra la poliomielitis, el sarampión y la rubéola. b) Inactivadas. Contienen microorganismos muertos, por lo que no se reproducen en el organismo y es preciso suministrar una dosis más alta para que la vacuna contenga los antígenos suficientes. Con frecuencia se necesitan dosis de recuerdo para estimular a los linfocitos B de memoria. Son ejemplos la vacuna contra la rabia, tos ferina y difteria. c) Acelulares. Cuando no contienen células completas, solo partes o productos de los microorganismos. Pueden ser:
Toxoides: si contienen toxinas alteradas por calor o agentes químicos, que conservan su capacidad inmunogénica, y se emplean en la inmunización de gérmenes que fabrican potentes toxinas, como por ejemplo la vacuna del tétanos.
Antígenos aislados: contienen solo antígenos del microorganismo, por lo que no provocan reacciones adversas. Se fabrican gracias a las técnicas de biotecnología, como la vacuna de la hepatitis B, meningitis meningocócica, virus del papiloma humano o la vacuna contra la malaria.
Biología 2º Bachillerato
Tema 7. Inmunología
1
ACTIVIDADES TEMA 7. INMUNOLOGÍA CUESTIONES DE SELECTIVIDAD Cuestiones generales sobre inmunidad, respuesta inmune y linfocitos 1. Defina los siguientes conceptos: inmunidad, sueroterapia y vacunación. 2. ¿En qué consisten las respuestas inmune primaria y secundaria?. 3. a. b. c. d.
Diferencia los siguientes términos: Anticuerpo/Antígeno Cadena ligera/Cadena pesada Linfocito B/Linfocito T Célula plasmática/Célula de memoria
4. a) b) c)
Responde : Explica que es el “sistema inmunitario” ¿Qué son las “defensas específicas”?. Indique cuáles son las células específicas principales de dicho sistema.
5. Enumere y explique las diferencias más importantes entre: inmunización activa (vacunación) y alergia. 6. Indique si la siguiente afirmación es cierta o falsa, razonando la respuesta: Los linfocitos T son responsables de la respuesta inmune celular y colaboran en la humoral. 7. Definir los conceptos: determinante antigénico y linfocito B. 8. a) b) c) d)
Defina los conceptos siguientes: Macráfagos Antígenos Linfocitos T Alergia
9. Describa las características e importancia de la vacunación, así como los distintos tipos de vacunas.
Cuestiones sobre antígenos y anticuerpos 10. Definición de antígeno y anticuerpo. Señale algún tipo de molécula con propiedades antigénicas. 11. Ciertos organismos producen anticuerpos en respuesta a la presencia de un antígeno. Al respecto: a) ¿Qué tipo de biomoléculas son los anticuerpos?. b) ¿Qué tipo de biomoléculas son los antígenos?. c) ¿Qué características principales tiene la reacción antígeno-anticuerpo?. d) ¿Qué células del organismo producen anticuerpos?. 12. Describa un proceso de fagocitosis mediada por anticuerpos.
Biología 2º Bachillerato
Tema 7. Inmunología
2
Cuestiones sobre el VIH y el SIDA 13. Con respecto al SIDA: a) Relacione los conceptos siguientes, explicando brevemente el porqué de su elección: 1) 2) 3) 4) 5) 6)
VIH SIDA Seropositivo Caso de SIDA AZT Portador del virus del SIDA
a) b) c) d) e) f)
Enfermo Virus Enfermedad Medicamento Persona con anticuerpos VIH en sangre Persona con el virus VIH en sus células
b) Resuma las etapas del ciclo de infección de un retrovirus, como el VIH. 14. Explique el ciclo vital de un retrovirus. 15. Con respecto al SIDA : a) ¿Cómo se desarrolla el SIDA a partir de la infección de un organismo por VIH?. b) Enumere las vías de transmisión del VIH. c) Distinga un seropositivo de un portador del virus del SIDA. 16. Contesta: a) ¿Qué significan las siglas SIDA y VIH?. b) ¿Cuáles son las vías de transmisión del VIH?. c) ¿Qué relación tienen los linfocitos T y los macrófagos con el sistema inmune?. 17. El virus VIH del SIDA infecta a los linfocitos T4, provocando su destrucción con el tiempo. Al respecto: a) ¿Cuál es la función principal de los linfocitos T4?. b) ¿Qué consecuencias generales ocasiona la destrucción de estos linfocitos T4 por el virus?.
2º BACHILLERATO
IES Fuentesnuevas
BLOQUE I LA BASE MOLECULAR Y FISICO-QUÍMICA DE LA VIDA
TEMA 1. LA BASE FÍSICO QUÍMICA DE LA VIDA
Parte 1. La Materia de los seres vivos Parte 2. Glúcidos y Lípidos Parte 3. Proteínas y ácidos nucleicos
TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA Parte 1. LA MATERIA DE LOS SERES VIVOS. LOS COMPUESTOS INORGÁNICOS 1. LAS CARACTERÍSTICAS DE LOS SERES VIVOS. 1.1. 1.2. 2.
NIVELES DE ORGANIZACIÓN DE LOS SERES VIVOS COMPOSICIÓN QUÍMICA DE LOS SERES VIVOS BIOELEMENTOS
Propiedades del carbono Clasificación de los bioelementos Funciones de los bioelementos 3.
LAS BIOMOLÉCULAS
4.
EL AGUA
Estructura química Propiedades físico-químicas Funciones biológicas 5.
LAS SALES MINERALES
Funciones biológicas de las sales minerales
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
1
1. CARACTERÍSTICAS DE LOS SERES VIVOS La vida se define sobre una serie de características comunes a todos los seres vivos: ■ Todos los seres vivos están formados por células y todas las células, a su vez, están compuestas por los mismos tipos de moléculas, moléculas que intervienen en la construcción de los distintos componentes celulares, en las reacciones metabólicas o en la conservación y transmisión de la información genética. ■ En todos los organismos existen distintos niveles de organización, de forma que los organismos están constituidos por células y éstas pueden presentar distintas estructuras y orgánulos. ■ Nutrición: los seres vivos tienen la capacidad de crecer a expensas de los nutrientes que toman del medio externo. Dichos nutrientes son transformados, a través de una serie de reacciones metabólicas, en energía (catabolismo) y compuestos orgánicos (anabolismo o biosíntesis). ■ Relación con el medio ambiente y con otros organismos por medio de: La recepción e intercambio de señales (incluso dentro del propio organismo existen moléculas, como las hormonas, que llevan distintos tipos de señales de un órgano a otro, y de una célula a otra dentro de un mismo tejido). La capacidad de elaborar respuestas a distintos tipos de estímulos tanto internos como externos. ■ Las células y los organismos tienen además la capacidad de reproducirse y originar descendientes, que pueden ser genéticamente idénticos al individuo parental (reproducción asexual) u originarse por el intercambio de genes de distintos sexo (reproducción sexual). Estas tres últimas características (nutrición, relación y reproducción) son las funciones típicas de los seres vivos, y se conocen como funciones vitales. Hasta hace algunos años, a los seres vivos se les caracterizaba a través de sus funciones vitales, pero hoy en día, de acuerdo con la Teoría de Sistemas, también los podemos describir como un sistema ordenado de moléculas, ya que en definitiva los fenómenos vitales son reacciones reguladas por las biomoléculas presentes en los seres vivos. Todos los organismos se caracterizan por poseer, entre otras, dos biomoléculas: ácidos nucleicos y proteínas. Por ello, una definición moderna de ser vivo es aquella que considera a los seres vivos como cuerpos naturales que poseen ácidos nucleicos y proteínas y que son capaces de sintetizar dichas moléculas por sí mismos.
Las formas acelulares Pese a todas las características que acabamos de señalar para definir a un ser vivo, existen algunas formas de vida que se encuentran en la frontera entre lo vivo y lo inerte, son las formas acelulares de vida: virus, tiroides y priones. Los virus son complejos moleculares de proteínas y ácidos nucleicos que penetran en las células que parasitan y donde se multiplican con ayuda del material de la célula huésped, por lo que son parásitos obligados. Fuera de la célula son totalmente inertes y algunos han podido ser cristalizados. Gozan por tanto de algunas características de los seres vivos, como la capacidad de reproducción y mutación, por lo que no se pueden considerar seres inertes, pero no son capaces por sí mismos de fabricar sus propias proteínas y ácidos nucleicos y para ellos se ven obligados a parasitar una célula. Los viroides son moléculas de ARNm (ARN monocatenario circular) que carecen de envolturas externas. Son causantes de enfermedades en las algunas plantas (tomates, tubérculos,…) ya que interfieren en la regulación de los genes. Los priones son proteínas causantes de enfermedades neurodegenerativas (scrapie, enfermedad de las vacas locas,…). Las proteínas patógenas provocan cambios conformaciones en las proteínas normales.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
2
La dificultad para diferenciar la materia viva de la inerte es lógica su consideramos que los seres vivos se originaran a partir de la materia inerte, por un proceso gradual que fue la evolución biológica. Ahora bien, estas tres formas acelulares (virus, tiroides y priones), no son seres vivos primitivos o formas de transición entre la materia inerte y la materia viva, ya que son parásitos y necesitan de células para sobrevivir. 1.1. NIVELES DE ORGANIZACIÓN EN LOS SERES VIVOS Si algo caracteriza a los seres vivos y los diferencia de la materia inerte es su complejidad, su elevada organización y su diversidad. Estas propiedades están presentes en todos sus niveles de organización y son consecuencia de una característica intrínseca a la materia y que consiste en que bajo ciertas condiciones (consumiendo energía) evoluciona hacia formas más complejas. El siguiente cuadro muestra los niveles de organización en los seres vivos, desde lo más simple a lo más complejo, diferenciando los niveles abióticos (sin vida) y los bióticos (con vida).
En concreto, en lo que respecta a los niveles molecular y macromolecular, la mayoría de las moléculas que forman parte de los seres vivos son orgánicas, o sea, moléculas formadas por cadenas de átomos de carbono que adquieren una gran longitud y complejidad. Para comprender la enorme diversidad de compuestos orgánicos que se podrían formar, basta señalar la cantidad de palabras que se podrían escribir (no solo las que existen) en todas las lenguas con alfabeto latino. No obstante, esta gran variedad de compuestos orgánicos parte de muy pocos elementos estructurales sencillos que, combinados, constituyen las complejas macromoléculas. De forma que con unas pocas clases diferentes de moléculas sencillas (moléculas sillares o monómeros) se pueden obtener una gran diversidad de macromoléculas. Así, por ejemplo, con solo 20 aminoácidos combinados en numerosas secuencias distintas, se pueden originar miles de proteínas diferentes. Las moléculas sillares o monómeros son idénticos en todos los organismos. El hecho de que todos los seres vivos empleen estas mismas moléculas, indica que proceden de un antepasado común, origen de la gran biodiversidad actual. Aunque las “casas” sean diferentes, todos los organismos están hechos de los mismos “ladrillos”.
http://www.educa.madrid.org/web/ies.rayuela.mostoles/deptos/dbiogeo/recursos/Apuntes/ApuntesBioBach2/Tablas/TabCompQimCelulares.png
http://www.educa.madrid.org/web/ies.rayuela.mostoles/deptos/dbiogeo/recursos/Apuntes/ApuntesBioBach2/Tablas/TabCompQimCelulares.png05/11/2007 19:19:59
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
3
1.2. COMPOSICIÓN QUÍMICA DE LOS SERES VIVOS Como hemos visto, todos los seres vivos estamos formados por los mismos tipos de moléculas, que por este motivo, se denominan biomoléculas. Estas biomoléculas están formadas a su vez por una serie de elementos químicos o bioelementos. Entre las moléculas inorgánicas presentes en los seres vivos se encuentran principalmente el agua y algunas sales minerales. El agua es la molécula más abundante y es esencial para que tengan lugar los procesos bioquímicos necesarios para la actividad vital. En cuanto a las sales minerales, pueden encontrarse tanto en forma insoluble (como en las conchas o los caparazones de muchos animales), como soluble (participando en procesos enzimáticos o fisiológicos). Los constituyentes orgánicos de los seres vivos se pueden clasificar en cuatro grandes grupos o principios inmediatos: glúcidos, lípidos, proteínas y ácidos nucleicos (ADN y ARN). Estos últimos, los ácidos nucleicos, contienen toda la información genética de la célula y aseguran la herencia de ésta y la traducción del “código genético” en las proteínas necesarias para las funciones vitales. La combinación de los cuatro principios inmediatos orgánicos da lugar a la gran variedad de estructuras celulares, que permiten la nutrición, el metabolismo, la percepción y la respuesta a estímulos externos y la división y la reproducción de las células y los organismos. La vida no solo es la suma de todas estas moléculas independientes, sino que es el resultado de una interacción compleja entre dichas moléculas, que origina una estructura y unas funciones que definimos como vitales. Así por ejemplo, una hoja de papel esta formada por celulosa, pero no está viva; sin embargo, las células vegetales son formas vivas que presentan celulosa como uno de los constituyentes de su pared celular.
2. BIOELEMENTOS La materia que forma parte de los seres vivos está compuesta por moléculas, también denominadas biomoléculas, formadas a su vez por la unión de átomos de ciertos elementos químicos. Estos elementos presentes en las biomoléculas reciben el nombre de bioelementos o elementos biogénicos, de los que existen unos 70 diferentes. Todos los bioelementos se encuentran incluidos en la tabla periódica, es decir, no hay elementos exclusivos de los seres vivos. Sin embargo, los bioelementos mayoritarios no coinciden (salvo el oxígeno) con los elementos más abundantes de la corteza terrestre, que son el O, el Si y el Al. Los bioelementos más abundantes en los seres vivos son el C, el H, el O, el N, el P y el S. Estos elementos químicos fueron seleccionados por las propiedades que presentan: Los seis elementos tienen capas electrónicas externas incompletas, lo que les permite formar fácilmente enlaces covalentes y así originar las biomoléculas constituyentes de las estructuras biológicas. Poseen un número atómico bajo, por lo que los electrones compartidos en la formación de los enlaces covalentes se hallan próximos al núcleo y las moléculas originadas son estables. Dado que el oxígeno y el nitrógeno son elementos electronegativos, muchas biomoléculas son polares y, por ello, solubles en agua, requisito imprescindible para que tengan lugar las reacciones biológicas fundamentales de la actividad vital. Se pueden incorporar fácilmente a los seres vivos desde el medio externo, ya que se encuentran en moléculas (CO2, H2O, nitratos, sulfatos, fosfatos) que se pueden captar de manera sencilla. Esto asegura el intercambio constante de materia entre los organismos vivos y su ambiente.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
4
Propiedades del carbono Entre los bioelementos, el carbono desempeña un papel fundamental. El carbono se localiza en el grupo 14 del sistema periódico y tiene cuatro orbitales con electrones desapareados que se disponen en una estructura tetraédrica (configuración tetraédrica). Los electrones desapareados del carbono le permiten formar enlaces covalentes (simples, dobles y triples) con otros átomos de carbono, dando lugar a la formación de cadenas carbonadas estables de tamaño y forma variables (lineales, ramificadas y anilladas). Estas cadenas carbonadas actúan como el esqueleto molecular de las biomoléculas, permitiéndoles formar estructuras espaciales complejas y estables. Por otra parte, los átomos de carbono pueden formar enlaces covalentes con otros átomos distintos (hidrógeno, oxígeno, nitrógeno y azufre), dando lugar a diferentes grupos funcionales, que confieren propiedades concretas a las moléculas que los poseen. CLASIFICACIÓN DE LOS BIOELEMENTOS De los 70 bioelementos descritos, 25 de ellos están presentes en todos los seres vivos y el resto solo aparece en determinados grupos. Según la proporción en que se encuentran en la materia viva se clasifican en: Bioelementos primarios o plásticos. Son el grupo formado por el carbono (C), hidrógeno (H), oxígeno (O), nitrógeno (N), fósforo (P) y azufre (S). Constituyen, aproximadamente el 99% del total de la materia viva y son los componentes fundamentales de las biomoléculas. Bioelementos secundarios. Forman parte de todos los seres vivos, aunque menor proporción que los anteriores (a excepción del calcio). Se incluyen en este grupo el sodio (Na), potasio (K), calcio (Ca), magnesio (Mg) y el cloro (Cl). Oligoelementos o elementos traza. Se encuentran en proporciones inferiores al 0,1 %, pero son elementos imprescindibles ya que desempeñan funciones especiales en diferentes procesos bioquímicos y fisiológicos. Algunos oligoelementos, como el hierro (Fe), el cobre (Cu), el cinc (Zn), el manganeso (Mn), el yodo (I), el níquel (Ni) y el cobalto (Co), aparecen en la mayoría de los seres vivos y otros, como el silicio (Si), el fluor (F), el cromo (Cr), el litio (Li), el boro (B), el molibdeno (Mo) y el aluminio (Al), solo están presentes en grupos concretos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
FUNCIONES DE LOS BIOELEMENTOS PRIMARIOS y SECUNDARIOS
5
Biología 2º Bachillerato. Tema 1. Bioelementos OLIGOELEMENTOS ESENCIALES El ser humano no puede producir oligoelementos pero los necesita para vivir y preservar su salud. Son sustancias que intervienen en las funciones respiratoria, digestiva, neurovegetativa y muscular, como reguladores y equilibrantes. Todos ellos deben estar presentes en nuestra alimentación porque, si no ingerimos las pequeñas pero importantes dosis de ellos que precisa nuestro organismo, podemos enfermar. HIERRO: Los pulmones no podrían captar el oxígeno y transportarlo a todas las células sin la presencia del hierro. La carencia de ese oligoelemento puede frenar la producción de glóbulos rojos, ocasionar fatiga y aumentar la sensibilidad a diversas afecciones respiratorias. La carne, el pescado, el hígado, los riñones, el cacao, las espinacas, las habichuelas, el perejil, los mejillones, las habas, la soja, los frutos secos y el pan son alimentos ricos en hierro. COBRE: Estimula el sistema inmunitario. Podemos obtenerlo en los vegetales verdes, el pescado, los guisantes, las entejas, el hígado, los moluscos y los crustáceos. CROMO: Potencia la acción de la insulina y favorece la entrada de glucosa a las células. Su contenido en los órganos del cuerpo decrece con la edad. Los berros, las algas, las carnes magras, las hortalizas, las aceitunas y los cítricos (naranjas, limones, toronjas, etc.), el hígado y los riñones son excelentes proveedores de cromo. YODO: Forma parte de las hormonas tiroideas, que influyen fundamentalmente en el crecimiento y maduración del organismo, y afecta sobre todo a la piel, el pelo, las uñas, los dientes y los huesos. Las algas, los pescados, los mariscos, lo cereales, la carne magra, los huevos, la leche, el ajo, la cebolla, el limón, la naranja, la piña, las hortalizas de hoja verde y los frutos secos con ricos en yodo. MANGANESO: Es necesario para los huesos y juega un papel importante en las funciones reproductoras. Se puede encontrar en el pan integral, las hortalizas, la carne, la leche y sus derivados, los crustáceos y los frutos secos. SELENIO: Es un potentísimo antioxidante. Además, garantiza el buen funcionamiento de los músculos, protege nuestro sistema cardiovascular y puede evitar la aparición de cataratas. Está presente en las carnes de ave, vacuno y cerdo, en los cereales integrales, la levadura de cerveza, el germen de trigo, el ajo, el limón, la cebolla, las setas, el salmón, las verduras y los mariscos. ZINC: Interviene en el funcionamiento de ciertas hormonas y desempeña un importante papel en el crecimiento, la producción de insulina, las funciones psicológicas, la formación de espermatozoides y la defensa del sistema inmunitario. Se halla en alimentos como las ostras, el hígado de pato, la leche, el pan integral, las carnes de vacuno y cerdo, las legumbres, los pescados, las verduras de hoja verde y las nueces COBALTO: Es un componente esencial de la vitamina B12. Contribuye a reducir la presión arterial y a dilatar los vasos sanguíneos, y favorece la fijación de la glucosa en los tejidos. Podemos encontrarlo en las ostras, las legumbres, los cereales integrales, la cáscara de arroz, el ajo, la cebolla, el sésamo y el ginseng. FLÚOR: Previene la aparición de caries al mantener el esmalte de los dientes en buenas condiciones, ayuda a frenar la aparición de osteoporosis y tiene incidencia en el crecimiento. E pescado, los mariscos, el te, las verduras, las hortalizas, los cereales integrales, las legumbres y la cebolla son ricos en flúor. LITIO: Actúa sobre el sistema nervioso y es útil en las afecciones cardiacas. Se encuentra en los cereales integrales, las legumbres, a patata, el tomate, el nabo, el pimiento, las fresas, las frambuesas y la soja germinada. NÍQUEL: Potencia el crecimiento y es recomendable para combatir anemias, y enfermedades infecciosas, y en general, para estados carenciales y convalecencias. Los moluscos, la levadura de cerveza, el arroz integral y las legumbres son las principales suministradores de níquel. SILICIO: Aumenta la elasticidad y resistencia de los huesos, previene la arteriosclerosis, retrasa el envejecimiento y equilibra el sistema nervioso. Se encuentra en los cereales integrales, la levadura de cerveza, el maíz, la calabaza, la sandía y la cola de caballo.
Principales Elementos Químicos de los Seres Vivos Nombre Símbolo
N.A. Valencia P.A.
Electneg
% At
% Peso
Formas químicas
Función
Hidrógeno H
1 2
-1 +1
2.1
63
10
C-H
H+ H2 O
Protón Agua
Agua Iones ácidos H+ Compuestos orgánicos: Saturación de los grupos orgánicos
Carbono C
6 12
-4 +4
2.5
10
12
C-C C=C
CO3= CO3H-
Carbonato Bicarbonato
Compuestos orgánicos : Esqueleto de las moléculas orgánicas Carbonatos
Nitrógeno N
7 14
-3 +5
3.0
1.5
3.3 C-NH2 C=N-
Amino
Oxigeno O
8 16
-2
3.5
25
63
Alcohol COOH Aldehido.Cetona H2O
Azufre S
16 32
-2 +6
2.5
0.05
0.25 C-SH C-S-S-C
Fósforo P
15 31
+5
2.1
0.20
0.98 PO4---
Fosfato
Uniones entre compuestos orgánicos Enlaces ricos en energía. Tampones de pH
Sodio Na
11 23
+1
0.9
0.03
0.11 Na+
Ión Sodio
Ión en disolución: Principal catión extacelular
Potasio K
19 39
+1
0.8
0.05
0.31 K+
Ión Potasio
Ión en disolución : Principal catión intracelular
Magnesio Mg
12 24
+2
1.2
0.01
0.04 Mg++
Ión Magnesio
Ión en disolución Enzimas
Calcio Ca
20 40
+2
1.0
0.30
1.9 Ca++
Ión Calcio
Ión en disolución Mensajero celular Ión precipitado : esqueletos
Cloro Cl
17 35
-1
3.0
0.10
0.56 Cl-
Ión Cloro
Ión en disolución: Principal anión inorgánico
C-OH C=O
Sulfhidrilo Bisulfuro
Compuestos orgánicos: Grupos reacctivos con carga +
SO4=
Acido Agua
Agua Compuestos orgánicos : Grupos reactivos con carga -
Sulfato
Compuestos orgánicos : Enlaces reversibles
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
6
3. LAS BIOMOLÉCULAS Los átomos de los diferentes bioelementos se unen entre sí mediante enlaces químicos para formar las moléculas constituyentes de los organismos vivos, que reciben el nombre de biomoléculas o principios inmediatos. Mediante diferentes técnicas de análisis basadas en métodos físicos, como la filtración, la destilación, la centrifugación y la decantación, es posible separar las biomoléculas de un ser vivo sin destruirlas. A pesar de la gran variedad de biomoléculas (una célula contiene más de 10.000 moléculas distintas), todas se agrupan en dos grandes clases, según su naturaleza: Biomoléculas inorgánicas: agua y algunas sales minerales. Biomoléculas orgánicas: glúcidos, lípidos, proteínas y ácidos nucleicos. Algunas como las enzimas, vitaminas y hormonas, se encuadran químicamente en los grupos de biomoléculas orgánicas.
El enlace químico en las biomoléculas La mayoría de las sustancias que existen en la naturaleza son sustancias compuestas, en las que los átomos tienden a unirse de forma espontánea mediante un enlace químico. Existen dos tipos básicos de enlaces entre átomos: iónico y covalente. Además, unas moléculas se pueden unir a otras mediante enlaces intermoleculares. Todos estos enlaces contribuyen a la formación de las distintas biomoléculas, pero en la materia viva son especialmente importantes los enlaces covalentes e intermoleculares. Enlace iónico: se produce entre átomos con electronegatividades (tendencia a ganar electrones) muy diferentes; se produce por la atracción electrostática de cargas opuestas, resulta de la pérdida de electrones por parte de un átomo y la ganancia por parte de otros. El átomo que capta los electrones se transforma en un ión negativo o anión, y el que los pierde, en un ión positivo o catión. En solución los iones están libres, mientras que en estado sólido unos iones se rodean de otros de carga opuesta, formando un entramado ordenado que origina una estructura cristalina. De esta forma (sólidas o solubilizadas), se encuentran las sales minerales presentes en los seres vivos. Enlace covalente: se produce entre átomos que comparten uno o más pares de electrones, cuya electronegatividad es igual o parecida. En el primer caso se originan moléculas apolares (como el N2, O2 e H2). Cuando unos átomos atraen más que otros los electrones, se originan moléculas polares, con un polo positivo (+) y otro negativo (-), formando dipolos moleculares, como el H2O, NH3, SH2, etc.,… Enlaces intermoleculares: se establecen entre átomos de moléculas distintas y por lo tanto unen moléculas. Entre los enlaces intermoleculares destacan: ▪ Puentes o enlaces de hidrógeno: se estable entre un átomo de H y otros átomos muy electronegativos, como F, O y N. Los átomos de H quedan próximos a otros átomos de moléculas adyacentes y se establecen pequeñas fuerzas de atracción entre ellos. Este enlace asegura la cohesión entre las moléculas de agua y contribuye a la conformación espacial de moléculas como las proteínas y los ácidos nucleicos. ▪ Interacciones iónicas: se producen entre moléculas que poseen grupos funcionales con cargas eléctricas distintas. Se da en las proteínas. ▪ Interacciones hidrofóbicas: se deben a que las moléculas apolares tienden a agruparse en un medio acuoso. Son importantes en la formación de las membranas celulares. ▪ Otros: el enlace glucosídico, que une monosacáridos; el enlace peptídico, que une aminoácidos; el enlace fosfodiéster, que une nucleótidos. Son todos enlaces de tipo covalente que se establecen entre átomos de diferentes moléculas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
7
4. EL AGUA El agua es un componente fundamental de los seres vivos, ya que es la molécula más abundante en todos los organismos (supone, aproximadamente, entre el 50 y 90 % de su peso). La cantidad de agua presente en los seres vivos depende de tres factores: ▪ Especie. Los organismos acuáticos contienen un porcentaje de agua muy elevado, que puede alcanzar el 99% de su peso, mientras que los valores más bajos corresponden a especies adaptadas a zonas desérticas. ▪ Edad del individuo. Las estructuras biológicas de los individuos jóvenes presentan una mayor proporción de agua que la de los individuos de más edad. ▪ Tipo de tejido u órgano. Dado que las reacciones biológicas se llevan a cabo en un medio acuoso, los tejidos con mayor actividad bioquímica contienen una proporción de agua mayor que los más pasivos. En cambio, las estructuras esqueléticas animales que constituyen órganos de sostén del individuo, poseen los porcentajes más bajos. El agua en los organismos pluricelulares se encuentra en forma de agua intracelular (en el interior de las células) aproximadamente en dos tercios del total, y en forma de agua extracelular (en los espacios intersticiales de las células o como parte del agua circulante en la sangre o en la savia vegetal) en otro tercio. El elevado contenido de agua en los seres vivos pone de manifiesto, además, la importancia de las funciones que desempeña en ellos, las cuales derivan de sus propiedades físico-químicas y estas, a su vez, de su estructura química.
Estructura química del agua La molécula de agua consta de un átomo de oxígeno y dos de hidrógeno, unidos mediante enlaces covalentes, en los que cada átomo de hidrógeno de una molécula comparte un par de electrones con el átomo de oxígeno. Como la electronegatividad del oxígeno es mayor que la del hidrógeno, los pares de electrones compartidos se ven atraídos con más fuerza por el núcleo del oxígeno que por el del hidrógeno. Esto, unido al hecho de que el oxígeno posee cuatro electrones más sin compartir, da lugar a dos consecuencias: Los enlaces no se disponen en línea recta, sino formando un ángulo de 104,5º. El átomo de oxígeno presentan una cierta carga negativa (-) y los átomos de hidrógeno cierta carga positiva (+), creándose una asimetría eléctrica. Por esta razón, a pesar de ser eléctricamente neutra en su conjunto, la molécula de agua tiene carácter dipolar, es un dipolo eléctrico.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
8
Esta polaridad favorece que las moléculas de agua próximas entre sí tiendan a asociarse, de manera que la zona con carga negativa de una de ellas es atraída por la zona con carga positiva de otra, estableciéndose entre ambas un tipo de enlace denominado enlace o puente de hidrógeno, que convierte al agua en una sustancia altamente cohesiva, ya que cada molécula de agua puede establecer cuatro puentes de hidrógeno con otras tantas moléculas.
Propiedades físico-químicas del agua Las propiedades físicas y químicas del agua derivan de su polaridad y de la cohesión entre sus moléculas. Las más importantes y sus consecuencias biológicas son: Gran poder disolvente. El agua es uno de los mejores (por no decir el mejor) disolventes líquidos. El agua disuelve compuestos iónicos y polares y dispersa moléculas anfipáticas (como los ácidos grasos) y de elevado peso molecular (como las proteínas). Si se introduce en un medio acuoso un compuesto iónico o polar, las moléculas de agua rodean a cada ión o polo con sus zonas de carga opuesta, fenómeno conocido como solvatación. Como consecuencia de ello, se produce un reparto en toda la extensión de la masa de agua, o sea, una verdadera disolución. Elevada tensión superficial. En la superficie de o con otro medio, la polaridad de las moléculas de agua no se equilibra y la cohesión entre ellas es mayor, lo que proporciona una especie de película superficial bastante resistente. Esta propiedad es la causante de la mayoría de las deformaciones celulares y de los movimientos citoplasmáticos.
Capilaridad. La unión entre las moléculas de agua mediante puentes de hidrógeno les confiere un grado de cohesión muy alto, lo que combinado con la adhesión a la superficie de otras estructuras (debida a su polaridad), permite que el agua pueda ascender a lo largo de conductos estrechos. Esta propiedad resulta fundamental para el ascenso de la savia bruta por los tubos del xilema en las plantas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
9
Líquido prácticamente incompresible. El volumen de agua líquida no disminuye apreciablemente aunque se apliquen presiones muy altas, debido al elevado grado de cohesión entre sus moléculas. Esta propiedad permite que el agua actúe como esqueleto hidrostático en las células vegetales y determina las deformaciones citoplasmáticas. Elevado calor específico. El calor específico de una sustancia (Ce) es la cantidad de calor (medida en calorías) necesaria para elevar 1º C la temperatura de un gramo de dicha sustancia. A unos 15 ºC, el Ce del agua es de 1 cal/g ºC, lo que comparado con otros compuestos es muy elevado. Esto se debe a que parte de la energía comunicada al agua se emplea en romper los puentes de hidrógeno y no en elevar la temperatura. Esto permite que el agua sea un amortiguador térmico, o sea, el agua absorbe o libera grandes cantidades de calor sin que haya grandes variaciones en su temperatura. Alta conductividad. La conductividad del calor del agua es relativamente alta y evita la acumulación local de calor. Elevado calor de vaporización. Para pasar del estado líquido al gaseoso es necesario que los puentes de hidrógeno se rompan, lo que requiere un aporte considerable de energía. Esta energía se toma del entorno, por lo que la evaporación del agua absorbe mucho calor y disminuye la temperatura de su entorno. Por eso, la formación y evaporación del sudor en los humanos y el jadeo en los perros son mecanismos refrigerantes que ayudan a regular la temperatura corporal. Mayor densidad del hielo que del agua líquida. Cuando la temperatura del agua disminuye por debajo de 4 ºC, cada molécula de agua puede formar enlaces de hidrógeno con otras cuatro, y cuando la temperatura alcanza los O ºC se forma una red espacial de moléculas de agua que ocupa un mayor volumen que el agua líquida, por lo que el hielo formado es menos denso y flota en ella. Esta propiedad permite la vida acuática en los climas fríos, ya que se forman capas de hielo superficiales que actúan como aislante térmico, lo que permite la supervivencia de las especies acuáticas en invierno.
Bajo grado de ionización. En el agua líquida existe una pequeña cantidad de moléculas ionizadas (disociadas en sus iones), debido a la pequeña masa del hidrógeno y a que su electrón se halla fuertemente unido al oxígeno. Cuando una molécula de agua se ioniza se obtienen dos iones, H3O+ y OH-, con carga opuesta y en igual concentración (los H3O+ suelen representarse simplemente como H+). El producto de las concentraciones de los iones (H3O+ y OH-) es constante, y se denomina producto iónico. Su valor para el agua pura a 25 ºC es: Kw = [H3O ] [OH- ] = 1 1014
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
10
En el agua pura las concentraciones de iones H3O+ y OH- es la misma e igual a 1 10-7, sin embargo en una disolución acuosa la proporción de iones varía, pudiendo ser: Neutras, si la concentración de iones H3O+ y OH- es igual. Ácidas, si la concentración de iones H3O+ es mayor que la de OH-. Básicas, si la concentración de iones OH- es mayor de que de H3O+. El agua y sus productos de ionización participan en una serie de reacciones biológicas importantes, entre las que destacan las reacciones de hidrólisis, en las que una molécula de agua rompe una molécula orgánica. La hidrólisis es el procedimiento empleado para obtener moléculas sencillas a partir de macromoléculas, como sucede en la digestión.
Funciones biológicas del agua Las funciones que el agua desempeña en los seres vivos derivan de las propiedades que acabamos de ver. El agua en los seres vivos actúa, principalmente como: ▪ Medio de transporte de sustancias. Debido a su poder disolvente y dispersante, puede transportar sustancias de una zona a otra de los organismos (ejemplo: sangre y savia). Además, gracias al transporte de sustancias las células pueden intercambiar materia con el medio a través de las membranas celulares. ▪ Medio de reacción. Gracias al poder disolvente, la mayoría de las biomoléculas están disueltas en el agua y pueden reaccionar entre sí. ▪ Reactivo químico. Participa en algunas reacciones químicas, como las reacciones de hidrólisis, en las que se rompen enlaces introduciendo la molécula de agua. ▪ Agente regulador de la temperatura. El agua es un excelente amortiguador térmico, debido al elevado calor específico, evitando cambios bruscos de temperatura en los organismos. Las reacciones biológicas generan calor, pero no se produce un aumento de temperatura ya que el agua lo absorbe. Además la alta conductividad térmica evita la acumulación de calor en un determinado punto del organismo. Asimismo, el elevado calor de vaporización facilita la regulación de la temperatura corporal, refrigerando el organismo al evaporarse el sudor. Otras funciones del agua son: Función estructural: proporciona turgencia a las células debido a su carácter incompresible. Algunos animales (como gusanos perforadores), presentan esqueletos hidrodinámicos, que al hincharse les permite perforar el fondo marino. Amortigua los golpes, como el líquido cefalorraquídeo que protege al cerebro de los golpes que sufre el cráneo. Lubrica las articulaciones, como el líquido sinovial, que evita el rozamiento de los huesos en la articulación.
5. LAS SALES MINERALES y SUS FUNCIONES BIOLÓGICAS Los organismos vivos están formados también por sales minerales, compuestos inorgánicos que pueden encontrarse en dos formas: ■ En estado sólido, cuando son insolubles en agua y se encuentran precipitadas, formando parte de estructuras esqueléticas, como huesos, conchas o caparazones. ■ En disolución, cuando son solubles en agua y se encuentran disociadas en sus correspondientes iones (aniones y cationes). Entres los aniones y cationes más frecuentes figuran los siguientes: Aniones: Cl-; CO32- ; HCO-3 ; PO34- ; SO24 Cationes: Na+; K+; Ca2+; Mg2+; Fe2+; Fe3+ Algunos cationes pueden aparecer asociados a determinadas moléculas orgánicas (proteínas) como el ión ferroso, que interviene en el transporte de oxígeno asociado a la hemoglobina.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
11
Funciones de las sales minerales Constitución de estructuras esqueléticas. Los huesos, las conchas, los caparazones y las espículas de algunos organismos están formadas por sales precipitadas, como fosfatos (Ca3(PO4)2), carbonato cálcico (CO3Ca) e incluso sílice (SiO2). Funciones fisiológicas y bioquímicas. Muchos procesos biológicos solo se pueden realizar con la intervención de determinados cationes. En el cuadro de los bioelementos se recogen los más importantes. Regulación del equilibrio osmótico. Todos los medios líquidos biológicos (sangre, plasma intersticial, líquido cefalorraquídeo, etc.,…) constituyen disoluciones de sales en agua cuyo grado de concentración depende de la estabilidad celular y la realización de algunas funciones fundamentales. Cuando existen dos disoluciones de diferente concentración separadas por una membrana semipermeable que no deja pasar el soluto pero sí el disolvente, se produce el paso del disolvente (agua en los medios celulares) desde la disolución más diluida (hipotónica o hipoosmótica) hacia la más concentrada (hipertónica o hiperosmótica) a través de la membrana. Este fenómeno se conoce como ósmosis. Cuando el agua pasa a la disolución hipertónica, esta se diluye, mientras que la disolución hipotónica se concentra al perder agua. El proceso continua hasta que ambas disoluciones igualan su concentración, es decir, se hacen isotónicas o isoosmóticas (como el suero fisiológico, de 0,9% de concentración salina, que es una solución isotónica con las células del cuerpo humano). Para evitar el paso del agua sería necesario aplicar una presión, denominada presión osmótica, tanto más intensa cuanto mayor fuera la diferencia de concentración entre ambas disoluciones.
Como la membrana plasmática es semipermeable, es necesario mantener una concentración salina dentro de la célula igual a la del medio externo para que la célula no tenga pérdida ni ganancia de agua. Cuando esto no sucede se producen dos tipos de fenómenos osmóticos: ▪ Si la concentración del medio intracelular es mayor que la del medio externo, la entrada masiva de agua producirá un hinchamiento, conocido como turgencia celular. Si la célula es animal puede llegar a estallar (lisis osmótica) y si es vegetal se hincha ligeramente ya que la pared celular equilibra la presión osmótica, comprimiéndose el citoplasma contra la pared. ▪ Si, por el contrario, la concentración del medio interno es menor que en el medio externo, la célula pierde agua y disminuye su volumen, fenómeno conocido como plasmólisis. La célula se arruga y la pérdida de agua puede llegar a la muerte celular. En las células vegetales la vacuola disminuye su tamaño, arrastrando al citoplasma y la membrana se despega de la pared.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte I: Los compuestos inorgánicos
12
Todos los seres vivos, acuáticos o terrestres, están obligados a la osmorregulación o regulación de la presión osmótica. Muchos de ellos han conseguido sobrevivir en medios hipotónicos o hipertónicos mediante mecanismos físicos o químicos que evitan los cambios de presión osmótica en su medio interno. Mantenimiento del pH. En los líquidos biológicos siempre existen unas ciertas cantidades de iones H3O+ (hidrogeniones) y OH- (hidroxilos) que proceden de la disociación del agua y de sustancias ácidas y básicas. (los iones H3O+ suelen representar simplemente como H+). Cuando la [H+ ] es mayor que la [OH- ] la disolución es ácida y cuando la [H+ ] es menor que la de [OH ] decimos que dicha disolución es básica. Si ambas concentraciones son igual, dicha disolución es neutra. Para medir el grado de acidez de una disolución se utiliza el término pH, que se define como el logaritmo inverso de la [ H+]. pH = log
1 = - log [H+] [H ]
Así, por ejemplo, el pH de una disolución cuya [H+] es de 10-5 será de 5. La utilización de valores de pH permite simplificar el manejo de los valores exponenciales y bajo de la [H+]. Los valores de pH pueden oscilar entre 0 y 14. ▪ pH= 7 pH neutro ▪ pH < 7 pH ácido ▪ pH > 7 pH básico Para el buen funcionamiento, las células requieren un pH cercano al neutro. Sin embargo, como consecuencia de las reacciones metabólicas, continuamente se están produciendo sustancias ácidas o básicas que varían el pH. Para evitarlo, el organismo dispone de ciertos mecanismos químicos, los sistemas amortiguadores o tampón, que evitan los cambios de pH, constituidos por un ácido débil y una sal del mismo ácido. Existen diversos sistemas tampón, los más importantes son el sistema tampón bicarbonato que mantiene el pH de los líquidos extracelulares y el sistema tampón fosfato, que actúa en el medio intracelular. (más adelante se expone su forma de actuación).
Biología 2º Bachillerato APÉNDICE TEMA 1. FÍSICO-QUÍMICA DE LAS DISPERSIONES ACUOSAS El agua es el disolvente biológico ideal, disuelve con facilidad una gran variedad de constituyentes de los seres vivos, entre ellos iones, azúcares y muchos aminoácidos. Debido a su gran poder disolvente, el agua se encuentra en el interior de todos los seres vivos formando disoluciones de diversos solutos. Una disolución o dispersión es una mezcla homogénea de moléculas distintas, que son las del disolvente o fase dispersante y las de soluto o fase dispersa. Según el tamaño de las partículas dispersas en el agua se distinguen dos tipos de disoluciones: Disoluciones verdaderas: cuando el tamaño de las moléculas de soluto es pequeño, debido a lo cual el aspecto de la disolución es igual que el disolvente puro. Las disoluciones verdaderas poseen unas propiedades, llamadas coligativas que dependen de la concentración del soluto (como el aumento de la temperatura de ebullición). Forman disoluciones verdaderas las sales minerales y moléculas orgánicas de bajo peso molecular (monosacáridos, disacáridos, aminoácidos,…) Disoluciones o dispersiones coloidales: cuando las moléculas de soluto son de gran peso molecular y tamaño. No son disoluciones verdaderas porque las moléculas de soluto se pueden separar por ultracentrifugación. En estas dispersiones los solutos son macromoléculas como las proteínas, los ácidos nucleicos y los polisacáridos. Las partículas dispersas pueden provocar tres fenómenos en relación con su movimiento en el seno del agua: difusión, diálisis y ósmosis. La difusión sería el fenómeno por el cual las moléculas disueltas tienden a distribuirse uniformemente en el seno del agua. Puede ocurrir también a través de una membrana si es lo suficientemente permeable, de manera que las moléculas de soluto pueden atravesar la membrana desde una zona de alta concentración hacia otra de baja concentración, es decir, a favor del gradiente de concentración. Un ejemplo es el movimiento del CO2 hacia el exterior de la célula o el movimiento de los iones de Na hacia el interior de las células nerviosas cuando conducen el impulso nervioso. La ósmosis es la difusión de agua a través de una membrana semipermeable en presencia de al menos un soluto para el que la membrana es impermeable. La difusión de las moléculas de agua se realiza de la zona más diluida a la más concentrada hasta alcanzar un equilibrio de concentraciones (equilibrio osmótico). En clase ya hemos estudiado qué sucede cuando no se da tal equilibrio. La diálisis es un proceso relacionado con la ósmosis. En este caso pueden atravesar la membrana además del disolvente, moléculas de bajo peso molecular y éstas pasan atravesando la membrana desde la solución más concentrada a la más diluida. El movimiento se produce desde la zona de mayor presión a la zona de menor presión, como sucede en el riñón cuando el agua y los solutos pequeños salen de los vasos sanguíneos para formar la orina. Mediante la diálisis, si se tiene una disolución de dos tipos de sustancias, una de ellos de elevado peso molecular y otra bajo peso molecular, se puede conseguir una separación parcial de esta última. Para ello, se prepara la disolución en un recipiente separado, por medio de una membrana semipermeable, de otro que contiene agua destilada. El soluto de bajo peso molecular se distribuye a través de la membrana hasta que se alcanza la misma concentración en ambos recipientes, mientras que las moléculas de gran tamaño no atravesarán la membrana y se quedarán en el recipiente original. La diálisis es el fundamento de la hemodiálisis que intenta sustituir la filtración renal deteriorada. Mediante esta técnica se consigue eliminar las sustancias tóxicas de la sangre (como la urea) en caso de insuficiencia renal.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
1
ACTIVIDADES TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA. PARTE 1. LA MATERIA DE LOS SERES VIVOS. LOS COMPUESTOS INORGÁNICOS. 1. En qué nivel de organización de la materia incluirías: Proteína Pradera Rebaño de ovejas Epidermis Hueso Núcleo celular Oligoelemento Colonia de protozoos Bacteria Raíz 2. • • • • • • • • • • • • •
Busca qué ramas científicas de la Biología están relacionadas con el estudio de: Moléculas y procesos químicos en los seres vivos Células y orgánulos celulares Tejidos Microorganismos Animales Vegetación Características físicas animales y plantas Funcionamiento de órganos, aparatos y sistemas en animales y plantas ADN y transmisión de caracteres hereditarios Desarrollo embrionario en animales Fósiles Comportamiento animal Ecosistemas
3. El Silicio es un elemento muy abundante en la corteza terrestre. Busca datos referentes a sus propiedades físico-químicas y trata de explicar porqué el carbono y no el silicio, siendo tan abundante, ha permitido la formación de la materia viva. 4. Trata de explicar: a) ¿Porqué el oxígeno permite obtener tanta energía a partir de la materia orgánica?. b) ¿Porqué el fósforo permite almacenar energía de pronto uso?. c) ¿Porqué se cree que la vida apareció en el medio acuoso?. 5. ¿Qué es un Oligoelemento?. Cita cinco ejemplos y su importancia en los seres vivos. 6. ¿Significa lo mismo materia viva y materia orgánica?. ¿Las moléculas orgánicas se encuentran solamente en los seres vivos?. Razona la respuesta. 7. ¿Por qué la carne de ternera es más blanda que la de vaca, pero esta última, a igualdad de peso, proporciona más nutrientes?. 8. Explica sucintamente si la proposición que sigue es verdadera o falsa: “Todas las células viven en un medio acuoso, excepto las de los reptiles, que prefieren ambiente seco”. 9. ¿A qué se debe la fuerte cohesión entre las moléculas de agua?. 10. ¿Porqué a temperatura ambiente el agua es un líquido, siendo el SO2, un gas?. 11. ¿Porqué el agua es un gran disolvente?. ¿Porqué no disuelve los hidrocarburos?.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
2
12. Explica: a) ¿Porqué las regiones costeras tienen un clima más suave que las zonas interiores de los continentes?. ¿Qué relación tiene esta pregunta con los seres vivos?. b) ¿Porqué al depositar suavemente una hoja de afeitar sobre la superficie del agua esta no se hunde?. 13. ¿Cuál es el pH de dos disoluciones en las que [H+] es 1,4 x 10-8 y 4 x 10-6?. 14. Hasta hace poco tiempo, cuando una comida copiosa provocaba acidez de estómago, al segregarse gran cantidad de HCl, se tomaba bicarbonato sódico (HCO3Na) para su digestión. a) Explica cómo tiene lugar el proceso de neutralización en el estómago b) Actualmente no se aconseja abusar del bicarbonato, ¿sabes por qué?. 15. Busca en algún libro las diferencias entre ósmosis y diálisis. 16. Lee atentamente estos experimentos y responde a las siguientes cuestiones: Experimento 1. Extraemos un fragmento de tejido y lo introducimos en un recipiente con un medio acuoso (medio A), dejándolo reposar cinco minutos. Retiramos el tejido del medio y al observar el microscopio, vemos que sus células presentan un aspecto arrugado. Experimento 2. Realizamos un experimento similar, introduciendo esta vez el tejido en otro medio (medio B). Al observar las células al microscopio aparecen hinchadas. a) ¿Cómo sería el medio A y el medio B?. b) ¿Cómo se denomina el fenómeno que sufren las células en cada experimento?. c) Explica el proceso físico que ha sucedido en cada uno de los experimentos. 17. ¿Porqué las hojas de lechuga se ponen turgentes cuando se dejan en agua y luego al aliñar se arrugan?. 18. ¿Porqué las soluciones que se istran en inyección endovenosa deben ser isotónicas para las glóbulos rojos?. ¿Qué podría ocurrir si así no fuera?.
TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA PARTE II. GLÚCIDOS y LÍPIDOS 1.
CONCEPTO DE GLÚCIDO, FUNCIONES y CLASIFICACIÓN
2.
MONOSACÁRIDOS
2.1. 2.2. 2.3. 2.4. 2.5.
Composición química y nomenclatura Propiedades químicas Propiedades físicas Fórmulas cíclicas Importancia biológica de los monosacáridos
3.
ENLACE O-GLUCOSÍDICO
4.
DISACÁRIDOS
5.
POLISACÁRIDOS
6.
HETERÓSIDOS
7.
FUNCIONES BIOLÓGICAS DE LOS GLÚCIDOS
8.
LÍPIDOS: CARACTERÍSTICAS GENERALES y CLASIFICACIÓN
9.
LOS ÁCIDOS GRASOS
10. LÍPIDOS SAPONIFICABLES 10.1. LÍPIDOS SIMPLES SAPONIFICABLES
GRASAS CERAS
10.2. LÍPIDOS COMPLEJOS SAPONIFICABLES
FOSFOGLICÉRIDOS ESFINGOLÍPIDOS
11. LÍPIDOS INSAPONIFICABLES TERPENOS ESTEROIDES PROSTAGLANDINAS 12. FUNCIONES BIOLÓGICAS DE LOS LÍPIDOS
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
1
1. CONCEPTO DE GLÚCIDO, FUNCIONES y CLASIFICACIÓN Los glúcidos son moléculas orgánicas que contienen átomos de C, H y O. A menudo se les denominan azúcares, ya que muchos de ellos tienen sabor dulce y también reciben el nombre de hidratos de carbono o carbohidratos, porque muchos de ellos responden a la fórmula empírica Cn(H2O)n que parece corresponder a combinaciones de carbono con agua. Sin embargo, esta última denominación resulta incorrecta, pues los glúcidos son polialcoholes con un grupo funcional carbonilo (aldehído o cetona); es decir, son polihidroxialdehídos o polihidroxicetonas. Esta composición química es común a todos los glúcidos. Los glúcidos se encuentran en todos los seres vivos, donde desempeñan fundamentalmente una función energética, aunque también existen otros glúcidos no energéticos que cumplen otras funciones (estructural, reconocimiento celular, etc.) Los glúcidos se clasifican según su complejidad en: MONOSACÁRIDOS u OSAS: comprenden los glúcidos más simples y no pueden ser hidrolizados (no hidrolizables). Contienen entre 3 y 7 átomos de carbono. En este grupo se incluyen también sus derivados. Entre ellos se encuentran la glucosa, fructosa o la ribosa. ÓSIDOS: son glúcidos compuestos por la unión de varios monosacáridos ( o sus derivados). Estos glúcidos son hidrolizables, ya que pueden experimentar reacciones de hidrólisis que liberan los monosacáridos que los componen. Se subdividen en dos grupos: ▪ Holósidos: formados únicamente por monosacáridos. Según el número de monosacáridos que presentan pueden ser: - Oligosacáridos: compuestos por la unión de dos a diez monosacáridos. Entre ellos destacan los disacáridos, como la sacarosa, lactosa o maltosa. - Polisacáridos: formados por un elevado número de monosacáridos. Destacan el almidón, glucógeno, celulosa y quitina. ▪ Heterósidos: formados por una parte glucídica (monosacáridos) y otra no glucídica que recibe el nombre de aglucón. Si la parte no glucídica es una proteína hablamos de glucoproteínas y si se trata de un lípido, de glucolípidos.
2. MONOSACÁRIDOS Los monosacáridos son los glúcidos más sencillos, por eso las células pueden utilizarlos directamente como fuente de energía.
2.1.
Composición química y nomenclatura
Los monosacáridos contienen entre 3 y 7 átomos de carbono, denominándose triosas, tetrosas, pentosas, hexosas o heptosas si el número de carbonos es, respectivamente, 3, 4, 5, 6, o 7. Químicamente los monosacáridos son polihidroxialdehídos o polihidroxicetonas, es decir, están formados por varios grupos alcohol (-OH) con un grupo aldehído (-CHO) o cetona (-CO). Según el grupo funcional principal que lleven, se clasifican en : ■ Aldosas: tienen un grupo aldehído en el primer carbono (C1) y grupos hidroxilo en el resto de los carbonos. ■ Cetosas: tienen un grupo cetona en el segundo carbono (C2) y grupos hidroxilo en el resto. Los monosacáridos se nombran anteponiendo el prefijo aldo- o ceto- al nombre que indica el número de carbonos, seguido de la terminación –osa. Por ejemplo, un monosacárido de tres átomos de carbono cuyo grupo funcional principal es un aldehído se denomina aldotriosa y será cetotriosa si el grupo funcional es una cetona. Además de la nomenclatura sistemática, la forma de nombrar a los monosacáridos más utilizada es mediante nombres vulgares o comunes, que hacen referencia a alguna característica, utilizando la terminación –osa (glucosa, fructosa, ribosa, galactosa, etc.).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
FÓRMULAS DE LOS MONOSACÁRIDOS (PROYECCIÓN DE FISCHER)
2
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
3
2.2. Propiedades químicas Todos los monosacáridos tienen carácter reductor debido a la presencia de los grupos aldehído o cetona, que pueden oxidarse a carboxilos. Esta propiedad se utiliza para determinar la presencia de monosacáridos en un material biológico, mediante diferente tipo de reacciones. Entre ellas destaca la reacción de Fehling, en la que se emplea sulfato de cobre (SO4Cu) en un medio alcalino (NaOH) y es reducido a óxido de cobre (Cu2O), produciendo una coloración rojo ladrillo. Además el grupo aldehído o cetona participan en la formación de distintos enlaces: ▪ Hemiacetálicos internos, originando formas cíclicas ▪ Enlaces glucosídicos entre monosacáridos, originando disacáridos y polisacáridos.
2.3. Propiedades físicas Todos los monosacáridos son sólidos cristalinos y blancos, perfectamente solubles en agua, y tienen sabor dulce. Todos los monosacáridos, a excepción de la Dihidroxiacetona, presentan carbonos asimétricos, es decir, carbonos unidos a cuatro radicales distintos, lo que les otorga dos propiedades físicas muy importantes: Estereoisomería o isomería espacial Actividad óptica
Estereoisomería La estereoisomería es la existencia de moléculas que presentan la misma fórmula estructural pero distinta disposición espacial de sus átomos. Esto sucede debido a la presencia de algún átomo de CARBONO ASIMÉTRICO, es decir, un carbono que está unido a cuatro radicales diferentes. Los carbonos asimétricos son frecuentes en los glúcidos y se identifican en la molécula con un asterisco (*). carbono asimétrico
Cada carbono asimétrico determina la existencia de dos ISOMÉROS ESPACIALES o ESTEREOISÓMEROS (DIASTEROISÓMEROS), dos moléculas con la misma fórmula estructural pero diferente configuración espacial. Vamos a verlo, con el ejemplo del gliceraldehído, un monosacárido de tres carbonos con un grupo aldehído en el carbono primero. Para representar en el plano la molécula de gliceraldehído, se utiliza habitualmente la PROYECCIÓN DE FISCHER, en la que la cadena carbonada se dispone en vertical y los grupos unidos a los carbonos asimétricos se sitúan a la derecha y a la izquierda de estos.
Biología 2º Bachillerato
4
Tema 1. La base físico-química de la vida.
Los dos estéreo isómeros del gliceraldehído se representan de la forma siguiente según la proyección de Fischer:
Cada uno de los estereoisómeros del gliceraldehído recibe un nombre distinto, de manera que se pueden distinguir dos formas espaciales: Forma D: en la que el grupo –OH del carbono asimétrico está situado hacia la derecha. Se denomina D-gliceraldehído. Forma L: en la que el grupo –OH del carbono asimétrico está situado hacia la izquierda. Se denomina L-gliceraldehído. Pero, la mayoría de los monosacáridos llevan más de un carbono asimétrico, por lo que el número de isómeros espaciales o estereoisómeros de cada sustancia es mayor de dos. Para poder calcular el número de esteroisómeros posibles de un monosacáridos aplicaremos la fórmula 2n, siendo n el número de carbonos asimétricos. Para todos aquellos monosacáridos que posean más de un carbono asimétrico, se ha establecido, por convenio, que los prefijos D y L se refieran sólo al carbono asimétrico más alejado del grupo carbonilo, es decir, el carbono asimétrico de mayor numeración.
Formas D
Formas L
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
5
Dentro de los estereoisómeros se pueden diferenciar: ■ ENANTIÓMEROS o ENANTIOMORFOS: son imágenes especulares entre sí y no superponibles. Los enantiómeros conservan el mismo nombre, añadiendo la denominación D o L. ■ EPÍMEROS: no son imágenes especulares entre sí y se diferencian en la posición de un grupo –OH diferente al que se toma como referencia para la serie D o L. No conservan el mismo nombre.
Actividad óptica La presencia de carbonos asimétricos determina una importante propiedad de los monosacáridos en disolución: la actividad óptica. Esta es la capacidad que poseen para desviar el plano de polarización de un haz de luz polarizada que atraviesa la disolución. Cuando desvían el plano de polarización a la derecha se denominan dextrógiros y se simboliza con el signo (+). Cuando desvían el plano de polarización a la izquierda se denominan levógiros y se simboliza con el signo (-). Hay que aclarar que no existe relación entre la actividad óptica, dextrógira o levógira , y el carácter D o L de un determinado estereoisómero. Así el D-gliceraldehído o la D-glucosa son dextrógiros, mientras que la D-fructosa es levógira.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
6
2.4. Fórmulas cíclicas Las fórmulas de los monosacáridos en Proyección de Fischer (cadena lineal) son correctas para las triosas y las tetrosas. Sin embargo, en el caso de las aldopentosas y las hexosas, no explican algunas de sus propiedades en disolución. Esto es debido a que estos monosacáridos adoptan estructuras cíclicas de forma pentagonal o hexagonal, la denominada proyección de Haworth. Estas formas cíclicas se originan al reaccionar el grupo carbonilo con uno de los grupos hidroxilo. Se obtiene así un enlace hemiacetal (en las aldosas) o hemicetal (en las cetosas). Este enlace no implica pérdida ni ganancia de átomos, sino una reorganización de los mismos. Las formas cíclicas resultantes pueden tener forma pentagonal, denominados los monosacáridos furanosas o hexagonal llamándose piranosas. Como resultado de la ciclación, el carbono del grupo carbonilo (llamado ahora carbono anomérico), pasa a ser asimétrico y, por tanto se originan dos nuevos estereoisómeros, denominados ANÓMEROS: Anómero alfa (): el –OH del carbono anomérico queda por debajo del plano, en posición TRANS (distinto lado) respecto al –CH2OH unido al penúltimo carbono. Anómero beta (): el –OH del carbono anomérico queda por debajo del plano, en posición CIS (mismo lado) respecto al –CH2OH unido al penúltimo carbono. La conformación real de los monosacáridos en disolución varía con respecto a la propuesta por Haworth, ya que, debido a la presencia de enlaces covalentes sencillos, las moléculas no pueden ser planas, adoptando una configuración en silla y en bote (figura 7). La configuración en silla es más estable porque existen menos repulsiones electrostáticas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
7
2.5. Importancia biológica de los monosacáridos Los monosacáridos tienen una gran interés, por ser los monómeros constituyentes de todos los glúcidos. También se presentan libres y actúan como nutrientes de las células para la obtención de energía, o como metabolitos intermediarios de importantes procesos biológicos, como la respiración o la fotosíntesis. Los monosacáridos más importantes son: Triosas: son el D-gliceraldehído y la dihidroxiacetona. Su importancia radica en que son compuestos intermediarios del metabolismo de la glucosa y otros glúcidos. Tetrosas: destaca la D-eritrosa, que es un compuesto intermediario de la fotosíntesis. Pentosas: D-ribosa: es un componente de nucleótidos en estado libre, como el ATP y, de ácidos nucleicos, como el ácido ribonucleico (ARN). D-desoxirribosa: se encuentra en el ácido desoxirribonucleico (ADN). D-ribulosa: actúa como intermediario activo en la fijación del CO2 atmosférico en la fotosíntesis. Hexosas: D-glucosa: también llamada azúcar de la uva. Es la molécula energética más utilizada por los seres vivos. Se localiza en estado libre en el citoplasma celular, en el plasma sanguíneo (en concentraciones constantes) y en algunos frutos, como las uvas o los dátiles. Constituye asimismo, la unidad componente de los polisacáridos más comunes (almidón, glucógeno y celulosa). D-galactosa: forma parte de la lactosa (disacárido de la leche), de polisacáridos complejos y de heterósidos. D-fructosa: se encuentra libre en las frutas o unido a la glucosa formando el disacárido sacarosa. Se encuentra en el semen como nutriente de los espermatozoides. Las células hepáticas la transforman en glucosa, por lo que tiene un valor nutritivo equivalente.
3. ENLACE O-GLUCOSÍDICO Los monosacáridos se pueden unir entre sí para formar otros glúcidos más complejos. Esta unión se lleva a cabo al reaccionar dos grupos hidroxilo (-OH) de dos moléculas distintas. Se produce entonces la liberación de una molécula de agua y la unión de los dos monosacáridos por el oxígeno de uno de los grupos hidroxilo implicados. El enlace así creado se denomina O-glucosídico.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
8
4. DISACÁRIDOS
Los disacáridos están formados por la unión de dos monosacáridos mediante un enlace O-glucosídico. La unión entre los monosacáridos puede ser de dos tipos: Enlace monocarbonílico: se establece entre dos grupos –OH, en el que uno de ellos pertenece al carbono anomérico. El disacárido resultante tiene poder reductor, ya que le queda un grupo anomérico libre, como a los monosacáridos. El disacárido que se origina puede aparecer en forma o en forma , según el segundo monosacárido tenga una u otra conformación. Ejemplos de este enlace se encuentran en la maltosa, lactosa y celobiosa. Enlace dicarbonílico: se establece cuando los dos grupos –OH implicados en el enlace son anoméricos. El disacárido resultante no tiene carácter reductor, pues no posee grupos –OH anoméricos libres, como sucede en la sacarosa.
Nomenclatura El nombre del disacárido debe indicar claramente los monosacáridos constituyentes y los carbonos que participan en el enlace O-glucosídico. Se siguen las siguientes reglas: 1º. Se escribe el nombre del primer monosacárido, con la terminación –osil. 2º. Se expresa entre paréntesis los carbonos participantes en el enlace, separados por una flecha corta. 3º. Se escribe el nombre del segundo monosacárido, con la terminación –osa, si el enlace es monocarbonílico, o con la terminación –ósido si es dicarbonílico. Sin embargo, normalmente se emplea una denominación más corta, que alude a los productos donde se encuentra. Por ejemplo, la D-galactopiranosil (14) -D-galactopiranosa recibe también el nombre de lactosa, por estar presente en la leche. Propiedades de los disacáridos Los disacáridos presentan las mismas propiedades que los monosacáridos: son solubles en agua, cristalizables, blancos y tienen sabor dulce. Su capacidad reductora está condicionada por la existencia de un grupo anomérico libre. Disacáridos más importantes Maltosa: -D-glucopiranosil (14) -D-glucopiranosa. La maltosa procede de la hidrólisis del almidón y del glucógeno. Se encuentre en las semillas en germinación (como la malta), que comienzan a emplear la reserva de almidón acumulada. La maltosa puede estar constituida por una glucosa y otra (la que emplea su carbono 4 en el enlace O-glucosídico). Esta forma se denomina y esta más estable en las disoluciones que la forma . Lactosa: -D-galactopiranosil (14) -D-glucopiranosa. La lactosa se encuentra libre en la leche y unida a otras moléculas constituyendo algunos glucolípidos. Sacarosa: -D-glucopiranosil (12) -D-fructofuranósido. La sacarosa es el azúcar de consumo habitual, tanto de caña como de remolacha. Es uno de los principales componentes de la savia elaborada. No tiene carácter reductor. Celobiosa:-D-glucopiranosil (14) -D-glucopiranosa. La celobiosa se obtiene de la hidrólisis de la celulosa. En la página siguiente están representadas las fórmulas y los constituyentes de cada uno de estos disacáridos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
9
5. POLISACÁRIDOS Los polisacáridos están formados por largas cadenas de monosacáridos unidos mediante enlaces Oglucosídicos, por lo que se trata de macromoléculas. La formación de los polisacáridos a partir de monosacáridos es un ejemplo de polimerización, en la que se libera una molécula de agua por cada enlace O-glucosídico creado. La rotura de estos enlaces de realiza, pues, por hidrólisis.
Propiedades Al ser macromoléculas, los polisacáridos no se disuelven fácilmente en agua y pueden ser insolubles, como la celulosa, o formar dispersiones coloidales, como el almidón. Además no son cristalinos, ni tienen sabor dulce. Tampoco tienen carácter reductor, ya que no poseen carbonos anoméricos con grupos hidroxilo libres.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
10
Clasificación Según sus componentes se distinguen dos grupos de polisacáridos: Homopolisacáridos: formados por un tipo de monosacáridos. Son los más abundantes en la naturaleza, y desarrollan dos tipos de funciones biológicas: De reserva energética: presentan enlaces de tipo , y se pueden hidrolizar fácilmente liberando los monosacáridos que los componen. Los más importantes son el almidón y el glucógeno. Estructural: presentan enlaces de tipo , que les confieren gran resistencia a la hidrólisis. Los más importantes son la celulosa y la quitina. Heteropolisacáridos: formados por más de un tipo de monosacáridos. Entre ellos se encuentran los peptidoglucanos, pectinas, agar-agar, goma arábiga, ácido hialurónico y heparina.
Homopolisacáridos de reserva Se localizan, generalmente, en forma de grandes gránulos en el citoplasma celular. Los más importantes son el almidón, el glucógeno y los dextranos. Almidón. Es un homopolisacárido de -D-glucopiranosa, formado por dos constituyentes distintos: ▪ Amilosa. Está formada por largas cadenas de -D-glucopiranosa, no ramificadas, en las que las moléculas de glucosa se unen mediante enlaces (14). Las cadenas adoptan formas helicoidales y tienen seis moléculas de glucosa por vuelta. ▪ Amilopectina. Está formada por cadenas de -D-glucopiranosa con enlaces (14), con ramificaciones. En los puntos de ramificación los enlaces son (16). Las ramificaciones están formadas por 12 unidades de glucosa y, aparecen, por término medio, cada 24 a 30 restos del glucosa. El almidón es el polisacárido de reserva en los vegetales y se acumula en los órganos de reserva, como semillas, raíces y tubérculos, en forma de granos en el interior de los amiloplastos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
11
Glucógeno. Constituye el polisacárido de reserva propio de los hongos y de los animales, en los que forma gránulos visibles y abundantes en el hígado y en los músculos estriados. El glucógeno es un polímero de -D-glucopiranosa con una estructura semejante a la amilopectina, aunque con más ramificaciones (aproximadamente, cada ocho o diez moléculas de glucosa), lo que facilita su hodrólisis. Dextranos. Son los polisacáridos de reserva en las bacterias y levaduras y están compuestos por -D-glucopiranosas que dan lugar a cadenas ramificadas, pero las uniones son variadas: (12), (13),…
Homopolisacáridos estructurales Este tipo de polisacáridos tienen enlaces O-glucosídicos de tipo , por lo que son difíciles de hidrolizar, característica que les permite constituir estructuras biológicas resistentes. Destacan entre ellos: Celulosa. Es un polímero lineal de -D-glucopiranosa, con enlaces (14), formado por largas cadenas (en ocasiones de hasta 15.000 glucosas) sin ramificar. La celulosa es el principal componente de las paredes celulares de los tejidos vegetales, siendo el compuesto orgánico más abundante de la biosfera. Se encuentra por tanto, en productos de consumo humano, como el papel, la madera o el algodón. La mayoría de los animales no pueden utilizar la celulosa como nutriente porque carecen del enzima celulasa, que la hidroliza. No obstante, herbívoros e insectos fitófagos (como las termitas) se nutren con celulosa ya que, su aparato digestivo posee microorganismos simbiontes capaces de hidrolizarla. Sin embargo, a pesar de no poderla utilizar como nutriente, la celulosa es necesaria en la dieta humana porque forma parte de la llamada fibra alimentaria: restos de alimentos no digeribles, que pasan al intestino grueso y estimulan los movimientos peristálticos, con lo que se facilita la eliminación de las heces fecales.
Quitina. Es un polímero de N-acetil--Dglucosamina, un derivado de la glucosa. La quitina es una molécula lineal, con enlaces (14), y es el principal componente del esquelete externo de los insectos, crustáceos y de la pared celular de los hongos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
Heteropolisacáridos Por hidrólisis dan lugar a diferentes monosacáridos o derivados de estos. 1. Origen bacteriano: PEPTIDOGLUCANOS o MUREÍNAS Formados por NAG (N-acetil glucosalina) y NAM (N-acetil murámico). Aparecen en la pared bacteriana Destruidos por la lisozima (enzima de la saliva) 2. Origen Vegetal PECTINAS Formados por Metil-D-galacturonato Aparecen en la pared de las células vegetales (manzana, pera, membrillo, ciruela) Al hidratarse formar geles que se aprovechan para fabricar MERMELADAS AGAR-AGAR Formado por galactosa y ácido sulfúrico Se obtiene de las algas rojas Utilizado para preparar medios de cultivo GOMA-ARÁBIGA Formada por galactosa, arabinosa, ácido glucurónico y ramnosa Es segregada por las plantas para cerrar sus heridas Utilizada para fabricar cola 3. Origen Animal (MUCOPOLISACÁRIDOS o PROTEOGLUCANOS ) ÁCIDO HIALURÓNICO: aparece en la sustancia intercelular de tejidos conjuntivos, óseos y cartilaginosos. Abunda en líquido sinovial y humor vítreo. CONDROITINA: aparece en la matriz extracelular del cartílago, córnea y hueso. HEPARINA: aparece en la matriz extracelular de pulmón, hígado, y paredes arteriales. Actúa como anticoagulante (saliva de insectos hematófagos)
6. HETERÓSIDOS Son moléculas formadas por la asociación de glúcidos con otras sustancias NO glucídicas (AGLUCÓN). GLUCOLÍPIDOS: componentes de las membranas celulares GLUCOPROTEÍNAS: Peptidoglucanos Mucopolisacáridos Mucoproteínas: sustancias muy viscosas. Tracto digestivo: lubrican el bolo alimenticio Tracto respiratorio: mucus Glucoproteínas de la sangre: Inmunoglobulinas (Anticuerpos) Glucoproteínas de las membranas celulares: función antigénica OTRAS: Digitalina: utilizada en tratamiento de enfermedades cardiovasculares Estreptomicina: antibiótico Amigdalósidos: hueso de melocotón y albaricoque Antocianósidos: responsables del color de las flores Nucleótidos: derivados de la ribosa y desoxirribosa.
12
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
7. FUNCIONES BIOLÓGICAS DE LOS GLÚCIDOS
13
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
14
8. CARACTERÍSTICAS GENERALES y CLASIFICACIÓN DE LOS LÍPIDOS Los lípidos son un grupo muy heterogéneo de moléculas, tanto en lo que se refiere a su composición química, como a la función que desempeñan. No obstante todos los lípidos comparten una serie de propiedades físicas que permite agruparlos juntos: Básicamente están formados por largas cadenas hidrocarburadas, que pueden estar sustituidas o no por grupos alcohólicos, aminos, fosfatos, etc. No son solubles en agua ni en otros disolventes polares, pero sí lo son en disolventes orgánicos (no polares), como el benceno, éter, acetona, etc. Presentan un aspecto graso, es decir, poseen un brillo característico y son untuosos al tacto. Los lípidos contienen átomos de C, H y O, y algunos también de P y N. Los lípidos desarrollan funciones muy variadas: - Reserva energética: como las grasas. - Estructural: como los lípidos de membrana. - Protectora: como las ceras. - Vitamínica: como las vitaminas liposolubles. - Hormonal: como las hormonas sexuales. Clasificación de los lípidos Dado que los lípidos son un grupo de moléculas tan diverso, su clasificación ofrece cierta dificultad, ya que se pueden aplicar diferentes criterios. La clasificación más aceptada actualmente es la que los divide en dos grupos: lípidos saponificables e insaponificables. Lípidos saponificables: contienen ácidos grasos en su composición, que se liberan por hidrólisis. El término saponificable hace referencia a que al calentarlos en medio alcalino originan jabones. Químicamente son ésteres. Se dividen en dos grupos: ▪ Lípidos simples: incluyen los glicéridos (grasas) y las ceras. Contienen únicamente átomos de C, H y O. ▪ Lípidos complejos: incluyen los fosfoglicéridos y los esfingolípidos. Contienen además de C, H y O, átomos de N y P. Lípidos insaponificables: no contienen ácidos grasos en su composición, por lo que no pueden originar jabones. Comprenden un grupo muy variado de compuestos: terpenos, esteroides y prostaglandinas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
15
9. LOS ÁCIDOS GRASOS Uno de los componentes de los lípidos saponificables son los ácidos grasos. Son ácidos carboxílicos formados por largas cadenas carbonadas, con un número par de carbonos. Los más comunes son los ácidos grasos de 16 a 18 carbonos. En resumen, los ácidos grasos son largas cadenas hidrocarburadas (o hidrocarbonadas) con un grupo carboxilo en el extremo. Pueden ser de dos tipos: Saturados: cuando solo tienen enlaces simples en la cadena, como el ácido palmítico (16 C) y el esteárico (18 C). Insaturados: cuando presentan uno o más dobles enlaces en la cadena, como el ácido oleico, linoleico y araquidónico. Dependiendo del número de dobles enlaces, se distinguen: ▪ Monoinsaturados: presentan un doble enlace. El más importante es el ácido oleico presente en el aceite de oliva, que se representa de forma sistemática como 18:1 9. ▪ Poliinsaturados: presentan más de un doble enlace. Entre ellos se encuentran: ─ Ácido linoleico, de nombre sistemático 18:2 6. Se encuentra presente en el aceite de semillas (girasol, maíz, etc.). ─ Ácido -linolénico, de nombre sistemático 18:3 3. Abunda en los aceites de pescado graso (atún, salmón, sardina,etc.).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
16
Los ácidos grasos que necesitan los mamíferos, los consiguen mediante síntesis metabólica o en la dieta. Sin embargo, existen unos ácidos grasos denominados esenciales, que el organismo no los puede fabricar y por tanto, tiene que incorporarlos necesariamente en la dieta, por lo que en ocasiones se designan con el término vitamina F. En el ser humano son el ácido linoleico, linolénico y araquidónico, y su carencia impide la síntesis de otras moléculas, como las prostaglandinas.
Propiedades de los ácidos grasos A. Propiedades físicas: Son moléculas anfipáticas (del griego amphi, ambos), ya que la cadena carbonada o alifática es apolar, y por lo tanto insoluble en agua (hidrófoba) y, por otra parte, el grupo carboxilo (-COOH) es polar y soluble en agua (hidrófilo). Esto permite que en cada molécula haya una parte soluble en agua, representada por una cabeza, y otra parte insoluble en agua, representada por una cola. Debido a esta característica, al entrar en o con el agua, los ácidos grasos orientan las cabezas polares hacia ella, mientras que las colas apolares se sitúan en la posición opuesta. Esto da lugar a la formación de diferentes estructuras en empalizada, que pueden ser monocapas o bicapas o estructuras esféricas (micelas). ▪ Monocapas: se produce cuando los ácidos grasos se sitúan en la interfase entre el agua y el aire, las colas se sitúan en el medio aéreo (apolar) y las cabezas se introducen dentro del agua. (A) ▪ Micelas: son agrupaciones esféricas que se forman en el agua, en las que en el interior están las colas y en el exterior las cabezas. (B) ▪ Bicapas: son agrupaciones que separan dos medios acuosos, en las que las cabezas se orientan a cada uno de esos medios y las colas se sitúan enfrentadas. (C)
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
17
El punto de fusión de los ácidos grasos aumenta con el tamaño del ácido graso y disminuye con el grado de instauración (dobles enlaces). Esto es debido a que los ácidos grasos saturados presentan cadenas extendidas que se pueden empaquetar mediante interacciones de Van der Waals entre los átomos de las cadenas vecinas. Esto provoca que a temperatura ambiente, los ácidos grasos saturados adquieran una consistencia cérea y se encuentren en estado sólido. Por el contrario, las cadenas insaturadas muestran ángulos que no permiten un empaquetamiento tan fuerte como las saturadas, por lo que las interacciones entre ellas son más débiles y más fáciles de desordenar por efecto del calor. Por esta razón su punto de fusión es más bajo, y a temperatura ambiente son líquidos oleosos.
Propiedades químicas Las propiedades químicas dependen de la presencia del grupo carboxilo, lo que permite la realización de varias reacciones que dan lugar a la formación de ésteres y sales. Forman ésteres mediante una reacción de esterificación. Los ácidos grasos son capaces de formar enlaces éster al reaccionar el grupos carboxilo (-COOH) con los grupos alcohol (-OH) de otras moléculas, con la eliminación de una molécula de agua. Mediante este tipo de reacciones se originan las grasas, ceras y lípidos complejos. La reacción inversa es la hidrólisis del éster, que origina el ácido graso y el alcohol. Formas sales, mediante la reacción de saponificación. Los ácidos grasos reaccionan con álcalis (una base o hidroxilo), y se obtienen las sales correspondientes de los ácidos grasos, denominadas jabones.
La presencia de dobles enlaces facilita la oxidación de los ácidos grasos, sobre todo de los poliinsaturados, lo cual puede conducir a la rotura de sus cadenas con la consiguiente formación de aldehídos volátiles de cadena corta responsables del olor y sabor a rancio. Este proceso de oxidación se contrarresta en los seres vivos con la presencia de vitamina E, que tiene carácter antioxidante.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
18
10. LÍPIDOS SAPONIFICABLES Todos los lípidos saponificables son ésteres formados por la unión de ácidos grasos y un alcohol. Según el tipo de alcohol presente se les clasifica en triglicéridos o grasas, ceras, fosfoglicéridos y esfingolípidos. 10.1. LÍPIDOS SIMPLES SAPONIFICABLES GRASAS (TRIACILGLICÉRIDOS, TRIGLICÉRIDOS) Son moléculas orgánicas abundantes en todos los organismos vivos. Son ésteres del alcohol glicerina (propanotriol) con tres ácidos grasos. Los triglicéridos se forman mediante reacciones de esterificación. Se trata pues de sustancias hidrolizables y en los seres vivos se hidrolizan por acción de unas enzimas llamadas lipasas, separándose los ácidos grasos y la glicerina.
Las grasas se pueden clasificar en varios tipos según diferentes criterios: 1. Según sean los ácidos grasos iguales o distintos: ▪ Grasas simples: si los tres ácidos grasos son iguales. Se nombran con el prefijo tri- seguido del nombre del ácido graso, al que se le añade la terminación –ina. Por ejemplo, la trioleina o aceite de oliva, donde el ácido graso es el ácido oleico. ▪ Grasas mixtas: cuando los ácidos grasos son distintos. Se designan según cuáles sean los ácidos grasos, cambiando la terminación –ico por –oil, indicando su posición y añadiendo la palabra glicérido. 2. Según el punto de fusión, pueden ser: ▪ Líquidas (aceites): con un punto de fusión inferior a 15 ºC, debido a que presentan una mayor proporción de ácidos grasos insaturados, como el aceite de oliva, aceite de girasol o aceites de pescado. Los aceites, a excepción del pescado, predominan en las plantas. ▪ Sólidas (mantecas y sebos): poseen un punto de fusión por encima de 40 ºC, porque en ellas predominan los ácidos grasos saturados. Son la grasa de cerdo, buey, cordero, propias de los animales. ▪ Semisólidas: se encuentran en un punto intermedio, como las mantequillas y las margarinas, que contienen ácidos grasos saturados e insaturados.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
19
3. Según el grado de instauración de los ácidos grasos: ▪ Grasas saturadas: presentan ácidos grasos saturados en su composición. Son las grasas animales presentes en la carne, leche, huevos y el aceite de coco. Son perjudiciales para el organismo, ya que elevan los niveles de colesterol en sangre. ▪ Grasas insaturadas: presentan ácidos grasos insaturados. Son los aceites vegetales (oliva y girasol) y de los pescados azules. Son beneficiosas para la salud ya que disminuyen los niveles de colesterol sanguíneo. Función biológica Las grasas son las moléculas que generan más cantidad de energía: un gramo de grasa metabolizada produce 9 Kcal, más del doble de energía que un gramos de glúcido (3,75 kcal/g). Por esta razón, y debido también a su insolubilidad en agua (lo que permite almacenarlas en grandes cantidades sin afectar a la presión osmótica celular) las grasas constituyen la reserva energética de los seres vivos, sobre todo de los animales, donde se acumulan en el tejido adiposo formando el tocino y las mantecas de las membranas mesentéricas. Si en la dieta se aporta un exceso de glúcidos hasta que se satura la capacidad de almacenamiento del glucógeno, dicho exceso se transforma en grasas, por eso los glúcidos en exceso engordan. Por el contrario, las grasas no podemos transformarlas en glúcidos. Las plantas también almacenan grasas, principalmente en frutos y semillas, pero en ellas la principal reserva de energía es el almidón. Las grasas desempeñan, además, otras funciones y actúan como amortiguadores mecánicos (grasa de la palma de las manos y la planta de los pies), como aislantes térmicos (animales de climas fríos presentan una gruesa capa de grasa debajo de la piel) y como vehículos de transporte de las vitaminas liposolubles (A, D, E y K). CERAS (CÉRIDOS) Las ceras o céridos son moléculas estructurales que se pueden encontrar en algunos animales y, especialmente, en las plantas. Su composición química es simple, ya que son ésteres de un ácido graso de cadena larga y un monoalcohol de cadena larga también. Debido a su elevado grado de insolubilidad, las ceras desempeñan principalmente una función de protección, ya que protegen de la humedad y evitan la pérdida de agua. Aparecen recubriendo la superficie de órganos vegetales paras evitar la evaporación, como frutos y hojas; y en los animales impermeabilizan algunas estructuras tegumentarias, como las plumas de las aves, y la piel y el pelo de los mamíferos. Algunas ceras son la cera de las abejas, la lanolina de la lana y el cerumen de los oídos.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
20
10.2 LÍPIDOS COMPLEJOS SAPONIFICABLES Son compuestos de carácter antipático, que forman parte de las membranas celulares, por lo que se conocen también como lípidos de membrana, junto con el colesterol, que es un lípido insaponificable.
FOSFOGLICÉRIDOS Al igual que las grasas, los fosfoglicéridos son ésteres de glicerina con ácidos grasos, pero solo llevan dos ácidos grasos, ya que el tercer alcohol de la glicerina está unido a un ácido ortofosfórico, por eso se denominan también fosfolípidos. La molécula resultante se denomina ácido fosfatídico, igual en todos los fosfoglicéridos. A ella se une un aminoalcohol al ácido ortofosfórico, formando el fosfoglicérido completo. Los fosfoglicéridos se caracterizan por su comportamiento antipático, es decir, presentan una parte polar (y, por tanto, soluble en agua) y otra apolar (insoluble). La zona polar corresponde a la porción donde se sitúa el ácido ortofosfórico y el aminoalcohol, mientras que la zona apolar corresponde al resto de la molécula (ácidos grasos). De esta propiedad deriva su función biológica. Todas las membranas celulares están formadas por una doble capa de fosfolípidos en la que las colas apolares de ambas capas se quedan enfrentadas, mientras que las cabezas polares se orientan hacia el medio externo e interno, ambos acuosos. Según el aminoalcohol presente, se diferencian varias clases de fosfoglicéridos: cefalina (fosfatidiletanolamina) si el aminoalcohol es la etanolamina; lecitina (fosfatidilcolina) si contiene colina y fosfatidilserina si tiene serina.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
21
Comportamiento anfipático de los fosfolípidos y su disposición en las membranas
ESFINGOLÍPIDOS Los esfingolípidos también son componentes de las membranas celulares, y abundan en el tejido nervioso. Al igual que los fosfoglicéridos, tienen carácter antipático. Los esfingolípidos son ésteres formados por la unión del alcohol esfingosina y un ácido graso mediante un enlace amida, que da lugar a una molécula denominada ceramida, a la que se une una molécula polar para constituir el esfingolípido completo. Según la naturaleza de la molécula polar que se une a la ceramida se distinguen dos clases de esfingolípidos: Esfingolmielinas. Presentan una molécula de fosforilcolina o fosforiletanolamina unida a la ceramida. Son abundantes en las vainas de mielina que rodean los axones neuronales. Glucoesfingolípidos. Su molécula polar es un glúcido. Estas moléculas desempeñan un papel fundamental como antígenos celulares, es decir, moléculas identificativas de células concretas que permiten el reconocimiento entre ellas. Los antígenos se relacionan con múltiples procesos, principalmente inmunitarios. Se diferencian dos tipos: Cerebrósidos: si el glúcido es un monosacárido (frecuentemente galactosa). Gangliósidos: si el glúcido es un oligosacárido.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
22
11. LÍPIDOS INSAPONIFICABLES Se incluyen en este grupo los lípidos que no contienen ácidos grasos en su composición (tampoco son ésteres) y, por tanto, no pueden formar jabones mediante reacciones de saponificación. Aunque aparecen en menor cantidad que los lípidos saponificables, este grupo comprende algunos compuestos biológicamente muy activos que desempeñan importantes funciones. Se distinguen tres tipos de lípidos insaponificables: terpenos, esteroides y prostaglandinas.
TERPENOS Químicamente, los terpenos son polímeros de la molécula de isopreno (2-metil-1,3-butadieno), por lo que también se les denomina lípidos isoprenoides. Estas moléculas se encuentran en las plantas.
Según el número de isoprenos que componen el terpeno se clasifican en: ▪ Monoterpenos. Contienen dos moléculas de isopreno. Este grupo comprende compuestos volátiles responsables de ciertos aromas (mentol, alcanfor, geraniol,…) ▪ Diterpenos. Están formados por la unión de cuatro isoprenos. El fitol, componente de la clorofila, se incluye en este grupo. ▪ Triterpenos. Formados por seis moléculas de isopreno. Entre ellos se encuentra el escaleno, un precursor del colesterol. ▪ Tetraterpenos. Formados por la unión de ocho moléculas de isopreno. Destacan en este grupo los carotenoides, pigmentos que participan en la fotosíntesis absorbiendo energía lumínica de longitudes de onda distintas a la que absorbe la clorofila. Entre los carotenoides más importantes se encuentran la xantofila (amarilla), el licopeno (rojo) y el -caroteno (anaranjado). El -caroteno es también un precursor de la vitamina A, ya que la rotura del enlace central del -caroteno origina dos moléculas de esta vitamina, que interviene en la visión y protege los tejidos epiteliales. Politerpenos. Formados por muchas moléculas de isopreno. El caucho es el politerpeno más importante y se encuentra en el látex del árbol Hevea brasilensis (árbol del caucho).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
23
ESTEROIDES Constituyen un grupo de lípidos muy importante, que derivan del esterano o ciclopentano perhidrofenantreno (F). Este compuesto cíclico está formado por tres anillos de ciclohexano y uno de ciclo pentano, en donde se unen diferentes radicales.
Los esteroides son sustancias muy abundantes y desempeñan funciones muy variadas. Se diferencian en la existencia de dobles enlaces y en la presencia de diferentes sustituyentes en algunas posiciones. En los siguientes cuadros se exponen los esteroides más importantes y sus funciones.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
24
PROSTAGLANDINAS Las prostaglandinas son lípidos presentes en la mayor parte de los tejidos animales. Se forman por la ciclación de ácidos grasos poliinsaturados, como el ácido araquidónico. Todas estas moléculas poseen una estructura química semejante. Se consideran hormonas locales, ya que actúan en las células que las sintetizan y en la adyacentes. Las funciones de las prostaglandinas son muy variadas: - Estimulan la agregación de plaquetas. - Activan las respuestas inflamatorias de los tejidos al iniciar la vasodilatación de los capilares. - Provocan la subida de la temperatura corporal(fiebre). - Controlan el descenso de la presión arterial al favorecer la eliminación de sustancias en el riñón. - Intervienen el la contracción del útero durante el parto. - Disminuyen la secreción de jugos gástricos. - Regulan la secreción de mucus protector del tracto digestivo (estómago e intestino). Además de las prostaglandinas, existen otros compuestos químicamente relacionados con ellas. Son los tromboxanos y los leucotrienos, que tienen funciones fisiológicas variadas entre las cuales destacan las respuestas inflamatorias. Prostaglandinas, tromboxanos y leucotrienos son conocidos como eicosanoides, por ser moléculas derivadas de ácidos grasos poliinsaturados de 20 átomos de carbono (eicosa=veinte).
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
12. FUNCIONES BIOLÓGICAS DE LOS LÍPIDOS
25
DE LA ACEITUNA AL ACEITE La recogida Tiene lugar entre los meses de octubre y enero, en función de la maduración que se desee y del clima de la región. Cuanto mayor sea la madurez de la oliva, más intenso será el sabor y el aroma del aceite. La recogida debe realizarse de la forma que dañe menos el fruto. Las aceitunas que cayeron solas al madurar suelen estar un poco estropeadas y producen peores aceites.
El lavado y almacenaje Las aceitunas se lavan, con el fin de eliminar las sustancias extrañas que pudieran contaminar el aceite y transmitir sabores extraños. Si se almacenan temporalmente, las aceitunas necesitan estar ventiladas para evitar su fermentación.
La selección Una vez en la almazara, la aceituna se clasifica según su estado y su destino.
El prensado 1 , batido 2 y centrifugado 3 La pasta se prensa (así se extrae aceite en frío, aunque en una cantidad mínima), luego se calienta moderadamente (con resistencias) y, por último, se centrifuga hasta obtener los diferentes aceites de oliva virgen.
La molturación Las aceitunas se trituran hasta formar una pasta que se recoge en unos moldes circulares.
Orujo Es el residuo de los huesos y las pieles de aceituna, que todavía contiene cierta cantidad de aceite que se extrae por medio de disolventes. Una vez eliminados y refinado se mezcla con aceite de oliva virgen y se comercializa como aceite de orujo de oliva.
1 2 Aceite de oliva virgen Es el que se obtiene de la aceituna por medios físicos, sin ayuda de disolventes. Según su calidad se clasifica en:
A
3 Aceite lampante No es apto para el consumo. Presenta una excesiva acidez (superior a 3,3º) y necesita ser refinado.
B
Apto para el consumo
A
Aceite de oliva virgen extra Tiene que tener una acidez inferior a 0,8º y una determinada puntuación en la cata Nuestro de expertos. análisis
Apto para el consumo
Refinado Durante el proceso el aceite pierde su acidez, aroma, sabor y color característicos. Aceite de oliva refinado
B
Aceite de oliva virgen Acidez máxima de 2º y una puntuación en la cata menor que el extra.
Aceite de oliva Es la mezcla de aceite de oliva refinado y aceites de oliva virgen, que le aportan su acidez y su sabor (más intenso cuanto mayor es la proporción de aceite virgen).
OCU-COMPRA MAESTRA 319 OCTUBRE 2007
11
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte II: glúcidos y lípidos
1
ACTIVIDADES TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA. PARTE II: GLÚCIDOS y LÍPIDOS GLÚCIDOS o HIDRATOS DE CARBONO 1. Define químicamente un glúcido e indica con qué otros nombres se conocen. ¿Porqué?. 2. ¿Qué diferencia existe entre osa y ósido?. ¿Y entre holósido y heterósido?. 3. ¿Qué se entiende por hidrólisis de un compuesto?. ¿Porqué los disacáridos y polisacáridos son moléculas hidrolizables?. 4. ¿Cuantos estereoisómeros existen en una aldohexosa?. ¿Y en una aldopentosa?. 5. Construye las fórmulas de los epímeros de la D-Fructosa. 6. Se puede deducir se la D-eritrosa es levógira o dextrógira?. 7. Dibuja todos los pasos de la ciclación de una D-galactosa hasta llegar a la siguiente sustancia: α-DGalactopiranosa. 8. La diabetes es una enfermedad hormonal ocasionada por un mal funcionamiento de páncreas endocrino, que no produce insulina. Esta hormona es responsable, entre otras cosas, de facilitar el paso de glucosa a través de la membrana celular. ¿Qué efectos puede producir la ausencia de glucosa en las células?. 9. Algunos disacáridos de interés biológico son la maltosa, sacarosa y lactosa. Fíjandote en sus fórmulas contesta a las siguientes cuestiones: a) b) c) d) e) f) g)
¿De qué monómeros está formado cada uno de estos disacáridos?. ¿Qué carbonos intervienen en la formación del enlace glucosídico en cada caso?. ¿Son anoméricos o no?. ¿Cuáles son los grupos funcionales implicados en la formación del enlace glucosídico?. ¿Qué se desprende?. ¿Su formación ha liberado o consumido energía?. ¿Cuáles de estos disacáridos son reductores?. ¿Porqué?.
10. ¿Porqué el almidón, celulosa y glucógeno son polisacáridos diferentes si todos están formados por moléculas de D-glucopiranosa?. 11. Porqué la glucosa se almacena en forma de almidón en los vegetales, en vez de estar libre en la célula. 12. ¿Porqué la celulosa no es un nutriente?. ¿Cuál es su importancia en la alimentación?. 13. Habrás visto en anuncios publicitarios papillas infantiles compuestas a base de cereales dextrinados. ¿Qué significa esto?. ¿Qué beneficio ofrece a los bebés?. 14. ¿Cuál es la importancia biológica de los siguientes glúcidos: celulosa, ribulosa, lactosa, galactosa, quitina, gliceraldehido y N-acetil-glucosamina?.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida. Parte II: glúcidos y lípidos
2
LÍPIDOS 15. ¿Cuál es característica fundamental de los lípidos, que permite reunirlos en un grupo y cuál es la que diferencia entre los dos grupos principales?. 16. Señala a qué tipo de lípido son estas sustancias: ácido cólico, aceite, gangliósido, aldosterona, xantofila, cera, progesterona, esfingomielina y vitamina A. 17. ¿De qué depende que los ácidos grasos sean sólidos o líquidos?. ¿A qué se denominan ácidos grasos esenciales y qué importancia tienen?. 18. Completa las siguientes reacciones, indicando el tipo de compuesto que se origina: O a) CH3-(CH2)10-C-O-CH2 O I CH3-(CH2)10-C-O-CH O I CH3-(CH2)10-C-O-CH2
+ 3 NaOH →
b) Ácido linoleico + 4 O2 → 19. Cómo forman los jabones emulsiones estables con las grasas. ¿Qué sustancias hay en nuestro organismo que también emulsionan las grasas?. Busca en alguna enciclopedia cómo se fabrica el jabón casero. 20. ¿Porqué las grasas son reservas de energía a largo plazo?. ¿Qué las diferencia de las ceras?. 21. Cuáles de las siguientes moléculas son anfipáticas: Colesterol, vitamina A, ácido lignocérico, triacilglicérido, cefalina. 22. ¿Porqué los lípidos saponificables simples son muy insolubles en agua mientras que los lípidos saponificables complejos son algo solubles?. 23. Las vitaminas liposolubles A, E y K son terpenos compuestos por 5 unidades de isopreno. ¿Porqué crees que las industrias lácteas añaden estas vitaminas a la leche desnatada?. 24. Porqué la aspirina es antipirética, antiinflamatoria y analgésica. Porqué la aspirina y otros antiinflamatorios pueden provocar la aparición de ulceras gastroduodenales. 25. Define los conceptos de: lípido, anfipático, jabón, hidrófobo, esterificación, manteca, micela, emulsión y polar. 26. Lee el artículo “Relación del colesterol con el tipo de dieta”, y responde a las cuestiones que se plantean.
Biología 2º Bachillerato
GLÚCIDOS EJERCICIO TIPO DE ISOMERÍA ESPACIAL EN MONOSACÁRIDOS A partir de las siguientes fórmulas de monosacáridos, se pide: 1. Señalar los carbonos asimétricos presentes. 2. Calcular el número de isómeros espaciales o estereoisómeros posibles de cada uno de ellos. 3. Indicar si pertenecen a la serie D o L 4. Formular y nombrar los enantiómeros de cada uno de ellos. 5. Formular y nombrar un epímero de cada uno de ellos. 6. Formular y nombrar los anómeros de cada uno de ellos.
CHO H C OH HO C H HO C H H C OH CH2OH GALACTOSA
CH2OH C= O H C OH HO C H H C OH CH2OH SORBOSA
Biología 2º Bachillerato
Actividades refuerzo
1
MONOSACÁRIDOS. ACTIVIDADES ISOMERÍA ESPACIAL 1. Señala los CARBONOS ASIMÉTRICOS y calcula el NÚMERO DE ESTEREOISÓMEROS posibles de cada uno de los siguientes monosacáridos.
2. Escribe la fórmula de los ENANTIÓMEROS de los siguientes monosacáridos: D-eritrulosa; D-idosa; L-ribulosa: L-arabinosa y D-sedoheptulosa. 3. Qué monosacáridos del ejercicio 1 son EPÍMEROS de los siguientes:
Biología 2º Bachillerato
Actividades refuerzo
2
4. Señala en las siguientes fórmulas, cuáles son ANOMÉROS y .
5. ¿Existen ANÓMEROS y de los siguientes monosacáridos?. Justifica la respuesta. D-lixosa; D-sicosa; D-ribulosa; D-gliceraldehído; L-idosa. 6. Dibuja las fórmulas de los ANÓMEROS y de cada uno de los siguientes monosacáridos, y nombra cada uno de ellos según su estructura cíclica.
BIOLOGÍA 2º BACHILLERATO LÍPIDOS. ACTIVIDAD TIPO DE REACCIONES QUÍMICAS.
Completa las siguientes reacciones químicas, escribiendo: Fórmulas y tipos de productos resultantes Tipo de reacción química llevada a cabo a)
CH3- (CH2)18-COOH + HO-CH3 → ácido araquídico
b)
metanol
CH3- (CH2)7-CH=CH-(CH2)7-COOH + NaOH → ácido oleico
c)
CH3-(CH2)5-CH=CH-(CH2)7-COOH + 2 O2 → ácido palmitoleico
+
d)
ácidos grasos
e)
→
glicerina
+ NaOH →
triglicérido
f)
+ 3 H2O →
triglicérido
TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA PARTE III. PROTEÍNAS y ÁCIDOS NUCLEICOS 1. PROTEÍNAS y ÁCIDOS NUCLEICOS: BIOPOLÍMEROS PORTADORES DE LA INFORMACIÓN GENÉTICA 2. PROTEÍNAS: CONCEPTO, FUNCIONES y CLASIFICACIÓN 3. LOS AMINOÁCIDOS
▪ ▪
Clasificación
Propiedades de los aminoácidos
4. EL ENLACE PEPTÍDICO 5. ESTRUCTURA DE LAS PROTEÍNAS ▪ ▪ ▪ ▪
Estructura primaria Estructura secundaria Estructura terciaria Estructura cuaternaria
6. PROPIEDADES DE LAS PROTEÍNAS ▪ ▪ ▪
Solubilidad Especificidad Desnaturalización
7. CLASIFICACIÓN DE LAS PROTEÍNAS 8. FUNCIONES BIOLÓGICAS DE LAS PROTEÍNAS 9. LOS ÁCIDOS NUCLEICOS: CONCEPTO, TIPOS y FUNCIONES. 10. LOS NUCLEÓTIDOS: COMPONENTES DE LOS ÁCIDOS NUCLEICOS 11. FUNCIONES DE LOS NUCLEÓTIDOS 12. POLINUCLEÓTIDOS 13. ÁCIDO DESOXIRRIBONUCLEICO (ADN) 13.1. ESTRUCTURA DEL ADN. Modelo de la doble hélice 13.2. TIPOS DE ADN
13.3. DESNATURALIZACIÓN e HIBRIDACIÓN DEL ADN
14. ÁCIDO RIBONUCLEICO (ARN) ▪ ARN mensajero (ARNm) ▪ ARN ribosómico (ARNr) ▪
ARN de transferencia o ARN transferente (ARNt)
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
2
1. PROTEÍNAS y ÁCIDOS NUCLEICOS: BIOPOLÍMEROS PORTADORES DE LA INFORMACIÓN GENÉTICA Las proteínas y los ácidos nucleicos son biomoléculas que presentan una serie de características comunes, que conviene resaltar antes de empezar su estudio por separado. Proteínas y ácidos nucleicos son biopolímeros o macromoléculas, formadas por la unión mediante enlaces covalentes de moléculas más sencillas (monómeros). Las proteínas se forman por la polimerización de aminoácidos y las ácidos nucleicos por la polimerización de nucleótidos. En las proteínas y en los ácidos nucleicos, el ordenamiento o la secuencia de los monómeros (aminoácidos y nucleótidos) es característico y particular de las distintas cadenas moleculares de las proteínas y de los ácidos nucleicos, y es el que determina su función biológica. El ordenamiento de los monómeros no es arbitrario. En los ácidos nucleicos existe unas instrucciones almacenadas en forma de secuencias de nucleótidos que deciden el ordenamiento de los aminoácidos de las proteínas. Por esta razón, los ácidos nucleicos y las proteínas son biopolímeros portadores de la información genética, ya que el ordenamiento de sus monómeros no obedece al azar, sino a instrucciones heredadas de nuestros antecesores a lo largo del proceso evolutivo. En la célula la información genética contenida en los ácidos nucleicos se utiliza para fabricar proteínas.
2. PROTEÍNAS: CONCEPTO, FUNCIONES y CLASIFICACIÓN Las proteínas son biomoléculas orgánicas formadas, al menos, por cuatro bioelementos: C, H, O y N; pero muchas de ellas contienen S, P y otros bioelementos (Fe, Cu, I, Mg, etc.,…). Químicamente las proteínas son polímeros de moléculas relativamente sencillas, no hidrolizables, denominadas aminoácidos (aa). La unión de aminoácidos origina péptidos, que según su tamaño molecular pueden ser: Oligopéptidos: formados por no más de 10 aminoácidos. Polipéptidos: formados por más de 10 aminoácidos. Las proteínas son polipéptidos, formados por más de 50 aminoácidos o con un peso molecular mayor de 5.000 daltons, normalmente entre 6.000 y 106 daltons, por lo que se trata de macromoléculas. Las proteínas se clasifican en dos grandes grupos: ▪ Holoproteínas: formadas exclusivamente por aminoácidos. ▪ Heteroproteínas: formadas por aminoácidos más otros componentes no proteicos. La parte no proteica se la designa como el grupo prostético, y dependiendo de su naturaleza química se pueden diferenciar: Glucoproteínas: el grupo prostético es un glúcido. Lipoproteínas: el grupo prostético es un lípido. Fosfoproteínas: el grupo prostético es un ácido fosfórico. Nucleoproteínas: cuando contienen nucleótidos. Cromoproteínas: si el grupo prostético es un pigmento. Las proteínas son los compuestos orgánicos más abundantes de la materia viva, constituyendo alrededor del 50% de su peso seco. Las funciones que desempeñan son muy variadas: Estructural: las proteínas son el principal material de construcción de los seres vivos, formando parte de casi todas sus estructuras: desde la membrana celular hasta ser el principal componente del tejido conjuntivo (colágeno), el pelo o las uñas (queratina). Enzimática: las reacciones metabólicas están catalizadas y controladas por unas proteínas, denominadas enzimas. Inmunológica: los anticuerpos, que intervienen en la defensa del organismo frente a los agentes patógenos, son proteínas. Hormonal: algunas hormonas, como la insulina y el glucagón, que regulan la concentración de glucosa en sangre, son proteínas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
3
Transporte: pueden transportar gases, como la hemoglobina que transporta el oxígeno, o lípidos, como las lipoproteínas de la sangre. Movimiento: las proteínas son elementos esenciales en el movimiento muscular, ya que la actina y la miosina de las células musculares, son las responsables de la contracción de los músculos. De reserva: algunas proteínas sirve de reserva de aminoácidos durante el desarrollo biológico, como la ovoalbúmina del huevo, la caseína de la leche o la gliadina del trigo. Homeostática: ciertas proteínas mantienen el equilibrio osmótico del medio celular y extracelular.
3. LOS AMINOÁCIDOS Los aminoácidos son los componentes de las proteínas. Químicamente son ácidos orgánicos que presentan un grupo amino (-NH2), un grupo carboxilo (-COOH) y un átomo de hidrógeno (H) unidos covalentemente a un carbono central, que se designa como carbono . El enlace que le queda al carbono está ocupado por un grupo lateral o un grupo R (de radical) que varía en los distintos aminoácidos. Existen 20 aminoácidos proteicos o -aminoácidos, que son los constituyentes básicos de las proteínas. Además, hay otros 150 aminoácidos que se encuentran libres o combinados en las células y en los tejidos, pero que no se encuentran en las proteínas, y se conocen como aminoácidos no proteicos. Algunos de ellos son intermediarios de las reacciones metabólicas (citrulina y ornitina) o forman parte de las paredes bacterianas, como el ácido-D-glutámico.
Clasificación Los aminoácidos se clasifican atendiendo a las características de su grupo radical, según su ionización, polaridad y reactividad, en: ▪ Neutros polares: no tienen carga eléctrica neta, y su grupo R contiene grupos polares (alcohol, tiol o amida), por lo que son solubles en agua. ▪ Neutros apolares: no tienen carga eléctrica neta, y su grupo R está formado por largas cadenas hidrocarbonadas, lo que hace que sean poco solubles en agua. ▪ Ácidos: cuando el grupo R lleva un grupo ácido, de manera que a pH neutro, tienen carga negativa. ▪ Básicos: cuando el grupo R lleva un grupo básico (amino), de tal modo que a pH neutro, tienen carga eléctrica positiva. La mayoría de los aminoácidos pueden sintetizarse unos a partir de otros, pero algunos no pueden ser sintetizados y deben obtenerse de la dieta, son los denominados aminoácidos esenciales. Los aminoácidos esenciales son diferentes para cada especie. En la especie humana los aminoácidos esenciales son diez: Thr, Lys, Arg, His, Val, Leu, Ile, Met, Phe y Trp.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
4
PROPIEDADES DE LOS AMINOÁCIDOS Las propiedades de los aminoácidos están determinadas por el radical, que es distinto en cada aminoácido, y determina sus propiedades físicas y químicas. Los aminoácidos son sólidos, solubles en agua (excepto los hidrófobos), cristalizables, incoloros o poco coloreados y con un punto de fusión alto, por encima de 200 º C. Además de las propiedades mencionadas, hay dos propiedades que conviene destacar: Estereoisomería y actividad óptica: al igual que los monosacáridos, los aminoácidos poseen al menos un carbono asimétrico, que es el carbono , excepto la glicina que no tiene ninguno. Debido a esto, los aminoácidos presentan estereoisomería y actividad óptica. Los aminoácidos pueden presentar dos configuraciones espaciales, D y L, dependiendo de la posición del grupo amino (-NH2), a la derecha e izquierda, respectivamente del carbono . Estas dos configuraciones espaciales se denominan estereoisómeros. Ambos estereisómeros son imágenes especulares y no superponibles. Todos los aminoácidos proteicos son de la serie L, pues las células los sintetizan utilizando enzimas estereoespecíficas.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
5
Los aminoácidos muestran, además, actividad óptica, denominándose dextrógiros (+) o levógiros (-), según desvíen la luz polarizada hacia la derecha o hacia la izquierda. De la misma forma que los glúcidos, la disposición D o L es independiente de la actividad óptica: un L-aminoácido puede ser dextrógiro o levógiro. Carácter anfótero: la presencia de los grupos carboxilo y amino confiere a los aminoácidos un comportamiento ácido-base o comportamiento anfótero, que significa que se comportan como ácidos o bases dependiendo el pH del medio acuoso en el que estén disueltos. Cuando los aminoácidos se encuentran disueltos en agua (pH=7) los grupos amino aceptan protones, comportándose como bases, y quedan cargados positivamente (NH3+) y los grupos carboxilo, desprenden protones, comportándose como ácidos, y quedan cargados negativamente (COO-), por lo que los aminoácidos están doblemente ionizados y forman iones híbridos, que se denominan formas dipolares o zwitteriones, y poseen igual número de cargas positivas y negativas. El valor del pH en el que un aminoácido tiende a adoptar la forma dipolar neutra se denomina punto isoeléctrico, y es diferente para cada aminoácido. Cuando el valor del pH del medio se desvía del punto isoeléctrico, el aminoácido se comportará como ácido o base (en medio ácido como base y en medio alcalino como ácido), permitiendo la regulación del pH.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
6
4. EL ENLACE PEPTÍDICO Los aminoácidos se pueden unir entre sí mediante el denominado enlace peptídico (un enlace amida de tipo covalente). El enlace peptídico se establece entre el grupo carboxilo (-COOH) de un aminoácido y el grupo amino (-NH2) de otro, liberándose una molécula de agua. La unión de dos aminoácidos origina un compuesto que denominamos dipéptido.
Los átomos de C, N y O que forman parte del enlace comparten electrones, lo que hace que aparezcan dos formas resonantes. Se puede así afirmar, que el enlace peptídico tiene un carácter parcial de doble enlace. Este hecho impide que se efectúen torsiones alrededor del enlace peptídico, lo que determina que los átomos de C, N y O se sitúen en el mismo plano. Solamente se pueden efectuar torsiones alrededor en los carbonos . El dipéptido presenta un grupo amino y un grupo carboxilo libres, los cuales pueden unirse a otros aminoácidos, y así sucesivamente. De esta forma se originan cadenas de aminoácidos (cadenas peptídicas), de longitud variable, que según el número de aminoácidos se denominan tripéptidos, tetrapéptidos, etc., hasta polipéptidos. El resultado es que la cadena peptídica presenta una forma más o menos en zig-zag. En los enlaces peptídicos no participan los radicales de los aminoácidos, que quedan “colgando” de la cadena peptídica.
Biología 2º Bachillerato
7
Tema 1. La base físico-química de la vida.
Por convenio, el extremo amino se considera el comienzo de la cadena peptídico y el grupo carboxilo el final. amino →
← carboxilo
Como al establecer cada enlace peptídico se libera una molécula de agua, también será posible la reacción contraria; es decir, la ruptura de dichos enlaces por acción de agua; los péptidos son polímeros hidrolizables y su hidrólisis total origina aminoácidos.
5. ESTRUCTURA DE LAS PROTEÍNAS Cada proteína está compuesta por una o varias cadenas polipeptídicas y, aunque solo hay 20 aminoácidos, en cada célula existen miles de proteínas distintas con funciones características. Las cadenas polipeptídicas no son moléculas lineales, sino que se pliegan en el espacio y adquieren una forma característica, que determina su función biológica. La conformación o la estructura de una proteína es la disposición espacial que adoptan las cadenas polipeptídicas. La compleja estructura de las proteínas puede estudiarse en diferentes niveles de complejidad, conocidos como estructura primaria, secundaria, terciaria y cuaternaria. Cada nivel informa de la disposición espacial del nivel anterior. ESTRUCTURA PRIMARIA La estructura primaria de una proteína es la secuencia de aminoácidos de la cadena polipeptídica, es decir, el número, tipo y orden de los aminoácidos que constituyen la proteína. La secuencia de aminoácidos es diferente en cada proteína y determina la conformación tridimensional de la proteína y, por tanto, su función biológica. Siempre existe un extremo con un aminoácido cuyo grupo amino está libre y otro extremo con un aminoácido con un grupo carboxilo libre. Por convenio, lo aminoácidos se numeran comenzando por el que posee el extremo amino libre.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
8
ESTRUCTURA SECUNDARIA La estructura secundaria de una proteína es la forma en que la secuencia de aminoácidos se pliega en el espacio. A medida que los aminoácidos se van uniendo para formar la cadena polipeptídica, giran y adoptan una disposición espacial lo más estable posible, que es la estructura secundaria. Existen dos tipos básicos de estructura secundaria: -hélice y la lámina plegada o lámina . En las proteínas coexisten ambos, aunque uno de ellos puede predominar sobre el otro. Estructura en -hélice: el nombre alude a la -queratina, proteína muy abundante en las células de la epidermis. La estructura en -hélice se produce cuando una cadena polipeptídica gira sobre sí misma, de manera que la molécula adopta una disposición en hélice, donde los radicales se sitúan hacia el exterior. La -hélice se mantiene estable gracias a la formación de puentes de hidrógeno entre los grupos –NH y –CO de los enlaces peptídicos que quedan enfrentados. Si los puentes de hidrógeno se rompen, la estructura secundaria se pierde.
Lámina plegada o lámina : este tipo de estructura está presente en la -queratina, presente en uñas, pelos y plumas. Las cadenas polipeptídicas se disponen en paralelo y se pliegan formando una especie de fuelle o lámina plegada en zigzag, quedando unidas transversalmente mediante puentes de hidrógeno análogos a los que estabilizan la -hélice. Las cadenas laterales de los aminoácidos se disponen alternativamente por encima y debajo de la lámina plegada.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
9
ESTRUCTURA TERCIARIA Las proteínas no se disponen linealmente en el espacio, sino que sufren nuevos plegamientos que hacen que la molécula adopte una disposición espacial tridimensional estable denominada estructura terciaria. La estructura terciaria se mantiene estable gracias a la formación de diferentes enlaces entre los radicales de los aminoácidos, que pueden ser: Puentes disulfuro: son enlaces covalente fuertes entre dos grupos –SH pertenecientes de dos moléculas de cisteina. Fuerzas electrostáticas: son enlaces de tipo iónica entre grupos con cargas eléctricas opuestas. Puentes de hidrógeno: se establecen entre grupos polares no iónicos en los que existen cargas parciales en su cadena lateral. Fuerzas de Van der Waals e interacciones hidrofóbicas: son las uniones más débiles y se producen entre aminoácidos polares. En general, existen dos tipos de estructuras terciarias en las proteínas: Globulares: poseen un alto grado de plegamiento y dan lugar a estructuras con forma de esfera. Las proteínas globulares suelen ser solubles en agua y presentan funciones enzimáticas, de transporte u hormonales. Las proteínas globulares suelen tener diferentes fragmentos con -hélice y láminas , pero las disposiciones suelen disponerse en la periferia y las hélices en el centro de la molécula. Además, las proteínas globulares se doblan de tal manera que, en solución acuosa, los restos hidrófilos quedan hacia el exterior y los hidrófobos hacia el interior y, por el contrario, en un ambiente lipídico, los restos hidrófilos quedan en el interior y los hidrófobos en el exterior. Filamentosas: el plegamiento de la cadena polipeptídica es menor, por lo que estas estructuras presentan formas alargadas. Las proteínas filamentosas son insolubles en agua y disoluciones salinas y suelen tener función estructural, como la queratina, el colágeno o la elastina.
Proteína filamentosa
Proteína globular
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
10
ESTRUCTURA CUATERNARIA Cuando una proteína está formada por varias cadenas polipeptídicas, adquiere un nivel estructural superior, la estructura cuaternaria. Cada cadena polipeptídica es una subunidad de la proteína o protómero, y la estructura cuaternaria es, sencillamente, la disposición relativa de las subunidades proteicas entre sí. La unión entre las subunidades se realiza mediante los mismos enlaces que mantienen la estructura terciaria. Dependiendo del número de subunidades tendremos dímeros, tetrámeros, pentámeros, etc. Un ejemplo de estructura cuaternaria es la hemoglobina, formada por cuatro subunidades de globina (dos y dos ) unidas a una parte no proteica (el grupo hemo).
6. PROPIEDADES DE LAS PROTEÍNAS Las propiedades de las proteínas están determinadas por su composición química y estructura. Solubilidad Normalmente las proteínas fibrilares o filamentosas son insolubles en agua, mientras que las proteínas globulares son solubles. La solubilidad de estas proteínas se debe a que los radicales polares se localizan en la periferia de la proteína en o con las moléculas de agua, formándose una capa de solvatación de agua alrededor de cada proteína que impide la unión entre ellas. Debido a su elevada masa molecular, cuando las proteínas son solubles forman dispersiones coloidales en el agua y no se difunden generalmente a través de las membranas biológicas. La solubilidad se puede ver afectada por diferentes factores, como el pH, la temperatura o la concentración salina. Así por ejemplo, al añadir sales al agua, estas compiten con las cargas de los aminoácidos por las moléculas de agua, se rompe la capa de solvatación que rodea a cada proteína, y estas acaban precipitando. Especificidad A diferencia de las biomoléculas estudiadas hasta ahora, las proteínas son moléculas específicas, es decir, cada especie posee algunas proteínas que otros organismos no tienen. Incluso proteínas que presentan la misma función y una estructura tridimensional muy semejante suelen tener una secuencia de aminoácidos algo diferente en cada especie. Este hecho permite llevar a cabo estudios
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
11
filogenéticos y establecer el grado de parentesco entre especies, analizando las semejanzas que existen entre algunas de sus proteínas. Además, incluso dentro de la misma especie, los individuos se diferencian por las proteínas que tienen. La especificidad de las proteínas es la causa del rechazo en el transplante de órganos y en las transfusiones sanguíneas. Desnaturalización La función biológica de una proteína depende de su estructura tridimensional, también denominada conformación. Cualquier cambio que suponga una alteración de esta conformación, afecta a la funcionalidad de una proteína. Cuando una proteína sufre una alteración en su estructura o conformación y deja de ser funcional, hablamos de desnaturalización. Los factores que pueden producir la desnaturalización de las proteínas son variados: aumento de temperatura, variaciones de pH, cambios en la concentración salina, etc. En la desnaturalización proteica, no se rompen los enlaces peptídicos, pero sí los enlaces que mantienen la estructura terciaria y secundaria, alterándose el plegamiento de las cadenas peptídicas, y adquiriendo la proteína una conformación abierta. La desnaturalización puede ser: Irreversible: cuando los factores responsables han sido tan intensos o tan duraderos que la proteína no puede recuperar su forma original. Un ejemplo es la coagulación por el calor de la clara del huevo, por desnaturalización de la ovoalbúmina. Reversible: si los factores responsables actúan con escasa intensidad y durante poco tiempo, la proteína recupera su conformación original cuando cesa la acción de los factores responsables de la desnaturalización. Un ejemplo sería el moldeado del cabello, debido a la desnaturalización de la queratina.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
12
7. CLASIFICACIÓN DE LAS PROTEÍNAS 1. HOLOPROTEÍNAS: formadas exclusivamente por aminoácidos A) PROTEÍNAS FILAMENTOSAS: insolubles en agua. Aparecen principalmente en animales. Colágeno: tejido conjuntivo, cartílago y hueso Queratina: cabello, uñas, plumas, cuernos, pezuñas,... Elastina: tendones, vasos sanguíneos B) PROTEÍNAS GLOBULARES: solubles en agua o disoluciones polares. Histonas: asociadas al ADN Prolaminas*: semillas vegetales ( zeína del maíz, gliadina del trigo, hordeína de la cebada) Gluteínas*: orizanina del arroz, glutenina del trigo. ( * Insolubles en agua ) Albúminas: seroalbúmina de la sangre, ovoalbúmina del huevo, lactoalbúmina de la leche, globina de la hemoglobina Globulinas: ovoglobulina del huevo, lactoglobulina de la leche, gammaglobulinas o inmunoglobulinas (anticuerpos) 2. HETEROPROTEÍNAS: formadas por una parte proteica de aminoácidos y un grupo prostético (no proteico) A) CROMOPROTEÍNAS: el grupo prostético es una sustancia coloreada. PORFIRINAS: el grupo prostético es un anillo tetrapirrólico o porfirina. En el centro de este anillo aparece un catión metálico: Grupo hemo: catión Fe2+ . Hemoglobina, Mioglobina (transportan O2), Citocromo C (transporta electrones) Grupo hemino: catión Fe3+. Peroxidasas, Catalasas. NO PORFIRINAS: Hemocianina: contiene Cu, aparece en crustáceos y moluscos Hemeritrina: contiene Fe, aparece en anélidos y braquiópodos B) GLUCOPROTEÍNAS: el grupo prostético es un glúcido Hormonas: FSH, LH, TSH Proteoglucanos: liquido sinovial, tendones, huesos y cartílagos Glucoproteínas de las membranas celulares Inmunoglobulinas (anticuerpos) C) LIPOPROTEÍNAS: grupo prostético formado por ácidos grasos Lipoproteínas de las membranas celulares Lipoproteínas de la sangre: transportan lípidos D) FOSFOPROTEÍNAS: el grupo prostético es el ácido fosfórico (H3PO4). Caseína: en la leche Vitelina: en el huevo E) NUCLEOPROTEÍNAS: el grupo prostético es un ácido nucleico. Son nucleoproteínas las asociaciones de histonas o protaminas con ADN.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
8. FUNCIONES BIOLÓGICAS DE LAS PROTEÍNAS
13
Biología 2º Bachillerato
14
Tema 1. La base físico-química de la vida.
9. LOS ÁCIDOS NUCLEICOS: CONCEPTO, TIPOS y FUNCIONES. N y P.
Los ácidos nucleicos son biomoléculas de la mayor importancia biológica, formadas por C, H, O,
Son macromoléculas o polímeros formados por la unión de moléculas hidrolizables denominadas nucleótidos. Todos los seres vivos contienen dos tipos de ácidos nucleicos: - ADN o DNA (ácido desoxirribonucleico). Se encuentra en el núcleo celular y en algunos orgánulos, como las mitocondrias y los cloroplastos. - ARN o RNA (ácido ribonucleico). Se encuentra en el núcleo y en el citoplasma, formando parte de los ribosomas. Los virus poseen solamente un tipo de ácido nucleico, bien ADN o ARN. El ADN es el material genético, portador de los caracteres hereditarios, que cumple dos funciones en los seres vivos: ▪ Almacena la información genética, lo que significa que: ─ El ADN contiene la información para el crecimiento y desarrollo de un ser vivo, con las características típicas de su especie. ─ El ADN contiene las instrucciones para sintetizas proteínas, y por tanto dirige la síntesis de proteínas en la célula. ▪ Transmite la información genética en cada generación, copiándose exactamente antes de que la célula se divida, mediante el proceso de replicación o duplicación del ADN. La función del ARN es expresar la información genética, es decir, ejecutar las órdenes contenidas en el ADN. Por tanto, el ARN es el encargado de sintetizar las proteínas. En la célula la información genética se transmite de ADN a ADN, y fluye del ADN al ARN y de éste a las proteínas. Este flujo de información se conoce como “el dogma central de la biología molecular”. ADN → ARN → Proteínas
10. LOS NUCLEÓTIDOS: NUCLEICOS
COMPONENTES
DE
LOS
ÁCIDOS
Los componentes de los ácidos nucleicos son los NUCLEÓTIDOS. Los nucleótidos están formados por tres componentes: ácido fosfórico, una pentosa y una base nitrogenada, por lo que se trata de moléculas hidrolizables. La pentosa puede ser de dos tipos: ─ Ribosa (-D-ribofuranosa): forma parte de los nucleótidos del ARN denominados ribonucleótidos. ─ Desoxirribosa (-2-desoxi-D-ribofuranosa): forma parte de los nucleótidos del ADN o desoxirribonucleótidos. Las bases nitrogenadas de los nucleótidos son derivadas de dos compuestos heterocíclicos: purina y pirimidina, por lo que se clasifican en: ▪ Bases púricas: derivan de la purina. Las más importantes son: ─ Adenina (A): se encuentra tanto en el ADN como en el ARN. ─ Guanina (G): se encuentra tanto en el ADN como en el ARN. ▪ Bases pirimidínicas: derivan de la pirimidina. Las más importantes son: Citosina (C): se halla tanto en el ADN como en el ARN. ─ Timina (T): se encuentra sólo en el ADN. ─ Uracilo (U): se encuentra sólo en el ARN.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
15
La unión entre una base nitrogenada (púrica o pirimidínica) y una molécula de pentosa, origina un NUCLEÓSIDO. La unión entre ambos componentes se lleva a cabo mediante un enlace de tipo covalente, denominado enlace N-glucosídico, que se establece entre el nitrógeno 1 de las bases pirimidínicas o e 9 de las base púricas y el átomo 1´de la pentosa. Base nitrogenada + Pentosa = Nucleósido Los ribonucleósidos se designan con el nombre de la base nitrogenada, haciéndola termina en –osina si es una base púrica, y en –idina si se trata de una base pirimidínica. Los desoxirribonucleósidos se nombran igual, pero anteponiendo el prefijo desoxi-. La unión entre un nucleósido y un ácido fosfórico origina un NUCLÉOTIDO. Los nucleótidos son ésteres fosfóricos de los nucleósidos, de manera que entre el ácido fosfórico y el grupo –OH del carbono 5´de la pentosa se forma un enlace éster con la liberación de una molécula de agua. Los nucleótidos se nombran habitualmente con el nombre del nucleósido, eliminando la letra -a final y añadiendo el número de fosfatos unidos( monofosfato, difosfato, trifosfato). Frecuentemente se suelen emplear siglas para designarlos, como AMP que significa adenosín monofosfato.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
16
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
17
11. FUNCIONES DE LOS NUCLEÓTIDOS Los nucleótidos son moléculas de gran interés biológico, ya que, además de constituir los ácidos nucleicos, llevan a cabo diferentes funciones en los seres vivos. Algunas de ellas son:
Moléculas acumuladoras y donantes de energía. La energía desprendida en las reacciones metabólicas se utiliza para fabricar nucleótidos que actúan como monedas energéticas en la célula. Los dos principales son el ADP (adenosín difostato) y el ATP (adenosín trifosfato), que almacenan la energía en los enlaces fosfato-fosfato. Este tipo de enlaces son enlaces de alta energía, lo que quiere decir que se requiere una gran cantidad de energía para su formación, y por tanto su rotura libera la misma cantidad de energía (8 kcal/mol). La energía desprendida en las reacciones metabólicas se emplea para fabricar ATP a partir de ADP, y cuando se necesita energía se utiliza la almacenada en el ATP que se convierte de nuevo en ADP. De esta manera, el sistema ADP/ATP constituye una forma eficaz de transferir energía entre reacciones metabólicas.
Mensajeros químicos El adenosín monofosfato cíclico (AMPc) desempeña un papel clave en el desencadenamiento de las respuestas celulares ante estímulos del medio. Las hormonas y los neurotransmisores son moléculas mensajeras que se encuentran en el medio celular y se unen a ciertos receptores de las membranas celulares. Esto favorece la síntesis del AMPc, que actúa como mensajero químico dentro de la célula, permitiendo la ejecución de varios procesos bioquímicos, que en última instancia, originan una respuesta celular.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
18
Coenzimas Existen ciertos nucleótidos que actúan como coenzimas (moléculas necesarias para muchas enzimas) en algunas reacciones metabólicas importantes. Este es el caso de: Nicotínamín-adenín-dinucleótido (NAD+). Es un derivado de la vitamina PP o nicotinamida. Nicotínamín-adenín-dinucleótido fosfato (NADP+) Flavín-adenín-dinucleótido (FAD). Es un derivado de la riboflavina o vitamina B2. Estos tres coenzimas participan en reacciones de deshidrogenación, fundamentales en el metabolismo celular. Captan protones y electrones de moléculas oxidadas y los ceden fácilmente a otras moléculas. Al captar protones y electrones quedan como NADH, NADPH y FADH2 (formas reducidas).
12. POLINUCLEÓTIDOS La unión de un gran número de nucleótidos, mediante enlaces covalentes, formando largas cadenas de nucleótidos, da lugar a los polinucleótidos o ácidos nucleicos. La unión entre nucleótidos se realiza mediante enlaces o puentes fosfodiéster (enlace nucleotídico), que se establecen entre el grupo fosfato unido al carbono 5´ de un nucleótido y el grupo hidroxilo del carbono 3´ de una pentosa. Como la unión de los nucleótidos se produce entre pentosas y fosfatos, las bases nitrogenadas no participan en los enlaces. Se establecen así largas cadenas sin ramificar formadas por la secuencia pentosa-fosfato-pentosa-fosfato,… en las que las bases nitrogenadas quedan “colgando” lateralmente de las pentosas. Así el esqueleto de los polinucleótidos lo constituyen los grupos alternantes de pentosas y fosfatos y la secuencia de bases nitrogenadas es la que proporciona la especificidad a la cadena polipeptídica formada, y por tanto, la que determina la información genética. En todos los polinucleótidos existe un extremo (denomina extremo 3´) con una pentosa con el grupo –OH del carbono 3´ libre, y otro extremo (llamado extremo 5´), donde se localiza un grupo fosfato libre unido al carbono 5´ de otra pentosa. Para indicar la composición del polinucleótido se suele indicar la secuencia de bases nitrogenadas y los extremos 5´y 3´. Ya hemos visto que existen dos tipos de ácidos nucleicos o polinucleótidos: ADN, que es un polinucleótido compuesto de desoxirribonucleótidos de A, G, C y T. ARN, que es un polinucleótido compuesto de ribonucleótidos de A, G, C y U.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
19
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
20
13. ÁCIDO DESOXIRRIBONUCLEICO (ADN) Como ya hemos visto, el ADN está formado por la unión de desoxirribonucleótidos, es decir, nucleótidos que contienen desoxirribosa. En cuanto a las bases nitrogenadas pueden ser adenina, guanina, citosina y timina, pero nunca uracilo. Con excepción de algunos virus (como el X174), el ADN está constituido por dos largas cadenas de nucleótidos unidas entre sí en toda su longitud. Esta doble cadena puede disponerse en forma lineal (ADN del núcleo de las células eucariotas) o en forma circular (ADN de las células procariotas, de ciertos virus y de las mitocondrias y cloroplastos). La molécula de ADN porta la información genética necesaria para el crecimiento y desarrollo biológico de un individuo y contiene los mensajes e instrucciones para que las células realicen sus funciones. Es decir, lleva codificada la información a partir de la cual se forma un organismo vivo, por lo que constituye el material genético. 13.1. ESTRUCTURA DEL ADN El ADN es una molécula altamente estructurada en la que, de manera semejante a las proteínas, se distinguen varios niveles de complejidad: estructura primaria, estructura secundaria y estructura terciaria.
Estructura primaria La estructura primaria viene determinada por la secuencia de nucleótidos de una cadena de polinucleótidos. En uno de los extremos de dicha cadena existe un fosfato libre (extremo 5´) y en el otro un grupo –OH libre del carbono 3´ de una pentosa (extremo 3´). Como todos los nucleótidos contienen desoxirribosa, la diferencia entre las moléculas de ADN radica en el orden de las bases nitrogenadas que cuelgan de las pentosas. Por tanto, la secuencia precisa en la que aparecen los cuatro tipos de bases (A, G, C y T) del ADN es la que determina las características biológicas del individuo.
Estructura secundaria La estructura secundaria del ADN informa de la disposición especial de las dos cadenas de polinucleótidos que forman una molécula de ADN. Basándose en estudios de difracción de rayos X, James Watson y Francis Crick propusieron en 1953 un modelo molecular aceptado en la actualidad, que permite explicar las propiedades físicoquímicas y biológicas del ADN: el modelo de la doble hélice. Previamente al modelo de la doble hélice propuesto por Watson y Crick, hubo varios descubrimientos realizados por otros investigadores, que aportaron datos sobre la estructura del ADN. Entre ellos, destacan: ▪ 1950, E. Chargaff. Después de estudiar gran variedad de muestras de ADN de diferentes especies, observa que siempre existía la misma cantidad de bases nitrogenadas púricas y pirimidínicas. Descubrió que el número de adeninas era igual de al timinas, y el de guaninas al de citosinas. Estos resultados constituyeron la denominada ley de equivalencia de bases de Chargaff. ▪ 1953, Rosalin Franklin y Maurice Wilkins. Aplicando el método de difracción de rayos X al ADN, dedujeron que esta molécula posee una estructura helicoidal con dos periodicidades, una cada 0,34 nm y otra cada 3,4 nm.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
21
Modelo de la doble hélice de ADN. Watson y Crick, 1953 A partir de estos datos, Watson y Crick elaboraron su modelo de estructura tridimensional del ADN (“modelo de la doble hélice”), que presenta las siguientes características: El ADN está constituido por dos cadenas de polinucleótidos unidas entre sí en toda su longitud. Las dos cadenas son antiparalelas, lo que significa que el extremo 3´de una de ellas se enfrenta al 5´de la otra. La unión entre las cadenas se realiza mediante puentes de hidrógeno entre las bases nitrogenadas de ambas: concretamente, la adenina forma dos puentes de hidrógeno con la timina y la guanina tres con la citosina. Resulta evidente que las dos cadenas no son idénticas, sino complementarias, ya que cada una de ellas tiene la secuencia de bases complementaria a la otra. (Si se conoce una secuencia es posible deducir inmediatamente la complementaria). Las dos cadenas están enrolladas en espiral formando una doble hélice alrededor de un eje imaginario. Las bases nitrogenadas quedan en el interior de la doble hélice, mientras que los esqueletos pentosafosfato se sitúan en la parte externa. De esta forma, las cargas negativas de los grupos fosfato se unen a las cargas positivas de otras moléculas o de cationes, estabilizando la estructura. Los planos de las bases nitrogenadas enfrentados son paralelos entre sí y perpendiculares al eje de la hélice. El enrollamiento de la doble hélice es dextrógiro, es decir, giran en el sentido de las agujas del reloj, y además plectonémico, o sea, las cadenas no se pueden separar sin desenrollarlas. La anchura de la doble hélice es de 2 nm, mientras que la longitud de cada vuelta es de 3,4 nm y cada 0,34 nm se encuentra un par de bases complementarias. Puede deducirse, por tanto, que existen 10 pares de nucleótidos por cada vuelta.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
22
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
23
Otros modelos de doble hélice La estructura secundaria del ADN descrita por Watson y Crick se conoce como B-ADN, y es la más abundante en la naturaleza. Pero existen otras estructuras secundarias descubiertas posteriormente: A-ADN: es una doble hélice dextrógira, cuya hélice es más ancha y más corta, mide 2,3 nm y en cada vuelta hay 11 pares de bases. Los pares de bases están inclinados respecto al eje central. Z-ADN: la doble hélice es levógira y cada vuelta mide 3,8 nm y contiene 12 pares de bases. Presenta un aspecto en zig-zag. Este tipo de hélice se debe a que las bases púricas alternan repetidamente con las pirimidínicas, como sucede en las secuencias CGCG o CACA.
Estructura terciaria La estructura en doble hélice del ADN sufre nuevos plegamientos que dan lugar a un tercer nivel estructural: la estructura terciaria. Es necesario por dos razones: Las largas cadenas de ADN deben acoplarse en el reducido espacio disponible en el interior celular. La regulación de la actividad del ADN dependen en gran medida del grado de plegamiento que sufra la molécula. La estructura terciaria es compleja y sabemos que existen proteínas (como las histonas) asociadas al ADN que organizan la estructura y permiten su empaquetamiento en el interior celular. El resultado final es la formación de cromatina y cromosomas, que estudiaremos en el núcleo celular.
13.2. TIPOS DE ADN Dependiendo del número de cadenas de polinucleótidos y su forma de empaquetamiento, el ADN en los organismos puede ser: Células eucariotas: ADN bicatenario (ADN2C ó ADNbc) lineal, dos cadenas dispuestas en línea, como en el núcleo de las células eucariotas. Células procariotas: ADN bicatenario circular y superenrrollado, dos cadenas que se disponen formando un círculo cerrado, como en las bacterias (y también en mitocondrias y cloroplastos). Virus: ADN monocatenario (ADN1C ó ADNmc) o ADN bicatenario lineal o circular.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
24
13.3. DESNATURALIZACIÓN e HIBRIDACIÓN DEL ADN La molécula de ADN es muy estable en condiciones normales, debido a los numerosos puentes de hidrógeno que unen las bases nitrogenadas de las dos cadenas polinucleotídicas. Sin embargo, la estructura en doble hélice se puede perder, separándose las dos cadenas o hebras, cuando se alteran las condiciones de pH (por encima de 13) o se calienta a temperaturas en torno a 100 ºC. Este fenómeno se conoce como desnaturalización del ADN. La desnaturalización se produce al romperse los puentes de hidrógeno que unen las dos cadenas de polinucleótidos, ambas cadenas se separan y se enrollan individualmente al azar. La temperatura a la que el 50% de la doble hélice está separada se denomina temperatura de fusión (Tm). Su valor depende del número de pares guanosina-citosina que haya en la molécula, de tal manera que si este es elevado la Tm será elevada, ya que el número de puentes de hidrógeno que se debe romper es mayor, y por tanto se necesita más energía para hacerlo. La desnaturalización del ADN es un proceso reversible, ya que si las hebras se mantienen a una temperatura en torno a los 65 ºC durante un periodo de tiempo prolongado, forman una nueva doble hélice con total funcionalidad. Este proceso se denomina renaturalización o hibridación del ADN.
Técnicas de hibridación De la misma forma que dos hebras de un mismo ADN se pueden renaturalizar en condiciones de pH y temperatura adecuadas, también se puede conseguir que dos hebras de distinta procedencia lo hagan. Así, se pueden obtener moléculas híbridas a partir de dos hebras de cualquier tipo de ADN, siempre que entre ambas exista una secuencia complementaria. Cuanto más relacionados están los ADN, mayor porcentaje de renaturalización se producirá. En una misma especie, el porcentaje de hibridación será mayor entre individuos emparentados. En diferentes especies, habrá mayor hibridación cuanto más relacionadas evolutivamente estén las especies. Por ejemplo, si se forma un híbrido entre ADN de ratón y ADN humano, el porcentaje de hibridación se encuentra en torno al 25%. Las técnicas de hibridación pueden servir para detectar secuencias complementarias, localizar genes relacionados entre distintas poblaciones o diagnosticar enfermedades genéticas producidas por la alteración en la secuencia de ADN .
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
25
14. ÁCIDO RIBONUCLEICO (ARN) El ARN, al igual que el ADN, es un polinucleótido no ramificado, formados por una serie de nucleótidos unidos por enlaces éster fosfóricos. A diferencia del ADN, el ARN lleva ribosa como pentosa y como bases nitrogenadas adenina, guanina, citosina y uracilo (no leva timina). El uracilo, como sucede con la timina en el ADN, se puede emparejar con la adenina. A excepción de algunos virus (reovirus), el ARN está formado por una única cadena de nucleótidos, aunque en algunos tipos de ARN las bases se pueden emparejar originando tramos de ARN bicatenarios, originados por el plegamiento de la cadena sobre sí misma. Las cadenas de ARN son más cortas que las de ADN y pueden aparecer tanto en el núcleo como en el citoplasma celular. El ARN es la molécula encargada de fabricar las proteínas específicas de un organismo, transmitiendo el mensaje codificado por el ADN. Así, mientras el ADN contiene información, el ARN la utiliza para que se produzcan las proteínas específicas del individuo. Este proceso es sumamente complejo (lo estudiaremos en el tema 5) y requiere la intervención de varios tipos de ARN: ▪ ARN mensajero o ARNm ▪ ARN ribosómico o ARNr ▪ ARN transferente o ARNt
ARN mensajero (ARNm) El ARNm es una copia de parte del ADN (de un gen o un grupo de genes que vayan a expresarse), cuya información será utilizada por los ribosomas para fabricar proteínas con una secuencia concreta de aminoácidos. El ARNm es lineal, sin zonas bicatenarias y constituye del 2 al 5% del ARN. Su función es llevar el mensaje genético del ADN hasta los ribosomas. El ARNm se forma mediante un proceso denominado transcripción, a partir de cualquiera de las dos cadenas del ADN. Cada vez que se necesita fabricar una proteína, la célula fabrica el ARNm correspondiente, ya que esta molécula tiene una vida muy corta (es destruida por ribonucleasas) y si no fuera así habría una superproducción de proteínas. La información contenida en el ARNm se presenta en una secuencia de bases nitrogenadas. Cada grupo de tres bases del ARNm que codifica para un aminoácido se denomina triplete o codón.
5´ ... AUG G C A U G C C G A A U A UAA... 3´ ARN ribosómico (ARNr)
Tripletes o codones
El ARNr forma parte de los ribosomas y participa, por tanto, es el proceso de unión de los aminoácidos para sintetizar las proteínas. La cadena de nucleótidos del ARNr, a diferencia del ARNm, está muy plegada, con muchos tramos bicatenarios. Se encuentra asociado a proteínas y de esta asociación se forman los ribosomas. Constituye entre el 80-85% del ARN celular total. Las células procariotas y eucariotas tienen cadenas de ARNr ligeramente distintas, que se diferencian por su coeficiente de sedimentación, tal como se aprecia en el siguiente cuadro: Subunidad ribosómica menor Subunidad ribosómica mayor
Procariotas
Eucariotas
16 S
18 S
5S 23 S
5S 5,8 S 28 S
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
26
ARN de transferencia o ARN transferente (ARNt) Las moléculas de ARNt están formadas por cadenas muy cortas (entre 70 y 90 nucleótidos). Su estructura secundaria es muy característica, ya que existen tramos de doble cadena, por emparejamiento de bases. Estos tramos se denominan brazos y hay cuatro en cada molécula. En los extremos de los brazos existen zonas sin emparejar que se denominan bucles, y cada uno de ellos desempeña una función particular. El extremo 3´de la cadena siempre tiene la secuencia de bases CCA y es por donde se unen los aminoácidos. En el extremo 5´siempre existe G. La estructura extendida del ARNt tiene forma de hoja de trébol, aunque en realidad los brazos se pliegan formando una estructura acodada que recibe el nombre de “estructura de boomerang”. El ARNt constituye, aproximadamente, el 15% del ARN total. El ARNt se encarga de transportar los aminoácidos presentes en el citoplasma hasta los ribosomas, donde se unirán para formar proteínas. Cada molécula de ARNt transporta un aminoácido concreto. Las diferencias entre las moléculas de ARNt son debidas a una secuela de tres bases nitrogenadas, el anticodón, que varía en los distintos ARNt y es la zona por donde se unen al ARNm. Existen más moléculas de ARNt diferentes que aminoácidos, por lo que un aminoácido puede ser transportado por diferentes moléculas de ARNt.
Expresión de la información genética
original papers
NATURE | VOL 421 | 23 JANUARY 2003 | www.nature.com/nature
© 2003 Nature Publishing Group
397
original papers
398
© 2003 Nature Publishing Group
NATURE | VOL 421 | 23 JANUARY 2003 | www.nature.com/nature
GENÓMICA y PROTEONÓMICA Genómica La Genómica es un área de la Biología cuyo objetivo es el estudio de los genomas. El “Genoma” es el conjunto de genes que especifican todos los caracteres que pueden ser expresados en un organismo. Es el juego completo de instrucciones hereditarias para la construcción y mantenimiento de un organismo en determinadas condiciones medioambientales. El término “Genómica” fue introducido en 1986, considerando el genoma como una unidad funcional y para distinguir el estudio de genomas completos, o de grandes regiones del mismo, de estudios genéticos más tradicionales centrados en un gen o un pequeño grupo de genes relacionados funcional o estructuralmente. A mediados de los años ochenta se disponía de la secuencia completa de algunos virus y orgánulos celulares. Los avances en las técnicas de secuenciación y análisis informático de secuencias permitieron el abordaje de proyectos de secuenciación de organismos más complejos. A partir de 1995 se produjo un incremento exponencial en la aparición de secuencias de genomas completos, iniciado con los de las bacterias Haemophilus influenzae y Mycoplasma genitalium . En 1996 se dio a conocer la primera secuencia de un organismo eucariota, Saccharomyces cerevisiae , y en 1998 se finalizó la secuenciación de un organismo eucariota pluricelular, Caenorhabditis elegans . En 2003 se publicó la secuencia completa del genoma humano, un hito indiscutible por la apertura a nuevas investigaciones y aplicaciones en el área de la Biomedicina. Hasta la fecha se han publicado la secuencia completa de cientos de organismos, incluyendo, además de los mencionados, numerosos microorganismos, animales y plantas modelo como Drosophila melanogaster , Rattus norvegicus o Arabidopsis thaliana . El conocimiento de estas secuencias no es más que el primer paso de lo que se ha dado en llamar “Genómica Funcional”, la posibilidad de caracterizar la función de los genes descubiertos en estos organismos mediante diferentes estrategias globales como el análisis de los perfiles de expresión génica mediante microarrays, análisis fenotípicos de mutantes o el análisis de interacciones proteícas. En paralelo, la caracterización en diferentes poblaciones de microsatélites o polimorfismos de nucleótidos (SNPs) asociados a determinados fenotipos abre enormes expectativas en la investigación biomédica.
Proteonómica La Proteómica es un área de la Biología cuyo objetivo es el estudio de los proteomas. Un proteoma es el conjunto de proteínas expresadas por un genoma, una célula o un tejido. El término Proteoma fue utilizado por primera vez en 1995. Hubo dos factores decisivos para el desarrollo de la proteómica: – Por un lado la secuenciación de los genomas a gran escala (se conoce la secuencia de los genes pero no su función). – Y por otro lado, el desarrollo de técnicas de separación y análisis de proteínas (Electroforesis Bidimensional y Espectrometría de Masas).
La secuenciación del genoma humano ha permitido conocer el número de genes que poseemos y que dicho número no es muy diferente del de otros organismos. La complejidad de los organismos parece radicar en las proteínas ya que un gen puede dar lugar a diferentes formas proteicas. Las proteínas van a sufrir diferentes modificaciones post-traduccionales para realizar su función. Además las proteínas van a interaccionar con otras proteínas formando complejos proteicos. La proteómica proporciona un conjunto de herramientas muy poderosas para el estudio a gran escala de la función de los genes a nivel de proteína. La aplicación de la proteómica tiene un enorme potencial en el área de la biomedicina para el desarrollo de fármacos (anticancerígenos, para el sistema nervioso, aparato cardiovascular, antimicrobianos, etc) métodos de diagnóstico, desarrollo de vacunas, etc.
Genómica, proteonómica y medicina La secuenciación del genoma humano, junto con el desarrollo de nuevas tecnologías “ómicas” de alto rendimiento (genómica, proteonómica, metabolómica), están aumentando de manera esencial el conocimiento de la enfermedad humana y estableciendo unas bases para la medicina personalizada (MP). La medicina personalizada (MP) es una modalidad de la medicina que utiliza la información de los genes, proteínas y metabolitos de cada paciente para prevenir, diagnosticar y tratar la enfermedad. Emplea la información del genoma de un individuo (y los datos que se derivan, expresión de proteínas, presencia de metabolitos) en pruebas de diagnóstico útiles y tratamientos específicos para cada enfermedad y para cada paciente. La medicina genómica hace uso de la información genómica y de las tecnologías complementarias (bioinformática) para determinar el riesgo y la predisposición a la enfermedad, diagnóstico y pronóstico y la selección y priorización de las opciones terapéuticas. Mientras que la farmacogenética se centra en el estudio de cómo un gen (o un número pequeño de genes) afecta al metabolismo, la farmacogenética lo hace en el estudio de cómo la variación genética del genoma afecta al metabolismo y respuesta frente a los fármacos. La medicina personalizada utiliza test moleculares para dividir a los pacientes según su respuesta a un tratamiento y mejora la eficacia del tratamiento seleccionando a los individuos que responden bien o excluyendo a los que van a tener un efecto adverso.
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
1
ACTIVIDADES TEMA 1. LA BASE FÍSICO-QUÍMICA DE LA VIDA PARTE III: PROTEÍNAS y ÁCIDOS NUCLEICOS PROTEÍNAS 1. a) b) c)
Utilizando como ejemplo la fórmula del aminoácido alanina, indica: ¿Qué es un carbono asimétrico?. ¿Cuántos y qué C asimétricos tiene la molécula de la figura?. ¿Qué propiedades poseen las moléculas que tienen C asimétricos?.
2. Los aminoácidos son compuestos anfóteros, ¿qué significa dicha propiedad?. ¿A qué se debe?. ¿Se podrían separar los distintos aminoácidos de una mezcla en función de su carga eléctrica?. Razona la respuesta. 3. Si el punto isoeléctrico de la alanina es 6, indicar la carga y estructura química de este aminoácido a pH 6, pH 2 y pH 9. 4. Se dispone de una disolución acuosa de alanina y treonina cuyos puntos isoeléctricos son 6,02 y 6,6 respectivamente. Explica razonadamente qué aminoácido se dirigirá hacia el ánodo y cuál hacia el cátodo si el pH de la solución es 6,3. Razona la respuesta. 5. a) b) c)
Con respecto al esquema adjunto: ¿Qué tipo de enlace observas?. ¿Tiene ese enlace capacidad de rotación?. Razónalo. ¿Son esos enlaces responsables de la estructura secundaria de las macromoléculas de las que forman parte?. Razónalo.
6. Escribe la fórmula desarrollada del siguiente péptido: H2N - Phe - Ser - Cis - Lys - COOH 7. La tripsina es un enzima que hidroliza los enlaces peptídicos en los que el grupo carboxílico lo aporta una lisina o una arginina. ¿Cuál será el resultado de la hidrólisis por medio de la tripsina sobre estos péptidos?. a) H2N - Lys - Met - Ala - Arg - Met - Val - COOH b) COOH - Lys - Arg - Met - Cys - Lys - Phe - NH2 8. a) b) c)
Indica qué enlaces mantienen las siguientes estructuras proteicas: Hélices estabilizadas Estructuras globulares Estructura cuaternaria
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
2
9. ¿De qué depende la actividad biológica y la especificidad de una proteína?. 10. ¿Qué enlaces se rompen al someter a una proteína a una temperatura elevada?. ¿Cómo se denomina este proceso?. ¿Qué repercusión tiene en la funcionalidad de la proteína?. 11. ¿Cuál es la causa de que las proteínas filamentosas sean insolubles en agua?. 12. ¿Porqué las proteínas animales tienen mayor valor biológico que las vegetales?. 13. Cita las funciones biológicas de las siguientes proteínas: a) Ovoalbúminas b) Glucoproteínas c) Cromoproteínas d) Actina y miosina e) Queratinas ÁCIDOS NUCLEICOS 14. Observa el modelo molecular de la derecha y responde a las cuestiones: a) ¿A qué molécula corresponde?. b) ¿Cuáles son los monómeros que lo forman?. c) ¿Qué nombre reciben estos?. d) ¿Qué moléculas constituyen estos monómeros?. 15. ¿Qué diferencia existe entre un nucleósido y un nucleótido?. 16. La figura representa una molécula muy importante para los seres vivos. ¿Cómo se denomina?. ¿Qué función desarrolla en la célula?. ¿Qué tipo de enlaces químicos presenta esta molécula que la diferencian de otras similares?. Indícalos en la fórmula.
17. Ácidos nucleicos: a) Nombra las unidades estructurales que los forman y los enlaces que las unen. b) Explica las diferencias químicas y estructurales de los dos tipos de ácidos nucleicos. c) Menciona al menos una localización de cada tipo de ácido nucleico. 18. Dibuja el trinucleótido dAMP-dTMP-dCMP y señala todos los enlaces de tipo éster que hay. Para facilitar el dibujo, simboliza las bases nitrogenadas con las letras A, T y C. Dibuja de la misma forma la hebra complementaria. Recuerda que son antiparalelas. 19. Indica a qué tipo de ácido nucleico corresponden las siguientes secuencias de bases nitrogenadas: a) 5´...CCGATC...3´ b) 3´...GGATCC...5´ c) 3´...UACCGA...5´ d) 5´...ACCGGC...3´
Biología 2º Bachillerato
Tema 1. La base físico-química de la vida.
3
20. En una ADN bicatenario se ha hallado que en el total de bases nitrogenadas hay un 23 % de adenina. ¿Cuáles son los porcentajes de las demás bases?. 21. En un ácido nucleico se ha encontrado el siguiente porcentaje de bases nitrogenadas: Adenina 22% Guanina 19% Citosina 26% Uracilo 33% ¿Se trata de ADN o ARN?. ¿Es de una sola hebra o de doble hebra?. 22. ¿Cuál es la secuencia de ADN complementaria de 5´ TACCTCAT....3¨?. 23. La secuencia de bases de una molécula de ARNm es: A-A-U-U-U-G-C-C-A … a) Escribe la doble cadena de nucleótidos del ADN de la que se copió. b) Indica cuál de las dos sirvió de molde. c) Escribe los anticodones correspondientes. 24. Observa el esquema: a) ¿A qué estructura corresponde?. b) Explica su función.
I.E.S Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
1
ACTIVIDADES GENÉTICA
1. Escribe qué secuencias de ADN son complementarias a las siguientes: a) b) c) d)
3´ ....T T A G C G G C T A C G C C T A ....5´ 5´ ....A C C G T C G T A C C G T T C G ....3´ 5´ ....C G T A A C G T T C G A C C G T .....5´ 3´ ....A T T C G T T A C C G T A T T C C ...3´
2. Escribe las secuencias de ARN complementarias a las anteriores secuencias de ADN. 3. Escribe las secuencias de ADN que han dado lugar a las siguientes secuencias de ARN (escribe las dos cadenas de ADN, indicando su sentido y cuál es la cadena con sentido). a) 5´... A U C G C G C G G C U U A C G ....3´ b) 3´... C G C U U A A C G C U A A C U ....5´ c) 5´... U A C G C U A C C U U G C A C .....3´ 4. Las siguientes composiciones corresponden a diferentes cadenas de A.D.N.: - Cadena 1: A=30%; G=24%; T=20%; C=26% - Cadena 2: A=15%; G=60%; T=20%; C=5% - Cadena 3: A=45%; G=10%; T=35%; C=10% - Cadena 4: A=20%; G=40%; T=30%; C=10% a) Calcula la composición de las bases nitrogenadas de las cadenas de A.D.N. complementarias. b) Calcula la composición de las bases nitrogenadas de las cadenas de A.R.N. que resulten de la transcripción de las cadenas de A.D.N. complementarias.
5. Escribe las secuencias de aminoácidos que son codificadas por los siguientes fragmentos de ADN: a) 5´... T A A G C T A C G T A C ... 3´ b) 3´... G C C T T A G C C A T C ... 5´ c) 5´... T T A C C G T A T C G G ... 3´ d) 3´... A T A C T G G T T A C C ... 5´ 6. Escribe las secuencias de A.D.N. que codifiquen para la síntesis de los siguientes péptidos: a) H2N...Pro-Asp-Ser-Trp...COOH b) HOOC...Ile-Leu-Val-Tyr...NH2 c) H2N...Tyr-Thr-Ser-Val...COOH
BIOLOGÍA 2º BACHILLERATO ACTIVIDADES SECUENCIACIÓN DEL ADN Se han secuenciado dos muestras de ADN, una mediante el método enzimático de Sanger (muestra A) y otra mediante secuenciación automática (muestra B). Determina en cada caso cuál es la secuencia de bases nitrogenadas de cada una de las muestras, indicando el sentido de la cadena.
Muestra A
Muestra B
SECUENCIACION ADN SOLUCION
BLOQUE II LA CÉLULA, MORFOLOGÍA Y FUNCIÓN
TEMA 2. LA CÉLULA: ORGANIZACIÓN Y ESTRUCTURA TEMA 3. CICLO CELULAR Y DIVISIÓN CELULAR TEMA 4. NUTRICIÓN CELULAR: METABOLISMO
TEMA 2. LA CÉLULA: ORGANIZACIÓN y ESTRUCTURA 1. INTRODUCCIÓN A LA CÉLULA: LA TEORÍA CELULAR 2. LA ORGANIZACIÓN CELULAR 3. LA ORGANIZACIÓN PROCARIOTA 4. LA ORGANIZACIÓN EUCARIOTA 5. LA MEMBRANA PLASMÁTICA • Composición química • Estructura de la membrana: modelo de mosaico fluido. • Funciones de la membrana celular 6. LA PARED CELULAR • Composición y estructura • Funciones de la pared celular 7. CITOPLASMA 7.1. CITOSOL o HIALOPLASMA 7.2. EL CITOESQUELETO 7.3. CENTRIOLOS, CILIOS y FLAGELOS 7.4. RIBOSOMAS 7.5. LOS ORGÁNULOS MEMBRANOSOS 7.5.1. Retículo endoplásmico (RE) 7.5.2. Aparato o complejo de Golgi 7.5.3. Lisosomas 7.5.4. Vacuolas 7.5.5. Peroxisomas 7.5.6. Mitocondrias 7.5.7. Cloroplastos 8. EL NÚCLEO CELULAR 8.1. CARACTERÍSTICAS GENERALES 8.2. ESTRUCTURA y COMPOSICIÓN DEL NÚCLEO INTERFÁSICO • Envoltura nuclear • Nucleoplasma • Nucleolo • Cromatina 8.3. LOS CROMOSOMAS • Estructura y composición • Cariotipo • Células diploides y haploides
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
1
1. INTRODUCCIÓN A LA CÉLULA: LA TEORÍA CELULAR El primero en observar células fue el científico inglés Robert Hooke en 1665 sobre una preparación de corcho y con un microscopio muy rudimentario. El corcho, observado en aumento, parecía estar constituido por pequeñas celdillas rodeadas por una pared rígida. Fue Hooke el primero en acuñar el término célula para referirse a estas estructuras. Sin embargo no llegó a reconocer la verdadera estructura de las células y, en realidad, lo que vio en el corcho no eran células sino sus paredes celulares muertas. El primero que observó células vivas fue Antón van Leeuwenhoek entre finales del s.XVII y principios del XVIII, describió los glóbulos rojos y observó espermatozoides, protozoos e incluso bacterias, todo ello con microscopios muy rudimentarios (en realidad simples lupas) fabricados por él mismo. Los progresos en el estudio de las células (Citología) dependen muy directamente del desarrollo de la microscopía; por ello hubo que esperar casi dos siglos hasta que se empezó a entender la verdadera significación de las células. En 1831 ya se conocía la existencia del núcleo celular; en 1839 se había descrito minuciosamente el proceso mitótico y en ese mismo año nacía la Teoría celular, atribuida a Schleiden y Schwann, que introducía el concepto fundamental de que la célula es la unidad básica de todos los seres vivos. Este principio fue ampliado finalmente por Virchow en 1859 con lo que la Teoría celular quedó definitivamente establecida. Se puede resumir en tres principios: 1.- Todos los organismos vivos están constituidos por una o varias células; la célula es, por tanto, la unidad vital de los seres vivos. 2.- Las células son capaces de una existencia independiente; las células son, por tanto, la unidad anatómica y fisiológica de los seres vivos. 3.- Toda célula proviene de otra célula ya existente; la célula es, por tanto, la unidad genética de los seres vivos. Hasta finales del s.XIX se consideraba que el tejido nervioso constituía una excepción a la teoría celular ya que se creía que no estaba formado por células independientes sino por una red o retículo de fibras y células interconectadas en la que no era posible diferenciar los elementos celulares, las neuronas. Fue Ramón y Cajal quien resolvió este problema al enunciar su teoría de la neurona en la que se demostraba que las neuronas eran elementos independientes y constituían la unidad anatómica y funcional del sistema nervioso. De esta manera, la teoría celular quedó definitivamente generalizada a todas las células, tanto vegetales como animales.
2. LA ORGANIZACIÓN CELULAR En todos los seres vivos , las biomoléculas se encuentran reunidas en conjuntos organizados a los que llamamos células. Las células son las asociaciones más simples de biomoléculas que son capaces de mantenerse estables frente al medio, para lo cual realizan las funciones de nutrición y relación, y además se pueden perpetuar en el tiempo gracias a la capacidad de reproducción. La célula es, por tanto, la unidad básica de un ser vivo, tanto a nivel estructural, como funcional y genético. Todas las células presentan una serie de componentes comunes: • Membrana plasmática: delgada membrana superficial que separa el contenido interno de la célula del exterior, y además regula el intercambio de moléculas entre la célula y el medio. • Citoplasma: es el interior celular, bañado por un liquido viscoso, donde se desarrollan numerosas reacciones metabólicas. En el seno del citoplasma se encuentran dispersos diversas estructuras conocidas como orgánulos celulares. • Material genético: está representado por el ADN, que dirige las actividades celulares y posibilita la transmisión de los caracteres hereditarios a la descendencia. A pesar de estas características “universales”, no todas las células presentan el mismo nivel de complejidad, pudiéndose distinguir dos modelos diferentes de organización celular: células procariotas y células eucariotas. Las células procariotas son las más sencillas y fueron las primeras en aparecer hace 3.600 m.a. Durante más de 1.500 m.a fueron el único tipo de células existentes en el planeta, hasta que por endosimbiosis surgieron hace unos 2.000 m.a las primeras células eucariotas.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
2
3. LA ORGANIZACIÓN PROCARIOTA Las células procariotas son mucho más sencillas que las eucariotas y se sitúan en la base evolutiva. La estructura procariota es característica y exclusiva de las bacterias, que constituyen el Reino Monera. La mayoría de las células procariotas son de pequeño tamaño, desde menos de una micra (μm) hasta unas pocas micras, equivalentes en tamaño a algunos orgánulos celulares eucariotas como mitocondrias o cloroplastos. Básicamente, una célula procariota típica presenta la siguiente estructura: • Una pared celular rígida que rodea a la membrana y responsable de la forma celular. La composición de la pared es diferente a la pared de las células vegetales, abundando los peptidoglucanos. Las únicas células procariotas desprovistas de pared son los micoplasmas, que son los organismos celulares más pequeños (0,1 a 0,8 μm de diámetro). • Una membrana plasmática que delimita el citoplasma celular y que presenta unas invaginaciones denominadas mesosomas, donde se localizan las enzimas respiratorias. • El citoplasma de aspecto granuloso, con ribosomas más pequeños que los eucariotas, con un coeficiente de sedimentación de 70 S, e inclusiones formadas por materiales de reserva (glúcidos, nitrógeno, fósforo, etc.). • La zona del nucleoide, situada en el centro de la célula, que contiene el material genético no rodeado por ninguna membrana, por lo que los procariotas no presentan un verdadero núcleo. El material genético está formado por una molécula de ADN circular, lo que se denomina cromosoma bacteriano, y otras pequeñas moléculas de ADN bicatenario circular denominadas plásmidos. Algunos tipos de bacterias contienen además otros elementos, como flagelos, pelos y fimbrias, cápsula y capas mucosas.
4. LA ORGANIZACIÓN EUCARIOTA A excepción de las bacterias, el resto de los seres vivos (reinos Protoctistas, Hongos, Animales y Plantas), presentan una organización eucariota. Las células eucariotas son más complejas y de mayor tamaño que las procariotas, con un diámetro que oscila entre los 10 y 30 mm, aunque puede variar ampliamente. También presentan una gran variedad de formas, en relación con su modo de vida si se trata de organismos unicelulares o con la función que desempeña el tejido al que pertenecen, si se trata de seres pluricelulares. Una de las características más notables de la célula eucariota es la “compartimentalización”, es decir, la existencia de diversos compartimentos u orgánulos delimitados por membranas que permiten que distintas funciones se lleven a cabo es diferentes partes de la célula. La estructura de una célula eucariota típica consta de los siguientes elementos: • La membrana plasmática, que constituye el límite externo de la célula y regula en transporte e intercambio de sustancias con el medio externo. Además es esencial en el intercambio de señales con otras células, ya que dispone de moléculas receptoras que responden a distintos estímulos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
3
• En ocasiones, rodeando a la membrana existe una pared celular rígida, fundamentalmente de celulosa en las células vegetales y de quitina en el caso de algunos hongos. Las células animales poseen un glicocálix adherido a la membrana que contribuye a la cohesión de los tejidos. • El citoplasma celular contiene los orgánulos celulares y está ocupado por un entramado de filamentos proteícos que constituyen el citoesqueleto o esqueleto celular, implicado también en la formación de cilios y flagelos, los movimientos celulares y la división celular. Las células animales poseen unos orgánulos, los centriolos, formados por filamentos del citoesqueleto. Los ribosomas presentan un coeficiente de sedimentación de 80 S, mayor que en las células procariotas. En el interior del citoplasma existe un sistema interna de membranas complejo constituido por el Retículo Endoplásmico (conectado a la membrana nuclear) y el Complejo de Golgi, orgánulos relacionados con la biosíntesis de moléculas y su distribución en el interior de la célula, así como la secreción de sustancias al exterior. Otros orgánulos membranosos son las vacuolas, muy desarrolladas en las células vegetales, y los lisosomas, que contienen enzimas digestivas para la degradación de sustancias en el interior de las vacuolas digestivas. Presentan dos orgánulos relacionados con la obtención de energía, las mitocondrias y los cloroplastos, estos últimos exclusivos de las células vegetales. En las mitocondrias se realiza la respiración celular y en los cloroplastos la fotosíntesis. • Todas las células eucariotas presentan núcleo delimitado por una doble membrana porosa. En su interior se encuentra la cromatina, constituida por ADN asociado a histonas (proteínas) y el nucleolo donde se fabrican las subunidades de los ribosomas. Así pues, aunque la organización básica de todas las células eucariotas es semejante, se pueden distinguir dos grandes tipos, células animales y vegetales.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
4
5. LA MEMBRANA PLASMÁTICA La membrana plasmática es una delgada envoltura que rodea y limita completamente a la célula, permitiendo que el contenido celular tenga una composición distinta a la del medio. La membrana plasmática separa el interior del exterior celular y controla el intercambio de sustancias entre la célula y su medio. La estructura de la membrana es la misma en todas las células. En cortes ultrafinos visualizados al microscopio electrónico aparece como dos bandas oscuras separadas por una clara, con un espesor de 7,5, nm. Esta organización es común, además, al resto de membranas biológicas limitantes de los orgánulos celulares por lo que se denomina unidad de membrana. COMPOSICIÓN QUÍMICA Las membranas biológicas están constituidas mayoritariamente por lípidos (40%) y proteínas (60%), junto a una pequeña proporción de glúcidos. a) Lípidos de membrana: todos ellos son antipáticos, por lo que se orientan en presencia de agua. • Fosfolípidos: son los lípidos más abundantes. Poseen una zona hidrófila, que constituye las denominadas cabezas polares y otra zona hidrófoba, que forma la cola apolar. • Glucolípidos. Semejantes a los fosofolípidos. Aparecen solo en la cara externa de la membrana. • Colesterol. Abunda en las células animales. b) Proteínas de membrana: también son moléculas antipáticas, de manera que las zonas polares sobresalen en las superficies de las membranas, mientras que las regiones apolares se encuentran en el interior hidrófobo. Según su grado de asociación con los lípidos, se clasifican en: • Integrales: constituyen alrededor del 70% de las proteínas y están íntimamente asociadas a los lípidos. Algunas proteínas presentan hidratos de carbono unidos a ellas (glucoproteínas) y se disponen en la cara externa de la membrana. • Periféricas: están débilmente asociadas a los lípidos. Aparecen principalmente en la cara interna. c) Glúcidos de membrana: están unidos a los lípidos o a las proteínas, en forma de glucolípidos o glucoproteínas, y se encuentran sobresaliendo en la cara externa de la membrana. Forman una capa periférica que recibe el nombra de glucocálix, glicocálix o cubierta celular, que interviene en los procesos de reconocimiento y comunicación celular, y proporciona protección mecánica y química a la superficie celular. En el exterior del glucocálix se sitúa una capa secretada por la célula denominada matriz extracelular, rica en colágeno, elastina y otras proteínas, que permite la adhesión de las células y el mantenimiento de los tejidos. ESTRUCTURA DE LA MEMBRANA: MODELO DE MOSAICO FLUIDO. Después de conocida la composición de las membranas celulares, se propusieron diferentes modelos para explicar cómo están organizados sus componentes. En 1972, Singer y Nicholson, señalaron que la membrana no era una estructura rígida como se pensaba, sino fluida, y permitía el movimiento de las proteínas que podían encontrarse embebidas o asociadas a la bicapa de lípidos. Propusieron así un modelo, conocido como el modelo de mosaico fluido, vigente en la actualidad. Los lípidos de membrana, debido a su carácter antipático, se disponen formando una doble capa o bicapa lipídica, donde la parte polar de la molécula se coloca hacia fuera, en o con el agua, mientras que la parte no polar se orienta hacia el interior de la bicapa, evitando así el o con el agua. La bicapa lipídica es impermeable a las moléculas solubles en agua, de manera que actúa como barrera entre la célula y el medio y además es una estructura fluida, ya que los lípidos se pueden desplazar libremente dentro de la bicapa mediante distintos movimientos (difusión lateral, flexión, rotación y flip-flop).
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
5
La fluidez de la bicapa depende del grado de insaturación de sus cadenas hidrocarburadas (a mayor insaturación mayor fluidez), y a la presencia de colesterol, que inmoviliza parte de las cadenas hidrocarburadas de los fosfolípidos. Las proteínas integrales se encuentran dispersas, atravesando totalmente o parcialmente la doble capa de lípidos, con una disposición en mosaico. Las proteínas periféricas se sitúan sobre la superficie de la bicapa. Debido a la disposición de los lípidos y proteínas, las membranas celulares aparecen al microscopio electrónico con tres bandas: una banda central clara correspondiente a la bicapa lipídica, y otras dos bandas externas oscuras correspondientes a las regiones polares de las proteínas, que sobresalen de la bicapa. Así pues, el armazón básico de las membranas biológicas está formado por la bicapa lipídica, que actúa de barrera, mientras que las proteínas desempeñan funciones específicas actuando como receptoras de mensajes, transportadores de sustancias o enzimas.
Membrana al m.o. FUNCIONES DE LA MEMBRANA CELULAR La función principal de la membrana es actuar de límite celular,, y por tanto, separar el citoplasma y sus orgánulos del medio externo. Este papel no es pasivo, ya que la membrana actúa de barrera selectiva que regula el intercambio y transporte de sustancias entre el interior celular y el medio. La membrana celular además, cumple otras funciones: • Es responsable de la formación y control del gradiente electroquímico (diferencia de carga eléctrica) entre el interior y el exterior celular. • Intercambia señales con el medio externo y con otras células. • Interviene en la división del citoplasma o citocinesis. • Esta relacionada con la inmunidad celular, ya que en la membrana se localizan algunas moléculas con propiedades antigénicas, responsables por ejemplo del rechazo en el transplante de tejidos y órganos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
6
• Está relacionada con la captación de sustancias (endocitosis) y con la secreción de sustancias al exterior (exocitosis). Estos procesos implican la creación y destrucción de membrana celular.
6. LA PARED CELULAR
Las células vegetales poseen una envoltura externa a la membrana plasmática, altamente organizada y rígida, que constituye la pared celular. Composición y estructura La pared celular tiene dos componentes mayoritarios: • Un componente cristalino, constituido por fibras de celulosa. • Un componente amorfo, formado por una matriz de pectinas, hemicelulosa, glucoproteínas, agua, sales minerales y, en algunos casos, ligninas. En las células diferenciadas, la pared celular aparece como una estructura gruesa compuesta por varias capas, que se van depositando a medida que se produce el crecimiento celular: • Lámina media. Es la capa más externa y la primera en formarse después de la división celular, y puede ser compartida por dos células adyacentes. Está formada por pectinas y proteínas, unidas a iones de Ca2+. • Pared primaria. Es una gruesa capa presente en todas las células vegetales situada por debajo de la lámina media. Está formada por largas fibras de celulosa entrecruzadas y cohesionadas por hemicelulosa y pectinas. • Pared secundaria. Aparece en algunas tipos especiales de células vegetales (tejidos de soporte y vasculares) cuando finaliza el crecimiento celular y las células se hacen adultas. Se sitúa por debajo de la pared primaria, y consta de una mayor cantidad de fibras de celulosa que se ordenan paralelamente dando lugar a varias capas con distintas orientaciones. Carece de pectinas, y en ocasiones entran a formar parte de su composición otras polímeros, como la lignina (xilema y esclerénquima), ceras y cutina (haz de las hojas) o suberina (corcho). La pared celular de las células vegetales no es continua , ya que presenta una serie de canales denominados plasmodesmos, que permiten la comunicación y el intercambio de fluidos y moléculas. Los plasmodesmos pueden encontrarse en ocasiones en depresiones de la pared primaria (menos engrosada) y donde está ausente la pared secundaria. En este caso se llaman punteaduras. Funciones de la pared celular -
Confiere rigidez al organismo y contribuye al mantenimiento de la forma celular. Evita la rotura celular por choque osmótico, permitiendo a las células vegetales vivir en un medio hipotónico. Une las células adyacentes, conectando las células de los tejidos vegetales. Posibilita el intercambio de fluidos y la comunicación intercelular.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
-
7
Impermeabiliza la superficie vegetal en algunos tejidos, gracias a la cutina y a la suberina, evitando pérdidas de agua. Sirve de barrera frente al paso de agentes patógenos.
7. CITOPLASMA El citoplasma es todo el contenido celular, comprendido entre la membrana plasmática y la membrana nuclear. Está constituido por tres componentes: citosol o hialoplasma, el citoesqueleto y los diversos orgánulos celulares. 7.1. CITOSOL o HIALOPLASMA Es el líquido acuoso que baña el citoplasma. Contiene gran cantidad de sustancias disueltas: glucosa, aminoácidos, sales minerales, proteínas, etc. y su consistencia puede pasar de fluida (sol) a viscosa (gel). En el citosol se desarrollan ciertas reacciones metabólicas, como la glucolisis, la síntesis de glicógeno y las fermentaciones. Además en el citosol se pueden almacenar sustancias en forma de gránulos, denominadas inclusiones, como por ejemplo los depósitos de glicógeno, las gotas de grasa y algunos pigmentos. En este medio es donde se encuentran inmersos los orgánulos celulares y el citoesqueleto. 7.2. EL CITOESQUELETO El citoesqueleto está formado por una red de filamentos de proteínas, que se extiende por todo el citoplasma, sirviendo de soporte interno celular. El citoesqueleto determina la forma de la célula, su organización interna y su movimiento. Está formado por tres tipos de filamentos: •
Microfilamentos. Son los filamentos más delgados y están compuestos por la proteína actina. Los microfilamentos de actina intervienen en varios procesos, tales como la contracción muscular, la emisión de pseudópodos que posibilitan la fagocitosis y el movimiento ameboide y la formación del anillo contráctil que provoca el estrangulamiento de la célula al final de la división celular. Además mantienen la morfología de las microvellosidades del epitelio intestinal.
•
Filamentos intermedios. Presentan un diámetro intermedio entre los microfilamentos y los microtúbulos, y abundan especialmente en las células animales. Tienen una función estructural, como por ejemplo los filamentos de queratina que proporcionan fuerza mecánica a las células epiteliales y los neurofilamentos que dan resistencia a los axones de las neuronas.
•
Microtúbulos. Son los filamentos más gruesos, de 25 nm. de diámetro, y están formados por la polimerización de la proteína tubulina. Son cilindros huecos y se originan a partir de un punto o centro organizador de los microtúbulos (MTOC) o centrosoma. Los microtúbulos se pueden encontrar dispersos por todo el citoplasma, constituyendo parte del citoesqueleto, o bien formar estructuras estables como los centríolos que estudiaremos más adelante. Los microtúbulos abundan en la mayoría de las células y desempeñan varias funciones: − Contribuyen al mantenimiento de la forma celular y a la organización del citoesqueleto. − Participan en el transporte de orgánulos y partículas en el interior celular, actuando como carriles internos de la célula.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
8
−
Constituyen los elementos del huso acromático durante la división celular que permite el movimiento de los cromosomas. − Son los elementos estructurales de los centríolos y conforman el esqueleto interno de los cilios y flagelos.
7.3. CENTRIOLOS, CILIOS y FLAGELOS Los centríolos, cilios y flagelos son estructuras estables formadas por microtúbulos semejantes a los que constituyen el citoesqueleto, por eso se les considera orgánulos microtubulares.
Centríolos y centrosoma Son dos cilindros que aparecen en el interior del centrosoma o citocentro y no están rodeados por ninguna membrana. No están presentes en las células de los vegetales superiores. Cada centríolo está formado por nueve tripletes de microtúbulos, que se unen mediante una proteína, la nexina. Los centríolos se originan por duplicación de otros preexistentes, de forma que el nuevo centríolo se dispone perpendicular al original. Los centríolos están rodeados por un material denso o material pericentriolar (centrosfera), de donde irradian unos microtúbulos en todas las direcciones, que constituyen el áster. El conjunto formado por los dos centríolos, el material pericentriolar y el áster recibe el nombre de centrosoma o citocentro. En las células vegetales carentes de centríolos, los centrosomas aparecen como zonas densas de material amorfo. Los centríolos intervienen en la organización de los cilios y flagelos y del huso acromático, pero el material pericentriolar es el auténtico centro organizador de los microtúbulos del citoesqueleto.
Centriolos
Centrosoma
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
9
Cilios y flagelos Son apéndices móviles que aparecen en muchas células, que presentan una estructura común formada por tres elementos: el axonema, la placa basal y el corpúsculo basal. El axonema presenta nueve pares de microtúbulos dispuestos alrededor de un par de microtúbulos centrales (9+2), y el corpúsculo basal nueve tripletes (9+0). La diferencias entre los cilios y flagelos reside en la longitud, los flagelos son más largos y menos numerosos en las células. Además el mecanismo de movimiento es distinto, los flagelos se mueven describiendo ondas simples, mientras que los cirios presentan un movimiento más complejo de propulsión y retracción. Su función es la de provocar el desplazamiento de células aisladas (espermatozoides, protozoos), o el movimiento del líquido extracelular sobre la superficie de la célula o el arrastre de partículas (epitelio ciliar de la tráquea)
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
10
7.4. RIBOSOMAS Los ribosomas son pequeños gránulos, que están presentes en todo tipo de células, y en ellos se fabrican las proteínas en la fase de traducción de la información genética. No son orgánulos membranosos, y debido a su tamaño (200 Å de diámetro), solo son observables al microscopio electrónico. Los ribosomas de las células eucariotas (80 S) son mayores que los de las procariotas (70 S). Están compuestos por varias moléculas de ARN ribosómico (ARNr), asociadas a diferentes proteínas. Cada ribosoma está constituido por dos subunidades, una mayor (60 S en eucariotas y 50 S en procariotas) y otra menor (40 S en eucariotas y 30 S en procariotas). Las subunidades se originan por separado en el nucleolo y luego se combinan en el citoplasma cuando van a fabricar proteínas, para ello entre las dos subunidades queda un pequeño espacio donde se coloca el ARN mensajero (ARNm), portador de la información genética para la síntesis de proteínas. Los ribosomas se pueden localizar dispersos en el citosol o unidos a la cara externa del retículo endoplásmico rugoso. También aparecen en el interior de mitocondrias y cloroplastos. Suelen presentarse agrupados, formando polirribosomas o polisomas, donde todos los ribosomas traducen la misma molécula de ARN mensajero.
Polirribosoma
7.5. LOS ORGÁNULOS MEMBRANOSOS En la célula eucariota se pueden distinguir dos tipos de orgánulos con membrana atendiendo a su estructura y función: El retículo endoplásmico, el complejo de Golgi y las vesículas, que están formados por membranas ▪ simples e intervienen en la síntesis, clasificación y empaquetamiento de sustancias, así como en la digestión celular (lisosomas) y en la regulación osmótica (vacuolas). Se denomina sistemas de endomembranas al conjunto de orgánulos que están relacionados entre sí y con la membrana nuclear. Sus principales componentes son el retículo endoplásmico, el complejo de Golgi y la membrana nuclear. Debido a la conexión entre sus componentes, el sistema endomembranoso se podría considerar una red de cavidades que dividen el citoplasma en dos compartimentos: uno encerrado en el interior de las membranas y el otro situado fuera de ellas. Las mitocondrias, peroxisomas y los cloroplastos, implicados en el metabolismo energético, y ▪ constituidos, a excepción de los peroxisomas, por una doble mebrana. Las mitocondrias y los cloroplastos presentan ADN propio y ribosomas 70 S, por lo que se les ha atribuido un origen endosimbiótico y proceden de antiguas bacterias aerobias y cianobacterias respectivamente.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
11
7.5.1. RETÍCULO ENDOPLÁSMICO (RE) Es el componente más desarrollado del sistema de endomembranas celulares, y está formado por una serie de cavidades membranosas irregulares aplastadas y comunicadas entre sí. Se distinguen dos tipos de retículo, aunque están ampliamente intercomunicados: • Retículo endoplásmico rugoso (RER): localizado cerca del núcleo y formado por cavidades membranosas con forma de saco (sáculos), que presentan ribosomas adheridos a su cara externa. • Retículo endoplásmico liso (REL): más alejado del núcleo, y formado por estructuras membranosas tubulares (túbulos). Carece de ribosomas adosados.
Funciones biológicas • • • •
•
Actúa de soporte mecánico, al dividir en compartimentos el contenido acoso del citoplasma. Sirve de sistema de transporte intracelular de diferentes sustancias. Síntesis de lípidos: en el REL se fabrican los lípidos de membrana (fosfolípidos y colesterol) que luego son distribuidos por las diferentes estructuras membranosas de la célula. Síntesis de proteínas: en los ribosomas del RER se fabrican proteínas, que luego penetran en el interior de los sacos del retículo. Algunas de ellas pasan al REL y se transforman en lipoproteínas, y otras son transportadas hasta el Aparato de Golgi para transformarse en glucoproteínas. Detoxificación: el REL es capaz de metabolizar algunas toxinas liposolubles, transformándolas en compuestos menos tóxicos e hidrosolubles, para facilitar su eliminación por el organismo.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
12
7.5.2. APARATO o COMPLEJO DE GOLGI El aparato de Golgi es complejo membranoso que se suele situar cerca del núcleo, próximo al retículo endoplásmico, y en las células animales alrededor de los centríolos. Está formado por un conjunto de unidades, denominadas dictiosomas, en cada una de las cuales se distinguen los siguientes elementos: • Cisternas: vesículas aplanadas y agrupadas en pilas. • Vesículas de transición: pequeñas vesículas íntimamente asociadas a las cisternas, que sirven de vehículo de transporte de sustancias. Se sitúan en la cara del dictiosoma más próxima al RER (cara cis o de formación) • Vesículas de secreción: son vesículas de mayor tamaño que se sitúan en la cara del dictiosoma orientada a la membrana plasmática (cara trans o de maduración).
Función biológica El aparato de Golgi se encarga de dirigir el tráfico de macromoléculas, evitando la mezcla al azar de los centenares de enzimas, lo que produciría un caos metabólico en la célula. Además es el encargado de fabricar los lisosomas primarios, interviene en la secreción celular y participan en la formación de la pared celular vegetal. Su misión fundamental es la de transportar y concentrar las proteínas procedentes del RER, así como la de glucosilar (unir oligosacáridos) las proteínas y lípidos para producir glucoproteínas y glucolípidos. Así a la cara cis o de formación de los dictiosomas van llegando proteínas procedentes del RER encerradas en pequeñas vesículas de transición. Las proteínas van atravesando el dictiosoma de cisterna en cisterna, trnasportadas por otras vesículas, se les van añadiendo nuevos glúcidos y poco a poco maduran. Una vez completada su maduración, son clasificadas por grupos según su destino, y más tarde emitidas por la cara trans o de maduración encerradas en vesículas. Algunas forman vesículas de secreción que expulsan las proteínas al exterior; otras forman los lisosomas· y otras se unen a la membrana sirviendo de material de reparación.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
13
7.5.3. LISOSOMAS Los lisosomas son vesículas membranosas que están presentes en todas las células eucariotas, y en cuyo interior contienen gran cantidad de enzimas hidrolíticas o hidrolasas ácidas (porque actúan a un pH ácido) y que son capaces de digerir la mayoría de las macromoléculas biológicas, por lo que la función de estos orgánulos es digestiva. Una característica de la membrana de los lisosomas es que presentan una gran cantidad de glucoproteínas que les protegen del ataque de sus propias hidrolasas. Según su origen, los lisosomas se clasifican en dos tipos: • LISOSOMAS PRIMARIOS: son los que no han intervenido en el proceso digestivo. Proceden de las cisternas del aparato de Golgi. Estos lisosomas pueden verter su contenido fuera de la célula mediante exocitosis y digerir así material extracelular, lo que se denomina digestión extracelular. Así por ejemplo, los las células óseas van remodelando el hueso, y los espermatozoides pueden penetrar en las envolturas del óvulo gracias a un gran lisosoma primario llamado acrosoma. En otras ocasiones los lisosomas primarios se fusionan con otras vesículas portadoras de materiales exógenos o endógenos y se convierten en lisosomas secundarios. • LISOSOMAS SECUNDARIOS: son vesículas que realizan la digestión intracelular. En función del material sobre el que actúan pueden clasificarse en: − Vacuolas digestivas o heterofágicas. Resultan de la fusión de los lisosomas primarios con vesículas endocíticas que contienen materiales (nutrientes o microorganismos) que han sido incorporados a la célula por endocitosis. En el interior de las vacuolas digestivas las enzimas hidrolíticas ejercen su acción digestiva, y los productos de la digestión son aprovechados por la célula. Cuando la digestión es incompleta, queda una pequeña formación con sustancias no digeridas denominada cuerpo residual, que puede ser eliminada de la célula por exocitosis. Este tipo de digestión colabora en la nutrición celular y en la defensa contra microorganismos patógenos, como virus y bacterias. − Autolisosomas o vacuolas autofágicas. Proceden de la fusión de lisosomas primarios con vesículas originadas en el interior de la célula (autofagosomas) que rodean restos celulares u orgánulos inservibles. Las vacuolas autofágicas eliminan materiales inútiles y destruyen zonas lesionadas de la célula, asegurando el recambio de los componentes celulares y evitando la degeneración celular. Además también degradan el exceso de macromoléculas producidas por la célula. Intervienen también en procesos de metamorfosis, en los que se producen transformaciones de tejidos. Las vacuolas autofágicas aseguran, a su vez, la nutrición celular en condiciones de ayuno, en el que las células consumen sus propios materiales. Si la digestión es incompleta también se originan cuerpos residuales.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
14
7.5.4. VACUOLAS Las vacuolas son orgánulos rodeados de membrana y con un elevado contenido de agua, en los que se acumulan diversas sustancias. Aunque también existen en las células animales, están mucho más desarrolladas en las vegetales, donde el conjunto recibe el nombre de vacuoma. Las vacuolas proceden de vesículas derivadas del RE y del aparato de Golgi. Su membrana recibe el nombre de tonoplasto. El tamaño y forma de las vacuolas varía según el grado de desarrollo de la célula, de manera que a medida que la célula crece y envejece las vacuolas aumentan de tamaño y se unen gradualmente, por lo que muchas células adultas presentan una gran vacuola que ocupa la parte central del citoplasma (en algunos casos hasta el 90% del volumen celular). Las funciones que desarrollan en las células vegetales son muy variadas: − Sirven de almacén de reserva para diversos iones y sustancias, como glúcidos, aminoácidos, proteínas, pigmentos, así como productos tóxicos (alcaloides y compuestos aromáticos que sirven de defensa contra depredadores) y de desecho. − Contribuyen al mantenimiento de la turgencia celular y con ello se consigue aumentar el tamaño de la célula de forma económica acumulando agua. Esto incrementa la superficie celular y por tanto la capacidad de intercambio de sustancias con el medio. − Contienen enzimas lisosómicas. 7.5.5. PEROXISOMAS Inicialmente se los denominó microcuerpos, y se trata de pequeñas vesículas que contienen enzimas de oxidación (peroxidasas y catalasas). Su membrana se origina a partir del REL. Están presentes en todas las células eucariotas. Los peroxisomas están implicados en reacciones de oxidación y desempeñan un papel muy importante en la detoxificación, gracias a las enzimas que contienen. Las oxidasas oxidan una gran variedad de compuestos, como aminoácidos, ácidos grasos y purines, originando como subproducto peróxido de hidrógeno (agua oxigenada). RH2 + O2 → R + H2O2 (peróxido de hidrógeno) Las catalasas posteriormente utilizan el peróxido de hidrógeno para oxidar diversos compuestos tóxicos, como el etanol, los fenoles o el ión superóxido. H2O2 + CH3 – CH2OH → CH3 – CHO + 2 H2O Etanol
Acetaldehido
Este tipo de reacciones son muy importantes en el hígado y en el riñón, de manera que cerca de la mitad del etanol ingerido es oxidado a acetaldehído por las catalasas. Si existe exceso de peróxido de hidrógeno, dañino para la célula, es transformado también por las catalasas en agua y oxigeno. 2 H2O2 → 2 H2O + O2
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
15
7.5.6. MITOCONDRIAS Las mitocondrias son orgánulos rodeados por dos membranas, presentes en todas las células eucariotas. Son capaces de dividirse por sí mismas por estrangulación. En ellas se realiza el metabolismo respiratorio energético, cuya finalidad es la obtención de energía. Presentan un tamaño y forma variables, aunque generalmente son cilíndricas o alargadas, y su diámetro oscila entre 0,5 y 1 μm, y tienen una longitud máxima de 7 μm. El número de mitocondrias varía con el tipo de célula, y abundan en las células que precisan de una elevado cantidad de energía, como las fibras musculares, hepatocitos o los ovocitos. Estructura y composición • • •
•
De fuera hacia dentro, en las mitocondrias se pueden distinguir los siguientes elementos: Membrana mitocondrial externa: es lisa y permeable, gracias a la presencia de porina. Espacio perimitocondrial: se localiza entre las dos membranas y tiene una composición semejante al citosol. Membrana mitocondrial interna: presenta una serie de pliegues, dirigidos hacia el interior, denominados crestas mitocondriales. Es más impermeable a los iones que la membrana externa. En ella se encuentran las cadenas de transporte electrónico y las ATP sintetasas, denominadas partículas elementales F1, que constan de una cabeza dirigida hacia el interior de la mitocondria y un pequeño pedúnculo. Matriz mitocondrial: contiene ADN mitocondrial circular, ARN y ribosomas de coeficiente de sedimentación semejante al de las bacterias. Incluye, además, diversas enzimas que intervienen en el ciclo de Krebs y en la β-oxidación de los ácidos grasos y transportadores de electrones, como el NADH.
Función biológica La función de las mitocondrias es la obtención de energía para la célula, por lo que se pueden considerar como las centrales energéticas celulares. Esta función se halla compartimentada en la matriz mitocondrial y en la membrana mitocondrial interna, donde suceden diversos procesos. • En la matriz mitocondrial tienen lugar: − La β-oxidación de los ácidos grasos y la descarboxilación oxidativa del ácido pirúvico. Ambos procesos generan Acetil-CoA y moléculas reducidas (NADH + H+ y FADH2 ). − El ciclo de Krebs, donde mediante un ciclo de reacciones químicas se oxida el Acetil-CoA a CO2, obteniéndose intermediarios metabólicos y moléculas reducidas (NADH + H+ y FADH2 ). • En la membrana mitocondrial interna se realiza la cadena de transporte electrónico, cuya función es transportar electrones desde las moléculas reducidas anteriores hasta el oxígeno. Este transporte de electrones genera una energía que es utilizada por las ATPasas de las crestas mitocondriales para sintetizar ATP mediante el proceso de fosforilación oxidativa.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
16
7.5.7. CLOROPLASTOS Los cloroplastos forman parte de un conjunto de orgánulos membranosos característicos de las células vegetales que se denominan plastos o plastidios. Los plastos son orgánulos con doble membrana capaces de sintetizar y acumular diferentes sustancias. Pueden ser de tres tipos: • Leucoplastos: son plastos incoloros, que almacenan sustancias de reserva, como almidón grasas, etc. Abundan sobre todo en las raíces y en los rizomas. • Cromoplastos: son plastos coloreados que contienen abundantes pigmentos carotenoides (carotenos y xantofilas), responsables del color característico de frutos como el tomate, zanahoria, limón, etc., y de las flores. • Cloroplastos: son orgánulos verdes que fabrican y acumulan clorofila, que están relacionados con el metabolismo fotosintético. Su forma tamaño y distribución varía de unas células a otras y con las especies: las células de las algas suelen poseer un solo cloroplasto muy voluminoso y las plantas superiores contienen entre 20 y 40 cloroplastos por célula, y su forma más frecuente es ovoide. Los cloroplastos son más grandes que las mitocondrias: su tamaño oscila entre 2 y 10 μm.
Estructura de los cloroplastos La estructura de un cloroplastos consta de tres elementos característicos: • Envoltura. Formada por una membrana plastidial externa, muy permeable, y una membrana plastidial interna menos permeable. Ambas membranas son continuas y delimitan completamente al cloroplasto. Las dos membranas están separadas por un espacio intermembranoso. • Estroma. Es la región rodeada por la membrana plastidial interna. El estroma contiene ADN circular doble, ribosomas 70 S, granos de almidón e inclusiones lipídicas. En él se localizan enzimas implicadas la fijación del CO2 , como la ribulosa 1,5-difosfato-carboxilasa oxidasa (RuBisCo) y otras que participan en el ciclo de Calvin. • Tilacoides y grana. Se encuentran inmersos en el estroma. Son una serie de sacos membranosos que se disponen paralelos al eje mayor del cloroplasto. Se pueden presentar de dos formas: > Tilacoides de los grana: pequeños sacos lenticulares que se apilan formando grupos llamados grana. > Tilacoides del estroma o lamelas: vesículas alargadas que atraviesan el estroma conectando los grana entre sí. Todo el sistema de tilacoides están interconectado y forma un compartimento interno que recibe el nombre de espacio tilacoidal. Las membranas de los tilacoides contienen los pigmentos fotosintéticos, principalmente clorofilas, carotenoides y otros pigmentos asociados. Los pigmentos fotosintéticos se asocian en dichas membranas con proteínas formando los fotosistemas, que actúan como órganos captadores de luz que despreden electrones. Además en las membranas tilacoidales se localizan las cadenas de transporte electrónico y las ATPasas implicadas en el proceso de fotofosforilación.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
17
Función de los cloroplastos Los cloroplastos son los orgánulos donde tiene lugar la fotosíntesis oxigénica. En la fotosíntesis, la célula vegetal utiliza la luz como fuente de energía, el CO2 como fuente de carbono y el H2O como donador de electrones y fabrica materia orgánica desprendiendo oxígeno. La fotosíntesis abarca dos fases: • Fase luminosa: sucede en la membrana de los tilacoides y se producen una serie de reacciones que convierten la luz en energía química (ATP) y poder reductor (NADPH + H+). Para ello es imprescindible la presencia de pigmentos que absorben la luz y de H2O que cede electrones. • Fase oscura: sucede en el estroma y tiene lugar la fijación del CO2 y su reducción a moléculas orgánicas mediante el Ciclo de Calvin, utilizando el ATP y el NADPH obtenidos en la fase anterior. Las moléculas orgánicas obtenidas se almacenan en forma de polisacáridos, principalmente almidón. Todas estas reacciones suceden sin la presencia de luz.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
18
8. EL NÚCLEO CELULAR 8.1. CARACTERÍSTICAS GENERALES El núcleo es una estructura membranosa característica de las células eucariotas, que alberga la información genética (ADN) y fabrica el ARN, antes de su salida al citoplasma, donde se producirá la síntesis de proteínas. Esta separación espacial supuso un acontecimiento de especial importancia en el transcurso de la evolución, ya que dio lugar a la célula eucariota, la unidad funcional de los seres vivos superiores. En las células eucariotas el núcleo actúa como centro de control: interviene activamente en el desarrollo y división de la célula, y regula la organización, diferenciación y especialización celular. La mayoría de las células poseen un solo núcleo, que ocupa por término medio un 10% del volumen celular. Excepcionalmente, existen células plurinucleadas, que según su origen, pueden ser de dos tipos: sincitios, que resultan de la unión de varias células uninucleadas, como las fibras musculares; o plasmodios, originados por sucesivas divisiones del núcleo, sin que se divida el citoplasma, como sucede en los huevos de los insectos. La morfología del núcleo es muy variada; aunque predominan las formas esféricas u ovales, es posible encontrar núcleos fusiformes, aplanados, arrosariados, ramificados e incluso fragmentados. El núcleo se localiza, por lo general, en el centro de la célula. En algunos casos, sin embargo, puede aparecer desplazado por otros orgánulos, como en las células vegetales, que está apartado por la vacuola, o en las células secretoras, que se encuentra en la base. El tamaño del núcleo está en relación directa con el citoplasma, de manera que si el volumen de uno aumenta, también lo hará el otro. La relación entre el volumen del núcleo y del citoplasma es lo que se denomina relación nucleoplasmática (RNP), que se expresa de la siguiente manera:
RNP =
Vn Vc − Vn
Vn = volumen del núcleo
Vc = volumen celular
La relación nucleoplasmática es constante para cada célula y depende de la función celular. Cuando la RNP alcanza un valor mínimo se inicia la división celular. 8.2. ESTRUCTURA y COMPOSICIÓN DEL NÚCLEO DEL NÚCLEO INTERFÁSICO La estructura y composición del núcleo varía a lo largo de la vida de una célula (ciclo celular), diferenciándose dos períodos: período de división o mitosis, durante el que una célula se divida para originar células hijas, y período de interfase o de no división, durante el cual el ADN se transcribe y la célula realiza su actividad normal. A continuación vamos a estudiar la estructura y composición del núcleo en interfase o núcleo interfásico. El núcleo interfásico consta de los siguientes componentes: envoltura nuclear, nucleoplasma, nucleolo y cromatina.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
19
Envoltura nuclear La envoltura nuclear deriva del RE y está formada por dos membranas concéntricas, externa e interna, separadas por un espacio perinuclear. La membrana externa está conectada y se continua con el retículo endoplásmico rugoso. Por debajo de la membrana nuclear interna se observa una lámina nuclear fibrosa formada por filamentos intermedios, que interviene en la organización de la cromatina y en su desaparición y nueva formación durante la mitosis. Ambas membranas se comunican por medio de poros nucleares (80 nm de diámetro), a través de los cuales se produce el intercambio de moléculas grandes, como el ARN y las proteínas, entre el núcleo y el citoplasma. Cada poro está rodeado por un anillo de bloques de proteínas dispuestos en forma octogonal. En el centro del anillo contiene un material amorfo y denso formado por finas fibrillas. Todo el conjunto constituye el complejo del poro, lo que significa que los poros nucleares no son simples aberturas, sino que seleccionan específicamente las moléculas que lo atraviesan. Desde el interior nuclear, a través de los poros, pasan al citoplasma moléculas de ARN mensajero y las subunidades de los ribosomas, mientras que desde el citoplasma pasan al núcleo nucleótidos, proteínas ribosómicas y enzimas implicadas en la duplicación y transcripción.
Nucleoplasma El nucleoplasma, también llamado carioplasma, el es medio interno acuoso donde se encuentran inmersos los demás componentes del núcleo. Está compuesto por proteínas, principalmente enzimas relacionadas con la duplicación del ADN y la transcripción a ARN.
Nucleolo El nucleolo es una estructura esférica visible en el interior del núcleo interfásico, que carece de membrana. Su función principal es la síntesis y ensamblaje de las subunidades de los ribosomas. Algunas células presentan más de un nucleolo. El nucleolo está compuesto de proteínas y ácidos nucleicos, ADN (1- 3%) y ARN (10 – 30%). Estructuralmente, en cada nucleolo se distinguen dos zonas: • Zona fibrilar: ocupa la parte central. Contiene ADN y ARN. El ADN nucleolar que contiene los genes para la síntesis de ARNr y puede formar parte de cromosomas distintos constituye el organizador nucleolar, y contínuamente se está transcribiendo a moléculas de ARNr, originando unas estructuras plumosas. • Zona granular: ocupa la parte periférica. En esta zona las moléculas de ARNr se combinan con proteínas para originar las subunidades ribosómicas 60 S y 40 S, que posteriormente emigrarán al citoplasma atravesando los poros nucleares y se unirán formando ribosomas completos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
20
Nucleolo y formación de ribosomas Estructuras plumosas del organizador nucleolar
Cromatina La cromatina está compuesta por ADN plegado, asociado a proteínas básicas: las histonas. En la cromatina el ADN se asocia a las histonas y forma unos complejos denominados nucleosomas. Cada nucleosoma contiene ocho moléculas de histonas que forman un núcleo central cilíndrico, donde se enrolla la molécula de ADN, que da dos vueltas alrededor de dicho cilindro. Se podría decir que los nucleosomas son las “unidades estructurales” de la cromatina. Al observar una fibra elemental de cromatina al microscopio electrónico se distingue una fibra de “cuentas” ensartadas, semejante a un collar (estructura de collar de perlas). Cada una de las “cuentas” equivale a un nucleosoma (ADN-histonas), y entre cada unidad hay un fragmento de ADN libre que correspondería al “hilo” del collar. La cadena de nucleosomas es la unidad o fibra elemental de cromatina, de unos 10 nm de grosor. Esta fibra elemental se enrolla helicoidalmente hasta formar un solenoide o fibra de 30 nm, que contiene seis nucleosomas por cada vuelta de hélice. La fibra de 30 nm es la cromatina tal como se visualiza al microscopio electrónico. A su vez las fibras de 30 nm se pliegan en el núcleo formando bucles radiales, que se van compactando y enrollando sucesivamente durante la división del núcleo, hasta formar los cromosomas metafásicos.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
21
Eucromatina y heterocromatina
Cromatina y collar de perlas
Tipos de cromatina • Eucromatina. De aspecto laxo o difuso, corresponde a zonas de cromatina activas (aproximadamente, el 10% de la cromatina celular), donde se produce la transcripción. • Heterocromatina. De aspecto más denso, son zonas de cromatina condensada (el 90% del total), que corresponde a zonas inactivas que no se transcriben. A su vez se distinguen dos tipos de heterocromatina: constitutiva, que aparece condensada siempre durante todo el ciclo celular, y cuyo ADN no se transcribe nunca; y facultativa, cuya condensación depende del estado de desarrollo del organismo y del tipo de célula, y cuyos genes se inactivan a lo largo de la diferenciación celular. La heterocromatina facultativa es escasa en tejidos embrionarios y aumenta cuando se especializan las células. 8.3. LOS CROMOSOMAS Estructura y composición Cuando una célula se divide por mitosis, la cromatina se condensa, originando los cromosomas. Los cromosomas son estructuras cilíndricas que representan el máximo grado de empaquetamiento del ADN, y por tanto, de la cromatina. Durante la metafase de la mitosis, cada cromosoma está formado por dos partes o cromátidas iguales (que se corresponden con dos filamentos de cromatina idénticos), y unidas por un estrechamiento denominado centrómero. Los extremos de las cromátidas se denominan telómeros, y en ellos se encuentran secuencias repetitivas de ADN cuya función es asegurar la integridad del cromosoma y evitar la pérdida de información genética en la duplicación. El centrómero recibe también el nombre de constricción primaria, y en él se encuentran el cinetocoro, que es una placa de
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
22
proteínas donde se conectan los microtúbulos del huso acromático durante la mitosis. Existen otras zonas de estrechamiento, denominadas constricciones secundarias, algunas de las cuales corresponden a los organizadores nucleolares y por tanto contienen genes para la síntesis de ARN ribosómico. Estas constricciones son constantes en su posición y tamaño, por lo que resultan útiles para identificar los cromosomas. Algunos cromosomas (cromosomas-SAT) presentan zonas esféricas denominadas satélites separadas del resto del cromosoma por una constricción secundaria. El centrómero divide cada cromátida en dos brazos, los brazos cromosómicos. Según la posición del centrómero y la longitud de los brazos, los cromosomas se dividen en cuatro tipos: • Metacéntricos: centrómero central y brazos iguales. Durante la anafase aparecen en forma de V. • Submetacéntricos: un brazo más largo que el otro. Durante la anafase aparecen en forma de L. • Acrocéntricos: cromosomas con forma de bastón, con un brazo muy corto y otro muy largo. Durante la anafase mantienen su forma cilíndrica. • Telocéntricos: cromosomas con el centrómero situado en uno de los extremos, por lo que solo presenta un brazo distinguible. Cariotipo El cariotipo es el conjunto de rasgos característicos de los cromosomas de cada especie (tamaño, forma, número, etc.). Cada cromosoma o pareja de cromosomas se designa con un número, excepto los cromosomas sexuales que se denominan con las letras X e Y. Así pues el cariotipo de una célula presenta dos tipos de cromosomas: • Autosomas: cromosomas ordinarios, iguales en individuos masculinos y femeninos, que no deciden el sexo del individuo. • Heterocromosomas o cromosomas sexuales: son normalmente una pareja de cromosomas, diferente según el sexo. Así en la especie humana, se distinguen dos cromosomas sexuales: el cromosoma X y el cromosoma Y. El primero está presente en los dos sexos, y el segundo es propio del sexo masculino. Así pues en la especie humana el cariotipo femenino esta formado por 44 autosomas + XX, y el masculino es 44 autosomas + XY. La representación gráfica del cariotipo, ordenados los cromosomas de mayor a menor, se denomina idiograma o cariograma.
I.E.S. Fuentesnuevas Biología 2º Bachillerato Tema 2. La célula: organización y estructura
23
Células diploides y haploides El número de cromosomas es constante en cada especie, y según esto, las células pertenecientes a una especie determinada pueden ser de dos tipos: • Diploides (2n): presentan dos cromosomas iguales (en forma y tamaño) de cada tipo, denominados cromosomas homólogos, ambos tienen los genes para los mismos caracteres. Estas células presentan por tanto dos series o dotaciones de cromosomas, cada una de ellas heredada de un progenitor. • Haploides (n): presentan solo una serie o dotación de cromosomas, todos diferentes entre sí, por lo que no presentan cromosomas homólogos. Así pues, en una célula diploide, los cromosomas están en parejas y hay dos genes para cada carácter (genes alelos), mientras que en una haploide todos los cromosomas son distintos y hay un solo gen para cada carácter. Por ejemplo, en la especie humana, las células somáticas (no intervienen en la reproducción) tienen 46 cromosomas, pero como son 2n, en realidad se trata de 23 parejas. Los gametos humanos (óvulos y espermatozoides), al ser n, tienen 23 cromosomas todos distintos. Algunos organismos tienen células poliploides, en las que el número de cromosomas de cada tipo es mayor de dos.
CARIOTIPO HUMANO
Los grupos que comprende el cariotipo humano son los siguientes: - Cromosomas grandes Grupo A, (cromosomas 1, 2 y 3), meta y submetacéntricos Grupo B, (cromosomas 4 y 5), submetacéntricos - Cromosomas medianos Grupo C, (cromosomas 7, 8, 9, 10, 11, 12 y además los cromosomas X), submetacéntricos Grupo D, (cromosomas 13, 14 y 15) acrocéntricos - Cromosomas pequeños Grupo E, (cromosomas 16, 17 y 18) submetacéntricos Grupo F, (cromosomas 19 y 20) metacéntricos Grupo G, (cromosomas 21 y 22) acrocéntricos Por acuerdo los cromosomas sexuales X e Y se separan de sus grupos correspondientes y se ponen juntos aparte al final del cariotipo.
I.E.S. Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
1
TEMA 2. LA CÉLULA: ESTRUCTURA y FUNCIÓN 1. ¿Cuántas veces es más grande el volumen de una célula eucariota globosa de 20 μ de diámetro que una bacteria tipo coco de 2 μ de diámetro?. 2. Un hepatocito humano posee un volumen aproximado de 5.000 μm3. Sabiendo que el porcentaje de volumen celular ocupado por el núcleo de esta célula es del 6%, calcula la relación nucleoplasmática (RNP). 3. Qué estructura u orgánulo celular desempeña las siguientes funciones dentro de la célula: a) Fabrica las proteínas b) Dirige el funcionamiento de la célula c) Forma los lisosomas d) Fabrica los lípidos de membrana e) Selecciona las sustancias dentro de la célula f) Da forma a las células animales g) Realiza la fotosíntesis h) Almacena sustancias de reserva y) Forma los cilios y flagelos j) Distribuye las sustancias fabricadas en el retículo endoplásmico k) Almacena granos de almidón l) Fabrica el ARN ribosómico m) Digiere nutrientes que toma la célula del medio externo 4. Identifica la letra entrecomillada de los siguientes ejercicios: 4.1 La “A” es una lámina que separa los medios intra y extracelular. Químicamente está constituida por una bicapa de “B” donde se incrustan las “C”. Esta lámina posee unas terminaciones glucídicas, muy ramificadas que forman el “D”. En las células vegetales, además de la lámina anteriormente citada, hay una envoltura gruesa: la “E”, formada principalmente por “F”. 4.2. Los “A” son orgánulos celulares constituidos por dos “B” de diferente tamaño. Poseen agua, proteínas y “C”. Varios de estos orgánulos se suelen unir una cadena de ARN mensajero, y a este conjunto se le denomina “D”. Los orgánulos en cuestión se encuentran libres en el “E”, o unidos a la membrana externa del “F” que, en este caso, recibe el nombre de “G”. 4.3. Los cilios y flagelos de las células animales derivan de unos orgánulos cilíndricos denominados “A”, y cuando estos se encuentran agrupados se disponen perpendicularmente formando el “B”. Este conjunto está rodeado por la “C”, de la que parten unos filamentos que se disponen radialmente: el “D”. Cada “E” está formado por “F” grupos de 2 ó 3 microtúbulos. Esta disposición contrasta con la de los “G” y “H” que, además tienen “Y” microtúbulos centrales. 4.4. Rodeando al núcleo celular o al centrosoma se suele encontrar un orgánulo celular denominado “A”, que está formado por unos sáculos aplanados que se originan del “B”, y que se agrupan formando los “C”. Este orgánulo forma vesículas cargadas de enzimas, los “D”, que se unen a los fagosomas y, con éstos, constituyen las “E”. 4.5. Las “A” están separadas del “B” por una doble membrana. La interna se invagina formando las “C”. El espacio interno o “D” es rico en enzimas, posee “E” circular y unos ribosomas denominados “F”. 4.6. Los “A” son unos orgánulos que no se encuentran en las células “B”. Presentan una doble membrana y en su interior hay un tercer tipo de membrana que se dispone formando saquitos discoidales llamados “C”. El espacio interno o “D” contiene enzimas, polisacáridos. ADN “F” y pequeños “G” que fabrican proteínas.
I.E.S. Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
2
4.7. El “A” es el que controla y gobierna todas las funciones celulares de la célula. Está constituido por una membrana (prolongación del “B”) que presentan una serie de “C” que comunican el medio interno de este o “D” con el “E”. También posee uno o varios “F”. Dispersas en su interior se encuentran unas masas densas de ADN unidas a proteínas, que son los filamentos de “G”. 4.8. Los “A” son los componentes celulares responsables de la información genética. En metafase se observan formados por dos “B” idénticas unidas por el “C”, que divide a los “A” en dos partes llamadas “E”, si son muy desiguales “F” y si uno de ellos no se aprecia se denomina “G”. 5. Ordena de mayor a menor tamaño las siguientes formas vivas: virus; ribosoma; núcleo; mitocondrias; óvulo humano; glóbulo rojo; bacteria. 6. Por ultracentrifugación es posible separar los diferentes componentes celulares y, generalmente, cuanto mayor sea el tamaño de la estructura celular menor será la fuerza centrífuga necesaria para sedimentarla. ¿En qué orden sedimentarán los siguientes componentes celulares?: mitocondrias, lisosomas, núcleos, proteínas y ribosomas. 7. Responde verdadero o falso a las siguientes cuestiones y explica el por qué: a) Los ribosomas están formados por ADN, ARN y proteínas. b) El retículo endoplásmico siempre tiene adosado ribosomas a su cara externa. c) Las vesículas de Golgi contienen proteínas que provienen del retículo endoplásmico. d) Los lisosomas son orgánulos exclusivos de las células vegetales que contienen enzimas formadas por el ergatoplasma. e) En las mitocondrias hay ADN monocatenario circular. f) La clorofila se encuentra dispersa en el estroma de los cloroplastos. g) La estructura del cilio es similar a la del flagelo. h) El conjunto de centrosoma, centrosfera y áster se llama centriolo. i) Los peroxisomas son orgánulos ricos en una hormona llamada peroxidasa. 8. En el interior de ciertos orgánulos, más pequeños que las mitocondrias, hay gran cantidad de enzimas que utilizan el oxígeno celular como aceptor de electrones y, como consecuencia, se forma una sustancia tóxica que debe ser eliminada. Esta sustancia es rápidamente reducida mediante una enzima cuya actuación produce agua y oxígeno. a) ¿De qué sustancia tóxica se trata?. b) ¿Cómo se llama la enzima que transforma esta sustancia?. c) ¿Cuáles son los orgánulos a los que se refiere el párrafo anterior?. 9. De las estructuras y orgánulos que se citan a continuación, hay algunos que no los poseen las células vegetales, otros de los que carecen, y los hay presentes en ambos tipos de células. Indica dónde aparecen cada uno de ellos: cloroplastos, mitocondrias, granos de glucógeno, ribosomas, pared celular, cilios, cromosomas, vacuolas, granos de almidón, centriolos, aparato de Golgi, peroxisomas, nucleolo.
I.E.S. Fuentesnuevas Biología 2º Bachillerato
Departamento de Ciencias Naturales
3
Cuestiones de selectividad • Dibuja, mediante un esquema, la estructura de una mitocondria. Indica sus componentes y explica las funciones biológicas de este orgánulo./ Estructura y función del retículo endoplásmico. • Indica qué orgánulos están delimitados por doble membrana. ¿Todas las células contienen dichos orgánulos?. Razona la respuesta./ A partir de un dibujo del núcleo, se pide identificarlo, identificar sus partes y describir su función. ¿Es posible hallarlo en todas las células?. • Estructura y funciones del citoesqueleto./A partir de un dibujo del Modelo de Mosaico fluido de la membrana plasmática se pide: Identificar las moléculas señaladas y definir su naturaleza química; Señalar las funciones principales de la membrana. • De las siguientes estructuras, indica las que son características de células animales, las que corresponde a células vegetales y las que son comunes a ambas, razonando la respuesta: a) Membrana plasmática, b) Pared celular. c) Cloroplastos. d) Mitocondrias. e) Centrosoma. f) Vacuolas. /Desarrolla la siguiente propuesta: “Cromatina y cromosomas son dos estados del mismo material nucleosómico”. • Indique si las siguientes afirmaciones son verdaderas o falsas, razonando la respuesta: a) Los componentes dominantes de los ribosomas son: agua, fosofolípidos y polisacáridos. b) Solo algunos ribosomas están adheridos a biomembranas. c) Todos los ribosomas tienen el mismo coeficiente de sedimentación. D) Las dos subunidades de los ribosomas son funcionales cuando están separadas. • Clasifica los orgánulos de una célula eucariota según sean membranosos, no membranosos o energéticos. Dibuja un esquema del Aparato de Golgi, denomina sus partes y explica las principales funciones de dicha estructura endomembranosa. • Representa mediante un dibujo, la arquitectura molecular de la membrana plasmática y denomina sus componentes. ¿Estimas que puede establecerse alguna relación entre la membrana plasmática y los lisosomas?. Razona la respuesta. • Describe, con ayuda de un esquema, la estructura y principales características de una célula eucariota animal. Indica un proceso fisiológico celular en el que participe el centrosoma./Dibuje una célula bacteriana y otra vegetal e indique las principales diferencias entre ellas. • Teniendo en cuenta que el retículo endoplasmático (RE) es una estructura membranosa intracelular, contesta a las siguientes cuestiones: a) ¿Qué dos propiedades del RE coexisten en la célula?. Si tuviera que observar una célula al microscopio electrónico, ¿qué característica morfológica le permitiría diferenciar una modalidad de la otra?. ¿Qué funciones básicas desarrolla cada una de los dos tipos de RE?. ¿Estima que el RE es exclusivo de células animales, de vegetales o de ambos tipos de células?. Razone la respuesta.
TEMA 3. LA REPRODUCCIÓN CELULAR 1. EL CICLO CELULAR 1.1. LA INTERFASE. MUERTE CELULAR. 1.2. LA MITOSIS 1.3. LA CITOCINESIS o CITODIÉRESIS 2. LA MEIOSIS 3. MITOSIS, MEIOSIS y REPRODUCCIÓN 4. DIFERENCIAS ENTRE MITOSIS y MEIOSIS 5. MEIOSIS y CICLOS BIOLÓGICOS
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
2
1. EL CICLO CELULAR El aumento en tamaño de los seres vivos superiores sólo es posible por un aumento en el número de células que los forman. Cuando una célula adquiere un tamaño adecuado, se divide para originar dos células hijas. El ciclo celular es el tiempo que transcurre desde que una célula se forma por división de una preexistente hasta que se divide y origina dos células hijas. La duración del ciclo es muy variable, como se expone en el siguiente cuadro:
El ciclo celular se divide en dos fases muy definidas: Interfase y mitosis o fase M.
1.1. LA INTERFASE Es la fase más larga del ciclo celular, ya que ocupa casi el 94 % de él, y transcurre entre dos mitosis, razón por la que también se la denomina intermitosis. En ella la célula aumenta de tamaño, expresa su mensaje genético y realiza una intensa actividad biosintética a todos los niveles. Desde el punto de vista citológico, la interfase se caracteriza por la ausencia de cromosomas visibles, visualizándose solo la cromatina. En la interfase se distinguen tres etapas: FASE G1: este período transcurre entre el final de una mitosis y el inicio de la síntesis o duplicación del ADN. En ella la célula aumenta de volumen hasta alcanzar el tamaño de su forma celular típica, aumenta el número de orgánulos celulares y fabrica y acumula las sustancias necesarias para la división celular. En un cierto momento de esta fase se alcanza el punto de no retorno o punto R, en el cual la célula ya está obligada a realizar todo el proceso. Una vez sobrepasado dicho punto la célula continua el ciclo hacia la fase siguiente. Previamente al punto R hay una fase de reposo o fase G0, y su duración depende de numerosos estímulos externos (nutrientes, cambios de temperatura, alteraciones de la membrana, ...). Hay células que permanecen de por vida en el estado G0, y que han sufrido un importante proceso de diferenciación, como las neuronas y las fibras musculares estriadas. Al final de la etapa G1, se produce una activa síntesis de proteínas (histonas y no histonas) y nucleótidos y enzimas necesarios para la duplicación del ADN. FASE S: en esta etapa se duplica el ADN del núcleo, y como resultado de ello, cada cromosoma que se origine en la mitosis estará formado por dos cromátidas idénticas (cada una con una molécula de ADN) unidas por el centrómero. Primero de replica la eucromatina y después la heterocromatina, más condensada. La duración de esta fase depende del tipo de célula y la temperatura. En los mamíferos dura unas siete horas. FASE G2: tiene una duración muy corta (alrededor de tres horas en mamíferos), y en ella la célula aumenta ligeramente de tamaño. Se transcriben y traducen genes que codifican las proteínas necesarias para la división celular y se duplican los centríolos. Al final de esta fase las células se redondean. La fase G2 finaliza en el momento en que se inicia la condensación de los cromosomas para comenzar la mitosis.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
3
Etapas del ciclo celular y mecanismos de control a lo largo del ciclo celular
FACTORES QUE CONTROLAN EL CICLO CELULAR A lo largo del ciclo celular existen una serie de puntos de control que actúan como frenos, que impiden a la célula continuar el ciclo si no está lo suficientemente preparada. Los tres principales puntos de control se encuentran: Al final de la etapa G1. El punto R o de no retorno es el primer punto de control del ciclo celular, donde la célula evalúa si está preparada para dividirse o no. Al final de la etapa G2. La célula evalúa si está preparada para entrar en mitosis. Este punto de control actúa como mecanismo de seguridad que garantiza que solamente entren en mitosis aquellas células que hayan completado la duplicación de todo su material genético. Durante la mitosis, en la metafase, existe un tercer punto de control, en el que la célula no continuará la mitosis si los cromosomas no están perfectamente alineados en el huso acromático, antes de empezar a separarse por sus cromátidas. En el control del ciclo celular intervienen diferentes factores que interactúan entre sí, que pueden hacer que la célula detenga su crecimiento y división. Algunos de los principales factores que controlan el ciclo celular son: 1. ENZIMAS: intervienen dos proteínas clave, las ciclinas y las proteínas quinasas dependientes de ciclinas (Cdk). Las proteínas quinasas (Cdk) se asocian con distintas ciclinas en las diferentes etapas del ciclo celular, formando el complejo CdK-ciclina. La activación de este complejo dispara procesos que conducen a la célula a través de las distintas etapas del ciclo. La degradación de las ciclinas inactiva el complejo. 2. FACTORES DE CRECIMIENTO (GF): son diferentes proteínas que actúan como hormonas, que activan los genes que intervienen en la proliferación celular, entre ellos los protooncogenes, que inducen a la célula a entrar en la Fase S y en división.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
4
3. FACTORES GENÉTICOS: existen diferentes genes que controlan el ciclo celular, entre ellos: Protooncogenes: intervienen en el crecimiento y la división celular. Genes supresores de tumores: detienen el ciclo celular, impidiendo la proliferación celular y por tanto las formación de tumores. Gen p53: paraliza el ciclo celular ante cualquier alteración del ADN. (leer artículo sobre gen p53) Gen p27 Una mutación en estos genes provocarían una división incontrolada de las células y la formación de tumores cancerosos. En muchos casos la presencia de genes alterados conduce a la proliferación descontrolada de las células que se encuentra en el origen de todo cáncer. 4. OTROS FACTORES: Tamaño celular: el crecimiento estimula a la célula a dividirse. o con otras células: el o con otras células impide el crecimiento celular y por tanto inhibe la división. Edad: a mayor edad, menor será el número de veces que las células se dividan en un cultivo. Oxigenación: la falta de oxigenación puede producir la muerte celular por necrosis. LA MUERTE CELULAR Las células no se multiplican indefinidamente, dependiendo del tipo celular se da un número limitado de divisiones. Cuando esto sucede la célula entra en una fase de senescencia (Fase G0) hasta que muere de forma programada, mediante un mecanismo denominado apoptosis celular. La apoptosis es un proceso necesario, ya que permite la renovación celular, de manera que las células muertas son reemplazadas por nuevas células jóvenes. Dicho proceso ha de estar controlado, tanto por factores externos del medio, como por factores internos de la propia célula. Si este control deja de producirse origina un descontrol en el ciclo celular que conduce a algunas patologías, como el Cáncer, Alzheimer, Parkinson y la Cardiopatía isquémica. Cuando las células mueren por un daño irreparable (infección, falta de O 2, lesión grave, presencia de toxinas,...) hablamos de necrosis celular, que provoca inflamación en la zona y esta acaba cicatrizando. Las dos formas de muerte celular, apoptosis y necrosis, originan diferentes fenómenos en la célula, tal y como muestra la figura:
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
5
1.2. MITOSIS La Mitosis o Fase M es una período de gran actividad celular. En él se produce la división nuclear o cariocinesis, y los cromosomas duplicados se distribuyen de manera idéntica en cada una de las células hijas mediante un estructura formada por microtúbulos denominada huso acromático. Al final de la mitosis se originan dos células hijas idénticas genéticamente y con la misma dotación cromosómica que la célula madre.
Etapas de la mitosis (cambios que se producen) PROFASE: Condensación de las fibras de cromatina y formación de los cromosomas. Cada cromosoma se formará a partir de dos fibras de cromatina idénticas genéticamente, generando cada una de ellas las dos cromátidas del cromosoma. Desaparición progresiva del nucleolo Formación de una nueva pareja de centríolos, de manera que las dos parejas de centríolos se desplazan a ambos polos de la célula quedando unidas por los filamentos del HUSO ACROMÁTICO o HUSO MITÓTICO. Entre las fibras del huso acromático se pueden diferenciar dos tipos: Fibras polares: van de un polo a otro de la célula Fibras cromosómicas: se unen a los cromosomas por el cinetocoro Entrada de agua en el núcleo celular, lo que provoca que se hinche y la membrana nuclear acabe rompiéndose, de manera que al final de la profase el núcleo ha desaparecido como estructura. METAFASE: Las fibras cromosómicas del huso acromático se alargan y provocan que los cromosomas se dispongan en el centro del huso acromático, formando la PLACA ECUATORIAL. Durante la metafase los cromosomas alcanzan su máximo grado de condensación, denominándose cromosomas metafásicos, cada uno de ellos con dos cromátidas, tal y como hemos estudiado. ANAFASE: Las fibras del huso acromático se acortan, provocando la separación de las dos cromátidas de cada cromosoma (cromátidas hermanas). Al final de la anafase existen dos grupos de cromátidas hermanas, uno a cada lado de la célula. Estas cromátidas, constituyen en sí cromosomas de una sola cromátida (cromosomas anafásicos). Los dos grupos de cromátidas son genéticamente idénticos. TELOFASE: Cada grupo de cromátidas o cromosomas anafásicos se va rodeando de fragmentos de membrana nuclear procedentes del retículo endoplásmico. Los cromosomas se van estirando y poco a poco se vuelven a convertir en filamentos de cromatina. Progresivamente se va formando un nuevo nucleolo, alrededor de cada nuevo núcleo. El huso acromático desaparece. Al final de la telofase la célula presentará dos núcleos claramente diferenciados, pero genéticamente idénticos.
1.3. CITOCINESIS o CITODIÉRESIS La división celular no termina con la mitosis, con ella se ha repartido la dotación genética de la célula, pero aún es necesario que el citoplasma se divida entre las dos células hijas y se repartan los orgánulos celulares de la manera más equitativa posible. Este proceso es la citocinesis o citodiéresis, y ocurre de forma diferente en las células animales y vegetales. Está sincronizada con la mitosis y se realiza al final de la telofase.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
6
a) Células animales: la división del citoplasma se realiza por estrangulamiento. En el centro de la célula se origina una especie de anillo contráctil que estrangula a la célula hasta que se cierra y provoca la separación de las células hijas. b) Células vegetales: la división de citoplasma se produce por tabicación. Entre los dos núcleos formados se origina una especie de tabique (fragmoplasto) a partir de vesículas del Aparato de Golgi, que separará las dos células hijas.
2. MEIOSIS ( R! ) La meiosis es una forma de división o reproducción celular mediante la cual, una célula madre se divide dos veces consecutivamente originando cuatro células hijas, con la mitad de cromosomas que la célula madre de la que proceden y genéticamente distintas entre sí. La meiosis solamente se produce en células diploides (células 2N), originando células hijas haploides (células N). En nuestro organismo las únicas células que se dividen por meiosis son las células madre de los gametos, espermatogonias y ovogonias, (células2N), generando así los espermatozoides y óvulos (células N). Fases de la meiosis MEIOSIS I o Fase reduccional (1ª división). Se generan dos células con la mitad de cromosomas que la célula madre PROFASE I: es la etapa más larga de la meiosis. Se distinguen los siguientes períodos: Leptotene: las cromátidas se condensan para formar cromosomas. Zigotene: los cromosomas homólogos se disponen por parejas (apareamiento de cromosomas homólogos) y se unen en determinadas zonas denominadas sinapsis. Paquitene: es cuando se produce la máxima condensación de los cromosomas. Se produce el intercambio de información genética (RECOMBINACIÓN GENÉTICA) entre cromátidas NO hermanas de cromosomas homológos, mediante un fenómeno físico denominada SOBRECRUZAMIENTO o ENTRECRUZAMIENTO. Diplotene: los cromosomas homólogos de cada pareja comienzan a separarse. Cada cromosoma tendrá cromátidas genéticamente distintas debido a la recombinación genética. Diacinesis: los cromosomas homólogos de cada pareja han completado su separación. Se rompe la membrana nuclear y se forma el huso acromático.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
7
METAFASE I: los cromosomas homólogos se colocan por parejas en el centro de la célula formando la PLACA ECUATORIAL. ANAFASE I: se separan los cromosomas homólogos de cada pareja, se forman dos grupos de cromosomas, cada uno con DOS cromátidas, y genéticamente distintos, uno a cada lado de la célula. Recuerda que las dos cromátidas de cada cromosoma son genéticamente distintas. TELOFASE I: al final de esta etapa se originan dos células hijas con la mitad de cromosomas que la célula madre de la que proceden y genéticamente distintas. Además son células N, ya que NO presentan parejas de cromosomas homólogos. MEIOSIS II (2ª división). Se trata de una mitosis normal, con sus correspondientes etapas (PROFASE II, METAFASE II,...). Al final de esta segunda división se originarán cuatro células, dos por cada una de las que se formaron en la 1ª división, todas ellas haploides (células N), con la mitad de cromosomas que la célula madre original y genéticamente diferentes.
3. MITOSIS, MEIOSIS y REPRODUCCIÓN Tanto la mitosis como la meiosis son dos tipos de división celular, sin embargo tienen una función diferente: La mitosis interviene en el crecimiento, la renovación celular y la regeneración de tejidos dañados en los organismos pluricelulares, y en la reproducción asexual de los organismos. La meiosis es imprescindible en la reproducción sexual, ya que gracias a ella se originan las células reproductoras o gametos. Además permite mantener el número de cromosomas generación tras generación y aporta un aumento de la variabilidad genética gracias a la recombinación genética entre cromosomas homólogos y a la distribución al azar de los cromosomas entre los gamitos (la fecundación al azar de los gamitos sería el tercer factor que aumenta la variabilidad genética).
4. DIFERENCIAS ENTRE MITOSIS y MEIOSIS MITOSIS Se produce UNA DIVISION celular
MEIOSIS Se producen DOS DIVISONES celulares consecutivas, sin interfase por medio. La célula madre origina DOS células hijas idénticas La célula madre origina CUATRO células hijas entre sí, y con igual número de cromosomas que la diferentes genéticamente y con la mitad de célula madre cromosomas que la célula madre En la PROFASE I se produce el La PROFASE se realiza SIN SOBRECRUZAMIENTO. SOBRECRUZAMIENTO de cromosomas homólogos NO hay RECOMBINACIÓN GENÉTICA. y la RECOMBINACIÓN GENÉTICA En METAFASE NO se emparejan los cromosomas En METAFASE I se EMPAREJAN los cromosomas homólgos homólogos En ANAFASE I se separan los cromosomas En ANAFASE se dividen los cromosomas por sus homólogos de cada pareja, formándose grupos de cromátidas, generando cromosomas con una sola cromosomas con dos cromátidas a cada lado de la cromátida célula La mitosis es la forma de división de las CÉLULAS La meiosis es la forma de división que origina las SOMÁTICAS CÉLULAS REPRODUCTORAS o GAMETOS Afecta a células 2N y N Afecta solamente a células 2N, originando células N
Biología y Geología 2º Bachillerato
8
Tema 3. La reproducción celular
5. MEIOSIS y CICLOS BIOLÓGICOS
CICLO DIPLONTE: Meiosis GAMETOGÉNICA Formación gametos ADULTO (2N)
R!
Gametos (N) Fecundación ZIGOTO (2N)
CICLO HAPLONTE: Meiosis ZIGÓTICA Sucede después de la formación del zigoto ADULTO (N)
Gametos (N) Fecundación
R!
ZIGOTO (2N)
CICLO DIPLOHAPLONTE: Meiosis ESPOROGÉNICA Formación de esporas ESPOROFITO (2N)
R!
Esporas (N)
ZIGOTO (2N) Fecundación
Gametos (N)
GAMETOFITO (N)
Mitosis y citocinesis vegetal
Mitosis y citocinesis animal
Las dos cromátidas del cromosoma profásico
Fibras (microtúbulos) del áster
Nuevo centríolo en formación
Fibras polares o continuas
Envoltura nuclear fragmentada PRINCIPIO DE LA PROFASE
PROFASE Cromosomas dispuestos en la placa ecuatorial
Fibras cromosómicas constituidas por microtúbulos cinetocóricos
PROFASE Semihuso Interzona
Cromosomas orientados por las fibras del huso
Semihuso
FINAL DE LA PROFASE
METAFASE Complejo centriolar
Fibras (microtúbulos) interzonales
Semihuso acortado
PRINCIPIO DE LA ANAFASE
Inicio de la nueva envoltura nuclear Interzona alargada
Surco de división Cilindros de sustancia densa
Semihuso acortado FINAL DE LA ANAFASE
INICIO DE LA TELOFASE
Cilindros de sustancia densa
Anillo contráctil
FINAL DE LA TELOFASE
Mitosis y citocinesis por estrangulación de una célula 2 n en que n 5 2.
Cromosomas homólogos
Inicio de la sinapsis
Nódulo de recombinación produciendo un entrecruzamiento Bivalente
Centrómero
PROFASE I
Bivalente (5 tétrada) Paquiteno
Zigoteno
Leptoteno
METAFASE I
Diacinesis
Diploteno
ANAFASE I
Quiasma: unión temporal resultante de un entrecruzamiento. Aparece en la desinapsis.
TELOFASE I
Las dos cromátidas hermanas de un solo cromosoma Bivalente: las cuatro cromátidas de los dos cromosomas homólogos unidos Citocinesis e intercinesis PROFASE II
METAFASE II
ANAFASE II
n
n
n TELOFASE II
Meiosis de una célula 2 n en que n 5 2.
n
Gen P53, asesino y policía MALÉN AZNÁREZ 27/01/2008 Es la estrella de los genes, un supergén temido y amado al tiempo, porque de su actuación depende que se desarrollen, o no, algunos de los cánceres más frecuentes. Policía y asesino, a p53 le persiguen médicos, investigadores y grandes laboratorios. Ahora se ha descubierto que también puede influir en el envejecimiento. Es una historia fascinante. Una historia en la que un malo, malísimo, un perfecto asesino, se convierte de repente en bueno, buenísimo, en un magistral guardián del bien. Pero, como el famoso protagonista de Stevenson, sigue siendo al mismo tiempo Dr. Jekyll y Mr. Hyde, a ratos asesino, a ratos policía. También es una historia con un toque calvinista de la que, en algún momento, se desprende la idea de que todo lo bueno esconde su parte de maldad. Y es una historia con suspense, porque en el aire flota un posible premio Nobel difícil de adjudicar. Por si fuera poco, en-globa bajo el mismo techo a dos de los ogros del siglo: el cáncer y el envejecimiento. Aunque lo parezca, no es un relato policiaco. Es sólo la trayectoria apasionante de un gen, el más famoso de todos los genes, un supergén. Porque p53, que así se llama el protagonista, ha conseguido traspasar la barrera investigadora de genetistas, bioquímicos, biólogos moleculares y médicos, para saltar a los medios de comunicación no especializados. Se le conoce como el guardián del genoma, el policía de los oncogenes, el gen asesino, el gen protagonista y muchas cosas más. Todavía es joven, no ha cumplido aún 30 años, lo que en investigación es una nadería, y por eso sorprende su rápida fama. En 1993 fue declarado “el gen más importante del año” y, desde entonces, no ha hecho más que ganar terreno. Es el único gen al que se dedica en exclusiva un congreso internacional cada dos años. Se le ha estudiado, y se le estudia, en todos los aspectos que puedan imaginarse, y su posible manipulación es una diana codiciada por los grandes laboratorios farmacéuticos del mundo que buscan contrarreloj un fármaco que se perfila cercano. ¿Qué le hace tan fascinante? El investigador Manuel Serrano, jefe del grupo de Supresión Tumoral del Centro Nacional de Investigaciones Oncológicas (CNIO), que lleva años trabajando en p53, lo tiene clarísimo. “Es un gen clave; por eso es la estrella de los genes”. La explicación de Serrano, como la de tantos investigadores que en todo el mundo se dedican al “gen estrella”, es sencilla: p53 es clave, porque es el gen que con más frecuencia se encuentra mutado en el cáncer. Para que haya un cáncer p53 tiene que estar inactivado, y lo está en el 55% de los cánceres más comunes: mama, colon, pulmón, vejiga, linfoma. “P53 es un gen que se activa sólo en situación de estrés, cuando hay daño en una célula. Es un detector de situaciones peligrosas, un sensor; por eso se le llama “guardián” o “policía”, porque cualquier alteración que haya en la célula, y hay muchas asociadas al cáncer, lo activa. Entonces, p53 bloquea o mata la célula alterada, impide su proliferación o división celular. En definitiva, imposibilita la propagación de la célula dañada por apoptosis (suicidio celular) o porque la mantiene bloqueada sin dejarla reproducirse”, explica Serrano. Crucial a la hora de prevenir el cáncer, p53 es un gen anticanceroso que en circunstancias normales nos defiende de la enfermedad. Cuando fue descubierto, en 1979 (su nombre se debe a que la proteína que lo codifica tiene un peso molecular aproximado de 53.000), entró enseguida a formar parte de la lista de los genes malos, los oncogenes o genes causantes del cáncer. Pero, en 1989, pasó a integrar el grupo de los buenos, el de los supresores tumorales que inhiben o detienen la división celular —el cáncer se produce por una acumulación de daños genéticos originados por células que se multiplican sin control—. Pasó que su primera identificación se hizo con una de sus formas mutadas, y nocivas, no con su estado natural. Esta curiosa doble función puede tener la culpa de que aún no se haya concedido el Nobel a los supresores tumorales, como se hizo en su día con los oncogenes. Quizá porque, como se pregunta Serrano, “¿a quién se lo dan?, ¿a los tres investigadores que descubrieron una versión mutada y pensaron que era un oncogén, o a quien, una década después, se dio cuenta de que era un gen supresor?
¿P53 es igual en todos los humanos? “Sí, en general, pero no es idéntico; hay minúsculas variaciones que tienen un pequeño impacto en su función”, dice Serrano, que añade: “Una cosa es clara: un cáncer no puede existir con p53 funcionando a tope”. Y el investigador señala un hecho importante recientemente descubierto que viene a añadir brillo al gen estrella. “Sabíamos que p53 está relacionado con el cáncer, y ahora se ha demostrado que también lo está con el envejecimiento”. Y es en esta faceta en la que el grupo de Serrano, junto con el de María Blasco, también del CNIO, investiga con notables resultados publicados en Nature. Su laboratorio ha fabricado unos superratones modificados genéticamente, con más p53, que son más resistentes al cáncer. “Eso era lo esperado, pero la novedad fue ver que esos animales envejecían más lentamente, vivían un poco más. Eso nos hizo pensar que p53 también podía estar protegiendo del envejecimiento. Una forma de explicarlo sencillamente es decir que el daño causado en la célula, del tipo que sea —de alta intensidad, asociado al cáncer, o de baja intensidad, asociado al envejecimiento—, es el responsable de que haya cáncer y haya envejecimiento. Y p53 estaría noqueando ese daño, disminuyéndolo”. En resumen: p53 protege del cáncer, pero también hace que el envejecimiento se retrase. Así que el famoso gen no sólo es vital para que, haciendo de policía o asesino, nuestro organismo desarrolle, o no, alguno de los cánceres más habituales, sino que, además, si pudiéramos aumentarlo sin contrapartidas perversas, podría ralentizar nuestro envejecimiento. Dos pájaros de un tiro. ¿Se puede hacer? Manuel Serrano sonríe: “¡Es el sueño! Y pensamos que manipulando unos pocos genes podría aumentarse muchísimo la longevidad”. Hasta llegar a los superratones del laboratorio de Serrano, se había demostrado que ratones manipulados genéticamente con p53 por investigadores estadounidenses estaban protegidos del cáncer, pero envejecían prematuramente. Eso hizo pensar que el beneficio anticanceroso de p53 tenía su contrapartida perversa obligada: más envejecimiento. Pero el equipo de Serrano demostró que sus ratones, además de estar protegidos del cáncer, vivían más tiempo. “De alguna manera”, dice el investigador, “la resistencia al cáncer y al envejecimiento tienen que estar sincronizada. Los ratones, en su entorno natural, para el que han sido seleccionados por la evolución, viven muy poco tiempo: seis meses. Los humanos somos de los mamíferos más longevos, tenemos una de las mejores resistencias al cáncer y al envejecimiento, pero la maquinaria molecular de un ratón y un humano es la misma. Eso quiere decir que en esta maquinaria tiene que haber alguna manera de sincronizar ambas cosas, y p53 podría ser el medio. Si se aumenta la potencia de p53, se está luchando contra el envejecimiento y aumentando la resistencia al cáncer simultáneamente”. En esta línea, Serrano recuerda que los genomas de un chimpancé y un humano son prácticamente idénticos en el 99,8%. Sin embargo, la vida máxima de un chimpancé es de 60 años y el humano rara vez sobrepasa los 110. La media de un chimpancé es de 40 años, y la de un humano, de 80. “Debe de haber algo muy sutil en nuestros genes que cambia el hecho de vivir 50 años a vivir 100. Entonces, junto con el equipo de María Blasco, nos disponemos a hacer unas manipulaciones genéticas para ver si somos capaces de aumentar la longevidad en los ratones mucho más. Ése es nuestro desafío. Si conseguimos que un ratón que en el entorno privilegiado de un laboratorio llega a vivir tres años pase a vivir seis, sería una prueba de que la longevidad es algo flexible y sabríamos cómo aumentarla”. ¿Manipular el p53 para estar más jóvenes? “Ésa sería otra posibilidad, prevenir o ralentizar el envejecimiento, pero por ahora es sólo una simple posibilidad, aunque se intuye cercana”, dice Serrano. “Nosotros usamos p53, que es la estrella del cáncer, pero la estrella de la longevidad es la telomerasa, y ahora, combinando ambos genes, hemos visto que los ratones viven mucho más tiempo. Pero éste es un proyecto que dirige María Blasco”. María Blasco, jefa del grupo de Telómeros y Telomerasa del CNIO, lo sabe casi todo sobre el llamado “gen de la inmortalidad”. No en balde, ha sido una de las investigadoras pioneras en el panorama internacional de la telomerasa, una enzima que, cuando se le pone a una célula normal, la convierte en inmortal, ya que se encarga de mantener los telómeros, unas estructuras que están al final de los cromosomas y que con la edad se van perdiendo. Y cuando alguien se queda sin telómeros en las células, no hay división posible de éstas. “No existe vida sin telómeros; si a una especie se le quita la telomerasa, desaparece. Es algo fundamental para la vida y también para la célula tumoral”, apostilla Blasco.
Así que parece obligado preguntar a la bióloga molecular si en esta batalla que tienen emprendida, conjuntamente contra el cáncer y el envejecimiento, es sólo cuestión de ponerle telomerasa a un ratón para hacerlo inmortal. “La respuesta es no, porque la telomerasa hace que haya más cáncer. Para que haya un tumor, tiene que activarse la telomerasa, y si un ratón tiene más telomerasa de lo normal, por ejemplo, haciendo ratones transgénicos, sabemos que tendrá más tumores. Lo que hemos hecho es utilizar los superratones de Manuel, porque el p53 protege del cáncer y alarga en un 18% la vida de los ratones, y si a eso le añadimos el gen de la inmortalidad, la telomerasa, conseguimos que estos ratones multitransgénicos vivan una media de un 50% más, sin cáncer, lo que son palabras mayores. Eso es lo que hemos descubierto ahora”. Palabras mayores. Porque esta prolongación de vida, de un 50%, en los superratones es la más larga que se ha descrito en mamíferos. Más de lo que se consigue con la restricción calórica, que es uno de los mecanismos más importantes para alargar la vida. “No hemos conseguido todavía hacer ratones inmortales, lo que quiere decir que probablemente haya más cosas, y ése es el siguiente paso. Ésta es la primera vez que se revela un efecto de la telomerasa en la longevidad. En ningún organismo, ni gusano, ni levadura, se había visto; sólo en células”, asegura Blasco, sin ocultar su satisfacción. Se sabía que la telomerasa es un gen que tiene que ver con el envejecimiento y que, cuando se quita, el organismo envejece antes. “Pero lo que no se sabía, al menos nadie lo había demostrado hasta ahora, es que, cuando se aumenta, también aumenta de forma notable la vida del ratón, que es un mamífero. Y hemos visto que si eliminamos el cáncer y a la vez aumentamos la telomerasa, conseguimos alargar mucho más su vida”, dice Blasco, que añade que en humanos, muy probablemente pasaría lo mismo. “Con seguridad, los dos procesos, cáncer y envejecimiento, han coevolucionado. Nos hace mucha ilusión ir extendiendo la vida en ratones, porque probablemente haya que tocar pocas cosas para cambiarla. Esto no es un mero juego genético; si conseguimos identificar la combinación de genes que alargan la vida de un ratón, podremos pensar en diseñar nuevos fármacos que hagan lo mismo en humanos”. Los deseos de Blasco son en estos momentos el sueño de cientos de investigadores en todo el mundo, pero sus trabajos pueden parecer todavía muy básicos y alejados de resultados, a corto o medio plazo, para tratamientos oncológicos. Pero no es así. P53 se ha convertido en una de las más perseguidas dianas de los grandes laboratorios farmacéuticos que buscan aceleradamente un fármaco inteligente capaz de actuar en la curación del cáncer. Y ya se perfilan resultados. En este terreno se hallaría Nutlin, un compuesto activador de p53 (fabricado por Roche) que se está probando en humanos y que entra en el apartado de las llamadas “drogas inteligentes”—está diseñada específicamente, se conoce su estructura tridimensional y cómo activa p53 con todo tipo de detalles—. Pero por el momento es todavía una droga, con problemas pendientes de solución para llegar a la categoría de fármaco, y no se utiliza en tratamientos oncológicos, pero los expertos confían en que podrá hacerse pronto. “La idea al utilizar esta droga, u otras similares, es activar p53 en los tumores donde es funcional pero está dormido”, dice Manuel Serrano, que se declara optimista en cuanto al tiempo que falta para poder usar estos nuevos fármacos. Un poco más cauto, Miguel Ángel Piris, director del programa de Patología Molecular del CNIO, reconoce que hay diversos compuestos como Nutlin que buscan activar p53 y se encuentran ya en ensayos clínicos para testar su utilidad en pacientes. “Pero una cosa es que en el laboratorio sean útiles para las células, e incluso tumores inducidos en ratones, y otra que tengamos un protocolo razonable para tratar pacientes. Además, los ensayos clínicos con drogas nuevas están muy regulados y requiere bastante tiempo alcanzar datos sólidos que justifiquen su uso clínico”. Todavía es pronto para hablar de fármacos, pero donde ya se utiliza habitualmente p53 es en el diagnóstico de algunos tumores como el de mama, donde cerca de un 20% o 30% de casos han perdido p53 frente a otros que no. ¿Cuál es el interés de identificar mutaciones de p53? “En muchos casos, porque identifican formas de cáncer que son más agresivas y que posiblemente requieran una terapia distinta, dado que el cáncer progresa más rápidamente y son pacientes que van a tener una respuesta más pobre a la terapia”, afirma Piris, que trabaja en linfomas. “Es un factor de pronóstico, pero no es un factor predictivo. Nos permite identificar a pacientes
que van a tener una evolución clínica más agresiva, pero, en la mayoría de los casos, lo que no sabemos todavía es cómo tratar adecuadamente a estos enfermos”. Los tipos de tumores en los que la mutación de p53 es más frecuente son los de ovario, esófago, colorrectal, cabeza y cuello, y pulmón. Y los pronósticos más desfavorables están asociados a los de pulmón, vejiga, linfomas y sarcomas. Pero Piris, que forma parte de un grupo internacional que acumula datos sobre mutaciones de p53 desde hace casi veinte años (en 500 casos de linfoma han visto que la mutación estaba presente en el 20% de los casos, y eso se correlacionaba con un pronóstico desfavorable), es optimista. “Hasta hace poco, no sabíamos siquiera que existieran mutaciones frecuentes en este gen o qué función tenía en las células normales o neoplásicas. Ahora conocemos más acerca de su función y cómo se inactiva, bastante acerca de la frecuencia de las mutaciones, y experimentalmente cómo se puede bloquear el efecto de esas mutaciones. Espero que en un futuro seamos capaces de recorrer de forma rápida el camino que va del conocimiento a la terapia”. Dado que el organismo humano está siempre expuesto a daños exógenos, además de los endógenos —en nuestras células hay a veces errores accidentales—, es bueno saber si se conocen agentes externos, como el alcohol, el tabaco, los insecticidas o la contaminación industrial, que faciliten la mutación de p53. “Lo cierto es que tanto el tabaco como la radiación ultravioleta han sido incriminados como potenciales mutágenos de p53. El cáncer de pulmón en los fumadores tiene un patrón característico de mutaciones de p53 que sugiere daño al ADN debido a los efectos de los carcinógenos del tabaco. Un fenómeno parecido se observa en las mutaciones de p53 en los tumores cutáneos atribuidos a la radiación solar”, afirma Piris, que añade sonriente: “Pero si pudiéramos inducir la activación de p53 nativo —no el mutado que ejerce como oncogén—, desaparecería el problema”. Doble juego, asesino y guardián. © Diario EL PAÍS S.L. - Miguel Yuste 40 - 28037 Madrid [España] - Tel. 91 337 8200 © Prisacom S.A. - Ribera del Sena, S/N - Edificio APOT - Madrid [España] - Tel. 91 353 7900
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
1
ACTIVIDADES UNIDAD 3. LA REPRODUCCIÓN CELULAR 1. Desde que una célula se origina hasta que se divide en dos células hijas, hay dos etapas claramente diferenciadas en el ciclo celular. a) ¿Qué nombre recibe cada una de esas etapas?. b) ¿En qué fases se divide cada etapa?. c) ¿En qué momentos del ciclo celular hay cambos en la cantidad de ADN?. d) Pon un ejemplo de célula que no experimente división celular una vez que ha alcanzado la diferenciación. 2. Relaciona los conceptos de ambas columnas: Célula somática Célula haploide Fase M Duplicación del ADN Cromosoma anafásico Célula diploide Gameto División celular Fase Go Una cromátida Cromosoma metafásico Dos cromátidas Fase S Diferenciación celular 3. La colchicina es una droga que inhibe la polimerización de la tubulina y, por tanto, la formación de microtúbulos. ¿Qué efectos tendrá sobre la mitosis?. 4. ¿Cuántas células se formarán después de 30 mitosis consecutivas, sufridas por todas y cada una de las células resultantes de una célula inicial?. 5. Las células hepáticas de cierta especie animal poseen dos cromosomas metacéntricos y dos telocéntricos. a) ¿Pueden tener los óvulos de las hembras de esta especie, solamente dos cromosomas metacéntricos? b) ¿Y las células renales? 6. Se sabe que, en los eucariotas, cada cromátida está constituida por una sola molécula de ADN. Indica el número de estas moléculas de ADN en las siguientes células de una especie con 2n = 6. a) Un espermatozoide. b) Una célula en metafase mitótica. c) Una célula en periodo G1. d) Una célula en periodo G2. e) Una célula en profase de la segunda división meiótica. 7. ¿Cómo se genera la variabilidad genética en la reproducción sexual?.
Biología y Geología 2º Bachillerato
Tema 3. La reproducción celular
2
DIBUJOS y ESQUEMAS 8. Dibuja una célula 2n = 4 en anafase mitótica. 9. Dibuja una célula 2n = 6 en estado de profase y anafase mitóticas y en profase I y anafase I meióticas.
10. En qué etapa de la mitosis se encuentran las siguientes células: A
B
C
11. La célula representada se encuentra en una etapa de la Meiosis. Indica de qué etapa se trata. ¿Qué diferencia encuentras entre esta misma etapa en Mitosis y Meiosis?.
12. La gráfica representa la variación en el contenido de ADN durante el ciclo celular. Responde: a) ¿Qué ocurre en el intervalo de tiempo 2 a 3?. ¿Cómo se denomina la fase que transcurre en ese intervalo?. b) ¿La gráfica corresponde a un ciclo mitótico o meiótico?. ¿Porqué?.
Biología 2º Bachillerato
ACTIVIDADES DE REFUERZO TEMA 3. REPRODUCCIÓN CELULAR 1. Observa la grafica y contesta: a) ¿Qué representa la gráfica?. Explica cómo cambia el contenido de ADN desde la fase A hasta la G. b) ¿Qué función tiene el cambio de contenido de ADN?. Suponiendo que los cromosomas se vieran visibles a lo largo de todo el ciclo, ¿en qué fases desde la C a la G, de la gráfica 1 encontrarías las estructuras cromosómicas (1 a 4) que se muestran en la figura 2?.
2. Las figuras (A-O) representan diferentes etapas de la meiosis masculina de una planta 2n = 6. Establece el orden correcto en que suceden.
3. El esquema representa de forma muy simplificada varios aspectos del comportamiento cromosómico en la primera división meiótica en un organismo 2n = 8. Identifica los procesos numerados 1, 2 y 3.
Biología 2º Bachillerato 4. En la figura aparecen tres células anafásicas (A, B y C) de una especie animal 2n = 6. ¿En qué división se encuentran cada una de ellas (mitosis, 1º división meiótica, 2ª división meiótica)?. Razona la respuesta.
5. En la figura aparecen tres células (A, B y C) de una especie animal 2n = 6. ¿En qué fase de la mitosis o de la meiosis está cada una de ellas?. Razona la respuesta.
6. En siguiente esquema representan una fase concreta del proceso meiótico. Explica razonadamente de qué fase y de qué división se trata. ¿Cuántos quiasmas se han producido como mínimo en este meiosis?. ¿Cuántos cromosomas tendrá el organismo adulto al que pertenece esta célula?.
TEMA 4. LA NUTRICIÓN CELULAR: EL METABOLISMO 1. VISIÓN GLOBAL DE LA NUTRICIÓN CELULAR 2. CAPTURA e INGESTIÓN DEL ALIMENTO: EL INTERCAMBIO DE SUSTANCIAS ENTRE EL INTERIOR y EL EXTERIOR DE LA CÉLULA 2.1. INTERCAMBIO DE PEQUEÑAS MOLÉCULAS e IONES A TRAVÉS DE LA MEMBRANA
• •
Transporte pasivo Transporte activo
2.2. INTERCAMBIO DE MACROMOLÉCULAS y PARTÍCULAS
• •
Endocitosis Exocitosis
3. INTRODUCCIÓN AL METABOLISMO CELULAR 3.1. CARACTERÍSTICAS DE LAS REACCIONES METABÓLICAS 3.2. CATABOLISMO Y ANABOLISMO 3.3. TIPOS DE METABOLISMO 3.4. LA ENERGÍA EN LAS REACCIONES METABÓLICAS: LA IMPORTANCIA DEL ATP
4. REGULACIÓN DE LAS REACCIONES METABÓLICAS: LAS ENZIMAS 4.1. CONCEPTO DE CATÁLISIS y DE ENZIMA 4.2. ACCIÓN ENZIMÁTICA 4.3. CINÉTICA ENZIMÁTICA 4.4. FACTORES QUE INFLUYEN EN LA VELOCIDAD DE LAS REACCIONES ENZIMÁTICAS 4.5. MECANISMOS PARA AUMENTAR LA EFICACIA ENZIMÁTICA 4.6. REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA 4.7. CLASIFICACIÓN DE LAS ENZIMAS
5. CATABOLISMO 5.1. INTRODUCCIÓN AL CATABOLISMO: LA OXIDACIÓN 5.2. CATABOLISMO DE LOS GLÚCIDOS 5.2.1. LA GLUCÓLISIS 5.2.2. LA RESPIRACIÓN AEROBIA
• • • •
Formación del acetil-CoA El ciclo de Krebs La cadena respiratoria Balance energético de la oxidación completa de la glucosa
5.2.3. LA FERMENTACIÓN
• •
Fermentación láctica Fermentación alcohólica
5.3. CATABOLISMO DE LÍPIDOS
•
β-oxidación de los ácidos grasos
5.4. CATABOLISMO DE PROTEÍNAS 5.5. CATABOLISMO DE ÁCIDOS NUCLEICOS
6. ANABOLISMO
6.1. LA FOTOSÍNTESIS 6.1.1. LOS PIGMENTOS FOTOSINTÉTICOS Y LOS FOTOSISTEMAS 6.1.2. MECANISMO GENERAL DE LA FOTOSÍNTESIS
• •
Fase luminosa Fase oscura
6.1.3. BALANCE GLOBAL DE LA FOTOSÍNTESIS 6.1.4. FOTOSÍNTESIS BACTERIANA 6.1.5. FACTORES QUE INFLUYEN EN LA FOTOSÍNTESIS 6.1.6. IMPORTANCIA DE LA FOTOSÍNTESIS 6.2. LA QUIMIOSÍNTESIS 6.3. OTRAS RUTAS ANABÓLICAS
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
1
1. VISIÓN GLOBAL DE LA NUTRICIÓN CELULAR Mediante las funciones de nutrición, la célula toma materia y energía del medio, y las transforma con dos objetivos: fabricación de nuevos materiales celulares y obtención de energía para realizar diferentes trabajos. En consecuencia, la nutrición celular comprende los siguientes procesos: entrada de materiales (ingestión y digestión), transformación de los mismos (metabolismo) y eliminación de productos (excreción y secreción). Ingestión y digestión. La ingestión es la entrada de nutrientes en la célula por diferentes mecanismos que veremos más adelante. Las moléculas de gran tamaño y las partículas, e incluso restos celulares y células enteras quedan englobadas en vesículas endocíticas y son digeridas, tal y como hemos visto en el tema anterior, por los lisosomas. Las moléculas pequeñas no precisan de digestión. Metabolismo. El metabolismo es el conjunto de reacciones químicas enzimáticas que sufren los nutrientes en el interior de las células, con los dos objetivos antes indicados. Las moléculas de las diferentes sustancias contienen energía química, almacenada en forma de enlaces, de modo que las reacciones metabólicas implica, conjuntamente, transformaciones de materia y energía, y cada una de ellas está catalizada por un enzima específica. Excreción y secreción. En ambos procesos, la célula elimina al exterior productos del metabolismo, por diferentes mecanismos. Se habla de excreción cuando se trata de productos de desecho y de secreción cuando las sustancias eliminadas tienen utilidad para otras células.
2. CAPTURA e INGESTIÓN DEL ALIMENTO: EL INTERCAMBIO DE SUSTANCIAS ENTRE EL INTERIOR y EL EXTERIOR DE LA CÉLULA Gracias a la membrana, la célula mantiene una composición diferente en su citosol, y en cada uno de sus orgánulos, a la que existe en el exterior. Pero la membrana no puede ser una barrera completamente impermeable, por lo que las células han tenido que desarrollar sistemas de permeabilidad selectiva para transportar nutrientes esenciales, excretar productos residuales del metabolismo y regular las concentraciones intracelulares de iones. 2.1. INTERCAMBIO DE PEQUEÑAS MOLÉCULAS e IONES A TRAVÉS DE LA MEMBRANA PLASMÁTICA De forma general, la membrana celular, debido a la presencia de la doble capa de fosfolípidos, permite el paso de moléculas hidrofóbicas por simple difusión. Sin embargo, es impermeable a iones y moléculas orgánicas polares, que pasan al interior por mecanismos de transporte específicos en los que intervienen proteínas. Las membranas de cada orgánulo tienen sus propias proteínas de membrana que determinan qué tipo de sustancias pueden entrar o salir. El intercambio de pequeñas moléculas e iones a través de la membrana puede ser por transporte pasivo o activo.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
2
Transporte pasivo El transporte pasivo es un proceso de difusión que ocurre espontáneamente y sin gasto de energía. Siempre sucede a favor de gradiente de concentración (de la zona de mayor a la de menor concentración) o a favor de un gradiente eléctrico (las cargas de distinto signo se atraen). La combinación de ambos gradientes constituye el gradiente electroquímico. El transporte pasivo puede tener lugar por difusión simple o difusión facilitada. • Difusión simple. Algunas moléculas se difunden libremente a través de la doble capa de fosfolípidos, sin la intervención de las proteínas. Pasan así moléculas pequeñas y solubles en lípidos. Concretamente moléculas no polares, como el O2 y el CO2, y moléculas polares sin carga, como el H2O, etanol y la urea. • Difusión facilitada. La bicapa lipídica es impermeable a los iones y a las moléculas polares más o menos grandes, como la glucosa o los aminoácidos. El transporte de dichas moléculas solo es posible mediante unas proteínas transmembrana, que pueden ser de dos tipos: proteínas de canal y proteínas transportadoras o permeasas. • Proteínas de canal. Son proteínas que forman canales o poros que atraviesan la membrana, permitiendo el paso de iones (Na+, K+, Cl-, Ca2+), por lo que también se denominan canales iónicos. La mayoría de estos canales son muy estrechos y solo permiten el paso de iones de manera selectiva, es decir, cada canal deja pasar un tipo de ión. Muchos de ellos no permanecen continuamente abiertos, y su apertura y cierre están regulados por diferentes mecanismos: algunos se abren por la interacción de una molécula señal o ligando (canales regulados por ligando) y otros, como los responsables de la excitación eléctrica de las células nerviosas y musculares, se abren en respuesta a un cambio en el potencial de membrana (canales regulados por voltaje). • Proteínas transportadoras o permeasas. Este tipo de proteínas se unen a la molécula que van a transportar en una parte de la membrana y la liberan en la otra, mediante un cambio conformacional reversible (modelo ping-pong). Cada transportador se encarga de transportar específicamente una determinada molécula o ión, de modo semejante a como la hace un enzima con un sustrato específico.
Transporte activo Se realiza en contra de gradiente electroquímico, y por tanto, lleva un consumo de energía. En todos los casos, el transporte activo tiene lugar mediante proteínas transportadoras que están acopladas a una fuente de energía metabólica, como es la hidrólisis del ATP, actuando como una bomba direccional. Las más importantes transportan cationes de Na+, K+, Ca2+ o H+. En las células animales destaca especialmente la llamada bomba de Na+-K+. Bomba de Na+-K+ La bomba de Na+-K+ es un sistema de transporte que acopla el transporte de Na+ hacia el exterior de la membrana con el tranporte de K+ hacia el interior, ambos en contra de su gradiente. El proceso de transporte se realiza con consumo de ATP, de manera que por cada molécula de ATP consumida se bombean tres Na+ hacia el exterior y dos K+ hacia el interior. Con ello se consigue, que al bombear tres
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
3
cargas positivas hacia fuera y dos hacia dentro, se genera una diferencia de potencial eléctrico a ambos lados de la membrana, de manera que el interior está cargado negativamente respecto al exterior. Esta diferencia de potencial permite mantener el potencial de membrana de las células musculares y nerviosas, lo que hace que sean eléctricamente excitables. La bomba de Na+-K + consume, aproximadamente, el 30 por 100 del ATP de la célula.
2.2. INTERCAMBIO DE MACROLÉCULAS Y PARTÍCULAS Muchas macromoléculas, así como partículas, no pueden pasar a través de las membranas plasmáticas por los mecanismos que hemos visto. La entrada de estos materiales se realiza mediante endocitosis y su salida por exocitosis.
Endocitosis Mediante la endocitosis, las células eucariotas pueden captar continuamente fluidos y moléculas, así como grandes partículas y células enteras. Para ello, el material que se ha de capturar es rodeado progresivamente por una pequeña porción de membrana plasmática, donde se produce un hundimiento o depresión. Después se formará una vesícula endocítica, que quedará en el citoplasma para su posterior utilización, y serán los lisosomas los encargados de digerir su contenido. Existen dos tipos de endocitosis: pinocitosis y fagocitosis. La mayoría de las células eucarióticas ingieren continuamente líquidos y solutos por pinocitosis, mientras que la fagocitosis queda restringida a los protozoos y a células especializadas como los macráfagos y algunos leucocitos, que eliminan microbios, células deterioradas y células cancerosas. • Pinocitosis. Consiste en la ingestión de fluidos y sustancias disueltas mediante la formación de vesículas pinocíticas. Se realiza continuamente en las células eucarióticas e implica pérdidas de membrana plasmática (a veces hasta el 100% en una hora). Normalmente tiene lugar en regiones especializadas de la membrana, que están revestidas por una proteína denominada clatrina. En algunos casos existen, además, receptores específicos en la membrana a los que se unen de forma específica las moléculas que van a ser capturadas. Tiene la ventaja de que así se pueden capturar y concentrar, de forma selectiva, ciertas moléculas específicas, como hormonas, factores de crecimiento, colesterol y otros componentes. • Fagocitosis. Es la ingestión de grandes partículas de tipo variado, incluso, restos celulares o células enteras y microorganismos, utilizando grandes vesículas llamadas fagosomas. Este proceso lo utilizan los protozoos para ingerir grandes cantidades de partículas variadas. En los organismos pluricelulares superiores realizan la fagocitosis unas pocas células especializadas con fines distintos a la nutrición: las células fagocitarias. Entre ellos se encuentran los macrófagos y los neutrófilos, que ingieren y destruyen microorganismos invasores y eliminan células viejas o lesionadas y restos celulares. Para ello proyectan hacia el exterior zonas de la membrana plasmática (pseudópodos) que rodean al microorganismo y terminan englobándolo, formando un fagosoma.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
4
Exocitosis Es un proceso, en cierto modo, contrario a la endocitosis. Se lleva a cabo mediante la fusión de vesículas del interior de la célula con la membrana plasmática. De este modo, las vesículas de exocitosis aportan los componentes de su membrana (fundamentalmente proteínas y lípidos) a la membrana plasmática, compensando las pérdidas de fragmentos de membrana por endocitosis. Mediante la exocitosis, las células eliminan al exterior productos de desecho o secretan moléculas, como hormonas o compuestos que forman la matriz extracelular.
3. INTRODUCCIÓN AL METABOLISMO CELULAR 3.1. CARACTERÍSTICAS DE LAS REACCIONES METABÓLICAS El metabolismo es el conjunto de reacciones químicas que ocurren en el organismo en el interior de las células. En todo momento en una célula suceden miles de reacciones químicas, de manera muy rápida y ordenada, ajustadas a las necesidades que tenga la célula en cada instante. Estas reacciones solo son posibles a temperatura ambiente gracias a las enzimas. El número de reacciones químicas es tan elevado que parece imposible su comprensión. Sin embargo, existen una serie de características generales, aplicables a todas ellas, que permiten clarificar los procesos metabólicos. • Los compuestos que penetran en la célula experimenta una serie de reacciones químicas sucesivas, cada una controlada por una enzima diferente. Estas secuencias ordenadas de reacciones son las rutas metabólicas. Las moléculas que participan en dichas rutas reciben el nombre de metabolitos. En estas rutas el producto final de una reacción constituye la molécula de partida de la siguiente. Las rutas metabólicas son variadas, ramificándose y conectándose una con otras. • Existen rutas metabólicas convergentes y divergentes. En las primeras se obtiene el mismo producto final a partir de distintas moléculas de partida. En las segundas, una única molécula origina diferentes productos. Una misma molécula puede formar parte de una ruta convergente y de otra divergente, originándose itinerarios metabólicos, en ocasiones, muy complicados. Algunas rutas son cíclicas, de manera que los productos de la última reacción son también sustratos de la reacción inicial. • Pese a la enorme variedad de seres vivos existentes, las rutas metabólicas más importantes, como las empleadas en la obtención de energía o para la síntesis de los grandes grupos de moléculas, son comunes en la mayoría de los organismos. Esto constituye un apoyo a la hipótesis del origen único de los seres vivos. • Todas las reacciones metabólicas son catalizadas, es decir, precisan de la presencia de ciertas moléculas, denominadas enzimas, para llevarse a cabo. Para cada una de las reacciones existe una enzima diferente que permite su realización. • Las reacciones metabólicas pueden clasificarse en dos grandes grupos: catabólicas y anabólicas. Las primeras son degradativas, es decir, en ellas se pasa de moléculas más complejas a otras más sencillas. Su
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
5
finalidad es la obtención de energía. Las reacciones anabólicas son, por el contrario, constructivas y, por tanto, sirven para la síntesis de nuevas moléculas. En ellas es necesario un aporte de energía.
3.2. CATABOLISMO y ANABOLISMO El metabolismo, tal como acabamos de ver, puede estudiarse como la suma de dos conjuntos de reacciones: catabólicas y anabólicas.
Catabolismo El catabolismo es el conjunto de reacciones metabólicas en las que los compuestos orgánicos se degradan en moléculas más sencillas y menos energéticas, lo que conlleva una liberación de energía. Se trata pues de reacciones exergónicas. Se pasa de polímeros a monómeros y de monómeros a compuestos orgánicos más pequeños o inorgánicos. En general, estas reacciones implican la rotura de enlaces covalentes y la oxidación de compuestos. La energía que se desprende es utilizada por la célula para fabricar intermediarios ricos en energía, principalmente en forma de ATP o de mediadores reducidos (NADH, NADPH, FADH2, etc.). Cada tipo de molécula (glúcido, lípido, proteína) será degradada en una ruta catabólica específica, y dichas rutas desembocan en rutas catabólicas centrales, por lo que las rutas catabólicas son convergentes. Así, en el catabolismo aerobio se pueden distinguir tres fases principales: ▪ Fase I. Los polímeros o macromoléculas se descomponen, por hidrólisis, en sus respectivos monómeros. ▪ Fase II. Los productos de la fase anterior se degradan en moléculas más simples, las cuales se transforman, mediante una serie de reacciones en una molécula denominada acetil-CoA. Así pues el acetil Co-A puede ser considerado como una encrucijada metabólica, donde confluye el catabolismo de glúcidos, proteínas y ácidos nucleicos. ▪ Fase III. El acetil Co-A se oxida totalmente a CO2 y H2O.
Anabolismo
El anabolismo es el conjunto de procesos de biosíntesis, por los cuales a partir de moléculas sencillas se originan compuestos más complejos y más energéticos. Se trata pues, de reacciones de síntesis, que son endergónicas y por lo tanto, hay un consumo de energía procedente de las rutas catabólicas o de procesos de captación de energía luminosa (como en la fotosíntesis).
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
6
Las reacciones anabólicas incluyen la formación de enlaces covalentes y la reducción de moléculas. A partir de moléculas inorgánicas o moléculas orgánicas sencillas, se sintetizan monómeros y a partir de ellos, los polímeros. El objetivo final del anabolismo es la fabricación de materiales de construcción y de sustancias de reserva. Las rutas anabólicas son divergentes, ya que a partir de unas pocas moléculas precursoras sencillas se sintetiza una gran variedad de macromoléculas. En el anabolismo también se podrían distinguir tres fases: una primera fase, de síntesis de moléculas precursoras pequeñas; una segunda fase, donde dichas moléculas se utilizan para formar monómeros; y una tercera fase, en la que los monómeros se emplean para la síntesis de polímeros (polisacáridos, grasas, proteínas). El anabolismo y el catabolismo, aunque son procesos opuestos, están interconectados y suceden de forma simultánea. Aunque sus caminos no son idénticos, existen rutas metabólicas comunes a ambos, y se denominan rutas anfibólicas, como el ciclo de Krebs, que puede utilizarse con fines anabólicos y catabólicos. 3.3. TIPOS DE METABOLISMO Toda célula necesita tomar del exterior alguna forma de energía que pueda aprovechar, así como alguna forma de materia a partir de la cual fabrique su propia materia. Existen diferentes tipos de metabolismo atendiendo a estas necesidades:
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
7
3.4. LA ENERGÍA EN LAS REACCIONES METABÓLICAS: IMPORTANCIA DEL ATP Las células obtienen la energía, tal y como hemos visto, degradando los compuestos orgánicos mediante reacciones de oxidación y en otras ocasiones (como las células fotosintéticas) a partir de la luz. En estos procesos exergónicos, la energía liberada se utilizara en procesos endergónicos o trabajos que precisen energía, como la síntesis de nuevas moléculas, el transporte activo de sustancias a través de la membrana y los movimientos celulares. Así pues, la energía desprendida en las reacciones exergónicas se puede aprovechar para que ocurran otras reacciones, que en el mismo sentido son energéticamente desfavorables. Esta propiedad se conoce con el nombre de acoplamiento energético entre reacciones. Es tan fundamental, que sin ella, el metabolismo celular sería imposible. En general, por cada reacción endergónica que se produce en la célula existe otra exergónica que, acoplada a la primera, sirve de fuente de energía. La molécula que va a actuar como “moneda de cambio energético” en las células para que se produzca el acoplamiento energético es el ATP.
El ATP El ATP o adenosín trifosfato es un nucleótido que actúa como moneda de energía dentro de la célula. Está formado por una adenina y una cadena de tres grupos fosfato, entre los cuales se establecen “enlaces de alta energía”. El ATP almacena grandes cantidades de energía en los enlaces P~P, pero durante muy poco tiempo, ya que es una molécula que no puede almacenarse (una persona consume unos 45 kg de ATP al día, pero en cada instante la cantidad de ATP es menor de 1 g.). Cuando una célula obtiene energía, bien a partir de la luz o bien por oxidación de moléculas que toma del exterior, utiliza parte de esa energía para fabricar ATP a partir del ADP y fosfato inorgánico. ADP + Pi + energía → ATP + H2O Cuando la célula necesita realizar algún proceso endergónico, lo acopla a la hidrólisis del ATP para dar ADP y fosfato inorgánico, liberándose unas 7 kcal por mol de ATP. ATP + H2O → ADP + Pi + energía (7,3 kcal/mol) Así el sistema ATP/ADP sirve como sistema universal de intercambio de energía, haciendo de intermediario entre los procesos exergónicos o productores de energía y los endergónicos o consumidores de energía. Las enzimas que catalizan la hidrólisis del ATP reciben el nombre general de ATPasas y participan en procesos como movimientos celulares o intercambios de sustancias a través de la membrana. Para activar un compuesto y que aumente su energía útil y pueda hacer reacciones que, por sí solo, serían endergónicas, se le suele transferir un grupo fosfato procedente de la hidrólisis del ATP. Este proceso se denomina fosforilación. El compuesto, al resultar fosforilado, recibe parte de la energía almacenada en el ATP y queda más reactivo. Este mecanismo es típico de reacciones de condensación, que resultarían muy endergónicas si tuvieran que juntarse las moléculas en su estado normal. Mecanismos de síntesis de ATP Como el ATP no puede acumularse en grandes cantidades, no sirve de reserva de energía. Las reservas celulares son sustancias orgánicas, como glúcidos y grasas, de donde ha de ser liberada para “recargar” el ADP en ATP. En otras ocasiones el ATP se forma a partir de compuestos fosfatados los que ceden un grupo fosfato directamente al ADP. En el caso de las células fotosintéticas, la energía de la luz se
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
8
emplea para fabricar ATP. Así pues, son varios los mecanismos de formación de ATP, que se pueden englobar en dos categorías: ▪
Fosforilación a nivel de sustrato: cuando un grupo fosfato procedente de una molécula fosfatada es transferido al ADP para formar ATP en una única reacción química.
▪
Fosforilación asociada a una cadena de electrones: cuando la energía liberada por el transporte electrónico, realizado a favor de gradiente de potenciales de oxido-reducción, es acoplada a la fosforilación del ADP. Existen dos fosforilaciones de este tipo: > Fosforilación oxidativa: que se lleva a cabo en la respiración aerobia al oxidar compuestos orgánicos, y es el principal mecanismo de síntesis de ATP en las células aerobias. > Fotofosforilación: que se lleva a cabo en la fase luminosa de la fotosíntesis y en ella se sintetiza ATP aprovechando la energía luminosa.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
9
4. LA REGULACIÓN DE LAS REACCIONES METABÓLICAS: LAS ENZIMAS. 4.1. CONCEPTO DE CATÁLISIS y DE ENZIMA Las células desarrollan su actividad por medio de un complejo entramado de reacciones químicas orgánicas. Si estas reacciones se produjeran sin catalizadores, serían tan lentas que prácticamente no se llevarían a cabo. Los catalizadores son sustancias que aceleran una reacción química hasta hacerla instantánea o casi instantánea. Los catalizadores biológicos o biocatalizadores son las enzimas. Las enzimas actúan disminuyendo la energía de activación necesaria para que se produzca la reacción, uniéndose temporalmente con las moléculas que están reaccionando. Para comprender el funcionamiento de las enzimas, vamos a estudiar algunos conceptos sobre catálisis química. Cualquier reacción química se inicia con la rotura de ciertos enlaces entre átomos que constituyen las moléculas de los reactivos, para formar, posteriormente, los nuevos enlaces que originan las moléculas de los productos. Este estado en que los enlaces de los reactivos están debilitados, pero en el que aún no se han formado los nuevos, se conoce como estado de transición o estado activado. Para alcanzar dicho estado, es preciso comunicar a los reactivos cierta energía, denominada energía de activación. Dicha energía añadida hace aumentar la energía cinética de las moléculas, o sea, las activa, y tiene dos efectos importantes: ▪ Vencer las fuerzas de repulsión entre los electrones que envuelven a las moléculas que van a reaccionar. ▪ Romper los enlaces químicos de las moléculas que reaccionan y hacer posible la formación de nuevos enlaces. Así pues, solamente las moléculas activadas podrán reaccionar, y por tanto cuanto mayor sea la proporción de moléculas activadas en una reacción, más rápida se desarrollará esta. En las reacciones espontáneas, la energía de activación es tan baja que se obtiene de la propia energía cinética de las moléculas o de la luz que incide en el lugar de la reacción. En las reacciones no espontáneas, esta energía es tan alta que no se produce si no se aplica calor. En química, existen dos formas de conseguir que una reacción transcurra más rápidamente: aplicando calor o utilizando un catalizador. Los catalizadores actúan disminuyendo la energía de activación necesaria para que las moléculas reaccionen, y para ello se unen temporalmente a dichas moléculas, o sea, a los reactivos o sustratos. Esa unión temporal se traduce en un acercamiento íntimo de las moléculas que reaccionan y puede debilitar sus enlaces químicos, con lo que se facilita la formación de otros nuevos enlaces. Como consecuencia de todo ello, los catalizadores al combinarse con los reactivos producen un estado de transición de menor energía de activación que la reacción no catalizada, así pues, es menor la energía inicial que debe usarse para empezar la reacción y, por ello, habrá una mayor proporción de moléculas activadas y la reacción transcurrirá más deprisa. Como el catalizador no se modifica durante el proceso, puede reutilizarse continuamente. Para entender todo este proceso, vamos a considerar una reacción química tal que S
P
S representa la molécula o moléculas reaccionantes (sustratos o reactivos), que constituyen el estado inicial y P representa el o los productos de la reacción, que constituyen el estado final. Pero hay una barrera de energía que los separa, la energía de activación (Ea), que corresponde al estado de transición. Sin la energía de activación, A no existiría, pues no sería estable y se habría transformado en P. S → [ Estado de transición ]→ P
Sustratos
Productos
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
10
Aunque en el laboratorio la energía de activación se puede conseguir con calor, las reacciones en las células se llevan a cabo a baja temperatura, de manera que solucionan el problema mediante el uso de unos catalizadores especiales o biocatalizadores, que denominamos enzimas (E). Las enzimas se combinan con los sustratos de forma reversible, formando el complejo enzima-sustrato (ES), que representa el estado de transición con menor energía de activación que la reacción no catalizada. Posteriormente el complejo enzima-sustrato se escinde, liberando la enzima (E) sin alterar y los productos (P) de la reacción.
E+S
[ ES ]
E+P
4.2. ACCIÓN ENZIMÁTICA Las enzimas son catalizadores muy potentes y eficaces. Las reacciones orgánicas son muy complejas y es habitual que en el laboratorio se formen subproductos. Las reacciones enzimáticas son tan específicas que no se forman productos secundarios y su velocidad es más de una millón de veces superior a la de la reacción sin catalizar. Para entender la catálisis enzimática, conviene resumir las características de las enzimas y de su actividad: • Todos los enzimas son proteínas, a excepción de ciertas moléculas de ARN con actividad catalítica, denominadas ribozimas. • Como catalizadores, las enzimas actúan en pequeñas cantidades y se recuperan después de la reacción. • La característica más sobresaliente de las enzimas es su elevada especificidad. Esta es doble y explica que no se formen subproductos: ─ Especificidad de sustrato. Sustrato es la molécula sobre la que el enzima ejerce su acción catalítica. ─ Especificidad de acción. Cada reacción está catalizada por un enzima específico. • La acción enzimática se caracteriza por la formación de un complejo enzima-sustrato que representa el estado de transición. • El enzima y el sustrato se unen mediante fuerzas débiles (puentes de hidrógeno, interacciones electrostáticas, interacciones hidrofóbicas, etc.) en un lugar específico del enzima denominado centro activo. El centro activo es una pequeña región del enzima que contiene los componentes moleculares
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
11
por los que se une al sustrato. Generalmente se trata de una pequeña depresión situada sobre la superficie de la enzima. La unión entre el enzima y el sustrato para formar el complejo ES se ha explicado tradicionalmente mediante el modelo de la “llave y la cerradura”: el sustrato se une al centro activo y encaja como la llave y la cerradura. Sin embargo, se ha observado que los centros activos de algunos enzimas cambian su forma como respuesta a la presencia del sustrato, hasta que encajan. Así pues, el sustrato induce la forma del enzima para que se produzca el ajuste, por lo que ha este modelo se le ha denominado de ajuste inducido. El proceso sería comparable a cómo se adapta un guante de goma a la mano. El guante vacío tiene una forma parecida a la mano, pero no la forma exacta de la persona que lo va a usar, la cual solo se adquiere una vez puesto en la mano. La complementariedad entre el centro activo del enzima y el sustrato explica la especificidad de la unión entre el enzima y el sustrato.
•
Los enzimas presentan las características de estructura y propiedades expuestas para las proteínas. Pueden ser holoproteínas y heteroproteínas. Algunos enzimas actúan con la ayuda de moléculas no proteicas, denominadas cofactores. En estos casos la proteína enzimática recibe el nombre de apoenzima y el conjunto apoenzima y cofactor se denomina holoenzima. Los cofactores pueden ser: − Inorgánicos: como iones metálicos (Mg2+, Fe2+, Zn2+, Ca2+, etc). − Orgánicos: en este caso se denominan coenzimas. Las coenzimas son moléculas orgánicas complejas, y no suelen ser específicos de una sola apoenzima, es decir, un mismo coenzima puede actuar como cofactor de muchas enzimas diferentes. Los coenzimas suelen unirse débilmente con la proteína enzimática, pero en otros casos se hallan unidos estrechamente, en cuyo caso se habla de grupo prostético. La naturaleza de los coenzimas es muy variada. Pueden actuar como coenzimas: ▪ Vitaminas: como las derivadas del complejo vitamínico B. ▪ Adenosín fosfatos: ATP y ADP. ▪ Piridín nucleótidos: NAD y NADP. ▪ Flavín nucleótidos: FMN y FAD. ▪ Coenzima A.
4.3. CINÉTICA ENZIMÁTICA La cinética enzimática estudia la velocidad de las reacciones catalizadas por enzimas. La velocidad de una reacción (cinética) se define como la cantidad de materia transformada en función del tiempo, y se mide por la desaparición del sustrato o por la aparición del producto, en función del tiempo y por métodos muy variables. En una reacción, la velocidad depende, entre otros factores, de la concentración del sustrato. En 1913, Michaelis y Menten propusieron una ecuación que relaciona la velocidad de reacción con la concentración del sustrato. Según ellos, la reacción enzimática se realiza, tal y como hemos visto, de la siguiente manera:
E+S
[ ES ]
E+P
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
12
Según esto, la enzima (E) se puede encontrar bajo dos formas: libre y combinada con el sustrato. La velocidad de la reacción será máxima cuando todo el enzima esté en la forma ES y la cantidad de enzima libre sea muy pequeña. Estas condiciones se dan cuando la concentración de sustrato es muy alta, ya que los enzimas libres que van apareciendo están intactos y se combinan de nuevo inmediatamente con otra molécula de sustrato, formándose nuevos complejos ES. Si representáramos gráficamente la velocidad (V) de la reacción enzimática respecto a la concentración de sustrato (S), se obtiene una curva hiperbólica típica. Al principio, la velocidad aumenta mucho según aumente la concentración de sustrato, pero llega un punto en que ya no aumenta más por mucho que aumente la [S], es cuando el enzima está saturada de sustrato, y por tanto no quedan enzimas libres. La ecuación de dicha curva es la ecuación de Michaelis-Menten:
v=
Vmax ⋅ [S] K M + [S]
Este dato experimental corrobora la hipótesis de Michaelis-Menten: si realmente se forma el complejo ES, cuando la [S] es suficientemente grande, todo el enzima disponible se encuentra en forma de complejo ES y la velocidad de la reacción es máxima. Uno de los valores que más se utilizan para caracterizar a los enzimas es la denominada constante de Michaelis (KM), que se define como la concentración de sustrato a la cual se alcanza la mitad de la velocidad máxima (Vmax). La KM se mide en moles/l, oscilando entre 10-2 y 10-5 moles/l. El valor de KM se puede determinar gráficamente y cada enzima posee una KM característica para cada sustrato. Por tanto, esta constante indica la afinidad del enzima por el sustrato, de forma que una KM baja indica que con una baja concentración de sustrato se consigue la mitad de la velocidad máxima y por tanto el enzima tiene una gran afinidad por el sustrato. 4.4. FACTORES QUE INFLUYEN EN LA VELOCIDAD DE LAS REACCIONES ENZIMÁTICAS Entre los factores que pueden modificar la velocidad de las reacciones enzimáticas se pueden citar los siguientes: X Concentración de sustrato. Como hemos visto, al aumentar la concentración de sustrato aumenta la velocidad de la reacción hasta un máximo, a partir de ese momento, un aumento de la concentración de sustrato no supone un aumento en la velocidad de la reacción, ya que no quedan enzimas libres al estar saturadas de sustrato. X El pH. Cada enzima tiene un pH óptimo. Los valores por encima o por debajo de este valor óptimo provocan un descenso de la velocidad enzimática, debido a cambios en los radicales que forman el centro activo. Por debajo de un pH mínimo y por encima de un pH máximo, se produce la desnaturalización de la enzima y su actividad se anula por completo. El pH óptimo suele ser bastante próximo al fisiológico, aunque hay enzimas que actúan a pH con valores extremos, como las enzimas digestivas: la pepsina a pH ácido (1,5.2,5) y la tripsina a pH básico (8-11).
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
13
La temperatura. Como en el caso anterior, existe también una temperatura óptima en la que la actividad enzimática es máxima. Las temperaturas inferiores a este valor óptimo provocan una disminución de la vibración molecular que hace más lento el proceso, mientras que temperaturas superiores a la óptima pueden provocar la desnaturalización de la enzima y la pérdida total de funcionalidad. En la especie humana la temperatura óptima es la temperatura corporal.
X
4.5. MECANISMOS PARA AUMENTAR LA EFICACIA ENZIMÁTICA Los procesos metabólicos que tienen lugar en las células se llevan a cabo mediante reacciones encadenadas a través de rutas metabólicas, de forma que el producto final de una reacción es el sustrato de la siguiente. Estas rutas pueden ser largas, por lo que el tiempo para llevarlas a cabo sería elevado. Para que las reacciones se produzcan de forma óptima, existen mecanismos que permiten aumentar la eficacia de la acción enzimática. Algunos de estos mecanismos son los siguientes: • Compartimentación celular. Las enzimas implicadas en algunos procesos metabólicos importantes se localizan juntas dentro del mismo orgánulo celular, y así se encuentran en mayor concentración que dispersas por el citoplasma, y además se asegura que se encuentran en las condiciones ambientales (pH, concentración de iones, etc) adecuadas para su actividad enzimática. • Reacciones en cascada. En este caso el producto de una reacción actúa como enzima de otra reacción, cuyo producto, a su vez, es la enzima de una nueva reacción, y así sucesivamente. Estas reacciones en cascada aumentan la eficacia de la actividad enzimática, ya que el número de moléculas obtenidas aumenta en cada paso de forma considerable. Esto es lo que sucede, por ejemplo, en la coagulación sanguínea, en la que la red de fibrina debe formarse rápidamente para evitar la pérdida de sangre. • Complejos multienzimáticos. Los complejos multienzimáticos son agrupaciones de enzimas que llevan a cabo reacciones consecutivas de una ruta metabólica, lo que permite realizar el proceso completo con gran rapidez, ya que nada más obtener un producto, este puede actuar como sustrato de una nueva reacción al estar en o con la enzima correspondiente. Un ejemplo es el de la piruvatodeshidrogenasa que descarboxila, oxida y activa el ácido pirúvico para formar acetil-CoA que ingresará en el ciclo de Krebs.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
14
4.6. REGULACIÓN DE LA ACTIVIDAD ENZIMÁTICA Las miles de reacciones que ocurren en el interior de las células están rigurosamente controladas ya que las necesidades celulares son cambiantes, y por tanto, la velocidad de las reacciones enzimáticas debe variar de acuerdo con ellas. La regulación de la actividad enzimática se basa en el principio de economía celular por el que solamente permanecen activas las enzimas precisas en cada momento, evitando así la fabricación innecesaria de productos, cuya acumulación, además, puede tener efectos negativos. Los mecanismos de regulación empleados son la activación y la inhibición enzimática y el alosterismo. X Activación enzimática. Se basa en la presencia de ciertos iones y moléculas que actúan como activadores y permiten que ciertas enzimas que se mantenían inactivas lleven a cabo su acción, es decir, se activen. Como activadores pueden actuar algunos cationes, como el Mg2+ o Ca2+, y en otras ocasiones, el propio sustrato es el que activa la enzima, de manera que el sustrato activa su propia metabolización.
X Inhibición enzimática. Los inhibidores enzimáticos son sustancias que disminuyen o anulan la actividad de un enzima. La enzima, previamente activa, deja de actuar en presencia del inhibidor, el cual puede ser algún ión o alguna molécula orgánica y, muy frecuentemente, el producto final de la reacción. En este último caso, en el que la enzima se inhibe cuando ya no es necesario obtener más cantidad de producto y la señal es el propio producto, se habla de inhibición feed-back o retroinhibición.
La inhibición puede ser irreversible, cuando el inhibidor, que se denomina en este caso “veneno metabólico”, se une covalentemente a la enzima, alterando su estructura e inutilizándola permanentemente. Un ejemplo es el cianuro, que actúa sobre la citocromo-oxidasa que interviene en la respiración aerobia, razón por la que este compuesto es un potente veneno. La inhibición reversible, mucho más común, tiene lugar cuando la enzima vuelve a tener actividad una vez eliminada la sustancia inhibidora. En este caso, la unión del inhibidor con la enzima se realiza mediante enlaces no covalentes más fáciles de romper. Si el inhibidor se une al centro activo de la enzima impidiendo, por tanto, la unión del sustrato, se habla de inhibición competitiva ya que el inhibidor y el
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
15
sustrato compiten por el centro activo. Si el inhibidor se une a otra zona de la enzima distinta del centro activo y modifica la estructura del enzima dificultando la unión del sustrato, se habla de inhibición no competitiva. X Alosterismo. El alosterismo es un sistema de regulación enzimática muy preciso. Las enzimas alostéricas catalizan algunas reacciones importantes como, por ejemplo, el primer paso de una ruta metabólica o un punto de ramificación de diferentes rutas metabólicas. Estas enzimas están formadas por varias subunidades (tienen estructura cuaternaria) y poseen varios centros de regulación, es decir, tienen varios sitios para la unión de activadores e inhibidores. Además adoptan dos conformaciones distintas, la forma R (de alta afinidad por el sustrato) y la forma T (de baja afinidad por el sustrato). La forma R se estabiliza cuando los centros reguladores están ocupados por activadores y por el contrario, los inhibidores alostéricos estabilizan la forma T. Entre las subunidades de un mismo enzima existe una cooperación, de manera que la activación o inhibición de una de ellas provoca el mismo efecto en las demás. Esto permite una regulación más rápida y con menor cantidad de activadores e inhibidores. La cinética de estas enzimas es distinta al resto, como puede observarse en la gráfica de la velocidad de reacción frente a la concentración de sustrato, que es una curva sigmoidea.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
16
4.7. CLASIFICACIÓN DE LAS ENZIMAS Se conocen alrededor de 2000 enzimas. En la nomenclatura tradicional, se nombran mediante términos que aluden al sustrato y al tipo de reacción catalizada, añadiendo el sufijo –asa. La nomenclatura recomendada por la Comisión Internacional de Enzimas (IEC) se basa en un código de cuatro números que hace referencia a la clase en que está incluida, a la subclase, a la subdivisión y a la enzima concreta de que se trate. Esta nomenclatura no resulta cómoda y se utiliza con menos frecuencia que la tradicional. Según el tipo de reacción que catalizan, las enzimas se clasifican en seis clases, según el cuadro:
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
17
5. CATABOLISMO 5.1. INTRODUCCIÓN AL CATABOLISMO: LA OXIDACIÓN El catabolismo es el conjunto de reacciones de degradación de moléculas orgánicas complejas. Las reacciones catabólicas tienen lugar en todos los seres vivos, autótrofos y heterótrofos, y su finalidad es proporcionar energía utilizable por la célula, poder reductor y precursores metabólicos. Las reacciones catabólicas más importantes consisten en la oxidación de moléculas orgánicas no hidrolizables, como monosacáridos, ácidos grasos, glicerina, etc. Así el catabolismo se puede considerar como un proceso de degradación oxidativa de moléculas orgánicas, cuya finalidad es la obtención de energía contenida en los enlaces químicos de dichas moléculas. Reacciones REDOX La oxidación es una pérdida de electrones y en las células, las sustancias orgánicas suelen oxidarse por deshidrogenación (pérdida de átomos de hidrógeno, o sea, de e- y H+), lo que implica la existencia de alguna sustancia que capte dichos electrones y protones y que, por tanto se reduzca, por lo que estas reacciones son del tipo oxidación-reducción o reacciones REDOX. Así, las oxidaciones se dan siempre simultáneamente con reacciones de reducción. El compuesto (A-H) que se oxida cede el hidrógeno y/o los electrones a otro que se reduce (B) captándolos. En el catabolismo, los átomos de hidrógeno perdidos por una molécula al oxidarse son captados por los transportadores de hidrógeno (nucleótidos como el NAD+, el NADP+ o el FAD+). Posteriormente estos los cederán al compuesto que se reduce.
Formas de oxidación ▪ ▪
La oxidación de los compuestos biológicos se puede realizar de dos formas distintas: Mediante la fermentación. Consiste en una oxidación incompleta de los compuestos orgánicos en la que el aceptor final de los electrones es otro compuesto orgánico. El ATP se forma por fosforilación a nivel de sustrato. Tiene lugar en el citoplasma. Mediante la respiración celular. Es un proceso de oxidación completa de compuestos orgánicos en el que el aceptor final de electrones es un compuesto inorgánico. Según cuál sea el aceptor, puede ser: > Respiración aerobia: si el aceptor final de electrones es el oxígeno. El ATP se forma por fosforilación asociada a una cadena de electrones (fosforilación oxidativa). En las células eucariotas tiene lugar en las mitocondrias. > Respiración anaerobia: si el aceptor final de electrones es otro compuesto inorgánico, distinto del oxígeno, como el NO3-, SO42-, etc. El ATP se origina por fosforilación oxidativa. La realizan algunas bacterias.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
18
5.2. EL CATABOLISMO DE LOS GLÚCIDOS Tanto si la oxidación se realiza por respiración como por fermentación, la degradación inicial de la glucosa se produce mediante un proceso denominado glucólisis. La glucólisis tiene lugar en el citosol y consiste en una serie de reacciones que conforman una ruta catabólica en la que una molécula de glucosa (seis carbonos) se transforma en dos moléculas de ácido pirúvico (tres carbonos). La glucólisis es, por tanto, una ruta central del catabolismo de la glucosa, común a todo tipo de organismos, tanto aerobios como fermentadores. La diferencia entre unos y otros radica en el destino posterior del ácido pirúvico formado: ▪ En condiciones aerobias, el ácido pirúvico se oxida hasta CO2 y H2O. ▪ En condiciones anaerobias, el ácido pirúvico sigue otros caminos que conducen a las diferentes fermentaciones. 5.2.1. LA GLUCÓLISIS La glucólisis es, probablemente una de las rutas metabólicas más antiguas, ya que se pudo dar en un ambiente anaerobio como el de la atmósfera primitiva y servir de mecanismo de obtención de energía. Consiste en una ruta metabólica que degrada cada molécula de glucosa en dos molécula de ácido pirúvico, obteniéndose como balance energético dos moléculas de NADH y dos moléculas de ATP. Tiene lugar en el citosol Las diez reacciones que componen la glucólisis se pueden agrupar para su estudio en dos etapas o fases: • Fase preparatoria: se activa la glucosa mediante fosforilación y posteriormente se descomponen en dos moléculas de gliceraldehido-3-fosfato (de 3 carbonos). En esta fase, por cada molécula inicial de glucosa se consumen dos ATP. • Fase de producción de energía: consiste en la transformación del gliceraldehido-3-fosfato en ácido pirúvico, mediante una serie de reacciones en las que destacan los siguientes hechos: − Oxidación del gliceraldehido-3-fosfato, liberándose dos átomos de hidrógeno por cada molécula consumida. Los protones y electrones de los átomos de hidrógeno son captados por el NAD+, reduciéndose a NADH + H+ (cada NAD+ capta dos electrones y un protón). − Transferencia del grupo fosfato, desde metabolitos intermediarios a moléculas de ADP, dando lugar a la síntesis de dos moléculas de ATP por gliceraldehido mediante fosforilación a nivel de sustrato. Como por cada molécula de glucosa se forman dos de gliceraldehido-3-fosfato, en conjunto se obtienen 4 ATP y 2 (NADH + H+). Pero al haberse gastado 2 ATP en la primera fase, el balance global es la ganancia de 2 ATP y 2 (NADH + H+) por molécula de glucosa consumida.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
19
5.2.2. LA RESPIRACIÓN AEROBIA Mediante la respiración celular, el ácido pirúvico formado durante la glucólisis se oxida completamente a CO2 y H2O, en presencia de oxígeno. Las etapas de la respiración aerobia son tres: 1. Formación de acetil Co A 2. Ciclo de Krebs 3. Cadena respiratoria
1. Formación de acetil- CoA El ácido pirúvico formado en la glucólisis en el citoplasma celular pasa a la matriz mitocondrial, atravesando las membranas mitocondriales externa e interna. En el interior de la matriz, el ácido pirúvico experimenta una descarboxilación oxidativa, catalizada por un complejo enzimático llamado piruvato-deshidrogenasa. Este oxidación se produce en dos etapas: − El grupo carboxilo se elimina en forma de CO2. − Oxidación del grupo ceto a grupo carboxilo. La energía liberada en este oxidación queda “atrapada” en el enlace de alta energía entre el resto acetilo y la coenzima A (CoA) que interviene en la reacción, y se origina acetil-CoA. Esta oxidación proporciona la formación de una molécula de NADH + H+. Así, por cada molécula de glucosa inicial se producen 2 acetil-CoA, 2 CO2 y 2 (NADH + H+). Los ácidos grasos y los aminoácidos también pueden transformarse en acetil-CoA, por rutas metabólicas distintas que veremos más adelante, y así se incorporan a la respiración aerobia.
2. El ciclo de Krebs El ciclo de Krebs o de los ácidos tricarboxílicos (CAT) es una conjunto cíclico de reacciones que produce la oxidación completa del acetil-CoA hasta CO2. Los electrones cedidos en esta oxidación son captados por las coenzimas FAD y NAD+, liberándose las correspondientes moléculas reducidas, FADH2 y NADH + H+. El ciclo de Krebs se lleva a cabo en la matriz mitocondrial y tiene distintos objetivos: − Obtención de poder reductor: NADH y FADH2. − Obtención de precursores metabólicos. − Obtención de energía en forma de GTP por fosforilación a nivel de sustrato. El acetil-CoA se incorpora al ciclo de Krebs al unirse con una molécula de ácido oxalacético (4 carbonos), separándose el CoA y obteniéndose una molécula de ácido cítrico (6 carbonos). A continuación tiene lugar una serie de reacciones encadenadas, en las que unos ácidos orgánicos se transforman en otros, regenerándose al final el ácido oxalacético con lo que el proceso puede continuar. Por cada vuelta completa del ciclo de Krebs (molécula de acetil-CoA que ingresa en el ciclo) se obtiene como balance: − Una molécula de GTP (convertible en ATP). − Tres moléculas de (NADH + H+) y una de FADH2, que permiten, posteriormente, la formación de moléculas de ATP en la cadena respiratoria. − Dos moléculas de CO2, que corresponde a los carbonos de una molécula de acetil-CoA completamente oxidados. Como se necesitan dos vueltas al ciclo de Krebs para terminar la oxidación de una molécula de glucosa, el rendimiento energético del ciclo de Krebs será: 2 ATP, 6 (NADH+ + H+) y 2 FADH2.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
20
3. La cadena respiratoria La molécula de glucosa que inició la glucólisis se encuentra completamente oxidada. Parte de su energía se ha utilizado en la síntesis de ATP. Sin embargo, la mayor parte de la energía se encuentra en los electrones que fueron aceptados por el NAD+ y el FAD. Estos electrones, procedentes de la glucólisis, la oxidación del ácido pirúvico y el ciclo de Krebs, se encuentran aún en un nivel energético alto. Las formas reducidas del NAD+ y el FAD (NADH y FADH2) tienen un elevado poder reductor y transfieren sus electrones al oxígeno molecular (O2) a través de una cadena de transporte de electrones o cadena respiratoria. Este proceso de transporte de electrones libera gran cantidad de energía libre que se emplea en la formación del ATP a partir de ADP + Pi, en la llamada fosforilación oxidativa. Transporte electrónico En este proceso, los electrones presentes en las moléculas de NADH y FADH2, son cedidos a moléculas transportadoras y pasan de unas a otras a favor de un gradiente de potenciales de oxidorreducción hasta el O2, que actúa como compuesto aceptor final de electrones. La cadena transportadora de electrones o cadena respiratoria que interviene en la respiración mitocondrial está formada por un conjunto de moléculas, asociadas a la membrana interna, capaces de oxidarse y reducirse, es decir, de aceptar electrones de una molécula anterior y cedérselos a la siguiente. Para que este proceso tenga lugar espontáneamente, las moléculas transportadoras deben estar situadas según un gradiente de potenciales de oxidorreducción, de manera que, al pasar de una molécula de la cadena a la siguiente, los electrones “descienden” a niveles energéticos inferiores. Este descenso a niveles energéticos más bajos libera energía, que será empleada posteriormente en la síntesis de ATP por fosforilación oxidativa. Los transportadores de electrones de la cadena respiratoria se agrupan en cuatro grandes complejos supramoleculares que están insertos en la membrana mitocondiral interna: ▪ Complejo I o Complejo NADH-deshidrogena ▪ Complejo II o Ubiquinona o Coenzima Q ▪ Complejo III o Complejo citocromo b-c1 ▪ Complejo IV o Complejo citocromo-oxidasa
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
21
Fosforilación oxidativa: hipótesis quimiosmótica Como hemos visto, la energía liberada en la cadena de transporte de electrones se emplea para fabricar ATP a partir de ADP + Pi, en un proceso denominado fosforilación oxidativa. El mecanismo por el que se sintetiza ATP mediante este proceso se explica por la hipótesis quimiosmótica o teoría del acoplamiento quimiosmótico, y fue propuesto por Peter Mitchell en 1961. Según la hipótesis quimiosmótica, la energía que los electrones van perdiendo al pasar por los complejos transportadores se emplea en bombear protones (H+) a través de la membrana mitocondrial interna, que se acumulan en el espacio intermembranal de la mitocondria. La acumulación de protones entre las dos membranas mitocondriales origina una diferencia de concentración de protones, y también una separación de cargas eléctricas, entre la matriz mitocondrial y el espacio intermembrana, lo que se denomina gradiente electroquímico. Este gradiente electroquímico es capaz de generar una fuerza protón-motriz de unos 230 mV que proporciona energía aprovechable para hacer funcionar cualquier proceso que esté acoplado a un canal por el que puedan circular los protones a favor de gradiente hacia la matriz. La fuerza protón motriz constituye el motor energético de la fosforilación del ADP en la síntesis de ATP. En la membrana mitocondrial interna se encuentran situadas las enzimas ATP sintetasas que contienen un canal en su interior, a través del cual los protones pueden volver a entrar en la matriz mitocondrial. El paso de los protones permite que las ATP sintetasas actúen para formar ATP. Por cada tres protones que pasan por las ATP sintetasas se forma una molécula de ATP a partir de ADP y Pi. Como el flujo de protones es impulsado por el gradiente electroquímico, este proceso tiene carácter quimiosmótico.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
22
Balance energético de la cadena respiratoria En la fosforilación oxidativa, cada par de electrones que son cedidos desde el NADH hasta la molécula de oxígeno proporciona energía para formar tres moléculas de ATP. Cuando los electrones proceden del FADH2, se obtienen dos moléculas de ATP, ya que las moléculas de FADH2 entran en la cadena en un nivel energético menor. BALANCE ENERGÉTICO GLOBAL de la OXIDACIÓN COMPLETA DE LA GLUCOSA Si se considera la producción neta de ATP en las etapas de la glucólisis hasta su conversión en acetil-CoA y su posterior oxidación, la oxidación completa de la molécula produce 36 moléculas de ATP. Esta producción de ATP representa un rendimiento del 40% de la energía contenida en una molécula de glucosa, y equivale a 266 kilocalorías obtenidas por la célula por mol de glucosa consumida. La célula viva es por lo tanto, considerablemente más eficaz que cualquier motor, que puede perder hasta el 75 % de la energía que se le proporciona. La mayor eficacia de la célula se debe principalmente a que la liberación de energía se produce en una serie de reacciones en cadena, en cada una de las cuales tiene lugar un cambio de energía pequeño. De los 36 ATP producidos, solamente dos moléculas de ATP y dos de GTP, se producen por fosforilación a nivel de sustrato. Los 32 ATP restantes se originan por fosforilación oxidativa, a partir del NADH y FADH2. Los NADH formados fuera de la mitocondria (producidos en la glucólisis), no pueden atravesar directamente la membrana mitocondrial interna, pero sus electrones se pueden incorporar a la cadena respiratoria gracias al funcionamiento de las llamadas lanzaderas de sustrato. Se conocen dos tipos: • Lanzadera del glicerol-fosfato: se encuentra en las células del cerebro y músculo esquelético. Los electrones del NADH pasan al FADH2 mitocondrial, con lo que la cadena respiratoria sólo rendirán 2 ATP. • Lanzadera del malato-aspartato: predomina en el hígado y en el corazón. Los electrones del NADH del citosol se transfieren al NADH mitocondrial y rendirán 3 ATP en la cadena respiratoria.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
23
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
24
5.2.3. LA FERMENTACIÓN La fermentación es un proceso de oxidación incompleta de los compuestos orgánicos, ya que no se libera toda la energía química que contienen. El objetivo final de la fermentación es la obtención de energía en forma de ATP, mediante la fosforilación a nivel de sustrato, por lo que no interviene la cadena respiratoria. La fermentación es un proceso anaerobio, por lo que el aceptor final de electrones es un compuesto orgánico, de manera que como productos finales se obtienen diversas sustancias orgánicas más sencillas. El rendimiento energético de las fermentaciones es muy bajo comparado con la respiración aerobia, ya que al tratarse de una oxidación incompleta, los productos orgánicos obtenidos aún conservan un contenido energético considerable. Además la obtención de ATP es por fosforilación a nivel de sustrato, lo que implica el consumo previo de ATP en las reacciones iniciales de activación. La fermentación es realiza principalmente por diversos microorganismos (levaduras y bacterias) que pueden vivir en condiciones anaerobias, pero también en las plantas y animales cuando escasea el oxígeno las células pueden utilizar la fermentación para producir energía. Los sustratos de la fermentación son, generalmente glúcidos, en particular glucosa. No obstante, las bacterias responsables de la putrefacción de la materia orgánica son capaces de llevar a cabo una fermentación de proteínas y aminoácidos, en cuyo caso se habla de fermentación pútrida o putrefacción y se obtienen como productos indol, cadaverina o escatol, responsables del olor de la materia orgánica en descomposición. Las fermentaciones de los glúcidos comienzan con la glucólisis y a continuación en una segunda fase el ácido pirúvico es transformado en diferentes productos finales, variables según el tipo de fermentación. Por lo tanto tienen lugar dos etapas: ▪ Etapa de oxidación de la glucosa hasta ácido pirúvico (glucólisis). Se consume NAD+ y se produce NADH. ▪ Etapa de reducción del ácido pirúvico para dar los productos finales. Se genera el NAD+, necesario para proseguir la glucolisis. La reducción del ácido pirúvico da lugar a los productos finales. Si se origina ácido láctico tiene lugar la fermentación láctica, mientras que si se produce etanol y CO2 se trata de la fermentación alcohólica.
Fermentación láctica Consiste en la degradación anaerobia de la glucosa a ácido láctico. En una primera etapa la glucosa se oxida a dos moléculas de ácido pirúvico, generándose NADH. Posteriormente el ácido pirúvico, al aceptar los electrones del NADH, se reduce a ácido láctico. El rendimiento energético es de 2 moléculas de ATP, obtenidas por fosforilación a nivel de sustrato.
Son muchas las bacterias que realizan este tipo de fermentación, entre las cuales destacan los lactobacilos (Lactobacillus), que se encuentran en la leche y también en el intestino. El queso, yogur y otras leches acidificadas son productos obtenidos por fermentación láctica. También se emplea esta fermentación como método de conservación de ciertos productos vegetales o cárnicos como algunos embutidos.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
25
La fermentación láctica descrita es lo que se conoce como fermentación homoláctica, ya que el ácido láctico es el único producto final. Pero hay bacterias (Lactobacillus bifidus, Lecuonostoc) que hacen una fermentación ligeramente diferente, denominada heteroláctica, en que se además de ácido láctico se producen otras sustancias. La fermentación láctica es un proceso que sucede en las fibras musculares cuando no reciben suficientemente aporte de oxígeno. El ácido láctico al precipitar en las fibras musculares contraídas provoca el dolor característico de las “agujetas”. Cuando el aporte de oxígeno vuelve a ser abundante, el ácido láctico se reconvierte en pirúvico.
Fermentación alcohólica o etílica Consiste en la degradación anaerobia de glucosa a etanol, originándose CO2 como subproducto. La glucosa se oxida a ácido pirúvico, generando NADH. Posteriormente suceden dos procesos: ▪ Descarboxilación del ácido pirúvico, que origina acetaldehído y se libera CO2. ▪ Reducción del acetaldehído a etanol, gracias al enzima alcohol-deshidrogenasa, y consumiendo los NADH producidos en la glucolisis. El rendimiento energético es de 2 ATP, como en la fermentación láctica.
La fermentación alcohólica es realizada principalmente por las levaduras y entre ellos la más conocida y utilizada es Saccharomyces cerevisiae. Ciertas cepas seleccionadas de esta levadura son utilizadas en la producción de vino y cerveza y otras en la fabricación del pan. Saccharomyces cerevisiae sigue un metabolismo fermentativo en condiciones anaerobias, pero cuando hay oxígeno realiza la respiración aerobia, y no produce alcohol. Este fenómeno se conoce como efecto Pasteur, y es importante en la industria de bebidas alcohólicas, pues para que la producción de alcohol sea correcta las levaduras deben desarrollarse en ausencia de oxígeno.
5.3. CATABOLISMO DE LÍPIDOS Por su importancia como reservas energéticas, nos vamos a centrar en el catabolismo de las grasas o triglicéridos. Las grasas son moléculas muy adecuadas como combustible de reserva, pues su catabolismo libera mucha energía, son insolubles en agua y, como tienen poca reactividad química, no provocan reacciones indeseadas en la célula. Muchas células almacenan en su citoplasma moléculas de grasa en forma de pequeñas gotitas, como en los tejidos adiposos. No obstante, estas mismas características hacen que su degradación no sea tan fácil, por lo que cuando la célula necesita un aporte energético utiliza los glúcidos como combustibles, y solamente si necesita un mayor aporte de lo habitual, degrada las grasas. La movilización de las grasas es más lenta que las reservas glucídicas, y además el transporte de las mismas, desde el tejido adiposo a otros lugares, requiere la utilización de moléculas especiales. El catabolismo de las grasas empieza por su hidrólisis, realizada por las enzimas lipasas, obteniéndose glicerina y ácidos grasos. triglicérido + agua → glicerina + ácidos grasos La glicerina se convierte fácilmente en gliceraldehido-3-fosfato y continúan la ruta de la glucólisis. Los ácidos grasas siguen una ruta catabólica especial denominada β- oxidación.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
26
β-oxidación de los ácidos grasos Los ácidos grasos constituyen una fuente de carbono y energía muy importante, ya que su degradación proporciona a la célula muchas más moléculas de ATP por unidad de peso que la glucosa. La β-oxidación consiste en un proceso de oxidación que da lugar a moléculas de acetil-CoA. Esta oxidación se produce en la matriz mitocondrial. El acetil-CoA generado se incorporará al ciclo de Krebs y, posteriormente se llevará a cabo la fosforilación oxidativa. La degradación de los ácidos grasos implica realmente dos procesos: 1. Activación del ácido graso en el citosol. El ácido graso se une a la CoA mediante un enlace éster para formar acil-CoA, que es la forma activa del ácido graso. En esta reacción se consume una molécula de ATP. El acil-CoA penetra en el interior de la mitocondria atravesando las membranas mitocondriales, ayudado por una molécula transportadora llamada carnitina. 2. β-oxidación propiamente dicha. En el interior de la matriz mitocondrial el acil-CoA experimenta un ciclo de reacciones que va escindiendo dos átomos de carbono a partir del extremo carboxilo. La β-oxidación se desarrolla en cuatro etapas: 1. Deshidrogenación. El acil-CoA se oxida por deshidrogenación, originándose una molécula con doble enlace y los átomos de hidrógeno se utilizan para formar FADH2 a partir del FAD. 2. Hidratación. Se añade una molécula de agua al doble enlace generado antes, originándose una grupo alcohol. 3. Oxidación. El grupo alcohol se oxida a cetona y los átomos de hidrógeno se utilizan para formar NADH + H+ a partir del NAD+. 4. Tiólisis. Se rompe el enlace que une los carbonos α y β por la incorporación de una molécula de CoA y se origina una molécula de acil-CoA con dos carbonos menos y otra de acetil-CoA. La nueva molécula de ácil-CoA experimentará un nuevo proceso de β-oxidación. Así en cada β-oxidación, el acil-CoA (ácido graso activado) perderá dos carbonos, por lo que para oxidar completamente un ácido graso activado (acil-CoA) serán necesarias varias β-oxidaciones, o lo que es lo mismo, varias vueltas en este ciclo de reacciones, por lo que el proceso de oxidación total de un ácido graso se suele representar mediante una hélice, denominada hélice de Lynen. En cada vuelta de dicha hélice, es decir, en cada β-oxidación, se obtienen los siguientes productos: − 1 acil-CoA con dos carbonos menos − 1 acetil-CoA, que se incorpora al ciclo de Krebs para su degradación aerobia. − 1 FADH2 y 1 NADH + H, que se oxidan en la cadena respiratoria, de forma que los protones y electrones son finalmente captados por el O2, originándose agua. El proceso genera ATP por fosforilación oxidativa. En consecuencia, los productos finales del catabolismo de los ácidos grasos son CO2, H2O y ATP.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
27
5.4. CATABOLISMO DE PROTEÍNAS Las proteínas y los aminoácidos, no son buenos carburantes metabólicos, ya desempeñan otras funciones (estructural, reguladora, transportadora, etc.). Sin embargo, si no hay suficiente aporte de glúcidos y lípidos (dieta de ayuno), los aminoácidos se pueden utilizar para obtener energía. Asimismo en las dietas excesivamente ricas en proteínas, en las que hay un excedente de aminoácidos o en la degradación normal de proteínas para su renovación, si hay exceso de algún aminoácido. El catabolismo de las proteínas empieza por la hidrólisis de los enlaces peptídicos, liberando los aminoácidos constituyentes. Posteriormente los aminoácidos sufren una degradación, que consiste en dos etapas: 1. Eliminación del grupo amino. El grupo amino se transfiere (transaminación) desde el aminoácido hasta una molécula aceptora, que generalmente es el α-cetoglutarato (a-KG), que se transforma en glutamato. Estas reacciones están catalizadas por las transaminasas y suceden en el hígado. Posteriormente se elimina el grupo amino del glutamato (desaminación oxidativa) en forma de amoníaco o ión amonio. Dicha reacción se lleva a cabo en el hígado y en los riñones, y está catalizada por la enzima glutamatodeshidrogenasa. El amoníaco posteriormente es eliminado en diversas formar: urea en los animales ureotélicos (mamíferos, anfibios, peces de agua salada): ácido úrico en los animales uricotélicos (insectos, aves y reptiles); y directamente como amoníaco en los animales amoniotélicos (invertebrados acuáticos y peces de agua dulce). 2. Oxidación e la cadena carbonada. La molécula carbonada que se origina tras la eliminación del grupo amino, se incorpora a otras rutas metabólicas, tanto catabólicas como anabólicas, distinguiéndose los aminoácidos glucogénicos, que se degradan a ácido pirúvico y otros compuesto y se pueden utilizar para fabricar glucosa) y los cetogénicos, que se utilizan para formar acetil-CoA, que en el hígado se puede transformar en unos compuestos llamados cuerpos cetónicos.
5.5. CATABOLISMO DE ÁCIDOS NUCLEICOS Los ácidos nucleicos, ADN y ARN, son hidrolizados por enzimas nucleasas, liberándose nucleótidos. Estos, a su vez, se descomponen en la pentosa, el fosfato y la base nitrogenada que los constituyen, y pueden ser reutilizados en la síntesis de nuevos nucleótidos o sino son catabolizados. En la degradación de las bases pirimidínas (C, U y T) se origina CO2 y NH3, y en la de las bases púricas (A y G) se origina ácido úrico y alantoína o ácido alantoico, según el animal que se trate.
6. ANABOLISMO El anabolismo es el conjunto de procesos bioquímicos mediante los cuales las células sintetizan la mayoría de las sustancias que las constituyen. Se pueden considerar dos grandes grupos de procesos anabólicos. Unos permiten la obtención de moléculas orgánicas a partir de moléculas inorgánicas y son, por tanto, exclusivos de organismos autótrofos. Según empleen como fuente primaria de energía la luz o la energía desprendida de de la oxidación de ciertas moléculas, se diferencian la fotosíntesis y la quimiosíntesis, respectivamente. Otros procesos anabólicos consisten en la síntesis de moléculas orgánicas a partir de otras, también orgánicas, y los realizan todos los seres vivos, tanto autótrofos como heterótrofos. 6.1. LA FOTOSÍNTESIS La fotosíntesis es un proceso anabólico por el cual las plantas, las algas y algunas bacterias pueden transformar la energía de la luz en energía química, almacenarla en forma de ATP y poder reductor, y luego utilizarla para sintetizar moléculas orgánicas. La vida en el planeta depende de los organismos fotosintéticos pues estos pueden sintetizar materia orgánica de novo. Por ello, constituyen la base fundamental de las cadenas tróficas, es decir, son los productores primarios de los ecosistemas.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
28
Las plantas verdes, algas y cianobacterias llevan a cabo la fotosíntesis mediante un proceso que libera oxígeno como producto final, y por esta razón se llama oxigénica. El oxígeno molecular liberado procede de la fotólisis del agua, que actúa como donador de electrones. Por en contrario, en la fotosínteis anoxigénica, proceso llevado a cabo por el resto de bacterias fotosintéticas, no se utiliza el agua como donador de electrones y, como consecuencia, no se libera oxígeno como producto final. Primeramente, vamos a estudiar la fotosíntesis oxigénica, que se realiza en el interior de los cloroplastos de las células vegetales. 6.1.1. LOS PIGMENTOS FOTOSINTÉTICOS Y LOS FOTOSISTEMAS Para que los organismos fotosintéticos pueden utilizar la energía de la luz, primero tienen que absorberla. Para ello, cuentan con unas sustancias, los pigmentos fotosintéticos. En las plantas verdes, los pigmentos son la clorofila y los carotenoides. En las cianobacterias se encuentran también las ficobilinas, y en algunas algas aparecen entre otros, la ficocianina y la ficoeritrina. La clorofila es un compuesto que contiene un anillo tetrapirrólico, en cuyo interior hay un átomo de magnesio, y una cadena lateral de un alcohol llamado fitol. Las más importantes son la clorofila a y la clorofila b. Los carotenoides, llamados también pigmentos rios, son lípidos de tipo isoprenoide, y absorben la luz a diferente longitud de onda que las clorofilas. Los más importantes son el β-caroteno y la xantofila. Las clorofilas y los carotenoides se encuentran asociados a proteínas, en las membranas tilacoidales de los cloroplastos, formando unas estructuras denominadas fotosistemas. En el interior de cada fotosistema se pueden diferenciar dos zonas: el complejo antena, formado por cientos de clorofilas y carotenoides, que se encargar de absorber la luz. Al hacerlo se excitan y transmiten la energía se excitación a una zona denominada centro de reacción, formado por una molécula especial de clorofila, que al recibir dicha energía libera electrones. Existen dos tipos de moléculas especiales de clorofila, conocidas como P700 y P680, y cada una presenta una máxima eficacia a diferente longitud de onda. Debido a esto, en las membranas de los tilacoides se pueden diferenciar dos tipos de fotosistemas: ▪ Fotosistema I (PSI): se localiza preferentemente en los tilacoides del estroma. El centro de reacción contiene dos moléculas de clorofila a del tipo P700, ya que su máxima absorción de produce a una longitud de onda de 700 nm. ▪ Fotosistema II (PSII): se localiza en los tilacoides de los grana. Su centro de reacción contiene dos moléculas de clorofila a del tipo P680, ya que su máxima absorción es a una longitud de onda de 680 nm. 6.1.2. MECANISMO GENERAL DE LA FOTOSÍNTESIS La fotosíntesis consta de dos fases, cada una de ellas sucede en un lugar diferente de los cloroplastos. ▪ Fase luminosa o lumínica. Se lleva a cabo en los tilacoides. Comprende un conjunto de reacciones dependientes de la luz, cuyo objetivo es absorción y transformación de la energía luminosa en energía química, en forma de ATP y NADPH. ▪ Fase oscura o biosintética. No necesita luz y se lleva a cabo en el estroma. En esta etapa se produce la biosíntesis de compuestos orgánicos a partir de CO2, utilizando el ATP y el NADPH obtenidos en la fase anterior.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
29
FASE LUMINOSA DE LA FOTOSÍNTESIS En la fase luminosa, la energía luminosa se convierte en energía química, originándose dos tipos de moléculas: el transportador de energía, ATP y el transportador de electrones, NADPH. La fase luminosa tiene lugar en la membrana de los tilacoides, que es donde se encuentran las estructuras moleculares que intervienen: − Los fotosistemas, PSI y PSII. Son los que absorben la energía luminosa y desprenden electrones hacia la cadena de transporte de electrones. − La cadena de transporte de electrones, semejante a la de las mitocondrias. Los transportadores de electrones que participan en la cadena son: la Plastoquinona (PQ), el complejo citocromo b6-f y la Plastocianina (PC). Existen dos formas de transporte de electrones: − Transporte no cíclico o acíclico − Transporte cíclico − La ATP sintasa, que genera ATP con la energía liberada en el transporte de electrones por la membrana tilacoidal.
Transporte no cíclico de electrones y fotofosforilación no cíclica (fase luminosa acíclica) El transporte no cíclico de electrones permite utilizar la energía luminosa para producir ATP y NADPH. En este transporte intervienen los dos fotosistemas (PSI y PSII), de manera que se produce un flujo lineal de electrones desde el agua hasta el NADPH. El esquema que representa el transporte no cíclico de electrones es lo que se conoce como esquema Z. Básicamente lo que sucede es que los dos fotosistemas al absorber la luz (fotones) emiten electrones, que pasan del PSII al PSI a lo largo de una cadena de transporte de electrones. El paso de los electrones desde un fotosistema a otro a lo largo de la cadena de transporte libera energía, que se utiliza para sintetizar ATP a partir de ADP y P, en un proceso conocido como FOTOFOSFORILACIÓN. Todo este proceso sucede de la forma siguiente: − El PSII al recibir dos fotones libera dos electrones que son recogidos por la plastoquinona (PQ). Los dos electrones que pierde el PSII son repuestos por el agua, para ello las moléculas de agua que se encuentran en el interior del tilacoide son destruidas por acción de la luz, liberándose O2, protones y electrones. Este proceso se denomina FOTÓLISIS del AGUA. Por cada molécula de H2O destruida: H2O −
½ O2 + 2 H+ + 2 e-
La plastoquinona (PQ) al recibir los dos electrones del PSII se activa y capta dos protones del estroma, reduciéndose de PQ a PQH2. Los dos electrones recogidos por la PQ los transfiere al citocromo b6-f y los protones captados se introducen hacia el interior del tilacoide. Esto provoca que el sistema formado por la Plastoquinona y el Citocromo b6-f actúe como una bomba de protones, que bombea protones del estroma hacia el interior del tilacoide. − Si tenemos en cuenta que las moléculas de H2O al destruirse liberan H+ hacia el interior del tilacoide, y que la Plastoquinona bombea también H+ hacia el interior del tilacoide desde el estroma, esto produce un gradiente electroquímico entre el interior del tilacoide y el estroma, de manera que la [H+] aumenta dentro del tilacoide respecto al estroma, lo que provoca un flujo de H+ desde el interior de los tilacoides hacia el estroma, esos H+ salen de los tilacoides a través de las ATP sintasas, activándolas y provocando la síntesis de ATP a partir de ADP y P. Este proceso se conoce como FOTOFOSFORILACIÓN. Como media, por cada tres H+ que atraviesan las ATP sintasas se genera una molécula de ATP. − Los electrones recogidos por la citocromo b6-f son recogidos por la plastocianina (PC), y esta hace llegar a los electrones al PSI. El PSI al igual que el PSII absorbe fotones, cada dos fotones que absorbe libera dos electrones, esos electrones que pierde son los repuestos por la Plastocianina. Los electrones liberados por el PSI son recogidos por la enzima ferredoxina NADP-reductasa, que se activa, capta dos H+ del estroma y reduce el NADP a NADPH + H+. A este proceso se le conoce como FOTORREDUCCIÓN del NADP.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
30
Esquema del transporte acíclico de lectrones y la fotofosforilación acíclica
Transporte cíclico de electrones y fotofosforilación cíclica (fase luminosa cíclica) En esta fase solamente interviene el fotosistema I (PSI), y se genera un transporte de electrones cíclico. Al no intervenir el PSII no hay fotólisis del agua, por lo que no se desprende oxígeno. Tampoco hay reducción del NADP, y solo se obtiene ATP. El PSI puede funcionar independientemente del PSII, cuando la longitud de onda de la luz es superior de 680 nm. Al absorber la luz, libera electrones, estos son recogidos por la ferredoxina que los pasa al citocromo b6-f por medio de la plastoquinona. Del citocromo b6-f los electrones vuelven al PSI por medio de la plastocianina. Al igual que en el transporte acíclico, la plastoquinona bombea protones hacia el interior del tilacoide, que salen al estroma atravesando las ATP sintasas, generandose así ATP. La finalidad de la fase cíclica es subsanar el déficit de ATP que se produce en la fase acíclica. La reducción de una molécula de CO2 en la fase oscura requiere de dos moléculas de NADPH y tres de ATP. En la fase acíclica se forma algo más de una molécula de ATP por cada molécula de agua destruida, por lo que es necesaria una síntesis adicional de ATP, que se consigue mediante el transporte acíclico. Este transporte permite utilizar la energía luminosa para generar ATP sin formar NADPH.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
31
FASE OSCURA DE LA FOTOSÍNTESIS En la fase oscura o biosintética, se utiliza el ATP y el NADPH obtenidos en la fase luminosa, para sintetizar materia orgánica a partir de compuestos inorgánicos. Como fuente de carbono se utiliza el CO2, como fuente de nitrógeno se utilizan los nitratos y como fuente de azufre los sulfatos. Como todas las moléculas tienen un esqueleto carbonado, es importante conocer el mecanismo que permite la incorporación de CO2 a los compuestos orgánicos. Este proceso se llama asimilación o fijación del CO2. El CO2 es asimilado mediante una ruta cíclica, que fue descubierta por Melvin Calvin en la década de 1950, denominada, por ello, ciclo de Calvin.
Ciclo de Calvin o ciclo de las pentosas El Ciclo de Calvin consta de tres fases: 1. Fijación del CO2. 2. Reducción del átomo de carbono procedente del CO2. 3. Regeneración de la ribulosa-1-5-difosfato.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
32
1. Fijación del CO2. El CO2 se incorpora al ciclo, uniéndose a una pentosa, la ribulosa-1-5-difosfato. Esta reacción está catalizada por la enzima ribulosa-1-5-difosfato carboxilasa oxidasa, también llamada rubisco, considerada la enzima más abundante del planeta. La unión entre ambas origina un compuesto inestable, que se disocia en dos moléculas de tres carbonos, el ácido- 3-fosfoglicérico. 2. Reducción del átomo de carbono procedente del CO2. La reducción del átomo de carbono incorporado tiene lugar en dos reacciones diferentes, una fosforilación y la reducción propiamente dicha, etapas que requieren la acción del ATP y el NADPH respectivamente. El resultado de estas dos reacciones es la transformación del ácido-3-fosfoglicérico en la molécula de gliceraldehido-3-fosfato. Como son dos ácidos fosfoglicéricos los que se transforman, se originan dos moléculas de gliceraldehido-3-fosfato. El gliceraldehido-3-fosfato puede tener tres destinos distintos: − Utilizarse para la síntesis de glucosa y otras hexosas. − Seguir la ruta de la glucólisis para formar ácido pirúvico. − Utilizarse en la regeneración de la ribulosa-1-5-difosfato para cerrar el ciclo de Calvin. 3. Regeneración de la ribulosa-1-5-difosfato. Para que el ciclo de Calvin pueda seguir funcionando y continúe fijando CO2 es preciso recuperar la ribulosa-1-5-difosfato. En esta etapa, a partir del gliceraldehido-3-fostato se originan una serie de intermediarios de tres, cuatro, cinco, seis y siete carbonos, y al final se obtiene ribulosa-5-fosfato, que por fosforilación con ATP, se convierte en ribulosa-1-5difosfato, y será la aceptora de nuevas moléculas de CO2.
Estequiometría del ciclo de Calvin En cada “vuelta” del ciclo de Calvin, se fija 1 átomo de carbono procedente del CO2. Vamos a calcular el gasto de ATP y NADPH que tiene que realizar un organismos autótrofo para fabricar una molécula de glucosa de seis carbonos. Para fabricar una molécula de glucosa se han de incorporar 6 moléculas de CO2, y se necesitan otras 6 de ribulosa y por tanto esto implicaría dar 6 vueltas al ciclo de Calvin.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
33
En esquema, sería necesario lo siguiente:
Por tanto, para obtener 1 molécula de glucosa a partir de CO2, los organismos fotosintéticos gastan 12 moléculas de NADPH y 18 moléculas de ATP. 6.1.3. BALANCE GLOBAL DE LA FOTOSÍNTESIS ¿Cuantas moléculas de CO2, H2O, ATP, NADPH y fotones (hν) hacen faltan para fabricar una molécula de glucosa?. ¿cuantas moléculas de O2 se desprenden? 1. ¿Cuántas moléculas CO2 son necesarias? Por cada molécula de GLUCOSA (C6H12O6) son necesarias 6 moléculas de CO2. Esas 6 moléculas se utilizan de la forma siguiente: • los 6 C son utilizados para fabricar una molécula de GLUCOSA (ya que tiene 6 C) • los 6 O2, que equivalen a 12 O, se utilizan así: ¬ 6 O se utilizan para fabricar una molécula de GLUCOSA (ya que tiene 6 O) ¬ 6 O se reducen y generan H2O. Como son 6 O se producirán 6 moléculas de H2O 2. ¿Cuántas moléculas de ATP y NADPH + H+ se necesitan? Según el ciclo de Calvin, cada CO2 fijado y reducido consume 3 ATP y 2 (NADPH + H+). Como se consumen 6 CO2, el total de ATP y NADPH consumidos serán 6 CO2
18 ATP + 12 (NADPH + H+)
3. ¿Cuántas moléculas de H2O se necesitan?. Los átomos de H del (NADPH + H+) que se forma en la fase luminosa proceden del H2O. Como se necesitan 12 (NADPH + H+) para formar una molécula de GLUCOSA, eso quiere decir que se consumen 12 moléculas de H2O, una por cada NADPH + H+. En resumen, hasta ahora tenemos que, para fabricar una molécula de GLUCOSA se consumen 6 CO2 + 12 H2O + 18 ATP + 12 (NADPH + H+) y se obtiene 1 GLUCOSA, se desprenden 6 O2 y se forman 6 H2O. BALANCE GLOBAL 18 ATP
18 (ADP + P)
6 CO2 + 12 H2O
C6H12O6 + 6 O2 + 6 H2O (GLUCOSA) 12 (NADPH + H+)
12 NADP+
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
34
4. ¿Cuantos fotones (hν) son necesarios?. Los fotones se absorben en la FASE LUMINOSA, por cada molécula de H2O que se descompone (FOTÓLISIS del AGUA) hacen falta 4 FOTONES (dos por cada FOTOSISTEMA). Como se consumen y descomponen 12 H2O, se necesitan en total 48 FOTONES.
6.1.4. FOTOSÍNTESIS BACTERIANA Las bacterias fotosintéticas, al no contener cloroplastos, los pigmentos fotosintéticos y los transportadores de electrones se localizan en invaginaciones de la membrana. Los pigmentos fotosintéticos, salvo en las cianobacterias, son las bacterioclorofilas, ligeramente diferentes a las clorofilas. La mayoría de las bacterias fotosintéticas tienen exclusivamente un fotosistema y obtienen el ATP por fotosfosforilación cíclica. La obtención de poder reductor no está ligada al proceso fotosintético. Al carecer de fotosistema II, estos microorganismos no pueden utilizar el agua como donador de electrones y, en consecuencia, no se desprende oxígeno en la fotosíntesis, por lo que es anoxigénica. Solamente las cianobacterias realizan una fotosíntesis prácticamente idéntica a la de las plantas verdes, la fotosíntesis oxigénica. 6.1.5. FACTORES QUE INFLUYEN EN LA FOTOSÍNTESIS La actividad fotosintética constituye un pilar básico en la fisiología de los organismos que la llevan a cabo. Su adecuada realización es fundamental para su supervivencia y por ello es un proceso muy bien regulado. En esta regulación intervienen varios factores. 1. La luz. Por lo general, al aumentar la intensidad luminosa, aumenta la actividad fotosintética. No obstante, las distintas especies de plantas están adoptadas a intensidades de luz diferentes; por eso hay plantas adaptadas a zonas de penumbra y otras que precisan una luz muy intensa. Si la intensidad luminosa supera ciertos límites, se produce el fenómenos de la fotooxidación, y los pigmentos fotosintéticos se oxidan de forma irreversible. Para la misma intensidad, las adaptadas a climas tropicales presentan mayor rendimiento que las plantas de climas templados, y nunca llegan a la saturación lumínica. 2. La concentración de CO2. La eficacia de la fotosíntesis aumenta al aumentar la concentración de CO2, hasta un valor máximo en que se estabiliza, debido a la saturación de la enzima rubisco en el ciclo de Calvin. 3. La temperatura. Todas las reacciones metabólicas, y por tanto la fotosíntesis, se aceleran al aumentar la temperatura, hasta un valor determinado. A partir de este se desnaturalizan las enzimas y el proceso se detiene. Cada especie tiene una temperatura óptima en la que la eficacia de la fotosíntesis es máxima. 4. La humedad. El grado de humedad en el suelo y en el aire son factores que condicionan el rendimiento fotosintético. Si el aire tiene poca humedad, las plastas cierran los estomas para evitar pérdidas de agua y esto dificulta la captación del CO2.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
35
5. La concentración de oxígeno. Cuando la concentración de O2 es muy elevada la eficacia de la fotosíntesis disminuye debido a un proceso denominado fotorrespiración. La fotorrespiración es un fenómeno que afecta a las plantas de climas templados (como España), denominadas también plantas C3, y sucede cuando el clima se vuelve más cálido y las plantas cierran sus estomas para evitar la desecación, aumentando así los niveles de O2 en el interior de la hoja. La enzima rubisco, además de catalizar la fijación del CO2, tiene actividad oxidasa, oxida a la ribulosa-difosfato incorporándole el O2, lo que tras varias reacciones, origina CO2 y H2O, lo que representan un saldo negativo para la economía de la planta. Se piensa que la fotorrespiración es un proceso que protege a las plantas de la fotooxidación.
Fotorrespiración y plantas C4 Las plantas de climas tropicales, donde el clima es mucho más cálido han resuelto este problema porque captan el CO2 de forma distinta. En sus hojas tienen dos tipos de células cargadas de cloroplastos donde realizan la fotosíntesis, las células del mesófilo y las células perivasculares (están alrededor de los nervios de las hojas). El CO2 que entra por los estomas de las hojas es fijado en las células del mesófilo por una molécula de tres carbonos, el ácido fosfoenolpirúvico (PEPA) y se convierte en una molécula de cuatro carbonos (por eso las plantas a las tropicales se las designa como C4), el oxalacetato. Este se transforma en otra sustancia, el ácido málico que sale de las células del mesófilo, se introduce en las células perivasculares y desprende CO2 que es fijado por la ribulosa, convirtiéndose el málico en ácido pirúvico, que regresa a las células del mesófilo y se transforma de nuevo en PEPA. Así pues el ácido málico se convierte en una sustancia que está continuamente bombeando CO2 y por lo tanto los niveles de CO2 en las células perivasculares se mantienen más elevados que los de oxígeno, evitando así la fotorrespiración. Esta vía C4 de fijación del carbono, llamada ciclo de Hatch-Slack, tiene un mayor consumo de ATP y NADPH que la fijación del CO2 de la forma habitual, pero compensa con creces las pérdidas que produciría la fotorrespiración.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
36
6.1.6. IMPORTANCIA DE LA FOTOSÍNTESIS La fotosíntesis es un proceso de enorme importancia hay en día en la Biosfera, pero a lo largo de la evolución ha sido crucial en la transformación de la atmósfera primitiva. A nivel de la Biosfera, es fundamental porque: ▪ Es el principal mecanismo de BIOSÍNTESIS de materia orgánica a partir de compuestos inorgánicos. La materia orgánica fabricada por los organismos fotosintéticos pasa de unos seres vivos a otros mediante las cadenas tróficas. ▪ Permite el equilibrio ecológico entre los organismos autótrofos y heterótrofos. ▪ Transforma la energía luminosa en energía química, que es la utilizada por los seres vivos. ▪ Libera oxígeno, utilizada en la respiración aerobia para oxidar la materia orgánica. A nivel evolutivo, la fotosíntesis fue el proceso responsable del cambio de la atmósfera primitiva reductora a una atmósfera oxidante, a medida que las cianobacterias, hace 2.000 millones años, liberaban oxígeno al realizar una fotosíntesis oxigénica. La aparición del oxígeno atmosférico supuso el fin de la síntesis abiótica de materia orgánica, la aparición de organismos aerobios y la formación de la capa de ozono protectora de la radiación ultravioleta. 6.2. QUIMIOSÍNTESIS La quimiosíntesis es un tipo de metabolismo exclusivo de procariotas, en concreto de las bacterias quimiosintéticas o quimilitotrofas. Estas bacterias son autótrofas, por lo que fabrican compuestos orgánicas a partir de la materia inorgánica que toman del medio, y para ello utilizan la energía que se desprende de la oxidación de compuestos inorgánicos (amoníaco, nitritos, sulfuros, ión ferroso, hidrógeno, etc.). Según esto, la quimiosíntesis se puede dividir en dos fases: > Obtención de energía. La energía desprendida en la oxidación de compuestos inorgánicos se utiliza para fabricar ATP y NADH. > Producción de materia orgánica. EL ATP y NADH obtenidos en la fase anterior se utilizan para la síntesis de materia orgánica por medio del ciclo de Calvin.
▪ ▪ ▪ ▪
Las bacterias quimiosintéticas se clasifican por el tipo de oxidación que realizan: Bacterias nitrificantes: oxidan compuestos de nitrógeno. Se distinguen dos géneros, Nitrosomas y Nitrobacter, que se complementan y comparten el mismo hábitat y están ampliamente distribuidas en el agua y en el suelo. Sulfobacterias: oxidan azufre o compuestos reducidos de azufre, como H2S o el tiosulfato. Ferrobacterias: oxidan el hierro ferroso a hierro férrico. Abundan en ciertas charcas de agua dulce con sales reducidas de hierro. Bacterias del hidrógeno: oxidan el H2, produciendo agua. Son frecuentes en hábitats donde se producen fermentaciones que liberan hidrógeno como producto final.
Biología 2º Bachillerato
Tema 4. La nutrición celular: el metabolismo
37
6.3. OTRAS RUTAS ANABÓLICAS
Gluconeogénesis La gluconeogénesis es una ruta metabólica por la que tiene lugar la síntesis de glucosa a partir de precursores más sencillos, y es una ruta inversa a la glucólisis. La célula utiliza esta ruta metabólica cuando necesita glucosa y no dispone de ella, de manera que los metabolitos intermedios que se producen en la glucólisis se utilizan para fabricar glucosa. La gluconeogénesis es un proceso energéticamente desfavorable, y consume unos 6 ATP por molécula de glucosa que se fabrica. Esta ruta tiene lugar preferentemente en el hígado y en parte en el riñón, y mediante ella es posible sintetizar glucosa a partir de ácido láctico, aminoácidos o algún metabolito del ciclo de Krebs. Así pues, evita un excesiva acumulación de ácido láctico en el músculo cuando no hay suficiente oxigenación.
Biosíntesis de ácidos grasos y triglicéridos Los ácidos grasos son el componente fundamente de todos los lípidos saponificables, por ello su formación es una etapa importante en la síntesis de lípidos. Los ácidos grasos se sintetizan a partir del acetil-CoA que se fabrica en la mitocondria. El acetilCoA sale al citosol y sufre unas reacciones de condensación, deshidratación y reducción que conducen a la síntesis de ácidos grasos. El complejo enzimático que lleva a cabo todo el proceso es el ácido grasosintetasa. Las grasas o triglicéridos posteriormente se formarán por esterificación de tres moléculas de ácidos grasos con una de glicerina. Para que se produzca ambos compuestos deben estar activados, los ácidos grasos se activan uniéndose a la coenzima A (CoA) y la glicerina a un grupo fosfato. Los triglicéridos se fabrican en el citoplasma de las células hepáticas y en los adipocitos.
Biosíntesis de aminoácidos Los aminoácidos son indispensables para cualquier ser vivo, ya que son los componentes de las proteínas y además son importantes precursores en la síntesis de otras moléculas, como hormonas, neurotransmisores, pigmentos, etc. La biosíntesis de aminoácidos tiene lugar en el citoplasma, y en ella intervienen dos procesos: la síntesis del esqueleto carbonado, a partir de precursores metabólicos; y la incorporación del grupo amino mediante reacciones de transaminación. Los aminoácidos suelen agruparse por familias según el precursor metabólico del que parte la síntesis del esqueleto carbonado, así se habla de aminoácidos de la familia del aspartato, de la familia del glutamato, de la familia del ácido pirúvico, etc. Las plantas y las bacterias quimiosintéticas pueden fabricar el grupo amino a partir de compuestos inorgánicos, como el nitrato, amoníaco, etc. Pero los animales y otros organismos heterótrofos, solo podemos sintetizar nuevos aminoácidos a partir de los aminoácidos adquiridos en la dieta, por medio de transaminaciones. Las reacciones de transaminación están catalizadas por las transaminasas del hígado. Aquellos aminoácidos que no se pueden fabricar a partir de otros se denominan aminoácidos esenciales, y en el ser humano son nueve.
Esquema de la nutrición celular
BIOLOGÍA 2º METABOLISMO CELULAR
FOTOFOSFORILACIÓN ACÍCLICA FOTORREDUCCIÓN DEL NADP
Estroma
PC Interior tilacoide
FOTÓLISIS DEL AGUA
FOTOFOSFORILACIÓN
Biología 2º Bachillerato
Tema 4: La nutrición celular. El metabolismo
ACTIVIDADES TEMA 4. LA NUTRICIÓN CELULAR: EL METABOLISMO TRANSPORTE, ATP y METABOLISMO 1. ¿Qué quiere decir que la permeabilidad de la membrana es selectiva y cuál es la causa de ello?. 2. ¿Qué tipos de proteínas de transporte hay en la membrana plasmática?. En qué proceso interviene cada una de ellas. 3. Si una célula se encuentra rodeada por un líquido cuya concentración de O2 y de aminoácidos es inferior a la del contenido celular, ¿podrían entrar dichas sustancias en la célula?. Razona la respuesta. 4. Si en una célula se impide la síntesis de ATP, ¿podría quedar afectada alguna de las funciones de la membrana plasmática?. ¿Porqué?. 5. Completa el cuadro: CATABOLISMO
ANABOLISMO
Energía: Consume/Desprende Materia: Degrada/Sintetiza Reacciones: Oxidación/Reducción 6. ¿Qué diferencias y semejanzas existen, respecto a los procesos metabólicos que realizan, entre las células autótrofas y heterótrofas?. ¿Y entre las fotosintéticas y quimiosintéticas?. 7. ¿Qué quiere decir que el acetil-CoA es una encrucijada metabólica?. 8. ¿Por qué una determinada via catabólica no es exactamente la inversa de su correspondiente anabólica?. 9. Considerando que la energía es el dinero con que se pagan los trabajos celulares, establece la relación entre las siguientes moléculas energéticas y sus equivalentes en términos monetarios, razonando la respuesta: Almidón, glucógeno, grasas Glucosa ATP
Dinero de bolsillo Libreta a plazo fijo Cuenta corriente
10. ¿Cómo se puede aumentar la velocidad de cualquier reacción y cómo se realiza en los seres vivos?.
Biología 2º Bachillerato
Tema 4: La nutrición celular. El metabolismo
11. Tanto en la respiración mitocondrial como en la fase luminosa de la fotosíntesis hay enzimas que trabajan con NADH o NADPH, una cadena de transporte de electrones y ATP-sintetasas, pero hay ciertas diferencias. Responde a las cuestiones del siguiente cuadro: RESPIRACIÓN
FOTOSÍNTESIS
a) La cadena transportadora de electrones está en: b) El transportador de hidrógenos es: c) ¿Se produce oxidación del NADH o reducción del NADP+?. d) Los protones (H+) son aportados por: e) Los protones (H+) son introducidos en: f) Los protones (H+) se unen a ......... para producir: g) La parte globosa de la ATP-sintetasa está dirigida hacia: h) La síntesis de ATP se denomina:
CUESTIONES DE SELECTIVIDAD Respecto al metabolismo intermediario: a) Indique los posibles orígenes del acetil-CoA que entra en el ciclo de Krebs para condensarse con el oxalacetato b) ¿A qué molécula da lugar dicha condensación?. c) Indique el compartimento subcelular en el que ocurre esta reacción Comenta brevemente y calcula el balance energético de la degradación total a CO 2 y H2O de una molécula de glucosa. Explica en los siguientes procesos metabólicos: a) Glucólisis; b) Ciclo de Krebs; c) Fosforilación oxidativa; cuáles son los productos finales que se obtienen en ellos e indica en qué compartimentos celulares y en que subestructuras de los mismos tienen lugar. Explique los factores que modulan la actividad de la fotosíntesis vegetal. Referido a la fotosíntesis: a) ¿Cuál es la ecuación global que la describe?. b) ¿Dónde se localiza la cadena de transportadores de electrones?. c) ¿Cuál es el dador final de electrones en la fotofosforilación cíclica?. ¿Y en la acíclica?. d) ¿Cuál es el compuesto aceptor del CO2 en el ciclo de Calvin?. La incubación de células con cianuro interrumpe el consumo respiratorio de oxígeno. Al respecto, contestar las preguntas siguientes, razonando la respuesta: a) ¿Qué proceso metabólico se inhibe por el cianuro?. b) ¿Cuál es la función principal del proceso inhibido?. c) ¿En qué orgánulo celular y en qué estructura de dicho orgánulo ocurre?.
Biología 2º Bachillerato
Tema 4: La nutrición celular. El metabolismo
ENZIMAS y CINÉTICA ENZIMÁTICA
Biología 2º Bachillerato CATABOLISMO
Tema 4: La nutrición celular. El metabolismo
Biología 2º Bachillerato
FOTOSÍNTESIS
Tema 4: La nutrición celular. El metabolismo
BIOLOGÍA 2º BACHILLERATO ACTIVIDADES REFUERZO TEMA 4. METABOLISMO Las siguientes figuras representan diversos procesos metabólicos estudiados en clase. representada, averigua: • ¿Qué representa?. • ¿En qué estructura y subestructura celular tiene lugar?. • Nombra los procesos o fases indicados con números (Fig. 1, 4) o letras (Fig. 2, 3). • Nombra los compuestos señalados con números (Fig 3, 5, 6).
De cada figura
Fig. 2
Fig. 4
Fig. 3
Fig. 5 Fig. 5
Fig. 6
BLOQUE III HERENCIA Y GENÉTICA MOLECULAR
TEMA 5. LA HERENCIA Y GENÉTICA MOLECULAR
TEMA 5. LA HERENCIA y GENÉTICA MOLECULAR 1. GENÉTICA: CONCEPTOS BÁSICOS 2. EXPERIMENTOS y LEYES DE MENDEL 3. TEORÍA CROMOSÓMICA DE LA HERENCIA 4. MODIFICACIONES A LAS PROPORCIONES DE LAS LEYES DE MENDEL 5. DETERMINACIÓN GENÉTICA DEL SEXO 6. HERENCIA LIGADA AL SEXO 7. EL ADN COMO PORTADOR DE LA INFORMACIÓN GENÉTICA 8. LA DUPLICACIÓN DEL ADN 8.1. 8.2. 8.3.
HIPÓTESIS PROPUESTAS PARA LA DUPLICACIÓN MECANISMO DE DUPLICACIÓN DEL ADN SISTEMAS DE REPARACIÓN DEL ADN
9. LA EXPRESIÓN DEL MENSAJE GENÉTICO 9.1. 9.2.
LA TRANSCRIPCIÓN TRADUCCIÓN o BIOSÍNTESIS DE PROTEÍNAS
10. EL CÓDIGO GENÉTICO 11. REGULACIÓN DE LA EXPRESIÓN DE LOS GENES 12. MUTACIONES 13. INGENIERÍA GENÉTICA
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
1
1. GENÉTICA: CONCEPTOS BÁSICOS Genética: es la ciencia que estudia la herencia biológica, es decir, la transmisión de los caracteres morfológicos y fisiológicos que pasan de un individuo a sus descendientes. Existen dos grandes vías de investigación para explicar todos estos fenómenos relacionados con la herencia biológica: Genética clásica o mendeliana: estudia la herencia a través de experimentos de reproducción, partiendo de los caracteres observables (fenotipo), comprueba su transmisión por herencia a los descendientes, y a partir de proporciones matemáticas intenta averiguar cuál es la información biológica de los individuos (genotipo). Genética molecular: estudia las moléculas que contienen la información biológica (ADN) y los procesos bioquímicos de transmisión y manifestación. El sentido de su estudio es inverso a la Genética clásica, partiendo de la información (genotipo), se deduce cómo serán los caracteres (fenotipo). Gen: es la unidad de material hereditario. Es un fragmento de ácido nucleico, generalmente ADN (salvo en algunos virus, en los que es ARN), que lleva la información para un carácter. Mendel desconocía su naturaleza, y los denominó caracteres hereditarios. Se encuentran localizados en los cromosomas, y la posición que ocupan se denomina locus. A los genes se les designa con símbolos, generalmente con letra cursiva. La letra que se utiliza suele ser la inicial del carácter. Otro tipo de notación es el uso de superíndices, que permite simbolizar más de dos genes que informan sobre el mismo carácter. Alelos: cada uno de los genes que informa sobre el mismo carácter. En los individuos diploides, cada caracteristica hereditaria viene determinada por dos copias del mismo gen, a cada copia se le denomina alelo, y cada uno se hereda de un progenitor. Los alelos se localizan en cada miembro de la pareja de cromosomas homólogos. Homocigótico o raza pura: son los individuos que para un carácter poseen los alelos iguales. Heterocigótico o raza híbrida: individuo que poseen para una carácter los alelos diferentes. Genotipo: conjunto de genes que presenta un individuo para una o varias características, y que ha heredado de sus progenitores. Fenotipo: es la manifestación externa del genotipo, es decir, la suma de los caracteres observables en un individuo. El fenotipo depende del genotipo y de la influencia del ambiente: Fenotipo = Genotipo + Ambiente Por ejemplo, dos plantas con igual genotipo se desarrollan de forma diferente, si una está al sol y otra a la sombra. Herencia dominante: se dice que un carácter tiene herencia dominante cuando en los individuos híbridos, solo se manifiesta uno de los dos alelos que rigen sobre ese carácter. El alelo que se manifiesta se denomina alelo dominante, y el que queda oculto alelo recesivo. Los alelos recesivos solamente se manifiestan en los individuos que son de raza pura para esa característica.
2. EXPERIMENTOS Y LEYES DE MENDEL Gregor Johann Mendel nació en 1822 en Heinzendorf (Austria) e ingresó en el monasterio agustino de Brno en 1843 para continuar su educación. Asistió durante dos años a la Universidad de Viena, donde se formó sólidamente en Matemáticas, Física y Ciencias Naturales. De vuelta al monasterio, emprendió sus experimentos con plantas de guisante (Pisum sativum). Realizó miles de cruzamientos, recogiendo una cantidad ingente de datos sobre las frecuencias con se transmitía cada una de las características de la planta. A partir de estos datos postuló una serie de leyes sobre la herencia de los caracteres biológicos. Mendel publicó sus descubrimientos en 1866, en una revista de poca difusión y en un momento en que el interés científico estaba muy polarizado sobre la teorías evolucionista de Darwin. La constancia de los factores hereditarios de Mendel no parecía compatible con la evolución de las especies, y lo que en realidad constituía su explicación científica fue ignorada. Pasaron treinta y cuatro años, en una de las coincidencias más sorprendentes de la investigación científica, tres autores por separado, el holandés De Vries, el alemán Correns, y el austríaco Tschermak, redescubrieron en el mismo año (1900) los hallazgos de Mendel.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
2
Primer experimento y Primera Ley de Mendel Mendel trabajó fijándose en siete caracteres, cada uno de los cuales podía tener dos manifestaciones o características diferentes: Forma de la semilla Color de los cotiledones Color de la cubierta Forma de la legumbre Color de la legumbre no madura Posición de la flor Longitud del tallo En su primer tipo de experimentos se fijó cómo se transmitían cada una de estas características por separado en la descendencia. Escogió plantas de guisantes con semillas amarillas y plantas con semillas verdes, y se cercioró de que se trataban de razas puras. Como la planta de guisante se reproduce normalmente por autofecundación, lo primero que comprobó es que siempre que se autofecundaban plantas nacidas de semillas amarillas, daban semillas amarillas, y si se trataba de la variedad de semillas verdes, siempre daban frutos con semillas verdes. Cruzó ambas variedades, cortando los estambres de las flores de una de las variedades antes de que maduraran y las fecundaba artificialmente con el polen recogido de las flores de otra variedad. Esperaba que aparecieran los nuevos frutos con sus semillas y anotaba sus características. Recogidas todas las semillas del cruzamiento, observó que todas ellas eran de color amarillo. De este experimento se deduce la primera ley de Mendel, llamada Ley de la uniformidad: “Todos los descendientes del cruce entre dos razas puras son iguales entre sí”. Segundo experimento y Segunda Ley de Mendel Surgió entonces la dificultad de encontrar una explicación científica al resultado anterior. Había que dar explicación a una interesante pregunta: ¿había desaparecido el otro carácter?. Para comprobarlo, plantó los guisantes del cruzamiento anterior, y dejó las plantas resultantes se autofecundaran, y el resultado fue la aparición de las dos clases de semillas, amarillas y verdes, en una proporción de 3 a 1 a favor de la variedad amarilla, que es la que había aparecido en todos los individuos de la primera generación. El hecho de que aparecieran variedades de semilla verde indicaba que las plantas que se habían autofecundado tenían información para esa característica. Si en ellas no se manifestaba, debía ser porque la otra información (semilla amarilla) era dominante. A la característica que se manifiesta, Mendel la denominó carácter dominante, y la que no se manifiesta carácter recesivo. A las partículas o sustancias responsables de transmitir dichas características las denominó factores hereditarios (lo que hoy llamamos genes). A partir de este segundo experimento, dedujo la segunda ley, llamada Ley de la segregación: “Los dos factores hereditarios que informan para un mismo carácter, no se fusionan o mezclan, sino que permanecen diferenciados durante toda la vida del individuo y se segregan, es decir, se separan y reparten en el momento de la formación de los gametos”.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
3
Tercer experimento y Tercera Ley de Mendel En su tercer tipo de experimento Mendel estudió la descendencia entre plantas que diferían en dos caracteres independientes, para estudiar si existían interrelaciones entre ellos, es decir, si uno influyen en la manifestación de otro. Realizó cruces entre plantas de guisante que siempre daban semillas amarillas y lisas y plantas de raza pura que daban semillas verdes y rugosas. Obtuvo una descendencia homogénea amarilla y lisa. Luego permitió la autofecundación de estas plantas, y de las 566 semillas recogidas, encontró que 3l5 eran semillas amarillas y lisas, 108 verdes y lisas, 101 amarillas y rugosas y 32 verdes y rugosas. Dividiendo todos estos resultados por el menor se obtiene: Amarillas lisas 315/32= 9/16 Amarillas rugosas 108/32 = 3/16 Verdes lisas 101/32 = 3/16 Verdes rugosas 32/32 = 1/16 La proporción entre ellas es de 9:3:3:1, la misma proporción que se obtiene si se combinan al azar cuatro tipo de factores hereditarios totalmente independientes entre sí, y de forma que haya dos que inhiban la manifestación de otros dos, que son sus antagónicos. Basándose en sus experimentos, se deduce la tercera ley de Mendel, llamada Ley de la independencia de los factores hereditarios: ”Cada uno de los factores hereditarios no antagónicos se transmiten a la descendencia con absoluta independencia de los demás”.
Aciertos de los experimentos de Mendel:
Utilizar una especie autógama, lo que permite obtener fácilmente razas puras para algunos caracteres Elegir caracteres cualitativos fácilmente visibles Iniciar sus experimentos fijándose en un solo carácter Dar un tratamiento estadístico a los datos Tener la suerte de seleccionar para su tercer experimento caracteres no ligados
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
4
3. TEORÍA CROMOSÓMICA DE LA HERENCIA Cuando se redescubrieron los trabajos de Mendel en 1900, dos investigadores por separado, W. S. Sutton en estados Unidos, y T. Boveri en Alemania observaron que el comportamiento de los cromosomas durante la meiosis era equivalente al de los genes de Mendel. Por ello, desde 1902 se estableció la teoría de que los genes estaban localizados en los cromosomas. Esta afirmación constituye la base de la Teoría cromosómica de la herencia. En poco tiempo, algunos experimentos confirmaron esta hipótesis. En 1.910, Thomas H. Morgan, de la Universidad de Columbia (EE.UU), trabajando con Drosophila melanogaster, descubrió que había algunos genes que se heredaban juntos, lo que contrastaba con la tercer ley de Mendel. Concluyó que debían estar en el mismo cromosoma y próximos entre sí, denominándose por ello genes ligados. En otros experimentos descubrió que dichos genes se heredan de forma independiente, pero aparecía en la descendencia con una frecuencia que no se ajustaba a los resultados de Mendel, lo que le hizo suponer que los genes se disponen linealmente en los cromosomas, y éstos se pueden entrecruzar e intercambiarse fragmentos. Así pues el contenido de la Teoría cromosómica de la herencia se resume en estas afirmaciones: 1.Los factores hereditarios o genes se encuentran situados en los cromosomas. 2.Cada gen ocupa un lugar determinado en un cromosoma concreto. Este lugar se denomina locus (en plural loci). Los alelos se encuentran en los loci de los cromosomas homólogos, por esta razón existe un par de alelos para cada carácter 3.La ordenación de los genes es lineal, de forma que aquellos que se encuentren próximos tienden a heredarse juntos, y se denominan genes ligados. 4.Los genes de un mismo cromosoma se pueden heredar de forma independiente por recombinación debido a un intercambio de material entre cromosomas o sobrecruzamiento.
4. MODIFICACIONES A LAS PROPORCIONES DE LAS LEYES DE MENDEL Existen algunos casos en los que las Leyes de Mendel parecen no cumplirse. En realidad, esto no es así, sino que las relaciones entre genes o el propio efecto génico alteran los resultados. Entre estos casos se pueden citar los siguientes: EPISTASIA. Consiste en la influencia que existe entre genes diferentes que afectan a la expresión del mismo fenotipo. En ella, un gen (epistático) suprime la acción de otro gen no alélico (hipostático). Así la proporción 9:3:3:1 se ve alterada. HERENCIA INTERMEDIA. Se produce cuando en un híbrido, los dos alelos tienen la misma “fuerza” para manifestarse, por lo que aparece un fenotipo intermedio entre las dos razas puras.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
5
CODOMINANCIA. Se da cuando dos alelos son equipotentes, de manera que en los híbridos se manifiestan los dos caracteres. Por ejemplo la herencia de los grupos sanguíneos, los individuos IAIA son del grupo A, los individuos IBIB son del grupo B, y los individuos IAIB son del grupo AB. GENES LETALES. Un gen letal es aquel que produce la muerte de un individuo antes de que alcance su madurez sexual. Lógicamente, los individuos que mueren no son incluidos en la descendencia y, por tanto las frecuencias se ven alteradas. ALELISMO MULTIPLE. Se produce cuando para un mismo carácter existen varios alelos (más de dos) que constituyen una serie alélica. Estos múltiples alelos siguen las leyes mendelianas, pero al existir más de dos alternativas, los fenotipos que aparecen son más variados. Un ejemplo son los grupos sanguíneos ABO en el ser humano. HERENCIA CUANTITATIVA, CONTÍNUA o POLIGÉNICA. Los caracteres habitualmente estudiados sonde tipo cualitativo, es decir, presentan pocas alternativas, y estas son claras y fáciles de observar. Los caracteres cuantitativos son los que presentan diferentes graduaciones entre dos valores extremos. Por ejemplo, la altura, el peso, el coeficiente de inteligencia,... El carácter cuantitativo depende de varios genes que contribuyen en determinada proporción. A estos genes se les denomina poligenes (Herencia poligénica), cada uno de ellos produce un efecto pequeño. Un ejemplo es el color de la piel, que depende de tres o cuatro pares de genes, además el ambiente ayuda a que se dé una serie de tonalidades.
5. DETERMINACIÓN GENÉTICA DEL SEXO Un aspecto importante del fenotipo de un organismo es su sexo, que en la mayoría de los casos se halla controlado por genes, situados en cromosomas específicos (cromosomas sexuales), aunque también existen organismos en los que el sexo depende de factores ambientales. Determinación cromosómica En numerosos organismos, entre ellos la especie humana, la determinación del sexo se realiza por la presencia de cromosomas especiales, llamados cromosomas sexuales o heterocromosomas, que se diferencian del resto, que son los autosomas o cromosomas autosómicos. Existen tres sistemas distintos de determinación cromosómica: Sistema XX/XY. El sexo femenino presenta dos cromosomas iguales (XX) y todos los gametos que producen llevan el cromosoma X (sexo homogamético), y el masculino presenta un cromosoma de cada tipo (XY) y por tanto la mitad de sus gametos llevan el cromosoma X y la otra mitad el cromosoma Y (sexo heterogamético). Es el tipo de determinación de la especie humana y de otros muchos animales (mamíferos, equinodermos, moluscos y gran número de artrópodos).
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
6
Sistema ZZ/ZW. Las hembras son el sexo heterogamético (ZW) y los machos el homogamético (ZZ). Es propia de las aves, algunos anfibios y reptiles y de las mariposas. Sistema XX/XO o ZZ/ZO. Se caracteriza por que uno de los dos sexos solo tiene un cromosoma sexual. Se da en muchos insectos.
Determinación por haplodiploidía En algunos insectos sociales (abejas, avispas, hormigas) no existen cromosomas sexuales, y el sexo está determinado por el número de dotaciones cromosómicas. Así los individuos diploides (2n) son hembras y los haploides (n) son machos. Las hembras se desarrollan a partir de óvulos fecundados y los machos a partir de óvulos sin fecundar por partenogénesis. Determinación génica En algunas plantas, y también en algunos animales, el sexo depende de una o varias parejas de genes. Un ejemplo muy estudiado es el de la planta Ecballium elaterium (pepinillo del diablo), en la que el sexo depende de una serie alélica (a0>a+>ad), en donde el alelo a0 determina el sexo masculino, el alelo a+ determina característica hermafroditas y el alelo ad determina características femeninas. Determinación ambiental En algunos animales, la determinación del sexo depende de circunstancias ambientales, como la temperatura. Así entre los grandes saurios (cocodrilos, caimanes y aligátores) el sexo está determinado por la temperatura a la que se incuban los huevos, si es superior a 27 ºC se obtendrán machos y si es inferior nacerán hembras.
6. HERENCIA LIGADA AL SEXO Hay características que no se expresan en la misma proporción en los dos sexos. Esto se debe a que los genes responsables de ellas se encuentran localizados en uno de los dos cromosomas sexuales. Los caracteres cuyo alelos están localizados en los cromosomas sexuales se dice que están ligados al sexo. El cromosoma X y el cromosoma Y, a pesar de ser distintos, tiene regiones que se aparean y entrecruzan durante la meiosis (segmento homólogo) y otras que no lo hacen (segmento diferencial). Los alelos localizados en el segmento homólogo o apareante están parcialmente ligados al sexo, y los que se localizan en el segmento diferencial están totalmente ligados al sexo.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
7
Los casos más llamativos de herencia ligada al sexo son: Herencia ligada al cromosoma Y. Todos los genes que se encuentren en el segmento diferencial del cromosoma Y son heredados únicamente por los hijos varones. Se llama herencia holándrica, ya que se manifiesta solo en los varones, como la presencia de pelos en las orejas o la ictiosis (piel gruesa, oscura y áspera). Herencia ligada al cromosoma X. Se debe a genes localizados en el segmento diferencial del cromosoma X. La condición aparece generalmente en los varones, mientras que en las mujeres, que lleven el gen, aunque son fenotípicamente normales, pueden transmitir el carácter a sus hijos. Dos ejemplos bien conocidos son el daltonismo y la hemofilia, enfermedades provocadas por un gen recesito localizado en el segmento diferencial del cromosoma X. Para que una mujer padezca la enfermedad debe ser homocigótica recesiva, mientras que los hombres, que son hemicigóticos, basta para que la padezcan que el gen se encuentre en el único cromosoma X. El daltonismo es un defecto visual que hace que la persona afectada tenga dificultades para distinguir con claridad el color rojo del verde. La hemofilia es una enfermedad que provoca problemas en la coagulación de la sangre debido a la falta de alguno de los factores de coagulación (factor VIII). Herencia influida por el sexo Hay ciertas características que se expresan dependiendo del sexo del individuo. Generalmente se comportan así los caracteres influidos por el ambiente hormonal del individuo. Así, la calvicie en la especie humana y la presencia o ausencia de cuernos en algunas razas ovinas, están determinadas por genes localizados en la región homóloga de las cromosomas sexuales o bien en autosomas, y cuya manifestación depende del sexo.
GENOTIPO: AaBb
PARENTALES
Más frecuencia
Igual frecuencia Menos frecuencia
RECOMBINANTES
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
8
7. EL ADN COMO PORTADOR DE LA INFORMACIÓN GENÉTICA A principios del siglo XX se produjeron grandes avances en genética, una vez, que se redescubrieron los trabajos de Mendel. Así fue a principios de este siglo cuando se formularon la teoría cromosómica de la herencia, que postulaba que las características hereditarias debían localizarse en los cromosomas, y la teoría neodarvinista que reformaba la teoría de la evolución de Darwin a partir de los conocimientos de genética. Pues bien, a pesar de todos estos avances, aún no se tenía claro cuál era la naturaleza de los genes. Se sabía que los cromosomas, que contenían los genes, estaban formados por proteínas y ADN, y parecía que eran las proteínas, debido a su compleja organización y a sus propiedades catalíticas, las que podían contener la información genética. Algunos datos a favor del ADN como portador del mensaje genético podrían ser:
La presencia de ADN en núcleo y en los cromosomas La cantidad de ADN en las células de los individuos de una misma especie es constante Al aumentar la complejidad de un organismo, aumenta su contenido de ADN El ADN absorbe la luz UV de 360 nm, causante de las mutaciones.
Tres experimentos cruciales en toda esta historia fueron los que despejaron las dudas: Griffith (1.928), Avery y col. (1.944) y Hersey y Chase (1.952). (Figuran como apéndice del tema) Fueron los experimentos de Avery y sus colaboradores los que identificaron al ADN como la molécula portadora de la información genética. Años después los experimentos de Chargaff y Watson y Crick demostraron la composición y estructura del ADN. El nacimiento de la Genética molecular comenzaría a partir de entonces, al conocer la estructura del ADN y su papel biológico.
8. LA DUPLICACIÓN DEL ADN Todos los seres vivos somos temporales, tarde o temprano nos llega la muerte. Para que la especie no se extinga, es preciso que nos reproduzcamos, dando lugar a nuevos individuos que continúen viviendo. Para originar estos nuevos individuos es necesario formar nuevas copias de ADN, a partir del ADN progenitor, que pasarán a los nuevos individuos. Cuando una célula se divide transmite su información genética a las células hijas, para lo cual duplica previamente su ADN mediante el mecanismo denominado replicación o duplicación. La estructura del ADN es idónea para este proceso, al estar formado por dos hebras, la replicación del ADN implicaría la separación de las mismas, actuando cada una de molde para la construcción de nuevas cadenas, según la complementariedad de las bases. Así la secuencia de nucleótidos se duplica con exactitud y la información genética permanece constante. 8.1. HIPÓTESIS PROPUESTAS PARA LA DUPLICACIÓN Se han propuesto tres hipótesis para explicar como se produciría la replicación del ADN: Conservativa: la doble hélice original permanecería intacta, originándose una doble hélice completamente nueva. Semiconservativa: cada nueva molécula de ADN está formada por una cadena vieja y otra nueva (fue la propuesta por Watson y Crick). Dispersiva: cada nueva molécula de ADN estaría formada por fragmentos de cadenas viejas y nuevas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
9
Para comprobar cuál de las tres hipótesis era correcta, dos investigadores, Meselson y Stahl (1.958) realizaron varios experimentos. Cultivaron E.coli (la bacteria más utilizada en Genética) en un medio con nitrógeno pesado (N15). Después lo pasaron a un medio con nitrógeno normal (N14) y compararon la densidad de los ADN aparecidos en sucesivas generaciones. Tras sus experimentos y otros similares realizados en otros organismos, los resultados apoyan la hipótesis semiconservativa. A continuación figura la interpretación de los resultados.
8.2. MECANISMO DE DUPLICACIÓN DEL ADN Conocer el mecanismo de replicación de¡ ADN ha supuesto multitud de estudios y experimentos. Algunos de los investigadores más importantes que han participado en ellos, han sido: Kornberg (1.956). Fue discípulo de Severo Ochoa. Aisló de Escherichia coli la enzima ADNpolimerasa. Esta enzima es capaz de fabricar ADN in vitro. Actúan añadiendo nucleótidos al extremo de una cadena de nucleótidos, llamada ADN cebador. Cairns (1.963). Descubrió la existencia de un punto origen de la replicación del ADN en bacterias, y confirmó mediante sus estudios la hipótesis semiconservativa. Okazaki (1.968). Fue el primero en explicar la duplicación bidireccional, como a partir de un determinado punto la replicación progresa en dos direcciones. FASES DE LA DUPLICACIÓN. La duplicación presentan ciertas diferencias en procariotas (bacterias) y eucariotas. Vamos a estudiar el proceso en procariotas, que en sus aspectos básicos es común a eucariotas, y luego hablaremos de las diferencias entre ambos. Duplicación en Procariotas 1. INICIACIÓN. La replicación comienza en un punto concreto de la molécula de ADN, una secuencia de nucleótidos denominada OriC o Punto de iniciación. En este punto se abre la doble hélice, para ello actúa un enzima, denominada HELICASA, que rompe los puentes de hidrógeno que unen las dos cadenas de nucleótidos. Debido a este desenrollamiento de ADN, se producen superenrollamientos en el resto de la molécula, capaces de detener la duplicación, lo que hace preciso el concurso de unas enzimas, denominadas TOPOISOMERASAS, que eliminan las tensiones de las cadenas (actúan por un mecanismo de corte y empalme).
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
10
Una vez que han comenzado a separarse las cadenas de nucleótidos es necesario mantenerlas separadas, para ello actúan unas proteínas que estabilizan la separación de las dos hebras, se denominan PROTEÍNAS SSB. Se inicia así la formación de la horquilla de replicación, actuando las helicasas en ambos sentidos, de manera que el proceso es bidireccional. Las dos horquillas se replicación originadas forman una BURBUJA DE REPLICACION. Para que actúen las ADN-polimerasas necesitan de un cebador, es decir, un pequeño fragmento de nucleótidos a los que poder unir los nuevos nucleótidos que van a constituir las nuevas cadenas de ADN. Esos fragmentos de nucleótidos que actúan de cebadores son pequeños fragmentos de ARN (de 10 nucleótidos) denominados PRIMER, y que son sintetizados por una ARN-polimerasa, denominada PRIMASA. 2. ELONGACIÓN. Una vez sintetizados los primer, actúan la ADN-polimerasa lII, que comienza a fabricar una hebra de ADN a partir del cebador, en sentido S’- 3’, a partir de nucleótidos 3 P. La energía necesaria para la síntesis es proporcionada por los propios nucleótidos, que pierden dos grupos fosfato. Esta nueva hebra es de crecimiento continuo, y se denomina hebra conductora. A medida que las helicasas actúen y sigan abriendo la horquilla de replicación, esta hebra irá creciendo, por la acción de la ADN-pol III que irá añadiendo nuevos nucleótidos, complementarios a los de la cadena molde. En la otra hebra, al estar orientada en sentido contrario, la replicación se produce de forma discontinua, a base de pequeños fragmentos formados por cientos de nucleótidos de ADN, denominados fragmentos de Okazaki. En la síntesis de esta hebra, denominada hebra retardada, porque tarda más en crecer que la hebra conductora, intervienen varias enzimas: ARN-pol: fabrica cebadores ADN-pol lII: fabrica los fragmentos nuevos de ADN (fragmentos de Okazaki) ADN-pol I: retira los fragmentos de ARN y rellena los huecos con fragmentos de ADN ADN-ligasa: empalma los fragmentos de ADN (fragmentos de Okazaki), para formar la hebra retardada, que crece por lo tanto de forma discontinuo. 3. TERMINACIÓN. El proceso de replicación termina cuando la ADN-pol llega hasta la secuencia de terminación (Ter C). Las nuevas hélices terminan de formarse y se separan, originándose dos moléculas de ADN.
Duplicación en Eucariotas La duplicación en eucariotas es diez veces más lento que en procariotas, debido al mayor tamaño de las moléculas de ADN y a la presencia de histonas. Para que el proceso sea más rápido, existen varios puntos de iniciación, de manera que se originan varias unidades de replicación (REPLICONES) que actúan de forma coordinada, progresando la síntesis de nuevas cadenas de ADN hasta que se ponen en o unas con otras. Las histonas sobre las que está enrollado el ADN se quedan con la hebra patrón de la hebra conductora, de manera que la hebra que sirve de molde a la retardada y esta misma se enrollan sobre nuevas histonas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
11
SISTEMAS DE REPARACIÓN DEL ADN Es muy importante que en el proceso de replicación del ADN, el ADN formado no tenga errores de copia, ya que podría dar lugar a mutaciones importantes, como las que provocan la formación de tumores. En los procariotas se ha calculado que aproximadamente cada 107 nucleótidos se produce un error, y en eucariotas la probabilidad es más pequeña, cada 1010 nucleótidos. Para que el ADN conserve escrupulosamente la información genética a través de inmunerables divisiones celulares existen tres procesos que cooperan para asegurar la alta fidelidad de la replicación. Dos de ellos se encargan de prevenir errores: seleccionar nucleótidos y corregir pruebas, y un tercero se encarga de la corrección de posibles errores. La selección de nucleótidos es llevada a cabo por la ADN polimerasa III La corrección de pruebas la lleva a cabo la ADN polimerasa I. La existencia de un nucleótido desemparejado detiene la adición del siguiente, y la ADN-pol I retira dicho nucleótido y busca la pareja adecuada. La corrección de errores es más complicada. Las enzimas recorren las hebras de ADN y reconocen los nucleótidos mal emparejados, los eliminan y sustituyen por otros correctos. Hay que tener en cuenta, que no todos los errores de la replicación de los mensajes genéticos son perjudiciales. Algunos no tienen consecuencias para el organismo y otros son ventajosos, y constituyen una fuente importante de la variación genética necesaria para que tenga lugar la evolución.
9. LA EXPRESION DEL MENSAJE GENETICO Francis Crick, en 1970, enunció el dogma central de la Biología molecular: la información genética contenida en el ADN es transcrita en forma de ARN y traducida a proteínas. En ADN contiene la información genética en forma de una determinada secuencia de nucleótidos, es decir, contiene las instrucciones sobre cómo debe funcionar la célula. Las proteínas ejecutan tales instrucciones. Para ello la información contenida en el ADN se copia a una secuencia de ARN (transcripción) denominada ARN mensajero (ARNm), que en los ribosomas al ser leído se traduce a proteínas (traducción). 9.1.LA TRANSCRIPCIÓN La transcripción es la síntesis de ARN a partir de fragmentos de ADN. La llevan a cabo unas enzimas, las ARN polímerasas (ARN-pol), que utilizan como molde una hebra de ADN. Las ARN polimerasas recorren el ADN en sentido 3’- 5’y añaden nucleótidos con bases complementadas a las de la hebra del ADN que se transcribe. La molécula de ARN crece en sentido 5’ 3’. Así pues en la transcripción intervienen: ADN: que actúa de molde Ribonucleótidos trifosfato (ATP,GTP,CTP,UTP) ARN-polimerasas Fases de la transcripción 1. INICIACIÓN. La transcripción comienza cuando la ARN-pol se asocia con el cofactor sigma (), que permite a esta enzima reconocer y unirse a una secuencia concreta del ADN, denominada promotor, que actúa se señal de inicio. A continuación la ARN-polimerasa, abre la doble hélice y comienza a añadir nucleótidos complementarios a una de las hebras de ADN, que actuará de patrón. 2. ELONGACIÓN. La ARN-pol avanza a lo largo de cadena patrón de ADN, hacia su extremo 5’, añadiendo nucleótidos (unos 40 por segundo), y sintetiza una hebra de ARN en dirección 5’ 3’. 3. FINALIZACIÓN. La finalización se produce al llegar a una secuencia rica en G y C, que actúa se señal de terminación. Se cierra el bucle de ADN y se separa la ARN polimerasa.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
12
Transcripción en eucariotas (Maduración del ARN) En procariotas el ARNm transcrito no precisa de maduración, pero en eucariotas, los genes están fragmentados, es decir, tienen fragmentos que no se transcriben (intrones) y fragmentos que sí lo hacen (exones). Así en el proceso de maduración es necesario eliminar las secuencias sin sentido o intrones y empalmar las secuencias con sentido o exones. En la transcripcion en eucariotas intervienen tres tipos de ARN-pol, cada una de ellas transcribe un tipo de ARN distinto. Las fases de la transcripción son similares a procariotas, primero la ARN-pol se une a la región promotora y empieza a añadir nucleótidos. Cuando se llevan transcritos unos 30 nucleótidos, al extremo 5’ se le añade una caperuza (Gppp). Al finalizar la síntesis al extremo final se le añade un segmento de 200 nucleótidos de adenina (cola poli A). Este ARN transcrito se denomina pre-ARN o ARN heterogéneo nuclear (ARNhn). Ahora tiene que madurar, para ello, un enzima provoca que se curven los intrones y se desprendan, y otra actúa empalmando los exones, para formar un ARNm maduro.
Transcripción
Maduracion del ARN en eucariotas
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
13
9.2. TRADUCCIÓN o SÍNTESIS DE PROTEÍNAS En la biosíntesis de proteínas se pueden distinguir las siguientes etapas: 1. Activación de los aminoácidos. 2. Traducción: iniciación de la síntesis, elongación o alargamiento de la cadena polipeptídica y finalización de la síntesis. 1. Activación de los aminoácidos: Los aminoácidos en presencia de la enzima aminoacil-ARNt sintetasa y de ATP, se unen a un ARNt específico y da lugar a un aminoacil-ARNt. Después de la unión de¡ aminoácido al ARNt, se libera la enzima, AMP y PPi (Pirofosfato inorgánico). 2. Traducción: INICIACIÓN: el ARNm, se une a la subunidad menor de los ribosomas gracias a una secuencia inicial llamada región líder (esta secuencia no se va a traducir). A éstos se asocia el aminoacil ARNt (o sea, una molécula de ARNt que lleva un aminoácido en uno de sus extremos). Los ARNt tienen en una de sus asas un triplete de nucleótidos, llamado anticodón, que se asociará al primer triplete o codón del ARNm, según la complementariedad de las bases (o sea, si el primer codón es AUG, el ARNt que se asocia es el que lleva UAC, que se corresponde según la clave genética con la metionina). A este grupo de moléculas se une la subunidad mayor de los ribosomas, formándose el complejo ribosomal. Este complejo posee dos sitios de unión: Centro P (centro peptidil): donde se sitúa el primer aminoacil-ARNt. Centro A (centro aceptor): donde se sitúan los nuevos aminoacil-ARNt que vayan llegando. Esta fase está catalizada por proteínas llamadas factores de iniciación (IF). ELONGACIÓN: al centro A llega el segundo aminoacil-ARNt. El primer aminoácido que se encontraba en centro P se va a unir a ese segundo amínoácido mediante un enlace peptídica. Esta unión es catalizada por el enzima peptidil-transferasa. El centro P queda, pues, ocupado por un ARNt sin aminoácido, este ARNt saldrá de¡ ribosoma. Se produce entonces la translocación ribosomal, que quiere decir que el ribosoma avanza tres nucleótidos del ARNm, (o sea, un codón), y el ARNt con dos aminoácidos que está en el ribosoma queda en el centro P, y por lo tanto el centro A queda libre para la llegada de otro aminoacil-ARNt. Así poco a poco, a medida que los ribosomas avanzan por el ARNm se va formando una cadena polipeptídica (o sea, una cadena de varios aminoácidos). Esta fase está catalizada por los factores de elongación (EF). FINALIZACIÓN DE LA SÍNTESIS: después de que los ribosomas hayan recorrido la secuencia de nucleótidos del ARNm, el final de la síntesis tiene lugar cuando el sitio A del ribosoma llega a un codón de terminación para el que no existe ningún ARNt complementario. Esos codones o tripletes sin sentido son tres: UAA, UAG y UGA. Ahora sobre el sitio A se sitúan unas proteínas llamadas factores de liberación que catalizan la separación de la cadena polipeptídica del ribosoma. A continuación se separan el ARNm, y las dos subunidades de los ribosomas.
BIOLOGÍA 2º BACHILLERATO. ESQUEMAS GENÉTICA MOLECULAR DUPLICACIÓN o REPLICACION ADN
Horquillas de replicación
Burbuja de replicación y duplicación bidireccional
BIOLOGÍA 2º BACHILLERATO. ESQUEMAS GENÉTICA MOLECULAR TRANSCRIPCIÓN Y TRADUCCIÓN
Maduración ARN eucariota
Síntesis de cadena de ARN
Etapas transcripción
Traducción
NH
|
ELONGACIÓN
3' NH2
NH2
Met
Met
|
|
UG A
INICIACIÓN
5'
UGA
AUG P
UCA A
NH2
Met
Met
Met
Ser
Ser
Ser
5'
AUG P
AUG 5'
UCA A
UCA P
CCG A
2
H
FINALIZACIÓN
3' 5'
UAU
etc.
AUA
NH2 HOOC
UAU
UGA
CGG CCG A
AUG
Primera translocación
Pro
UCA P
CCG A
2
5' AUG
UCA P
|
Pro
|
|
N
CAU
5'
CAU
3'
Ser
UGA
|
Me t Se r
5'
3' 5'
3'
NH2
UCA A
NH2
|
Met
AUG P
NH2
UGA
UCA A NH
5'
UGA
F
2
UCA A
UGA
NH2 | Ser
|
3'
AUG P
5' 3'
CGG
AUG P
NH
Enlace peptídico
A
CAU
AUG
NH2 | Met
5'
P
CGG
5'
A
CAU
P
AUG
5'
CAU
1
UAA
3'
G AU
5'
2
Ser
UAA
3'
Biosíntesis de las proteínas. En el nombre de los diferentes aminoácidos se ha señalado el lugar que ocupa el grupo amino, para resaltar que la unión con el ARNt o con el siguiente aminoácido se realiza mediante el grupo carboxilo.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
14
10. EL CÓDIGO GENÉTICO El código o la clave genética es el que establece la relación entre la secuencia de nucleótidos y la secuencia de aminoácidos de una proteína. Severo Ochoa recibió el premio Nobel de medicina por su contribución al desciframiento de¡ código genético. Consiguió una enzima (polinucleótido fosforilasa) capaz de fabricar ARN ín vitro sin necesidad de molde. Gracias a esta enzima, fabricó distintos ARN constituidos por un solo nucleótido (poliA, poliU .... ). Años después otros investigadores (Niremberg y Khorana), fabricando ARN sintéticos de secuencias conocidas y utilizando extractos de E. coli y distintos aminoácidos dedujeron las relaciones entre nucleótidos y aminoácidos. Dado que existen 20 aminoácidos diferentes y sólo hay cuatro tipos de nucleótidos, la relación (colinearidad) entre ambos no se podía establecer uno a uno, ni tampoco entre dupletes de nucleótidos (4 x 2 = 16), sino como mínimo, entre tripletes de nucleótidos (4 x 3 = 64) y aminoácidos. CARACTERÍSTICAS DEL CÓDIGO GENÉTICO
Es universal, pues es el mismo en todos los seres vivos, y no es ambiguo, ya que cada codón o triplete, especifica para el mismo aminoácido. Está degenerado, lo que quiere decir que un mismo aminoácido puede ser codificado por varios tripletes, ya que existen 64 tripletes distintos para los 20 aminoácidos. La tercera base suele ser variable para codificar un mismo aminoácido. Esto representa una ventaja, ya que aunque se produzca un error en la copia de un nucleótido, seguiría la colinearidad entre el triplete y el nucleótido. Por otro lado, si sólo hubiera veinte tripletes traducibles, habría 44 tripletes sin sentido (64 - 20 = 44) y un simple error en un nucleótido lo convertiría probablemente en un triplete sin sentido, interrumpiéndose así la biosíntesis de la proteína. Carece de solapamiento, lo que significa que los tripletes se disponen en el ARN, uno a continuación de otro y no comparten ninguna base.
11. REGULACIÓN DE LA EXPRESIÓN DE LOS GENES CONCEPTO DE GEN Los genes son las unidades de herencia de los cromosomas, al ser el material genético que se transmite de padres a hijos. Cada gen está formado por una secuencia de nucleótidos que codifica para una molécula de ARN o una cadena polipeptídica. Los genes presentan una triple capacidad: 1. Capacidad de mutar. Puede cambiar la secuencia de nucleótidos de un gen, apareciendo estados alternativos, que son los alelos (genes que informan sobre la misma característica, pero no llevan la misma información). 2. Capacidad de intercambiar secuencias de ADN con otros genes, mediante recombinación. 3. Capacidad de expresarse, es decir, poseen la información necesaria para la codificación de una proteína. EXPRESIÓN GÉNICA Las células no están continuamente sintetizando todos los tipos de proteínas sobre las cuales tienen información. Si así fuera, se produciría un caos metabólico. Es evidentemente, que debe existir un sistema de regulación. Como la cantidad de proteínas depende directamente de la cantidad de ARN, presente en el citoplasma, y como la vida media de este es muy corta (minutos), la cantidad de ARNm, regula los niveles enzimáticos del medio. Así pues, es suficiente con regular la síntesis de ARNm. En procariotas, como bacterias, la síntesis de ARN, depende de la cantidad de sustrato disponible, mientras que en eucariotas, depende fundamentalmente de hormonas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
15
12. MUTACIONES
Son alteraciones del material genético (ADN o ARN en algunos virus). Se puede alterar la secuencia de nucleótidos, el orden de los genes en un cromosoma o el número de cromosomas. Se producen al azar, durante la duplicación del ADN o la división celular Pueden ser beneficiosas para una población, ya que aumentan la variabilidad, y en caso de cambios en las condiciones del medio, aquellos individuos mutantes que presentaran características que les permitieran adaptarse mejor a las nuevas condiciones tendrían más posibilidades de sobrevivir (selección natural) y transmitir sus características a las descendencia. Así pues las mutaciones a lo largo de la historia biológica han permitido la evolución de las especies y con ello la continuidad de la vida. Ahora bien, hay que tener en cuenta que las mutación tienen más probabilidades de ser perjudiciales que beneficiosas para los organismos, ya que las variantes que existen en una población han sido escogidas por la selección natural. Son perjudiciales para la salud del individuo en la mayor parte de las ocasiones ya que producen deficiencias, como el Síndrome de Down, algunos tipos de cánceres y leucemias, trastornos metabólicos,...
TIPOS DE MUTACIONES En general de suele hablar de tres tipos: 1. Génicas o puntuales: afectan a la secuencia de nucleótidos de un gen. 2. Cromosómicas: si alteran el orden de los genes de un cromosoma. 3. Genómicas: si modifican el número de cromosomas de un individuo. Ejemplos 1. Génicas: La sustitución de un nucleótido por otro en el ADN, que puede provocar un cambio de aminoácido en la proteína correspondiente. Muchas veces la proteína no se ve afectada, pero en otros casos se ve alterada su función biológica, como en la anemia falciforme, donde debido a una mutación se fabrica una hemoglobina anormal, afectando a los glóbulos rojos y al desarrollo del individuo. La adición o deleción (pérdida) de un nucléotido, suele provocar grandes cambios en la proteína codificada. 2. Cromosómicas: La deleción cromosómica implica la pérdida de un fragmento de un cromosoma, con la pérdida de genes correspondiente, por lo que puede ser letal (provoca la muerte). La duplicación cromosómica, o aumento de un fragmento de cromosoma y por lo tanto un aumento del número de genes. Ambas se producen por apareamientos desiguales de cromosomas homólogos en la meiosis. Las translocaciones son cambios en la posición de los genes dentro de un cromosoma. 3. Genómicas: La aneuploidía es una alteración en el número normal de uno o más tipos de cromosomas, sin llegar al juego completo. Como ejemplo está el Síndrome de Down o Mongolismo, que es una trisomía del cromosoma 21 (las personas con Síndrome de Down tienen 3 ejemplares del cromosoma 21). La poliploidía es el aumento de dotaciones cromosómicas. Los individuos pueden ser triploides (3N), como en el plátano, tetraploides (4N) como en la patata,... Por último, si la mutación aparece de forma natural se dice que es una mutación espontánea, si es provocada por agentes mutágenos (como radiaciones o productos químicos) se dice que es inducida. Las mutaciones pueden afectar a las células somáticas y no se transmiten a la descendencia, como en el caso del cáncer, o a las células reproductoras o germinales, en cuyo caso se transmiten a la descendencia.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
16
13. EL ADN, BIOTECNOLOGÍA e INGENIERÍA GENÉTICA La Biotecnología es todo el conjunto de técnicas que emplea seres vivos o compuestos procedentes de ellos (como las enzimas) para la obtención de productos, bienes y servicios de distinto tipo para la humanidad. La Biotecnología abarca: Biotecnología tradicional: utilizada desde hace cientos de años y que emplea, por ejemplo, procesos de fermentación microbiana para la elaboración del pan, bebidas alcohólicas o yogur. Biotecnología moderna: nacida en los últimos 30 años, gracias a los progresos de la biología celular, bioquímica, microbiología, inmunología e ingeniería genética.
INGENIERÍA GENÉTICA Comprende todo el conjunto de métodos y técnicas que permiten el y manipulación del ADN y la transferencia de genes de un organismo a otro. De este modo se han podido obtener organismos transgénicos u Organismos Modificados Genéticamente (OMG). Existen varias técnicas de ingeniería genética, entre las que destacan: Obtención de ADN recombinante. Técnica que permite cortar el ADN de un organismo en múltiples fragmentos, aislar alguno de ellos, e introducirlo, mediante un vector, en otro organismo, originando un organismo transgénico. Clonación del ADN. Permite la producción de múltiples copias de un gen específico o de un fragmento de ADN. Reacción en cadena de la polimerasa (PCR). Técnica in Vitro, que permite obtener de forma muy rápido un elevado número de copias de un fragmento de ADN. Secuenciación del ADN. Técnica que permite conocer el orden de los nucleótidos que forman parte de un gen, o incluso del genoma completo de un organismo. (ya vista en el tema de ácidos nucleicos)
Tecnología del ADN recombinante El ADN formado por la unión de fragmentos de ADN procedente de organismos distintos se denomina ADN recombinante. Por eso todo el conjunto de técnicas que utiliza la ingeniería genética para conseguirlo recibe el nombre de tecnología del ADN recombinante. Los pasos que implica esta tecnología son, en esencia, estos: 1. Las moléculas de ADN de dos organismos diferentes se cortan en fragmentos con ENDONUCLEASAS DE RESTRICCIÓN. Las endonucleasas de restricción son enzimas fabricadas por bacterias y son capaces de cortar el ADN de cualquier organismo por secuencias específicas, dando lugar a fragmentos con extremos de una sola cadena, llamadas extremos cohesivos. Actualmente se conocen más de 1200 endonucleasas de restricción que reconocen y cortan el ADN por distintas secuencias. Una de ellas de la endonucleasa EcoRI, que reconoce la secuencia GAATTC y corta entre los nucleótidos G y A de cada una de las cadenas de las moléculas de ADN.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
17
2. Una vez obtenidos los fragmentos de ADN con extremos cohesivos complementarios, se ponen en o y se someten a la acción de la enzima ADN LIGASA, que une los extremos cohesivos, y forma una molécula de ADN recombinante, que contiene ADN de los dos organismos.
Clonación del ADN La clonación de un gen consiste en introducirlo en una célula, de manera que pueda ser copiada. Para ello se inserta en una molécula de ADN, llamado vector de clonación, capaz de entrar y replicarse independientemente en una célula huésped. El resultado es la formación de ADN recombinante y el vector de clonación actúa como medio de transporte. Para clonar genes se utilizar diferentes vectores de clonación, como los plásmidos bacterianos, pequeñas moléculas de ADN circular que se pueden replicar independientemente en las bacterias. El proceso de clonación de un gen en bacterias incluiría las siguientes etapas: 1. Obtención del plásmido recombinante formado por un plásmido que contenga un gen de resistencia a un antibiótico y el gen que se desea clonar. 2. Transformación de las bacterias incorporándoles el plásmido recombinante. 3. Selección de las bacterias transformadas, añadiendo al medio el antibiótico que 4. Crecimiento de las bacterias en medio de cultivo. 5. Aislamiento de los plásmidos recombinantes y de las copias del gen de interés.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
18
Reacción en cadena de la polimerasa (PCR) La reacción en cadena de la polimerasa (PCR) es un método que permite obtener múltiples copias de un fragmento de ADN en muy poco tiempo, lo que se denominan amplificación del ADN. Es una técnica in vitro, donde se reproduce la duplicación del ADN. Para amplificar el ADN se añaden en un tubo de ensayo los siguientes componentes: La muestra de ADN a amplificar Cebadores: pequeñas cadenas de nucleótidos complementarias a las secuencias de ADN que flanquean al gen que queremos copiar. Los cuatro tipos de desoxirribonucleótidos trifosfato (ATP. GTP, CTP, TTP). Una ADN polimerasa resistente al calor, obtenida a partir de la bacteria termófila Thermus aquaticus (Taq-polimerasa).
Biología 2º Bachillerato
19
Tema 5. Herencia y Genética Molecular
Para conseguirlo se utilizan varios ciclos, y en cada uno de ellos el ADN se duplica, siguiendo estas etapas:
1. Desnaturalización. Se calienta la muestra de ADN a 95 ºC, para desnaturalizar el ADN y separar las cadenas de nucleótidos.
2. Hibridación. Se enfría a 55 ºC la muestra, para que los cebadores hibriden con las secuencias complementarias en cada una de las cadenas del ADN.
3. Síntesis de ADN. Se calienta la muestra a 72 ºC para que la Taq-polimerasa fabrique las nuevas cadenas de ADN.
Las aplicaciones de la PCR son varias: Amplificaciones de ADN antiguos para estudios evolutivos o, paleontológicos. La obtención de la huella genética de ADN en medicina forense. Detección de ADN de genes de virus en etapas tempranas de infección, como por ejemplo el VIH, en pruebas de diagnóstico.
Primer ciclo Segundo ciclo
Tercer ciclo
100
T e m pe ra tu ra (C )
80
Ciclo 1
Ciclo 2
Desnaturalización
Ciclo 3
Síntesis
60
Apareamiento Tiempo
Técnica de PCR
APLICACIONES DE LA INGENIERÍA GENÉTICA Algunas de las aplicaciones de la ingeniería genética son: Agricultura y ganadería: Clonación de plantas o animales con características interesantes (que produzcan frutos de mejor calidad, mayor producción de leche, carne o lana, por ejemplo). Obtención de plantas y animales transgénicos, que al poseer genes de otro organismo adquieren características nuevas, como la resistencia a plagas o heladas, crecimiento más rápido, alimentos animales con menos colesterol, etc,… Control de plagas: algunos microorganismos, como bacterias, han sido utilizados como bioinsecticidas para controlar algunas plagas.
Biología 2º Bachillerato
Tema 5. Herencia y Genética Molecular
20
Medicina: Obtención de medicamentos, como la insulina, los factores de coagulación, interferón, hormona de crecimiento,…, o como en Farmacogenética, tratar de obtener medicamentos personalizados. Terapia génica, que se basa en la introducción de genes sanos en personas con genes defectuosos causantes de enfermedades, lo que permitiría la curación de la enfermedad. Para introducir el gen en el paciente se pueden emplear virus no patógenos que hayan sido modificados genéticamente y que porten el gen sano. Diagnóstico de enfermedades genéticas mediante el empleo de Biochips, que son pequeñas placas que contienen cientos de genes colocados en diminutas casillas, sobre las que se colocan gotas de sangre o saliva y que permiten detectar la presencia de genes causantes de enfermedades. Utilización de transgénicos para elaborar vacunas.
Medio ambiente (Biorremediación) Obtención de bacterias que degradan hidrocarburos como el petróleo para combatir las mareas negras o plantas transgénicas que permitan convertir algunos contaminantes en sustancias menos tóxicas.
Obtención de planta transgénica
Transposones Los descubre Barbara Mc Clintock en la década de los 40-50, en el genoma del maíz. Son elementos del genoma del maíz que tenían la capacidad de movilizarse favoreciendo la aparición de determinados fenotipos. Los transposones son fragmentos de DNA que pueden pasar de un cromosoma a otro sin una etapa de existencia independiente. En algunos casos se escinden del cromosoma y se insertan en otro lugar; otras veces, el fragmento original permanece en su sitio y una copia se inserta en otro lugar. Otras veces, se copian primero en RNA y, a través de una transcriptasa inversa, producen DNA que se inserta en un cromosoma. Cuando cambian de posición y abandonan el lugar en el que estaban, en ese sitio, se produce un deleción o pérdida de bases. Si el elemento transponible estaba insertado en el interior de un gen, puede que se recupere la función de dicho gen. De igual forma, si el elemento genético móvil al cambiar de posición se inserta dentro de un gen se produce una adición de una gran cantidad de nucleótidos que tendrá como consecuencia la pérdida de la función de dicho gen. Por consiguiente, los elementos genéticos transponibles producen mutaciones. En bacterias existen dos tipos de elementos genéticos móviles: – Transposón Simple, Secuencia de Inserción o Elemento de Inserción (IS): los transposones simples contienen una secuencia central con información para la proteína transposasa – Transposón Compuesto (Tn): contienen un elemento de inserción (IS) en cada extremo en y una región central que además suele contener información de otro tipo. Por ejemplo, los Factores de transferencia de resistencia (RTF), poseen información en la zona central para resistencia a antibióticos (cloranfenicol, kanamicina, tetraciclina, etc.). Transposones en mamíferos. En mamíferos se conocen tres clases de secuencias que son capaces de transponerse o cambiar de posición a través de un ARN intermediario: – Retrovirus endógenos: semejantes a los retrovirus, no pueden infectar nuevas células y están restringidos a un genoma, pero pueden transponerse dentro de la célula. Poseen largas secuencias repetidas en los extremos (LTR), genes env (con información para la proteína de la cubierta) y genes que codifican para la trasnrciptasa inversa, como los presentes en retrovirus. – Retrotransposones o retroposones: sólo contienen genes para la transcriptasa inversa y pueden transponerse. – Retropseudogenes: carecen de genes para la transcriptasa inversa y por consiguiente son incapaces de transponerse de forma independiente, aunque si pueden cambiar de posición en presencia de otros elementos móviles que posean información para la trasncriptasa inversa.
1
Problemas de Genética Biología 2º
GENÉTICA MENDELIANA
Problemas de uno y dos caracteres 1. En el hombre el color pardo de los ojos "A" domina sobre el color azul "a". Una pareja en la que el hombre tiene los ojos pardos y la mujer ojos azules tienen dos hijos, uno de ellos de ojos pardos y otro de ojos azules . Averiguar: a) El genotipo del padre b) La probabilidad de que el tercer hijo sea de ojos azules. 2. La acondroplasia es una anomalía determinada por un gen autosómico que da lugar a un tipo de enanismo en la especie humana. Dos enanos acondroplásicos tienen dos hijos, un acondroplásico y otro normal. a) La acondroplasia, ¿es un carácter dominante o recesivo?. ¿Por qué?. b) ¿Cuál es el genotipo de cada uno de los progenitores?. ¿Porqué?. c) ¿Cuál es la probabilidad de que el próximo descendiente de la pareja sea normal?. ¿Y de que sea acondroplásico?. Realizar un esquema del cruzamiento. 3. Una vaca de pelo retinto (rojizo), cuyos padres son de pelo negro, se cruza con un toro de pelo negro, cuyos padres tienen pelo negro, uno de ellos y pelo retinto el otro. a) ¿Cuál es el genotipo de los animales que se cruzan?. b) ¿Y el fenotipo de la descendencia?. 4. El gen R que rige el pelo rizado domina sobre el gen recesivo (r) del pelo liso. Una mujer con el pelo rizado se casa con un varón con el pelo liso y tienen una hija con el pelo rizado. El padre de la mujer tenía el pelo liso, el de la madre no lo recuerdan, pero sí saben que la abuela materna lo tenía liso y el abuelo materno lo tenía rizado, aunque el de la madre de éste era liso. ¿Cuál es el genotipo de todos ellos?. 5. Razona la veracidad o falsedad de la siguiente afirmación: El color de tipo común del cuerpo de la Drosophila está determinado por el gen dominante "N", su alelo recesivo "n" produce cuerpo de color negro. Cuando una mosca tipo común de raza pura se cruza con otra de cuerpo negro, la fracción de la segunda generación que se espera sea heterocigótica es 1/2 ?. 6. En el pollo las plumas sedosas están determinadas por un gen cuyo efecto es recesivo respecto al que rige las plumas normales. Si de un cruzamiento entre individuos heterocigóticos para dicho gen, se criasen 98 aves, ¿cuántas cabría esperar que fuesen sedosas y cuántas normales?. 7. El pelo rizado en los perros domina sobre el pelo liso. Una pareja de pelo rizado tuvo un cachorro
de pelo también rizado y del que se quiere saber si es híbrido o heterocigótico. ¿Con qué tipo de hembras tendrá que cruzarse?.
8. Como Mendel descubrió, las semillas de color amarillo en los guisantes son dominantes sobre los de color verde. En los experimentos siguientes, padres con fenotipos conocidos pero genotipos desconocidos produjeron la siguiente descendencia: a) Dar los genotipos más probables de cada parental b) En los cruces B, D, E, indíquese qué proporción de la descendencia amarilla producida en cada uno de ellos se esperaría que produjera descendientes verdes por autopolinización.
Parentales A. amarillo x verde
Amarillo Verde 82
78
B. amarillo x amarillo 118
39
C. verde x verde
0
50
D. amarillo x verde
74
0
E. amarillo x amarillo 90
0
Problemas de Genética Biología 2º
2
9. La fenilcetonuria (FCU) es un desorden metabólico que se hereda con carácter autosómico recesivo. Dos progenitores sanos tienen un hijo con FCU. Indica los fenotipos y genotipos de todos los apareamientos que teóricamente pueden dar un descendiente afectado de FCU. a) ¿A cuál de estos tipos de apareamiento pertenece el caso descrito ?. b) ¿Cuál es la probabilidad de que el siguiente hijo padezca también la enfermedad ?. c) ¿Cuál será la probabilidad de qué un hijo normal (sano) de estos padres sea portador heterocigótico para FCU ?. 10. En el conejo, la piel manchada (S) es dominante sobre la piel uniforme (s); y el negro (B) es dominante sobre el pardo (b). Un conejo manchado pardo se cruza con un ejemplar negro uniforme, todos los descendientes son negros manchados. ¿Cuáles son los genotipos de los padres?. ¿Cuál sería el aspecto de la F2 si dos de estos animales de la F1 se cruzan entre sí?. 11. En un cruce entre dos moscas Drosophila melanogaster normales se obtienen los siguientes descendientes con los fenotipos:
¿Cuáles de esos caracteres son dominantes y cuáles recesivos?. ¿Cuál es el genotipo de cada uno de los individuos de la descendencia?. ¿Cuál es el genotipo de los padres?. 12. En el guisante la altura del tallo está determinada por un gen con dos alelos, T (tallo largo) y t (tallo corto). La textura de la semilla está controlada por otro gen cuyo alelo L produce semillas lisas, mientras que el alelo l produce semillas rugosas. Estas dos parejas de genes se transmiten independientemente. Se cruza una variedad pura lisa de tallo alto con otra variedad pura de semillas rugosas y tallo corto. Indicar: a) El genotipo y fenotipo de la F1 b) Los fenotipos de la F2 y la proporción de cada uno de ellos que resultan de la autofecundación de las plantas de la F1. c) Si en la generación parental P, una de las variedades fuera lisa y corta y la otra rugosa y alta, ambas de raza pura, ¿variarán las proporciones fenotípicas en la F1?. Razone la respuesta. 13. En el guisante, el alelo dominante de un gen (T) determina que las flores crezcan en el eje del tallo, mientras que su alelo recesivo (t) determina que crezca sólo el extremo del tallo. Por otra parte, el alelo dominante de otro gen C, determina que las flores sean de color rojo, en tanto que las flores blancas están determinadas por su alelo recesivo c. Si una planta híbrida para las dos características, se cruza con otra de raza pura de flores rojas y localizadas en el eje del tallo, ¿qué proporciones genotípicas y fenotípicas podemos esperar en la generación F1?. 14. Los pollos con alas y patas recortadas reciben el nombre de trepadores. El apareamiento de este tipo de pollos con aves normales da lugar a una descendencia equilibrada entre pollos normales y trepadores. El apareamiento de pollos trepadores entre sí produce una descendencia formada por dos pollos trepadores y uno normal. El cruzamiento entre pollos normales da lugar a una progenie uniforme formada exclusivamente por aves normales. Explicar el fenómeno de forma razonada.
3
Problemas de Genética Biología 2º
15. En el tomate, el color púrpura del tallo está determinado por un alelo autosómico dominante "A". El alelo recesivo "a" determina tallo de color verde. Otro gen autosómico independiente controla la forma de la hoja: el alelo dominante "C" determina hoja con borde recortado y el alelo recesivo "c" determina hoja con borde entero. En la siguiente tabla se indican los resultados en tres cruces entre plantas de fenotipos diferentes. En cada caso, indique cuáles son los genotipos de los progenitores y por qué. Fenotipos de los progenitores
púrpura/recortada púrpura/entera verde/recortada verde/entera
púrpura, recortada x verde, recortada
321
101
310
107
púrpura, recortada x púrpura recortada
144
48
50
18
púrpura, recortada x verde, recortada
722
231
0
0
16. Los ratones gordos se pueden producir por dos genes independientes. El genotipo "oo" genera un ratón gordo y estéril, llamado obeso; su alelo dominante "O" da lugar a crecimiento normal. El genotipo recesivo "aa" también produce un ratón gordo y estéril llamado adiposo, mientras que su alelo dominante ocasiona crecimiento normal. ? Qué proporciones fenotípicas de ratones gordos frente a normales podemos esperar en F1, siendo los padres de genotipo OoAa. 17. La miopía es debida a un gen dominante, al igual que el fenotipo Rh+. Una mujer de visión normal Rh+, hija de un hombre Rh-, tiene descendencia con un varón miope heterocigótico y Rh-. Establece los posibles genotipos y fenotipos de esta pareja, y su frecuencia. 18. Dos condiciones anormales en la especie humana: las cataratas y la fragilidad de los huesos, parecen depender de alelos dominantes, que se heredan independientemente. Un hombre con cataratas y huesos frágiles, cuyo padre era normal para las dos características, tuvo un hijo con un mujer sin cataratas pero con huesos frágiles, cuya madre era de huesos normales. a) Cuál es la probabilidad de que su hijo: b) No tenga ninguna enfermedad c) Tenga cataratas y huesos normales d) Tenga huesos frágiles y ojos normales e) Padezca ambas enfermedades 19. En el ser humano, la presencia de uno de los antígenos Rh de la superficie de los eritrocitos y la forma ovalada de estos (eliptocitosis) son causadas por la existencia de sendos alelos dominantes situados en la misma pareja autosómica. Un hombre con eliptocitosis, cuya madre tenía glóbulos rojos normales y genotipos homocigótico Rh positivo, y cuyo padre era Rh negativo y heterocigótico para la eliptocitosis, se casa con una mujer normal y Rh negativa. a) ¿Cuál es la probabilidad de que su primer hijo sea Rh negativo y tenga eliptocitosis?. b) Si su primer hijo es Rh positivo, ¿cuál es la probabilidad de que tenga eliptocitosis?. ¿Y si es el segundo hijo?. 20. En el cruzamiento AaBbDDFf x AABbddFF, todos los genes segregan independientemente y muestran dominancia. c) ¿Cuántos gametos genéticamente diferentes puede formar cada parental?. d) ¿Cuántos cigotos genéticamente diferentes se podrían formar en este cruzamiento?. e) ¿Qué proporción de la descendencia será heterocigótica para todos los loci?.
Problemas de Genética Biología 2º
4
MODIFICACIONES A LAS PROPORCIONES DE LAS LEYES DE MENDEL Herencia intermedia (codominancia) 21. Una mariposa de alas grises se cruza con una de alas negras y se obtiene una descendencia formada por 115 mariposas de alas grises y 115 mariposas de alas negras. Si la mariposa de alas grises se cruza con una de alas blancas se obtienen 94 mariposas de alas blancas y 94 de alas grises. Razonar ambos cruzamientos, indicando cómo son los genotipos y fenotipos de las mariposas que se cruzan y la descendencia. 22. Dos plantas de dondiego (Mirabilis jalapa) son homocigóticas para el color de las flores. Una de ellas produce flores de color blanco marfil y la otra, flores rojas. Señale los genotipos y fenotipos de los dondiegos originados del cruce de ambas plantas, sabiendo que "B" es el gen responsable del color marfil, "R" es el gen que condiciona el color rojo y que los genes R y B son equipotentes ( herencia intermedia). 23. Las cobayas de pelaje color amarillo son homocigotos (CACA), el color crema se debe a un genotipo heterocigótico (CACB), y el blanco es debido al genotipo homocigótico (CBCB). ¿Qué proporciones genotípicas y fenotípicas se obtienen de un cruzamiento entre dos cabayas de color crema?. 24. En las plantas del género Antirrhinum, las flores rojas y las blancas presentan herencia intermedia. Lo mismo ocurre con las hojas estrechas y las hojas anchas. Suponiendo que las parejas alélicas correspondientes segregan de forma independiente, indicar las proporciones genotípicas y fenotípicas esperadas en: a) La autofecundación de una planta de flores rosas y hojas de anchura intermedia. b) El cruzamiento entre una planta igual a la anterior y otra de flores blancas y hojas estrechas. Genes letales 25. La ausencia de patas en las reses se debe a un gen letal recesivo. Del apareamiento entre un toro y una vaca, ambos híbridos, ? qué proporciones genotípicas se esperan en la F2 adulta?. Los becerros amputados mueren al nacer. 26. La enfermedad de Tay-Sachs es una enfermedad hereditaria recesiva que causa la muerte en los primeros años de vida cuando se encuentra en condición homocigótica. Se piensa que los dedos anormalmente cortos, braquifalangia,se deben al genotipo heterocigótico para un gen letal, siendo normal el individuo BB. ? Cuáles son los fenotipos esperados entre niños adolescentes hijos de padres braquifalángicos y heterocigóticos para la enfermedad de Tay-Sachs ?. 27. Una mujer lleva en uno de sus cromosomas X un gen letal recesivo, y en el otro, el alelo dominante normal. ¿Cuál será la proporción de sexos en la descendencia de esta mujer con un hombre normal?. 28. En los ratones de campo existe un gen que determina el color pelo amarillo y que es dominante sobre el que determina el color normal o de tipo salvaje. El tamaño de la cola está determinada por una pareja alélica, de tal manera que el gen dominante determina tamaño de cola corta mientras que el recesivo determina tamaño normal o de tipo salvaje. Ambas parejas de genes se transmiten a la descendencia independientemente la una de la otra. Aquellos embriones que son homocigóticos para uno o para los dos genes dominantes mueren antes de nacer. ¿En qué proporción y como serán los fenotipos de la descendencia de un cruzamiento entre un macho de color amarillo y cola corta con una hembra de las mismas características?.
Problemas de Genética Biología 2º
5
Alelismo multiple. Series alélicas. 29. Un hombre acusa a su esposa de infidelidad alegando que el cuarto de sus hijos no es suyo. Los dos primeros hijos tienen el grupo sanguíneo AB y el tercero es del grupo A. El hijo motivo de la demanda es del grupo B y los esposos son de los grupos sanguíneos A y AB. Con estos datos, ¿se puede probar la infidelidad de la esposa?. 30. Si un hombre del grupo sanguíneo AB se casa con una mujer del grupo A, cuyo padre era del grupo 0. ¿Qué grupos sanguíneos se puede esperar entre sus hijos y con qué frecuencia?. 31. En una determinada raza de ratones el color del pelo está controlado por una serie alélica: A1 determina el pelaje negro, A2 blanco, A3 rayado y A4 grisáceo. El alelo A1 domina sobre el A2, éste sobre el A3 y éste sobre el A4. Al cruzar un ratón negro y otro rayado se obtuvo una camada formada por dos ratones blancos y cuatro negros. a) ¿Cuáles serán los fenotipos de los ratones que se cruzan?. b) De los ratones de la camada, ¿cuántos se esperaba que fueran blancos?. 32. La herencia del color de la piel en las reses, está determinada por una serie de alelos múltiples, con la siguiente jerarquía de dominancia: S > sh > sc > s El alelo “S” determina una banda de color blanco alrededor del cuerpo que se denomina cinturón holandes. El alelo “sh” produce manchas de tipo Hereford, el color sólido es el resultado del alelo “sc” y las manchas tipo Holstein, están producidas por el alelo “s”. Machos con cinturón holandés homocigóticos son cruzados con hembras tipo Holstein. Las hembras de la F1 son cruzadas con machos tipo Hereford de genotipo “sh sc”. Predecir las frecuencias genotípicas y fenotípicas de la descendencia. 33. Una serie de alelos múltiples gobierna la intensidad de la pigmentación en el ratón. D = color completo; d = color diluido y dl = letal. El orden de dominancia es: D > d > dl Un ratón de color completo portador del gen letal es apareado con un individuo color diluido también portador del gen letal. a) ¿Qué proporción fenotípica puede esperarse de la descendencia viable?. b) ¿Qué porcentaje de la descendencia con color completo es portadora del gen letal?. c) ¿Qué porcentaje de la descendencia con color diluido lleva el gen letal?. Epistasia o interacción génica 34. El color del pelaje de una determinada raza canina es debido a dos parejas de genes independientes. El pelo negro es controlado por un gen dominante respecto a su alelo que determina el color café. En otro locus, un alelo dominante inhibe la pigmentación del pelo produciendo, por tanto, perros de pelo blanco; su alelo recesivo permite la coloración del pelaje. Calcular: a) El porcentaje de perros blancos que se espera obtener del cruzamiento de un perro diheterocigótico con otro de color café. b) La probabilidad de obtener una camada de seis, cinco perros de color café y uno negro. 35. En Salvia horminum el color de la flor está determinada por un par de loci independientes, cada uno con dos formas alélicas (dominante y recesiva). Al cruzar individuos doble heterocigóticos de flor color violeta se obtuvo la siguiente descendencia: 9 de flores violetas, 3 de flores rosas y 4 de flores blancas. ¿Cómo podría explicarse esta segregación?.
Problemas de Genética Biología 2º
6
HERENCIA LIGADA AL SEXO 36. El daltonismo es un carácter ligado al sexo en la especie humana. En un matrimonio, la mujer posee visión normal para los colores, mientras que su padre era daltónico; y su marido posee visión normal, siendo el padre de este también daltónico. ¿Qué descendencia cabe esperar de este matrimonio para dicho carácter?. 37. En la especie humana, la hemofilia es debida a un gen recesivo localizado en el segmento diferencial del cromosoma X. Su alelo dominante no origina esta enfermedad. Un hombre normal se empareja con una mujer normal cuyo padre sí lo era. Calcula la probabilidad de que la pareja tenga: a) Un varón hemofílico b) Un varón hemofílico y una mujer portadora c) Un niño y una niña normales 38. En la especie humana, la aparición de vello en los pabellones auriculares es debida a la existencia de un gen situado en el segmento no homólogo del cromosoma Y. De la descendencia de un hombre con pelo en las orejas y una mujer sin pelos. a) ¿Qué proporción de descendientes varones poseerán pelos en los pabellones auriculares?. b) ¿Cuál es la probabilidad de tener un varón sin pelos en las orejas?. c) ¿Con qué frecuencia las hijas tendrán pelos en los pabellones auriculares?. 39. En la especie humana el color azul de los ojos se debe a un gen autosómico, recesivo frente a su alelo dominante para el color pardo, y el daltonismo es controlado por un gen recesivo situado en el segmento diferencial del cromosoma X. Una mujer de ojos azules y portadora del daltonismo procrea con un varón daltónico y de ojos pardos (hijo de una mujer de ojos azules). Determinar, utilizando el cálculo de frecuencias, cuál es la probabilidad de la pareja de tener una niña daltónica y de ojos azules. 40. Una mujer de grupo sanguíneo A y de visión normal tiene cuatro hijos con dos hombres distintos. Uno de ellos es daltónico y de grupo sanguíneo AB. El otro es normal y de grupo sanguíneo A. Los hijos son: Varón daltónico de grupo sanguíneo O; Hembra normal de grupo sanguíneo B; Hembra normal de grupo sanguíneo O; Hembra daltónica de grupo sanguíneo A. a) ¿Cuál es el padre de cada niño?. b) ¿Son portadoras del daltonismo las dos niñas normales, es decir, no daltónicas?. HERENCIA INFLUIDA POR EL SEXO 41. El tipo mocho (sin cuernos) de las ovejas es producido por un gen que es dominante en las hembras, pero recesivo en los machos. Un macho homocigótico con cuernos se cruza con una hembra también homocigótica, pero mocha. Realiza la segregación respecto al sexo y al carácter mocho en F1 y F2. 42. Consideramos simultáneamente dos rasgos influidos por el sexo, la calvicie y la cortedad del dedo índice, ambos dominantes en el hombre y recesivos en la mujer. Un hombre calvo heterocigótico, con dedo índice largo, se casa con una mujer de dedo índice largo, heterocigótica y calva. Determinar las frecuencias genotípicas de sus hijos/as. 43. En ovinos la lana blanca (W) es dominante sobre la negra (w), y la presencia de cuernos (H) es dominante sobre la ausencia de cuernos (h) en machos, pero recesiva en hembras. Si un macho blanco con cuernos y homocigótico se cruza con una hembra negra sin cuernos y homocigoto, ¿qué descendencia obtendremos en la F1 y en la F2?.
Problemas de Genética Biología 2º
PROBLEMAS DE ÁRBOLES GENEALÓGICOS 44. En la siguiente figura se indica la transmisión de un carácter (individuos en negro) en una familia. a) Se trata de un carácter dominante o recesivo. b) Indica el genotipo más probable de cada uno de los individuos (utiliza las letras A y a). c) ¿El gen que determina este carácter es autonómico o está situado en el cromosoma X?.
45. En la figura se indica la transmisión de un carácter en una familia. El carácter representa las dos alternativas (blanco y negro) y está determinado por un solo gen. a) Indica si el alelo que determina la característica representada en negro es dominante o recesivo. b) Indica si el gen que determina ese carácter es autosómico o está ligado al sexo. c) Indica los posibles genotipos de todos los individuos (utiliza las letras a y a).
46. En la siguiente figura se indica la transmisión de un tipo de cataratas (individuos en negro) en una familia. Se sabe que esa enfermedad está producida por un gen ligado al sexo situado en el cromosoma X. a) Indica si ese tipo de cataratas es dominante o recesivo. b) Indica los posibles genotipos de los de la familia (utiliza los símbolos XA y Xa ). c) Indica la probabilidad de que la mujer señalada con la flecha tenga un hijo con cataratas.
7
Problemas de Genética Biología 2º
8
PROBLEMAS DE PAU CASTILLA y LEÓN
En una experiencia de laboratorio en la que se empleaban ratones negros, se obtuvo una variedad genética con pigmentación de color blanco, comprobándose que eran heterocigóticos respecto al carácter “pigmentación” (Pp), mientras que los ratones normales sin pigmentación eran homocigóticos (PP). Asimismo, pudo comprobarse que los embriones que tenían un genotipo recesivo homocigótico (pp) morían antes del nacimiento. Si los ratones pigmentados se aparean entre sí: ¿Qué genotipo y qué fenotipo y en qué proporción puede esperarse en la generación F1?. Y si dicha generación F1 se aparea libremente entre si, ¿qué fenotipos se obtendrían?
En el tomate el color rojo del fruto es dominante (R) sobre el color amarillo (r) y la forma biloculada (B) domina sobre la multiloculada (b). Si se desea obtener una línea de plantas de frutos rojos y multiloculados a partir del cruzamiento entre razas puras rojas y biloculadas con razas amarilla y multiloculadas. ¿Qué proporciones de la F2 tendrá el fenotipo deseado? ¿Qué proporciones de esta será homozigótica para los dos caracteres?.
Una mujer (cuyo padre era daltónico y su madre normal para la visión de los colores) tiene hijos con un hombre daltónico. ¿Cuales serán los genotipos de los progenitores y de su descendencia?. ¿Cuáles serán los fenotipos y en que proporciones?
Si suponemos que el color de ojos en humanos está controlado por un gen con dos alelos: b responsable de ojos azules y B que produce ojos marrones y es dominante sobre b: ¿Cuál es el genotipo de un hombre de ojos marrones que tiene un hijo de ojos azules con una mujer de ojos azules? Considerando el mismo apareamiento anterior ¿Que proporción de los dos colores de ojos cabría esperar en los descendientes? ¿Que proporción cabría esperar en cuanto al color de los ojos en la progenie de un apareamiento entre dos individuos de ojos marrones, cada uno de los cuales tenía un progenitor con ojos azules? ¿Cuál de las leyes de Mendel se supone se aplica en el cruzamiento propuesto en la cuestión c)? Razone la respuesta.
Dado el siguiente cruzamiento: SsYy x ssyy ¿Qué genotipos y en qué proporciones esperaría encontrar en la generación filial F1? Explique en que consiste el cruzamiento prueba y que utilidades tiene.
Una hembra Drosophila de genotipo desconocido respecto al color de ojos es cruzada con un macho de ojos color blanco (W) [ el color blanco de los ojos es un carácter ligado al cromosoma X y recesivo respecto al color de ojos rojo silvestre (W+)]. En la descendencia obtenida, la mitad de los machos y la mitad de las hembras pertenecen al fenotipo ojos rojos y la mitad de los machos y la mitad de las hembras pertenecen al fenotipo ojos blancos. Deduzca razonadamente: ¿Cuáles son los genotipo y fenotipo de la Drosophila hembra parental?. ¿Cuáles son los genotipos de los posibles individuos de la generación filial F1 obtenidos a partir del cruzamiento indicado?. Explique brevemente que se entiende por herencia ligada al sexo. Cite un ejemplo en la especie humana.
Los colores de las flores de una angiosperma pueden ser rojo, rosa o blanco. Se sabe que este carácter está determinado por dos genes alelos codominantes: rojo (R) y blanco (B). Haga un esquema del cruzamiento, indicando de qué color serán las flores de los descendientes del cruce entre plantas de flores rosa y en qué proporciones se encontrarán. Defina los conceptos de dominancia, recesividad y codominancia.
BIOLOGIA 2º BACHILLERATO SOLUCIONES PROBLEMAS GENETICA
1
a) Aa b) 1/2
24
2
a) Dominante b) Aa x Aa c) Normal: 1/4 Acondroplasia: 3/4
25
a) Roja estrecha (RRAA)=1/16; Roja intermedia (RRAa)=2/16; Roja ancha (RRaa)=1/16; Rosa estrecha(RrAA)=2/16; Rosa intermedia (RrAa)=4/16; Rosa ancha (Rraa)=2/16; Blanca estrecha (rrAA)=1/16; Blanca intermedia (rrAa)=2/16; Blanca ancha (rraa)=1/16. b) Rosa estrecha; rosa intermedia; blanca estrecha y blanca intermedia 1/4 de cada una. 2/3 Aa y 1/3 AA
3
a) rr (retinto) x Rr (negro) b) ½ retinto ½ negro
26
BbTt x BbTt → 3 Normales y 6 con Braquifalangia
4
Dominante: rizado Recesivo: liso. Todos los rizados heterocigóticos
27
2 mujeres y 1 hombre
5
Verdadero
28
6
3/4 normales y 1/4 sedosas
29
4/8 amarillo corta (AaCc); 1/4 amarillo normal (aacc); 1/4 normal corta; 1/4 normal normal No se puede probar.
7
Con hembras homocigóticas recesivas
30
1/2 grupo A; 1/4 grupo AB y 1/4 grupo B
8
a) Aa x aa b) Aa x Aa c) aa x aa d) AA x aa e) AA x AA ó AA x Aa
31
A1A2 x A3A3/A3A4 → 2 Blancos y 4 Negros
9
A: normal a: FCU
32
1/2 cinturón holandés (Ssh/Ssc); 1/4 hereford (shs); 1/4 sólido (scs)
a) Aa x Aa ; Aa x aa ; aa x aa
10
a) bbSS x BBss b) 9: 3 : 3 : 1
33
Ddl x ddl → F1: Dd; Ddl; ddl; dldl a) 2/3 completo y 1/3 diluido; b) 50%; c) 100%
11
a) Alas y cuerpo normal dominantes, alas cortas y cuerpo marrón recesivos. b) Padres AaBb x AaBb c) Descendencia 9 A_B_/ 3 A_bb / 3 aaB_ / 1 aabb
34
a) 2/4 b) (1/4)6
12
P) LLTT x lltt F1) LlTl F2) 9 L_T_/ 3 L_tt /3 llT_ / 1 lltt c) No varían
35
Epistasia simple recesiva. A: color; B: violeta; b: rosa; a: sin color (blanca). a>B,b
13
P) TcCc x TTCC F1) TTCC/TTCc/TtCC/TtCc 1/4 de cada
36
Las hijas normales (la mitad portadoras) y los hijos normales y daltónicos
14
A: trepador a: normal a) Aa x aa b) Aa x Aa c) aa x aa
37
a) 1/4 b) 1/16 c) 1/8
15
a) AaCc x aaCc b) AaCc x AaCc c) AACc x aaCc
38
XYi x XX → XYi XX a) 100% b) 0% c) 0%
16
9:3:3:1
39
aaXDXd x AaXdY → aaXdXd frecuencia 1/8
40
a) Los hijos del grupo 0 del padre del grupo A, la hija daltónica del padre del grupo AB y la hija del grupo B del padre del grupo AB. b) La hija del grupo B sí y la otra puede serlo si lo hereda de la madre
41
F1 Aa (macho con cuernos); F2 3/4 AA,Aa (con cuernos) 1/4 aa (mochos)
17
M aaRh+Rh- x H Aa Rh- Rh-
18
A:Cataratas; B: fragilidad ósea
19
a) 1/4; b) 50%; c) 25%
42
1/4 CCLl; 1/4 CcLl; 1/4 CCll; ¼ Ccll. C: calvo; c: normal; L: corto; l: largo
20
a) 8 y 2; b) 16; c) 2/16
43
F1: HhWw; F2: 9 H_W_; 3 H_ww; 3 hhW_; 3 hhww
21
a) AA (negras) x Aa (grises) b) aa (blancas) x Aa (grises)
44
a) Recesivo; b) ….; c) Autosómico
22
BB x RR → BR (rosa)
45
a) Recesivo; b) Autosómico; c) ….
23
1/4 amarillo (CACA); 1/2 crema (CACB); 1/4 blanco (CBCB)
46
a) Dominante; b) …. ; c) 1/4 (la mitad de los varones con cataratas)
AaBb x aaBb → a) 1/8 b) 1/8 c) 3/8 d) 3/8
BIOLOGÍA 2º BACHILLERATO ACTIVIDADES GENÉTICA. LIGAMIENTO y RECOMBINACIÓN 1. Dibuja todos los posibles gametos resultantes de una meiosis en cada una de las siguientes células. (Donde no se indica recombinación NO existe)
A b
c
b c A a b C
a
b
C
A
B B
A a
B B
a
C C c c
A
B B
A a
a
b b C C c c
PROBLEMAS DE RECOMBINACIÓN 2. Los genes “a” y “b” están situados en el mismo cromosoma. Escribe el genotipo de los descendientes del cruce entre un individuo diheterocigótico (aB/Ab) y un doble homicogótico recesivo en los siguientes casos: a) Sin recombinación entre a y b b) Con recombinación entre a y b ¿Se cumplen las proporciones mendelianas en alguno de los casos?. 3. Al cruzar un individuo doble heterocigótico con un doble homocigótico recesivo se obtuvo la siguiente proporción de descendientes: 1 Aabb: 1 aaBb ¿Cómo son posibles estos resultados?. Razona la respuesta.
4. El cuerpo negro (b) y los ojos púrpura (p) son mutaciones recesivas en Drosophila, frente al cuerpo (P) y ojos (b) silvestres o normales. En una serie de cruces de obtuvieron los siguientes resultados: Cruces
Descendientes
PpBb x ppbb
Normales 1/2- Negros púrpuras 1/2
PpBb x ppBb
Normales 1/4 - Púrpura normales 1/2 - Normal negras 1/4
PpBb x ppbb
Normales 1/3- Púrpura negras 1/3 -Normal negras -1/6 Púrpura normales 1/6
Explica dichos resultados 5. En un individuo triple heterocigótico (AaBbCc) en fase de acoplamiento, ¿cuáles son los tipos de gametos que puede transmitir a la descendencia?. Ordénalos de más a menos frecuentes.
ACTIVIDADES P.A.U. BIOLOGÍA
GENÉTICA MOLECULAR
1. La siguiente secuencia polinucleotídica corresponde a un fragmento de inicio de un gen bacteriano: 5’ ATGCGAGGGCCCTGCGTGCTG 3’ 3´ TACGCTCCCGGGACGCACGAC 5´ a) Escriba la secuencia de bases del ARNm que se pueda transcribir a partir de dicho fragmento (5) y señale su polaridad (1). b) Indique el número máximo de aminoácidos que puede codificar el ARNm transcrito (2) y el criterio en que se basa para dar su respuesta (2). 2. La siguiente secuencia de una monohebra de ADN corresponde al inicio de un gen bacteriano: 5’- ATGTTAAGGGCCCGTTGTGTG – 3’ 3’- TACAATTCCCGGGCAACACAC – 5’ a) Escriba la secuencia del ARNm correspondiente, indicando su polaridad. (2) b) ¿Cuántos aminoácidos puede codificar este fragmento? (2) c) ¿Qué características del código genético hay que aplicar para calcular el número de aminoácidos? (3) d) ¿Qué tipo de variación/es debería suceder en este fragmento de ADN para que produjera un polipéptido de 5 aminoácidos? Razone la respuesta. (3) 3. Dadas las secuencias de polinucleótidos siguientes: I) 5´- AGGCTACCTAAG – 3’ II) 5´- AGCGAUCAUGACA – 3’ III) 5´- CACCGACAAACGAA – 3’ a) Indique razonadamente, en cada caso, si se trata de ADN ó ARN (1) b) ¿Son iguales las dos cadenas que componen la doble hélice del ADN? Razone la respuesta (3) c) Dado el siguiente fragmento de ADN 5´- CGATATAGCCGTTAA - 3´, escriba cuál será su ARN mensajero y la secuencia peptídica sintetizada a partir de él, señalando con claridad cual será el extremo N- y C-terminal del péptido producido (6) (se incluye el código genético en hoja aparte) 4. Si la hebra codificante de un oligonucleótido de DNA es la siguiente: 5’ – ATTAGCCGAATGATT – 3’ a) b) c) d)
Escriba la secuencia de la hebra molde del DNA. Escriba la secuencia del mRNA. ¿Cuántos aminoácidos codifica dicha hebra? Si AUG codifica Met; CGA Arg; AGC Ser; AUU Ile y UGA stop (finalización), escriba la secuencia del oligopéptido codificado por dicha hebra. e) Si se produce una mutación por delección del 10º nucleótido, ¿cuál sería la secuencia del oligopéptido formado?
EXPRESIÓN DEL MENSAJE GENÉTICO
ADN cadena con sentido
3´... T A C C G T A C G G C T T A T A T T ... 5´ 5´... A T G G C A T G C C G A A T A T A A ... 3´ TRANSCRIPCIÓN
ARN 5´ ... A U G G C A U G C C G A A U A U A A ... 3´ codón inicial
CODONES
codón sin sentido
TRADUCCIÓN
PÉPTIDO NH2 -
Met - Ala - Cys - Arg - Ile - COOH
BLOQUE IV MICROORGANISMOS, INMUNOLOGÍA Y SUS APLICACIONES
TEMA 6. MICROBIOLOGÍA Y BIOTECNOLOGÍA TEMA 7. INMUNOLOGÍA TEMA 3. LAS NUEVAS TECNOLOGÍAS EN LA INVESTIGACIÓN DEL MEDIO AMBIENTE
TEMA 6. MICROBIOLOGÍA y BIOTECNOLOGÍA 1. CONCEPTO y PROPIEDADES DE LOS MICROORGANISMOS 2. ORIGEN y CLASIFICACIÓN DE LOS MICROORGANISMOS 3. VIRUS Estructura y clasificación de los virus Ciclos vitales 4. BACTERIAS Arqueobacterias Bacterias verdaderas (eubacterias) Morfología bacteriana Reproducción y genética bacteriana 5. MICROORGANISMOS EUCARIOTAS Algas microscópicas Hongos microscópicos Protozoos 6. BIOTECNOLOGÍA o MICROBIOLOGÍA INDUSTRIAL Aplicaciones de la biotecnología: Industrias alimentarias Industrias químicas Industria farmaceútica y medicina Agricultura Medio ambiente Minería
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
1
1. CONCEPTO Y PROPIEDADES DE LOS MICROORGANISMOS Los microorganismos son un conjunto de seres vivos de gran sencillez estructural y organizativa y que, debido a su reducido tamaño, sólo son visibles al microscopio. En cuanto a su diversidad, caben apuntes que dentro de los microorganismos encontramos toda gama de tipos nutricionales (vistos en el tema 4) y están representados cinco grupos de seres vivos: virus, bacterias, protozoos, hongos y algas, cuyas principales características figuran en esta tabla. Organización
Tamaño
Carácter distintivo
Grupo
Acelular
0,1 µm
Parásitos obligados
Virus
Procariota
10 µm
Anaerobios (la gran mayoría)
Arqueobacterias
Aerobios y anaerobios
Eubacterias
Eucariotas
>250 µm
Con pared celular
Algas
Con clorofila, autótrofos Sin clorofila, heterótrofos
Sin pared celular, heterótrofos
Hongos Protozoos
A pesar de esta variedad hay algunas características derivadas de su pequeño tamaño, comunes a la mayoría: a) Rápido intercambio de sustancias con el medio externo, dado que la disminución del tamaño celular supone un aumento en la relación superficie/volumen. b) Metabolismo muy rápido, pues los compartimentos celulares están muy próximos a los metebolitos y a los nutrientes. Por ello pueden alterar rápidamente el medio en el que viven, agotando los nutrientes e inundándolo de residuos. Esta propiedad la utiliza la industria biotecnológica, que se aprovecha de los microorganismos para la fabricación de diferentes productos (derivados lácteos, antibióticos, licores,...). c) Rápida multiplicación, basada en su eficaz metabolismo. Esta propiedad les otorga a los microorganismos patógenos una gran capacidad invasora.
2. ORIGEN y CLASIFICACIÓN DE LOS MICROORGANISMOS Los microorganismos son seres vivos muy poco evolucionados, de manera que fueron los primeros seres vivos en aparecer en el planeta, tanto es así que durante más de 2.000 millones de años han sido los únicos seres que poblaban en planeta. A partir de estudios de ARN, se ha establecido que el origen de los microorganismos actuales deriva de tres líneas evolutivas que derivaron de un ancestro común (progenote) : Línea Bacteria: que dio lugar a las bacterias y cianobacterias. Línea Archaea: que dio lugar a las arqueobacterias. Línea Eukarya: que originó protozoos, hongos, y algas unicelulares. A partir de esta línea evolutiva evolucionaron el resto de seres vivos actuales. La enorme cantidad de microorganismos ha hecho necesaria una clasificación. De los cinco reinos en que se clasifican a los seres vivos (Whittaker, 1969), los microorganismos se hallan en tres: Reino Monera: engloba a organismos unicelulares y procariotas. Dentro de este grupo se encuentran las ARQUEOBACTERIAS, y EUBACTERIAS o BACTERIAS verdaderas. Reino Protista: engloba a organismos unicelulares y pluricelulares sencillos. Incluye las ALGAS MICROSCÓPICAS y PROTOZOOS. Reino de los Hongos: Engloba organismos unicelulares y pluricelulares, heterótrofos y descomponedores de materia orgánica. En este reino se incluyen los HONGOS FILAMENTOSOS (Mohos) y las LEVADURAS.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
2
Además de todos estos seres vivos, un grupo aparte, dentro de los microorganismos lo constituyen los VIRUS, que son organismos acelulares, que aunque carecen de metabolismo y son parásitos obligados, su importancia como agentes transmisores de enfermedades hace que tienda a estudiárselos como microorganismos. Otras formas acelulares descubiertas en los últimos años son los viroides y priones, estos últimos causantes de la enfermedad de las vacas locas.
3. VIRUS Los virus son organismos sin estructura celular, carecen de metabolismo propio y para multiplicarse necesitan obligatoriamente parasitar un organismo. Su estructura es muy sencilla, presentan un ácido nucleico (genoma vírico), rodeado de una cubierta de proteínas (cápsida) y en algunos casos una envoltura membranosa. Son capaces de adherirse a la superficie de las células, introduciendo en ellas su genoma, y utilizarlas para multiplicarse y generar las envolturas de nuevos virus, utilizando para ello la materia, energía y el sistema enzimático de la célula que parasita, son por tanto, parásitos intracelulares obligados. En general, los virus se caracterizan por su pequeño tamaño (entre 0,02 y 0,03 m de diámetro) y su simplicidad estructural. Estructura de los virus Una partícula vírica o virión está formado por un fragmento de ácido nucleico (genoma vírico) encerrado en una cubierta proteíca o cápsida. Algunos virus presentan además, una envoltura membranosa procedente de la célula hospedadora. Estos virus se denominan virus con envoltura, en contraposición a los virus desnudos, que carecen de ella. Genoma vírico. Contienen un ácido nucleico, ADN en unos casos o ARN en otros, pero nunca los dos a la vez. Este ácido nucleico puede ser lineal, circular, simple o doble. Debido a su pequeño tamaño, evidentemente contienen muy pocos genes. Cápsida. Es una cubierta de proteínas que envuelve al virus. Le sirve de protección al ácido nucleico, y en aquellos que carecen de envoltura membranosa, es la que reconoce a las células que parasita. Las proteínas de la cápsida se denominan capsómeros, y se disponen de forma regular, dando lugar a diferentes tipos de cápsidas: icosaédricas (virus de la polio, hepatitis), helicoidales (virus de la rabia o del mosaico del tabaco) y complejas. Estas últimas son típicas de virus parásitos de bacterias, llamados BACTERIÓFAGOS, y constan de una cabeza y una cola. Envoltura membranosa. Algunos virus presentan una envoltura que rodea a la cápsida, que consta de una doble capa de fosfolípidos y glucoproteínas. Suelen proceder de las células que parasitan. Ejemplos son el virus de la hepatitis, gripe, viruela y el virus del SIDA.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
3
Clasificación a) b) c) d)
Los virus se pueden clasificar según varios criterios: Por la célula que parasitan: virus animales, vegetales o bacteriófagos. Por su forma: helicoidales, poliédricos o complejos. Por tener o no envoltura: virus envueltos o desnudos. Por su ácido nucleico: ADNmc; ADNbc; ARNmc o ARNbc.
CICLO DE LOS VIRUS Aunque los virus no se nutren, ni se relacionan, ya que an con las células de forma fortuita, presentan interesantes mecanismos que les permiten reproducirse dentro de la célula huésped. Los virus realizan las siguientes fases en su ciclo de multiplicación: a) Entrada en el citoplasma de la célula huésped. b) Reproducción de las partículas víricas (viriones). c) Salida de los virus al exterior de la célula infectada. Presentan una característica muy peculiar en su reproducción: la síntesis de cada uno de sus componentes se da por separado y, posteriormente, se produce el ensamblaje entre ellos. Su ciclo vital se ha podido descifrar, gracias al estudio de los bacteriófagos (o fagos), que parasitan a las bacterias, descubriéndose que pueden seguir dos tipos de ciclos, en unos casos se multiplican rápidamente dentro de las células (ciclo lítico) y las destruyen y en otros permanecen un tiempo dentro de ellas de forma latente (ciclo lisogénico).
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
4
Ciclo de un bacteriófago 1) Fase de fijación o adsorción: el virus se une a un receptor específico situado sobre la cubierta de la cápsula de la bacteria. 2) Fase de penetración: es esta fase, únicamente es inyectado el ácido nucleico del virus (ADN) en el interior de la bacteria. A partir de este momento pueden seguir dos ciclos diferentes: a) Ciclo lítico: el ADN del virus utiliza la maquinaria de la bacteria para multiplicarse, fabricar múltiples moléculas ARNm y a partir de estos fabricar las proteínas de la cápsida. Cuando se han sintetizado cantidades suficientes, comienza el ensamblaje de las partículas víricas, de tal forma que el ácido nucleico se rodea de las proteínas de la cápsida y la bacteria se lisa, liberando gran cantidad de bacteriófagos. b) Ciclo lisogénico: este caso, los virus una vez que infectan a la célula, en vez de destruirla, incorporan su ADN al ADN de la célula, de tal forma que no expresa sus genes y se replica junto al de la bacteria, permaneciendo en estado de vida latente. Cuando están en este estado, se les denomina virus atenuados o profagos. Pueden permanecer de esta forma varias generaciones de la célula huésped, de forma que las nuevas células hijas también estarán infectadas, hasta que se produzca un estímulo que haga que el profago se convierta en un virus activo, y se múltiple en el interior de la célula igual que en el ciclo lítico, hasta destruirla. Mientras la célula está infectada, y posea el ADN profago, será inmune frente a infecciones de otros virus del mismo tipo.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
5
4. MICROORGANISMOS PROCARIOTAS: ARQUEOBACTERIAS y BACTERIAS (EUBACTERIAS o BACTERIAS VERDADERAS). ARQUEOBACTERIAS
Es el grupo más antiguo de bacterias. Presentan una membrana plasmática cuyos lípidos carecen de ácidos grasos. Las paredes celulares carecen de peptidoglucanos. Su genoma está formado por una sola molécula de ADN circular, más pequeña que la de las eubacterias. Hay especies autótrofas, aunque la mayoría son heterótrofas. Son capaces de vivir en ambientes de condiciones extremas de temperatura, salinidad, pH y anaerobiosis. Dependiendo de las mismas, a las que han adaptado su metabolismo, se distinguen tres grupos: ▪ Halofíticas: en ambientes de elevada salinidad. ▪ Metanógenas: anaerobias, en ambientes pantanosos y cenagosos. ▪ Hipertermófilas: de ambientes geotérmicos (volcánicos), incluso submarinos, donde las temperaturas superan los 80-100ºC. BACTERIAS
Actualmente se piensa que existen unas 2.000 especies, que pueblan todos los hábitats terrestres. Tienen un tamaño comprendido entre 1 y 10 micras. Su forma puede responder a cuatro tipos: bacilos (forma de bastón), cocos (forma esférica), espirilos (alargadas y enrolladas espiralmente) y vibrios (con forma de coma ortográfica), pudiendo agruparse en colonias de forma específica.
MORFOLOGÍA Y ESTRUCTURA BACTERIANA Desde el exterior al interior presentan las siguientes estructuras: 1. CÁPSULA Es una capa gruesa (100-400 A) que no está presente en todas las bacterias y sin estructura definida. Confiere a la bacteria resistencia a la desecación y al ataque por células fagocíticas, pudiendo servir también como elemento de fijación al sustrato.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
6
2. LA PARED BACTERIANA La pared celular es una cubierta rígida, de 50-100 A, adosada a la cara externa de la membrana plasmática, que rodea totalmente a la célula. Le da forma a la célula y resistencia a las fuertes presiones osmóticas de su interior. Composición y estructura de la pared Esta compuesta por peptidoglicano o mureína (polisacáridos unidos a cortas cadenas peptídicas). El peptidoglicano o mureína, común a todas las paredes celulares de eubacterias está formado por cadenas de polisacáridos de dos glúcidos: N-acetilglucosamina (NAG) y ácido N-acetilmurámico (NAM), unidos por enlaces (1 4); una corta cadena de cuatro aminoácidos se une, a su vez, a los restos de NAM. Se pueden establecer enlaces peptídicos entre los aminoácidos de cadenas de polisacáridos adyacentes.
Dentro de las eubacterias, se distinguen dos tipos de pared celular: Tipo grampositivo (Gram +): tienen paredes anchas, con numerosas capas de muerína reforzadas con ácido teicoico. Las Gram + se tiñen de color violeta en la tinción de Gram Tipo gramnegativo (Gram -): tienen la pared más estrecha, con una capa de mureína interna y una membrana lipídica externa, permeable gracias a canales de porina. Las bacterias Gram – se tiñen de color rosado con la tinción de Gram
Funciones de la pared celular Mantiene la forma de la célula y previene la lisis osmótica Regula el intercambio de sustancia con el medio externo Proporciona carga negativa a la superficie celular Posee componentes con capacidad antigénica
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
7
3. EL CITOPLASMA El citoplasma bacteriano está formado por una matriz gelatinosa, el protoplasma, con alto contenido en agua y de aspecto granuloso, que contiene proteínas y enzimas y alberga los ribosomas 70 S característicos de los procariotas, así como diversas inclusiones de naturaleza muy variada, según el tipo de bacterias.
4. EL NUCLEOIDE En la célula procariota, el material genético se encuentra en el nucleoide, zona de aspecto fibrilar situada en la región central del citoplasma, que no está protegida por una membrana nuclear. En las bacterias, el material genético esta constituido por: ▪ Un único cromosoma formado por ADN bicatenario, circular y superenrrollado. ▪ Uno o varios plásmidos,, pequeñas moléculas de ADN circular extracromosómico que se replican de forma independiente. Pueden unirse temporalmente al cromosoma bacteriano, en ese caso se llaman episomas. 6. APÉNDICES EXTERNOS Flagelos. Son prolongaciones finas cuya longitud es varias veces la bacteria, y que aparecen en un número que oscila entre 1 y 100. Intervienen en el movimiento bacteriano. Dependiendo de la situación de los flagelos las bacterias pueden ser: monotricas, lofotricas, anfitricas y peritricas. Pelos y fimbrias. Son filamentos huecos y tubulares formados por proteínas, y no intervienen en el movimiento. Las fimbrias con cortas y numerosas, mientras que los pelos son largos y suele haber uno o dos por bacteria. Las fimbrias les permiten a las bacterias fijarse al sustrato (actuarían como raíces) y los pelos participan en el intercambio de material genético entre bacterias (CONJUGACIÓN BACTERIANA). REPRODUCCIÓN y GENÉTICA BACTERIANA La reproducción de las bacterias es asexual, por lo que las bacterias hijas son idénticamente iguales a sus madres. Esto hace que en una colonia donde existen miles de ellas, todas sean clónicas. La reproducción se realiza mediante bipartición, a la que precede la duplicación del ADN. Una vez que el ADN se duplica se forma un tabique entre las dos moléculas de ADN, que divide a la bacteria en dos, separándose posteriormente las células hijas. Las bacterias poseen, además, unos mecanismos definidos como parasexuales, mediante los cuales intercambian información genética con otras bacterias, sean o no de su misma especie. Existen tres tipos de mecanismos parasexuales: a) Conjugación. Es un proceso por el cual una bacteria, considerada donadora, transmite ADN, a través de las fimbrias, a otra bacteria receptora. Las bacterias donadoras poseen pequeñas moléculas de ADN, los plásmidos, que pueden ser transmitidos durante la conjugación.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
8
Existen dos tipos de bacterias donadoras: ▪ Bacterias F+: poseen plásmidos (factores F) no integrados en el genoma bacteriano. Las bacterias F+ suelen transferir únicamente el plásmido a la bacteria receptora, denominada F - y que queda convertida en F+. ▪ Bacterias Hfr: poseen plásmidos integrados en el genoma bacteriano (se llaman episomas). Antes de la conjugación, duplican su ADN, incluido e factor F. Transfieren un fragmento de ADN a la bacteria receptora F-, que se recombina con su ADN y se transforma en Hfr.
b) Transducción. Es un fenómeno de intercambio genético que requiere un agente transmisor, que generalmente es un virus, el cual transporta fragmentos de ADN procedentes de la última bacteria parasitada.
c) Transformación. Es un proceso por el que una bacteria introduce en su interior fragmentos de ADN, que aparecen libres en el medio procedentes de la lisis de otras bacterias. Este mecanismo es el responsable de la transformación de cepas bacterianas no virulentas (cepas R) en virulentas (cepas S), cuando se cultivan en medios que contienen fragmentos de ADN procedentes de la cepa S destruida previamente (por ejemplo, por calor). Los mecanismos de intercambio genético explican la variabilidad que pueden presentar algunas bacterias al habitar junto a otras distintas. Un ejemplo de este proceso es la resistencia a antibióticos que presentan ciertas bacterias patógenas al convivir en el intestino con bacterias simbiontes que resisten bien la acción de estos productos farmaceúticos.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
9
5. MICROORGANISMOS EUCARIOTAS ALGAS MICROSCÓPICAS -Las algas son protoctistas, es decir unicelulares o pluricelulares, talofíticas (sin vascularizar), que carecen de tejidos y autótrofas fotosintéticas. -Las algas microscópicas son en su mayoría unicelulares, viven en medios acuáticos formando el fitoplacton. Realizan la mayor parte de la fotosíntesis de la Tierra siendo el primer eslabón de las cadenas tróficas de los ecosistemas acuáticos, liberando grandes cantidades de oxígeno a la atmósfera. -Todas tienen clorofila pero el color verde puede estar enmascarado por otros pigmentos que provocaran el color final y su hábitat. Pueden acumular los excedentes de su metabolismo tanto en forma de almidón como en otras sustancias de reserva. -Su pared celular es de celulosa, (las más sencillas carecen de pared celular), pero pueden tener también otras sustancias que modifican su aspecto. -Se reproducen tanto asexualmente como sexualmente, presentando todo tipo de ciclos biológicos. -Los principales grupos de algas microscópicas unicelulares son: Euglenófitos: Algas de agua dulce que carecen de pared celular. Se mueven mediante dos flagelos. Pueden enquistarse en casos de sequía. Diatomeas: Contienen fucoxantina, pigmento amarillo que les da su color típico. La pared celular está cubierta por dos piezas de sílice que encajan entre sí como una caja y su tapadera. Cuando se acumulan forman la tierra de diatomeas que, además de su interés paleontológico, se usa en la fabricación de pasta de dientes. Dinoflagelados: Son básicamente marinas, con una cubierta o teca muy consistente y de formas caprichosas. Suelen ser de color rojo, pudiendo producir toxinas que en grandes cantidades forman las mareas rojas, contaminantes de los criaderos de moluscos. Los otros grupos de algas, predominantemente pluricelulares, Clorófitos (algas verdes), Feófitos (algas pardas) y Rodófitos (algas rojas), también tiene representantes unicelulares. HONGOS MICROSCÓPICOS -El heterogéneo reino de los hongos agrupa a organismos eucariotas, con pared celular rígida formada por quitina y otros compuestos, pero sin celulosa, heterótrofos y con digestión externa que realizan mediante enzimas secretadas al medio. Tras esta digestión absorben los nutrientes. -Su ecología es muy diversa. Aunque hay representantes acuáticos, principalmente son terrestres. En función de cómo consiguen la materia orgánica que necesitan, encontramos: hongos parásitos, tanto de plantas como de animales causando enfermedades conocidas como micosis. Ejemplo son las tiñas, royas, el cornezuelo, pie de atleta, candidiasis, etc... hongos saprofitos, ocupan en los ecosistemas el nivel trófico de los descomponedores siendo responsables de la mineralización de los bioelementos. hongos simbióticos, con los algas formando los líquenes, o con raíces de plantas en las microrrizas. -En los hongos pluricelulares las células se disponen linealmente formando unos filamentos o hifas. Las hifas pueden formar un entramado conocido como micelio, que en los hongos macroscópicos se hace observable formando el cuerpo fructífero o seta. -Se reproducen por esporas, que pueden ser asexuales, formadas en el extremo de hifas especiales o conidios, o sexuales, con dos tipos, internas (ascosporas) y externas (basidiosporas). Según este criterio taxonómico se originan dos grupos de hongos, los Ascomicetos y Basidiomicetos. -Los principales hongos microscópicos son las levaduras y los mohos, sin valor taxonómico.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
10
Levaduras Son hongos unicelulares que se reproducen asexualmente por gemación. Pertenecen al grupo de los ascomicetos. Viven en medios ricos en azúcares. Tienen una gran importancia económica, pues las fermentaciones del vino, cerveza y pan las realizan levaduras del género Saccharomyces. El género Cándida es una levadura patógena. Mohos Reúne hongos microscópicos, pluricelulares filamentosos. El moho es una fina capa pulverulenta, de diverso color, que forman estos hongos sobre materia orgánica como pan, fruta, queso, carne etc.. Los antibióticos son producidos principalmente por mohos para impedir el desarrollo de las bacterias que competirían con ellos por los nutrientes del medio.
PROTOZOOS -Los protozoos son microorganismos eucariotas unicelulares heterótrofos sin pared celular. La mayoría son de vida libre en medios acuáticos o húmedos, aunque algunos se han adaptado al parasitismo, pudiendo producir enfermedades en el hombre. -Toman la materia orgánica en disolución por pinocitosis o en estado sólido por fagocitosis. Predominan las formas móviles, mediante cilios, flagelos o seudópodos. -Se reproducen asexualmente y sexualmente, normalmente por conjugación. Pueden originar estructuras muy resistentes, llamadas quistes, con las que sobreviven en condiciones adversas. -Hay unas 30.000 especies que se encuentran en todo tipo de las charcas y que se pueden agrupar en cuatro clases Grupo
Locomoción
Hábitat
Ejemplos
Flagelados
Flagelos
Aguas dulces
Tripanosoma, enfermedad del sueño
Sarcodinos
Pseudópodos
Aguas dulces y marinas
Amebas y Foraminíferos
Ciliados
Cilios
Aguas dulces y marinas
Paramecios. Tienen dos núcleos
Esporozoos
Por contracciones
Parásitos
Plasmodium causa la malaria
DIFERENCIAS ENTRE TIPOS DE MICROORGANISMOS – VIRUS: Formas acelulares, parásitos obligados, sin metabolismo propio. – BACTERIAS, PROTOZOOS, ALGAS MICROSCÓPICAS, LEVADURAS y MOHOS: Seres vivos celulares, con metabolismo propio
DIFERENCIAS
1) ORGANIZACIÓN CÉLULAR:
PROCARIOTA: BACTERIAS EUCARIOTA: PROTOZOOS, ALGAS, LEVADURAS, MOHOS
UNICELULARES: BACTERIAS, PROTOZOOS, ALGAS UNICELULARES, LEVADURAS PLURICELULARES: algunas CIANOBACTERIAS (filamentosas), ALGAS FILAMENTOSAS, MOHOS
2) PARED CELULAR
SIN PARED CELULAR: PROTOZOOS CON PARED CELULAR: – De PEPTIDOGLUCANOS: BACTERIAS (excepto ARQUEOBACTERIAS) – De CELULOSA: ALGAS – De QUITINA: MOHOS y LEVADURAS
3) METABOLISMO
AUTÓTROFO FOTOSINTÉTICO: – ALGAS – BACTERIAS FOTOSINTÉTICAS: CIANOBACTERIAS (Fotosíntesis oxigénica), BACTERIAS VERDES Y PURPÚREAS (Fotosíntesis anoxigénica).
HETERÓTROFO TÍPICO: – PROTOZOOS – LEVADURAS y MOHOS (Saprófitos) – BACTERIAS HETERÓTROFAS (Parásitas, Saprófitas y Simbiontes)
AUTÓTROFO QUIMICOSINTÉTICO: – BACTERIAS QUIMIOSINTÉTICAS o QUIMIOLITOTROFAS
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
11
6. BIOTECNOLOGÍA La Biotecnología es la aplicación de procedimientos científicos y técnicas a la transformación de ciertas materias por agentes biológicos para producir bienes y servicios. Estos agentes biológicos son esencialmente microorganismos, y en otros casos enzimas o células vegetales y animales. Los bienes y servicios tienen que ver con la agricultura, pesca, así como con las industrias alimentarias y farmacéutica. El empleo de diferentes microorganismos con fines industriales para la obtención de diferentes productos, por lo que recibe el nombre de biotecnología microbiana o microbiología industrial. La biotecnología microbiana tradicional utiliza los microorganismos tal y como se encuentran en la naturaleza, pero recientemente se están utilizando microorganismos alterados genéticamente mediante métodos de ingeniería genética. Los microorganismos utilizados en la biotecnología proceden de la naturaleza, pero se han seleccionado a partir de sus capacidades para producir determinados productos o con determinados fines. Lo primordial es que el microbio sea capaz de crecer rápidamente, resista al ser cultivado a gran escala y pueda producir la sustancia útil en una cantidad apreciable y en el menor tiempo posible. APLICACIONES DE LA BIOTECNOLOGÍA 1. INDUSTRIAS ALIMENTARIAS Obtención de productos por fermentación: algunos microorganismos no patógenos son muy interesantes al ser capaces de transformar ciertas sustancias en productos de gran importancia para el hombre, mediante procesos de fermentación. La mayoría de estas fermentaciones se producen en condiciones anaerobias, no obstante algunas se llevan a cabo de forma aerobia, tratándose más bien de respiraciones aerobias con oxidación incompleta. Las fermentaciones a escala industrial se llevan a cabo en fermentadores. Se trata de depósitos de diferente capacidad en los que existe un líquido que actúa como medio de cultivo del microorganismo. El medio de cultivo y los microbios industriales se mezclan mediante un sistema de palas y estos van transformando por fermentación sustratos de ese medio y originan los productos de interés. Ejemplos de fermentaciones son: Fermentación alcohólica: llevada a cabo por levaduras del género Saccharomyces. Se utiliza para la obtención de bebidas alcohólicas como el vino y la cerveza, y algunas bebidas destiladas (whisky, ron). Fermentación láctica: llevada a cabo por las bacterias de la leche, como Lactobacillus bulgaricus. Degradan la lactosa y producen ácido láctico. Este proceso se utiliza para la elaboración de productos derivados de la leche, como el queso, yogur, o requesón. También las sales de ácido láctico pueden tener algunos fines, como el tratamiento de anemias (lactato de hierro) y deficiencias de calcio (lactato de calcio) o por ejemplo los lactatos de socio empleados como sustancias plastificantes. 45 Fermentación acética: se trata de un proceso aerobio, por el que diferentes bacterias del género Acetobacter y Gluconobacter degradan el etanol a ácido acético. Se utiliza industrialmente para la obtención de vinagre, utilizando como sustrato vino o sidra. Producción de vitaminas, aminoácidos: algunas vitaminas que se añaden a los alimentos y que su síntesis química resulta complicada, se obtienen por procedimientos de biotecnología. Ejemplos son la vitamina B12 y la riboflavina. Muchos microorganismos pueden sintetizar aminoácidos a partir de compuestos nitrogenados en mayor cantidad de la que necesitan. Estos aminoácidos producidos industrialmente se utilizan como aditivos alimentarios, para potenciar el sabor, como edulcorantes o antioxidantes. Son ejemplos el ácido glutámico, lisina, metionina, alanina y glicina. Fabricación de proteínas para pienso: se utilizan bacterias y levaduras que son ricas en proteínas y que consuman medios de cultivo baratos.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
12
2. INDUSTRIAS QUÍMICAS Producción de enzimas: diversos hongos y bacterias producen enzimas en grandes cantidades que son utilizadas en panadería, pastelería, farmacia, medicina, lavandería y en la industria textil. Producción de disolventes, como acetona y butanol 3. INDUSTRIA FARMACÉUTICA y MEDICINA (SECTOR BIOMÉDICO) Producción de antibióticos: los antibióticos son productos de síntesis, fabricados por algunos microorganismos. Hasta el momento se conocen cerca de 800 antibióticos producidos por hongos del género Penicillium y bacterias de los géneros Bacillus y Streptomyces. La producción industrial de antibióticos ha crecido espectacularmente desde los años 50 debido al descubrimiento de especies con mayor capacidad de producción, mejora de medios de cultivo y de extracción del antibiótico de la mezcla del cultivo. La ingeniería genética ha hecho posible el aislamiento de genes de cepas productoras de antibióticos y su por tranformación bacteriana obtener microorganismos capaces de producirlos a escala industrial. Obtención de hormonas como la insulina y la hormona de crecimiento a partir de bacterias transformadas con los genes responsables de estas moléculas. Otros medicamentos: mediante técnicas de ingeniería genética, empleando microbios como productores se han obtenido eritropoyetina, interferón, factor VIII plaquetario,... Elaboración de vacunas y sueros Empleo de virus para tratamiento de enfermedades infecciosas. Utilización de virus como vectores para introducir genes mediante métodos de terapia génica. 4. AGRICULTURA Control de plagas: Algunos microorganimos han sido utilizados como bioinsecticidas para controlar algunas plagas. Infectan a los insectos en estado adulto o larvario y los matan o bien fabrican alguna sustancia tóxica. Se han utilizado algunos virus y ciertas especies de bacterias y hongos. 5. MEDIO AMBIENTE Depuración de aguas residuales: en las plantas depuradoras de aguas residuales, el tratamiento secundario permite eliminar sustancias orgánicas indeseables mediante diferentes microorganismos, que las oxidan produciendo como desecho CO2 y metano. Limpieza mareas negras: ciertas bacterias, levaduras y algas transformar los hidrocarburos en compuestos más solubles e inestables, que son atacados por otros microorganismos hasta dar como productos finales CO2 y H2O. 6. MINERÍA En el lavado de ciertos minerales se emplean bacterias, así como en la recuperación de escombros mineros.
APLICACIONES BIOTECNOLOGÍA 1. SECTOR ALIMENTARIO
Fabricación de PRODUCTOS FERMENTADOS: – Por FERMENTACIÓN ALCOHÓLICA (realizada por levaduras del gen. Saccharomyces): PAN, BEBIDAS ALCOHÓLICAS FERMENTADAS (vino, cerveza). – Por FERMENTACIÓN LÁCTICA (realizada por bacterias lácticas del gen. Lactobacillus): QUESOS, YOGURES, LECHES FERMENTADAS (tipo Bífidus o similares). – Por FERMENTACIÓN ACÉTICA (realizada por bacterias del gen. Acetobacter): VINAGRE.
Otros: proteínas para pienso animal, algunas vitaminas y algunos aminoácidos como aditivos.
2. SECTOR BIOMÉDICO
Fabricación de ANTIBIÓTICOS por Actinomicetos (Bacterias gram + aerobias) y mohos del genero Penicillium.
Fabricación de HORMONAS: insulina, hormona de crecimiento.
Fabricación de MEDICAMENTOS: Proteínas sanguíneas (factores plaquetarios, EPO), inmunomoduladores (interferón, interleucina).
Fabricación de VACUNAS y SUEROS (tratado en tema 7).
Técnicas de TERAPIA GÉNICA que empleen virus como vectores de transmisión de genes sanos en personas con enfermedades genéticas.
3. MEDIO AMBIENTE
DEPURACIÓN de AGUAS RESIDUALES LIMPIEZA MAREAS NEGRAS (Biorremediación) CONTROL de PLAGAS con BIOINSECTICIDAS
1
ESTUDIO Y CONTROL DE MICROORGANISMOS Medios de cultivo Un cultivo es un conjunto de células microbianas que crecen en un medio con nutrientes. Los medios pueden ser de dos tipos, según su estado:
Medios líquidos o caldos de cultivo. Se elaboran con varios nutrientes líquidos, los cuales se introducen en un tubo de ensayo o en un matraz Errlenmeyer, tapados con algodón. Se utilizan para controlar el crecimiento de las poblaciones. Medios sólidos. Se preparan mezclando una solución con varios nutrientes líquidos con un agente gelificante, como agar-agar.
Los medios pueden tener distintos componentes que favorezcan o inhiban el crecimiento de algunos microorganismos, pudiéndose diferenciar tres tipos:
Medios de enriquecimiento. Incluyen sustancias que permiten el crecimiento de algunos microorganismos sobre otros. Medios selectivos. Contienen una o más sustancias que inhiben el crecimiento de algunos microorganismos. Medios indicadores. Presentan un indicador que permite que ciertas colonias de un microorganismo se diferencien claramente de otras.
Crecimiento de un cultivo microbiano Para representar el crecimiento en un cultivo microbiano se utiliza el logaritmo en base diez del número de células para construir la curva de crecimiento del cultivo a lo largo del tiempo.
2
Control de microorganismos Los agentes que actúan contra los microorganismos pueden ser físicos o químicos, y según el efecto que produzcan pueden ser: Microbicidas: si los matan (bactericida en caso de bacterias). Microbiostáticos: si inhiben su crecimiento (bacteriostático en caso de bacterias).
Agentes físicos a) Esterilización. Es uno de los métodos más utilizados. Se basa en la exposición de los microorganismos a altas temperaturas durante cierto tiempo. Con ello se destruyen las cubiertas bacterianas o se inactivan las enzimas. Dependiendo de los tipos de calor, se diferencian:
Calor húmedo. Produce la desnaturalización y coagulación de las proteínas de los microorganismos. Se diferencia entre: Esterilización clásica. Consiste en un calentamiento a 120 ºC durante 30 minutos. Se utiliza para esterilizar latas y frascos de vidrio con conservas. Esterilización tipo UHT. Es un calentamiento a 140 ºC durante tres segundos. Mantiene mejor las vitaminas de los alimentos, pero no proporciona tanto tiempo de conservación. Calor seco. Produce la oxidación de los componentes celulares.
b) Pasteurización. Se utiliza para eliminar la mayoría de los microorganismos de los alimentos, sin que estos pierdan sus principales características de sabor o aroma. En la pasteurización de la leche se eleva rápidamente su temperatura a 71,7ºC durante quince a veinte segundos. c) Congelación. Es un tratamiento bacteriostático, que permite conservar los alimentos. d) Radiaciones electromagnéticas. Pueden ser: Radiaciones ionizantes. Rayos X o rayos gamma que ionizan las moléculas orgánicas, como el ADN y las proteínas, modificando su composición. Radiaciones no ionizantes. Las radiaciones UV que provocan mutaciones en el ADN o alteran o inhiben su duplicación. d) Filtración. Se utilizan filtros de microporos para retener los microorganismos presentes en el aire o en líquidos.
Agentes químicos a) Esterilizantes. Destruyen toda forma de vida microbiana de las superficies que son tratadas. Se utiliza el formaldehído o glutaraldehído. b) Desinfectantes. Eliminan los microorganismos que producen enfermedades infecciosas, pero no las esporas microbianas. Se utilizan como desinfectantes la lejía (hipoclorito sódico), fenoles, sulfato de cobre, etc. c) Antisépticos. Se utilizan contra microorganismos presentes en heridas, como el alcohol al 70%, la solución de yodo, agua oxigenada, el jabón o los detergentes. d) Agentes quimioterapeúticos. Atacan a los microorganismos causantes de la enfermedad sin dañar las células del hospedador. Se pueden diferenciar dos tipos: Antibióticos. Son de origen natural, ya que son producidos por bacterias del grupo actinomicetales u ciertos hongos filamentosos. Se utilizan para el tratamiento de enfermedades infecciosas. (desarrollado en hoja aparte). Agentes quimioterapeúticos sintéticos, como las sulfamidas que inhiben el crecimiento bacteriano, el AZT que disminuye los efectos infecciosos del virus del SIDA, o la cloroquina que se utiliza contra la malaria.
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
1
TEMA 6. MICROBIOLOGÍA y BIOTECNOLOGÍA CUESTIONES DE SELECTIVIDAD Cuestiones sobre clasificación y diversidad de microorganismos. 1. Mencione los grandes grupos de microorganismos e indique sus principales características diferenciales relativas a la organización y al modo de obtener energía. 2. Diga si las siguientes afirmaciones son verdaderas o falsas, justificando la respuesta: a) En la estructura celular de un virus se encuentran siempre presentes: ácidos nucleicos, proteínas y lípidos. b) Las bacterias tienen mitocondrias y carecen de cloroplastos. c) Las levaduras son organismos procariotas autótrofos. d) Los protozoos y las cianobacterias son organismos procariotas heterótrofos. e) Las bacterias obtienen materia y energía por diferentes mecanismos. 3. Indique si las afirmaciones siguientes son verdaderas o falsas, justificando la respuesta: a) Las bacterias son responsables de la transformación de la materia orgánica de los cadáveres en materia mineral. b) Las levaduras son hongos de organización procariota que producen fermentación alcohólica. c) Los virus son capaces de parasitar a los seres vivos, pero existen también formas de vida libre. d) Las algas microscópicas, al igual que los mohos, son microorganismos autótrofos y fotosintéticos. e) Los estreptococos son bacterias esféricas que forman cadenas. 4. ¿Cuáles son los principales grupos de microorganismos eucariotas?. Indique las principales diferencias entre ellos. 5. ¿Qué grupos principales de microorganismos conoce?. ¿Cuáles son principales características? 6. Explique las diferencias estructurales y funcionales que conozca entre virus y bacterias. 7. Indique las principales diferencias entre las algas eucariotas microscópicas y los hongos filamentosos microscópicos. 8. Enumere y explique brevemente las diferencias más importantes entre Cianobacterias y Protozoos. 9. Indique los principales mecanismos de nutrición bacteriana. Cuestiones sobre virus 10. Explique el ciclo lítico de un bacteriófago 11. Indique los diferentes tipos de ácidos nucleicos que contienen los virus y explique esquemáticamente su modo de replicación. 12. Explique el ciclo vital de un retrovirus
Biología 2º Bachillerato. Tema 6. MICROBIOLOGÍA y BIOTECNOLOGÍA
2
13. Respecto a los virus y, utilizando dibujos esquemáticos: a) Describa el ciclo lítico de un bacteriófago. b) Describa un ciclo lisogénico. c) Indique las diferencias entre uno y otro. 14. En un laboratorio se obtuvo un bacteriófago que tiene la cápside del fago T2 y el ADN del fago T4. Con el bacteriófago obtenido en dicho laboratorio se infecta una bacteria. Conteste a las siguientes preguntas, razonando la respuesta: a) ¿Los fagos descendientes tendrán la cápside de T2 o de T4?. b) ¿Los fagos descendientes tendrán el ADN de T2 o de T4?. Cuestiones sobre Biotecnología y técnicas en microbiología 15. Explique una aplicación de la ingeniería genética a la industria farmacéutica, biomédica o alimentaria. 16. ¿Qué es la Biotecnología?. ¿Qué es un organismo transgénico?. Cite tres ejemplos de aplicación de la Biotecnología. 17. ¿Cuáles son los grupos de microorganismos de interés industrial?. ¿En qué condiciones pueden actuar?. Cite una aplicación industrial de estos microorganismos. 18. Explique el concepto de Biotecnología. Describa una aplicación de la biotecnología a un sector industrial alimentario. 19. Explique que es un antibiótico. ¿Qué tipo de organismos lo producen?. Describa brevemente un proceso tecnológico de producción de antibióticos. 20. Enumere las técnicas que conozca utilizadas para el estudio y la identificación de los microorganismos y explique una de ellas.
TEMA 7. INMUNOLOGÍA 1. MECANISMOS DE DEFENSA 2. EL SISTEMA INMUNITARIO. LOS ÓRGANOS LINFOIDES. LINFOCITOS y MACRÓFAGOS 3. ANTÍGENOS y ANTICUERPOS. REACCIÓN ANTÍGENO-ANTICUERPO 4. RESPUESTAS INMUNITARIAS
Respuesta inmune humoral y celular Respuesta inmune primaria y secundaria
5. INMUNIDAD. VACUNAS y SUEROS 6. ALTERACIONES DEL SISTEMA INMUNE
Alergia o Hipersensibilidad Anafilaxia Autoinmunidad Rechazo Cáncer Inmunodeficiencias: SIDA
Biología 2º Bachillerato Tema 7. Inmunología
1
1. MECANISMOS DE DEFENSA Los mecanismos de defensa son sistemas que han desarrollado los animales y el hombre frente a la invasión de microorganismos patógenos o sustancias extrañas. Pueden ser: ▪ Inespecíficos: impiden la entrada de cualquier gérmen o lo destruyen rápìdamente. La respuesta defensiva es la misma independientemente del tipo de gérmen. Existen tres barreras defensivas inespecíficas: piel y mucosas, microflora normal del organismo y la respuesta inflamatoria.
▪
Específicos: en este caso la respuesta defensiva es específica contra cada tipo de gérmen. Es llevada a cabo por el sistema inmunitario y se la conoce como respuesta inmunitaria.
2. EL SISTEMA INMUNITARIO. LOS ÓRGANOS LINFOIDES. LINFOCITOS y MACRÓFAGOS El Sistema inmunitario es el formado por todo el conjunto de órganos linfoides, que son los encargados de la formación, maduración y acumulación de los linfocitos. Los linfocitos se originan por diferenciación de células madre de la médula ósea y se transforman en uno u otro tipo según el lugar donde maduren. Así, los órganos linfoides se clasifican en: Órganos linfoides primarios: donde maduran los linfocitos. Son el timo, que produce linfocitos T y la médula ósea, que produce linfocitos B. Órganos linfoides secundarios: donde se acumulan los linfocitos que circulan por la sangre y por la linfa. Son los ganglios linfáticos, el bazo, amígdalas, apéndice, placas de Peyer y adenoides. El sistema inmunitario es el responsable de la respuesta inmunitaria, en la que participan dos tipos de células, los linfocitos y macrógafos y los anticuerpos.
Biología 2º Bachillerato Tema 7. Inmunología
2
Linfocitos: son un tipo de glóbulos blancos que presentan un gran núcleo redondeado. Reconocen a los gérmenes, gracias a la presencia de receptores de antígenos en sus membranas, y los atacan. Existen dos tipos: ▪ Linfocitos B: son los que fabrican los anticuerpos. Reconocen a los gérmenes extraños y se transforman en un tipo de células, denominadas células plasmáticas, que producen anticuerpos específicos contra el gérmen. Responsables de la respuesta inmune humoral.
▪
Linfocitos T: no producen anticuerpos. Responsables de la respuesta inmune celular. Existen diferentes tipos (Linfocitos CD4 o colaboradores, Linfocitos CD8 o citotóxicos, Linfocitos T supresores, Linfocitos T destructores), cada uno de los cuales interviene de forma distinta en la respuesta inmune, como veremos más adelante.
Macrófagos: células de gran tamaño que se desplazan con movimiento ameboide entre las células de los tejidos fagocitando a los microorganismos. Además, alertan al sistema inmunitario de la presencia de gérmenes o sustancias extrañas, al exponer moléculas de los gérmenes fagocitados o fragmentos de éstas en su superficie, presentando así el antígeno a los linfocitos para su reconocimiento.
La respuesta inmune es la respuesta específica que lleva a cabo el sistema inmunológico ante la presencia de gérmenes o moléculas extrañas. Puede ser de dos tipos: ▪ Respuesta inmune HUMORAL (mediada por anticuerpos): los linfocitos B fabrican anticuerpos específicos contra el agente infeccioso. ▪ Respuesta inmune CELULAR (mediada por células): los linfocitos T y los macrófagos destruyen al agente infeccioso.
Biología 2º Bachillerato Tema 7. Inmunología
3
3. ANTÍGENOS Y ANTICUERPOS. REACCIÓN ANTÍGENO-ANTICUERPO. Antígeno: toda sustancia extraña capaz de inducir en el organismo una respuesta inmunitaria, que provoca la formación de anticuerpos para destruirlos. En resumen los antígenos, son sustancias con las siguientes características: Son exógenas, es decir, extraños al organismo. Son de naturaleza química muy variada (proteínas, polisacáridos, lipoproteínas,...). Se localizan en la superficie de un agente patógeno o son producidas y liberadas por este. Son inmunológicas, es decir, capaces de inducir la formación de anticuerpos. Presentan una zona, denominada determinante antigénico o epítopo, que se une de forma específica al anticuerpo. Los epítopos son los responsables de la especificidad del antígeno por el anticuerpo. Cada antígeno puede poseer varios epítopos (antígenos polivalentes), que provocan la formación de anticuerpos distintos.
Anticuerpos: son las sustancias que fabrica el sistema inmunológico ante la presencia de un antígeno. Tienen naturaleza de glucoproteína. Están formados por cuatro cadenas polipeptídicas, dos ligeras (L) y dos pesadas (H). En cada anticuerpo existe una región variable que es la que se une al antígeno, y otra región constante, común a muchos anticuerpos.
Reacción antígeno-anticuerpo Es la unión del anticuerpo con el antígeno. Se produce mediante enlaces débiles (nunca covalentes). Es una unión tremendamente específica, cada anticuerpo es capaz de reconocer entre miles de antígenos, aquel que le es complementario. Existen cuatro formas de reacción antígeno-anticuerpo: ▪ Neutralización: el anticuerpo al unirse al antígeno lo anula y pierde su capacidad infectiva. ▪ Aglutinación: los anticuerpos se unen a los antígenos presentes en la superficie de gérmenes y forman agregados que precipitan fácilmente. ▪ Precipitación: parecido a lo anterior, pero en este caso se trata de antígenos solubles en agua (no unidos a la superficie bacteriana) ▪ Opsonización: los anticuerpo se unen a la superficie de los gérmenes (gérmenes opsonizados) y se facilita que sean fagocitados.
Biología 2º Bachillerato Tema 7. Inmunología
4
4. RESPUESTAS INMUNITARIAS Respuesta humoral También se conoce como “inmunidad mediada por anticuerpos”, ya que básicamente consiste en la síntesis de anticuerpos por los linfocitos B. Cuando un antígeno penetra en el organismo, acaba encontrando un linfocito B que posee el anticuerpo específico capaz de reaccionar con él. La unión del linfocito al antígeno estimula la división de los linfocitos y su diferenciación en dos tipos de células: Células plasmáticas: se consideran linfocitos B maduros y poseen un extenso RER, donde fabrican y exportan gran cantidad de anticuerpos (más de 10 millones de moléculas por hora). Estas células no salen de los órganos linfoides, sino que lo hacen los anticuerpos y viajan por la sangre hasta la zona infectada. Células de memoria: algunos linfocitos B se convierten en células de memoria, que permanecen en la sangre fabricando anticuerpos específicos, como si guardaran el recuerdo del antígeno, y ante una segunda infección se multiplican generando células plasmáticas que producen grandes cantidades de anticuerpos que acaban más rápidamente con el antígeno extraño. Respuesta celular También se conoce como “inmunidad mediada por células”, y se basa en la actividad de los linfocitos T y los macrófagos. Cuando un antígeno invade el organismo, los macrófagos lo fagocitan y digieren en pequeños péptidos. Los macrófagos fabrican el complejo proteíco MCH (complejo principal de histocompatibilidad) que reconoce los fragmentos del antígeno y los transporta hasta la superficie del macrófago, permaneciendo allí hasta que son reconocidos por un linfocito T. Al reconocerlos, el linfocito T se activa y se divide, diferenciándose en distintos tipos de linfocitos T que salen de los nódulos linfáticos y se dirigen a la zona afectada. Los diferentes tipos de linfocitos T son los siguientes: Linfocitos T CD4 o Cooperadores: colaboran con los linfocitos B en el reconocimiento de antígenos específicos. Linfocitos T CD8 o Citotóxicos: se unen a células que poseen antígenos extraños en su superficie y las destruyen. Linfocitos T Supresores: inducen el cese de la actividad de los linfocitos B, y por lo tanto, se interrumpe la producción de anticuerpos. Linfocitos T memoria: son linfocitos T activados que permanecen en el tejido linfático como células de memoria y que continúan dividiéndose durante años.
Biología 2º Bachillerato Tema 7. Inmunología
5
Respuestas inmune primaria y secundaria Respuesta inmune primaria: es la respuesta inmunitaria tras un primer o con el antígeno. El sistema inmune tarda tiempo en identificar el antígeno (periodo de latencia) y posteriormente empieza a fabricar anticuerpos. Respuesta inmune secundaria: es la respuesta inmunitaria ante un segundo o con el antígeno. Como el sistema inmunológico lo ha memorizado, la respuesta es más rápida, se tarda menos en fabricar anticuerpos y se producen más rápidamente. A esta capacidad de respuesta inmunológica a un antígeno, más rápida y eficaz, tras un primer o con él se la conoce como memoria inmunológica. Las vacunas aprovechan esta propiedad, al estimular al organismo a que produzca anticuerpos y células memoria. 5. INMUNIDAD. VACUNAS y SUEROS Inmunidad es la capacidad de un individuo para ser invulnerable a una enfermedad infecciosa. Se puede adquirir de forma natural, al haber contraído antes la enfermedad o durante el desarrollo embrionario y la lactancia (a través de la placenta y de la leche materna una mujer transmite anticuerpos al hijo) quedando protegido el recién nacido durante algunos meses. Otra manera de adquirir inmunidad es de forma artificial mediante: Sueros o antisueros: soluciones que contienen anticuerpos específicos (inmonoglobulinas) contra determinada enfermedad. Sus efectos son inmediatos, pero no duraderos (hasta que el organismo consuma los anticuerpos inyectados) Vacunas: soluciones que contienen gérmenes muertos o debilitados. La vacunación es una medida preventiva que persigue que el propio organismo fabrique anticuerpos y células memoria contra una determinada enfermedad, de manera que ante una posible infección la respuesta inmunitaria sea rápida y eficaz.
Biología 2º Bachillerato Tema 7. Inmunología
6
6. ALTERACIONES DEL SISTEMA INMUNE Alergia o hipersensibilidad: es una reacción inmunitaria perjudicial para el organismo, ya que el sistema defensivo reacciona de forma excesiva ante sustancias extrañas inocuas o poco peligrosas. En los procesos alérgicos a los antígenos se les denomina alérgenos, se producen un tipo de anticuerpos especiales (IgE) que se unen a la superficie de unas células denominadas mastocitos. Cuando se produce un segundo o con el alérgeno, los mastocitos segregan histamina y otras sustancias que dilatan y aumentan la permebalidad de los capilares sanguíneos provocando un enrojecimiento e hinchazón de la zona o estimulan la mucosidad. De ahí que para tratar ciertas alergias se empleen antihistamínicos.
Anafilaxia: es un proceso alérgico que afecta a todo el organismo debido a que el alérgeno se introduce en el sistema sanguíneo, llegando incluso a producir la muerte. Ejemplos claros son las personas sensibles a la penicilina o a la picadura de abejas. Autoinmunidad: es un proceso en el que el propio sistema inmunológico ataca determinados órganos o tejidos del cuerpo. Provoca una serie de infermedades denominadas genéricamente enfermedades autoinmunes (anemia perniciosa, diabetes mellitus insulinodependiente, artritis reumatoide, esclerosis múltiple,...).
Rechazo: casos en que el sistema inmunitario reconoce como extraño un órgano o tejido implantado y reacciona destruyéndolo. Esto es debido a que todos nuestros tejidos presentan en la superficie de las células sustancias que actúan como antígenos (antígenos de histocompatibilidad o HLA) que son diferentes en cada uno de nosotros. Por eso a la hora de realizar transplantes hay que hacer un estudio previo de los tejidos del donante y receptor (Test de histocompatibilidad) para conocer las probabilidades de éxito.
Biología 2º Bachillerato Tema 7. Inmunología
7
Cáncer: enfermedad que consiste en la aparición tumores malignos, formados por células cancerígenas, que se dividen sin control y destruyen los tejidos sanos. Cada tumor es una masa de células cancerígenas. Si algunas de esas células se desprenden del tumor y pasan al torrente circulatorio invaden otras zonas, es lo que denominamos metástasis, provocando que la enfermedad se extienda a otras zonas del cuerpo. El sistema inmunitario nos protege de la aparición de tumores, ya que las células cancerígenas presentan antígenos especiales en su superficie que pueden ser detectados como extraños y ser así atacadas por los linfocitos, de ahí que una de las terapias más modernas en la lucha contra el cáncer sea la inmunoterapia, que se basa en potenciar las propias defensas del paciente. Inmunodeficiencia: enfermedad que afecta al sistema inmunitario debilitándolo. Como ejemplo significativo está el SIDA. SIDA (Síndrome de Inmunodeficiencia Adquirida): enfermedad producida por un virus (VIH) que ataca fundamentalmente a los linfocitos CD4 (un tipo de linfocitos T). Algunos conceptos importantes en la enfermedad son: Seropositivo: persona que ha desarrollado anticuerpos anti VIH contra la enfermedad, por haber sido infectada. Puede transmitir la enfermedad. Portador del virus VIH: persona con el virus VIH en su organismo, pero que no ha desarrollado la enfermedad. Puede transmitir la enfermedad. Enfermo o caso de SIDA: persona que sufre la enfermedad y por lo tanto la puede transmitir. Microorganismos oportunistas: gérmenes presentes en el organismo o en el ambiente que aprovechan la oportunidad de que el sistema inmunitario está debilitado para infectar y dañar órganos, que en condiciones normales no podrían. Provocan infecciones oportunistas que acaban con la vida del enfermo, como meningitis, tuberculosis, candidiasis, micosis cutáneas, herpes,... Carga viral: cantidad de virus VIH que circula por la sangre. Se utiliza para controlar la enfermedad. AZT: medicamento para tratar el SIDA que impide su multiplicación al inhibir la transcriptasa inversa. Vías de transmisión: vía sanguínea y sexual, debido a relaciones sexuales, compartir jeringuillas u objetos cortantes infectados, transmisión madre-hijo. CICLO VIH
El VIH comienza su infección de una célula huésped susceptible mediante su unión a los receptores CD4 de la célula huésped. Los receptores CD4 están presentes en la superficie de muchos linfocitos, células que constituyen una parte crítica del sistema inmunológico del organismo. Algunos datos recientes indican que para que el VIH entre en la célula es necesario un correceptor. Este conocimiento del correceptor del VIH y los progresos llevados a cabo en los mecanismos de fusión del VIH con la célula han abierto nuevas posibilidades para el desarrollo de fármacos antivirales. En la actualidad se están diseñando diferentes fármacos nuevos que pretenden prevenir la infección mediante el bloqueo de la fusión del VIH con su célula huésped. Después de la fusión del virus con la célula huésped, el VIH entra en la célula. El material genético del virus, que está formado por ARN, se libera y sufre una transcripción inversa hasta ADN. Para catalizar esta conversión del virus del ARN a ADN es preciso que entre en funcionamiento una enzima del VIH, denominada transcriptasa inversa. Los inhibidores de la transcriptasa inversa, como AZT, han sido los primeros medicamentos anti-VIH y todavía desempeñan una función fundamental en el tratamiento de los pacientes VIH+. Los inhibidores de la transcriptasa inversa se dividen, en función de su estructura y el mecanismo de inhibición de la enzima, en 2 clases: inhibidores análogos nucleósidos e inhibidores análogos no nucleósidos de la transcriptasa inversa. Después del cambio del material genético del VIH en ADN, el ADN viral entra en el núcleo de la célula huésped donde puede integrarse en su material genético. Este proceso está catalizado por la enzima integrasa; actualmente se están estudiando los inhibidores de la integrasa como una nueva forma de bloquear la replicación del VIH. Después de que el ADN viral se haya integrado en el material genético del huésped, es posible que el VIH pueda persistir en un estado latente durante muchos años. Esta capacidad del VIH de permanecer de forma latente en ciertas células constituye la principal barrera para la erradicación o curación del VIH. Por dicho motivo, fundamentado en nuestros conocimientos, los pacientes deben seguir recibiendo tratamiento antiviral durante toda la vida.
8
Biología 2º Bachillerato Tema 7. Inmunología
La activación de las células huésped da la lugar a la transcripción del ADN viral en ARN mensajero (ARNm), que posteriormente se traduce en proteínas virales. El nuevo ARN viral forma el material genético de la siguiente generación de virus. El ARN viral y las proteínas virales se agrupan y forman en la membrana celular un virus nuevo. Dentro de las proteínas virales se encuentra la proteasa del VIH, que es necesaria para procesar otras proteínas del VIH hasta sus formas funcionales. Los inhibidores de la proteasa, uno de los tipos más potentes de fármacos antivirales, actúan bloqueando esta etapa crítica de la maduración. Después de su reunión en la superficie celular, el virus sale de la célula mediante gemación y se libera para infectar otra célula. A menos que el tratamiento interrumpa el ciclo de vida del VIH, esta infección se disemina por todo el organismo y origina la destrucción del sistema inmunológico. Los fármacos antivirales actuales, como los inhibidores de la transcriptasa inversa y los inhibidores de la proteasa, permiten controlar la infección. No obstante, deben conseguirse todavía muchos objetivos antes de poder pensar que la epidemia del SIDA está controlada. Un objetivo importante e inmediato es el diseño de nuevos fármacos más potentes, que sean más fáciles de tomar y que originen un número menor de efectos secundarios. Inhibidores de la transcriptasa inversa actualmente disponibles: zidovudina (AZT, ZDV); didanosina (ddI); zalcitabina (ddC); estavudina (d4T); lamivudina (3TC); abacavir (ABC) Inhibidores no nucleósidos de la transcriptasa inversa: nevirapina; efavirenz Inhibidores de la proteasa: indinavir; ritonavir; saquinavir; nelfinavir ESQUEMA CICLO VIH y TIPOS DE FÁRMACOS QUE INTERRUMPEN EL CICLO
Fármacos que inhiben la proteasa (indinavir; ritonavir; saquinavir; nelfiravir)
Fármacos que impiden la entrada del virus
Fármacos que inhiben la transcripción inversa (AZT;ddI;ddC;d4T;3ct; nevirapina;efavirenz...)
INMUNZACIÓN ACTIVA. VACUNACIÓN La inmunización activa se basa en la estimulación del propio sistema inmunológico, mediante el suministro de los antígenos necesarios para que el organismo pueda fabricar por sí mismo los anticuerpos contra ellos. La vacunación es una forma de inmunización activa, ya que estimula las defensas inmunitarias frente a determinados agentes patógenos o sustancias dañinas, sin desarrollar la enfermedad. La persona vacunada fabrica linfocitos de memoria que permiten producir una respuesta inmunitaria secundaria más rápida y mucho más intensa que la respuesta primaria.
Para que una vacuna pueda ser suministrada debe cumplir dos requisitos: Capacidad inmunogénica. Debe ser capaz de provocar una respuesta inmunitaria eficaz. Ser segura y no producir efectos secundarios.
Tipos de vacunas a) Atenuadas. Contienen microorganismos vivos, pero debilitados, que se reproducen en el individuo vacunado y originan una infección muy limitada. Los microorganismos atenuados se obtienen a partir de cepas virulentas que se cultivan en determinadas condiciones (como altas temperaturas) hasta que disminuye su virulencia. Son ejemplos la vacuna contra la poliomielitis, el sarampión y la rubéola. b) Inactivadas. Contienen microorganismos muertos, por lo que no se reproducen en el organismo y es preciso suministrar una dosis más alta para que la vacuna contenga los antígenos suficientes. Con frecuencia se necesitan dosis de recuerdo para estimular a los linfocitos B de memoria. Son ejemplos la vacuna contra la rabia, tos ferina y difteria. c) Acelulares. Cuando no contienen células completas, solo partes o productos de los microorganismos. Pueden ser:
Toxoides: si contienen toxinas alteradas por calor o agentes químicos, que conservan su capacidad inmunogénica, y se emplean en la inmunización de gérmenes que fabrican potentes toxinas, como por ejemplo la vacuna del tétanos.
Antígenos aislados: contienen solo antígenos del microorganismo, por lo que no provocan reacciones adversas. Se fabrican gracias a las técnicas de biotecnología, como la vacuna de la hepatitis B, meningitis meningocócica, virus del papiloma humano o la vacuna contra la malaria.
Biología 2º Bachillerato
Tema 7. Inmunología
1
ACTIVIDADES TEMA 7. INMUNOLOGÍA CUESTIONES DE SELECTIVIDAD Cuestiones generales sobre inmunidad, respuesta inmune y linfocitos 1. Defina los siguientes conceptos: inmunidad, sueroterapia y vacunación. 2. ¿En qué consisten las respuestas inmune primaria y secundaria?. 3. a. b. c. d.
Diferencia los siguientes términos: Anticuerpo/Antígeno Cadena ligera/Cadena pesada Linfocito B/Linfocito T Célula plasmática/Célula de memoria
4. a) b) c)
Responde : Explica que es el “sistema inmunitario” ¿Qué son las “defensas específicas”?. Indique cuáles son las células específicas principales de dicho sistema.
5. Enumere y explique las diferencias más importantes entre: inmunización activa (vacunación) y alergia. 6. Indique si la siguiente afirmación es cierta o falsa, razonando la respuesta: Los linfocitos T son responsables de la respuesta inmune celular y colaboran en la humoral. 7. Definir los conceptos: determinante antigénico y linfocito B. 8. a) b) c) d)
Defina los conceptos siguientes: Macráfagos Antígenos Linfocitos T Alergia
9. Describa las características e importancia de la vacunación, así como los distintos tipos de vacunas.
Cuestiones sobre antígenos y anticuerpos 10. Definición de antígeno y anticuerpo. Señale algún tipo de molécula con propiedades antigénicas. 11. Ciertos organismos producen anticuerpos en respuesta a la presencia de un antígeno. Al respecto: a) ¿Qué tipo de biomoléculas son los anticuerpos?. b) ¿Qué tipo de biomoléculas son los antígenos?. c) ¿Qué características principales tiene la reacción antígeno-anticuerpo?. d) ¿Qué células del organismo producen anticuerpos?. 12. Describa un proceso de fagocitosis mediada por anticuerpos.
Biología 2º Bachillerato
Tema 7. Inmunología
2
Cuestiones sobre el VIH y el SIDA 13. Con respecto al SIDA: a) Relacione los conceptos siguientes, explicando brevemente el porqué de su elección: 1) 2) 3) 4) 5) 6)
VIH SIDA Seropositivo Caso de SIDA AZT Portador del virus del SIDA
a) b) c) d) e) f)
Enfermo Virus Enfermedad Medicamento Persona con anticuerpos VIH en sangre Persona con el virus VIH en sus células
b) Resuma las etapas del ciclo de infección de un retrovirus, como el VIH. 14. Explique el ciclo vital de un retrovirus. 15. Con respecto al SIDA : a) ¿Cómo se desarrolla el SIDA a partir de la infección de un organismo por VIH?. b) Enumere las vías de transmisión del VIH. c) Distinga un seropositivo de un portador del virus del SIDA. 16. Contesta: a) ¿Qué significan las siglas SIDA y VIH?. b) ¿Cuáles son las vías de transmisión del VIH?. c) ¿Qué relación tienen los linfocitos T y los macrófagos con el sistema inmune?. 17. El virus VIH del SIDA infecta a los linfocitos T4, provocando su destrucción con el tiempo. Al respecto: a) ¿Cuál es la función principal de los linfocitos T4?. b) ¿Qué consecuencias generales ocasiona la destrucción de estos linfocitos T4 por el virus?.